вторичный иммунодефицит что это такое у взрослых лечение
Вторичные иммунодефициты
Вторичные иммунодефициты – это болезни иммунной системы, возникающие у детей и взрослых, не связанные с генетическими дефектами и характеризующиеся развитием повторных, затяжных инфекционно-воспалительных патологических процессов, плохо поддающихся этиотропному лечению. Выделяют приобретенную, индуцированную и спонтанную форму вторичных иммунодефицитов. Симптоматика обусловлена снижением иммунитета и отражает конкретное поражение того или иного органа (системы). Диагностика основана на анализе клинической картины и данных иммунологических исследований. В лечении используется вакцинация, заместительная терапия, иммуномодуляторы.
Общие сведения
Вторичные иммунодефициты – нарушения иммунитета, которые развиваются в поздний постнатальный период и не связаны с генетическими дефектами, возникают на фоне исходно нормальной реактивности организма и обусловлены конкретным причинным фактором, вызвавшим развитие дефекта иммунной системы.
Течение заболевания может быть скрытым (жалобы и клиническая симптоматика отсутствует, наличие иммунодефицита выявляется только при лабораторном исследовании) или активным с наличием признаков воспалительного процесса на коже и в подкожной клетчатке, верхних дыхательных путях, легких, мочеполовой системе, пищеварительном тракте и в других органах. В отличие от преходящих сдвигов в иммунитете, при вторичном иммунодефиците патологические изменения сохраняются и после ликвидации возбудителя заболевания и купирования воспаления.
Причины
Привести к выраженному и стойкому снижению иммунной защиты организма могут самые разнообразные этиологические факторы – как внешние, так и внутренние. Вторичный иммунодефицит нередко развивается при общем истощении организма. Длительное недоедание с дефицитом в рационе белка, жирных кислот, витаминов и микроэлементов, нарушения всасывания и расщепления питательных веществ в пищеварительном тракте приводят к нарушению процессов созревания лимфоцитов и снижают сопротивляемость организма.
Тяжелые травматические повреждения опорно-двигательного аппарата и внутренних органов, обширные ожоги, серьезные оперативные вмешательства, как правило, сопровождаются кровопотерей (наряду с плазмой теряются белки системы комплемента, иммуноглобулины, нейтрофилы и лимфоциты), а выброс кортикостероидных гормонов, предназначенных для поддержания жизненно-важных функций (кровообращения, дыхания и др.) еще больше угнетает работу иммунитета.
Ведущую роль в развитии вторичных иммунодефицитов играют хронические вирусные инфекционные заболевания (ВИЧ, цитомегаловирусная инфекция, вирусы Эпштейна-Барр и другие герпес-вирусы, реже корь, краснуха, вирусные гепатиты и т. д.), вызывая подавление клеточного и гуморального иммунитета. Неблагоприятное влияние на иммунный статус оказывает бактериальная и грибковая инфекция, паразитарные заболевания.
Выраженное нарушение обменных процессов в организме при соматических заболеваниях (хронические гломерулонефриты, почечная недостаточность) и эндокринных расстройствах (диабете, гипо- и гипертиреозе) приводит к угнетению хемотаксиса и фагоцитирующей активности нейтрофилов и, как следствие, к вторичному иммунодефициту с возникновением воспалительных очагов различной локализации (чаще это пиодермии, абсцессы и флегмоны).
Снижается иммунитет при длительном приеме некоторых лекарственных препаратов, обладающих подавляющим действием на костный мозг и кроветворение, нарушающих формирование и функциональную активность лимфоцитов (цитостатики, глюкокортикоиды и пр.). Схожий эффект оказывает и лучевое воздействие.
При злокачественных новообразованиях происходит продукция опухолью иммуномодулирующих факторов и цитокинов, в результате чего снижается количество T-лимфоцитов, увеличивается активность клеток-супрессоров, угнетается фагоцитоз. Ситуация усугубляется при генерализации опухолевого процесса и метастазировании в костный мозг. Вторичные иммунодефициты нередко развиваются при аутоиммунных заболеваниях, острых и хронических отравлениях, у людей старческого возраста, при длительных физических и психоэмоциональных перегрузках.
Симптомы вторичных иммунодефицитов
Клинические проявления характеризуются наличием в организме затяжного, устойчивого к этиотропной терапии хронического инфекционного гнойно-воспалительного заболевания на фоне снижения иммунной защиты. При этом изменения могут быть преходящими, временными или имеют необратимый характер. Выделяют индуцированную, спонтанную и приобретенную формы вторичных иммунодефицитов.
К индуцированной форме относят нарушения, возникающие вследствие конкретных причинных факторов (рентгеновское излучение, длительный прием цитостатиков, кортикостероидных гормонов, тяжелые травмы и обширные хирургические операции с интоксикацией, кровопотерей), а также при тяжелой соматической патологии (сахарный диабет, гепатиты, циррозы, хроническая почечная недостаточность) и злокачественных опухолях.
При спонтанной форме видимый этиологический фактор, вызвавший нарушение иммунной защиты, не определяется. Клинически при этой форме отмечается наличие хронических, трудно поддающихся лечению и часто обостряющихся заболеваний верхних дыхательных путей и легких (синуситы, бронхоэктазы, пневмонии, абсцессы легких), пищеварительного тракта и мочевыводящих путей, кожи и подкожной клетчатки (фурункулы, карбункулы, абсцессы и флегмоны), которые вызваны условно-патогенными микроорганизмами. В отдельную – приобретенную форму выделен синдром приобретенного иммунодефицита (СПИД), вызванный ВИЧ-инфекцией.
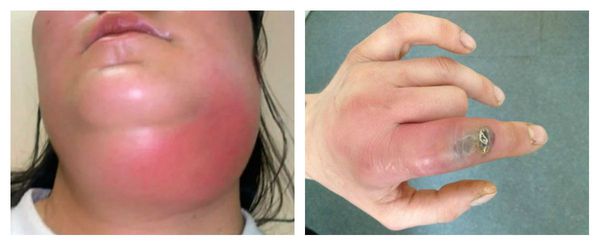
О наличии вторичного иммунодефицита при всех стадиях можно судить по общим клиническим проявлениям инфекционно-воспалительного процесса. Это может быть длительный субфебрилитет или лихорадка, увеличение лимфатических узлов и их воспаление, боли в мышцах и суставах, общая слабость и утомляемость, снижение работоспособности, частые простудные заболевания, повторные ангины, часто рецидивирующие хронические гаймориты, бронхиты, повторные пневмонии, септические состояния и т. п. При этом эффективность стандартной антибактериальной и противовоспалительной терапии невысока.
Диагностика
Выявление вторичных иммунодефицитов требует комплексного подхода и участия в процессе диагностики различных врачей-специалистов – аллерголога-иммунолога, гематолога, онколога, инфекциониста, оториноларинголога, уролога, гинеколога и др. При этом учитывается клиническая картина заболевания, свидетельствующая о наличии хронической инфекции, трудно поддающейся лечению, а также выявление оппортунистических инфекций, вызванных условно-патогенными микроорганизмами.
Необходимо изучение иммунного статуса организма с использованием всех доступных методик, применяемых в аллергологии и иммунологии. Диагностика основана на исследовании всех звеньев иммунитета, участвующих в защите организма от инфекционных агентов. При этом изучается фагоцитарная система, система комплемента, субпопуляции T- и B-лимфоцитов. Исследования выполняются путем проведения тестов первого (ориентировочного) уровня, позволяющего выявить грубые общие нарушения иммунитета и второго (дополнительного) уровня с идентификацией конкретного дефекта.
При проведении скрининговых исследований (тесты 1 уровня, которые можно выполнить в любой клинико-диагностической лаборатории) можно получить информацию об абсолютном количестве лейкоцитов, нейтрофилов, лимфоцитов и тромбоцитов (встречается как лейкопения, так и лейкоцитоз, относительный лимфоцитоз, повышенная СОЭ), уровне белка и сывороточных иммуноглобулинов G, A, M и E, гемолитической активности комплемента. Кроме того, можно выполнить необходимые кожные пробы для выявления гиперчувствительности замедленного типа.
При углубленном анализе вторичного иммунодефицита (тесты 2 уровня) определяется интенсивность хемотаксиса фагоцитов, завершенность фагоцитоза, субклассы иммуноглобулинов и специфические антитела к конкретным антигенам, продукция цитокинов, индукторов T-клеток и другие показатели. Анализ полученных данных должен проводиться только с учетом конкретного состояния данного пациента, сопутствующих заболеваний, возраста, наличия аллергических реакций, аутоиммунных расстройств и других факторов.
В процессе обследования проводится дифференциальная диагностика с первичными иммунодефицитами, затяжными инфекционными заболеваниями вирусной, бактериальной, грибковой и паразитарной природы, соматическими заболеваниями, эндокринными расстройствами, новообразованиями.
Лечение вторичных иммунодефицитов
Эффективность лечения вторичных иммунодефицитов зависит от правильности и своевременности выявления этиологического фактора, вызвавшего появление дефекта иммунной системы и возможности его устранения. Если нарушение иммунитета возникло на фоне хронической инфекции, применяются меры по ликвидации очагов воспаления с использованием антибактериальных препаратов с учетом чувствительности к ним возбудителя, проведением адекватной противовирусной терапии, использованием интерферонов и т. п. Если причинный фактор – недостаточное питание и авитаминоз, проводятся мероприятия по разработке правильного рациона питания со сбалансированным сочетанием белков, жиров, углеводов, микроэлементов и необходимой калорийности. Также устраняются имеющиеся нарушения обмена веществ, восстанавливается нормальный гормональный статус, проводится консервативное и оперативное лечение основного заболевания (эндокринная, соматическая патология, новообразования).
Важный компонент лечения больных вторичным иммунодефицитом – иммунотропная терапия с использованием активной иммунизации (вакцинации), заместительного лечения препаратами крови (внутривенное введение плазмы, лейкоцитарной массы, человеческого иммуноглобулина), а также использованием препаратов иммунотропного действия (иммуностимуляторов). Целесообразность назначения того или иного лечебного средства и подбор дозировки осуществляется врачом аллергологом-иммунологом с учетом конкретной ситуации. При преходящем характере иммунных нарушений, своевременном выявлении вторичного иммунодефицита и подборе правильного лечения, прогноз заболевания может быть благоприятным.
Что такое вторичный иммунодефицит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бычковой Е.Ю., остеопата со стажем в 22 года.
Определение болезни. Причины заболевания
Вторичный иммунодефицит формируется у людей старше 6 лет с исходно нормальным иммунитетом. До этого возраста происходит созревание иммунной системы, особенно полноценных механизмов противоинфекционной защиты, поэтому частое развитие инфекционных заболеваний у детей младше 6 лет не является признаком патологии.
Появление вторичного иммунодефицита обычно связано с воздействием окружающей среды или каких-либо других факторов, но у многих из пациентов можно выявить генетическую предрасположенность к нарушению иммунитета.
Иммунологически здоровый организм способен контролировать и предотвращать развитие инфекций и опухолевых процессов, то есть осуществлять иммунологический контроль внутренней среды.
Когда можно заподозрить вторичный иммунодефицит
Причины развития вторичных иммунодефицитных состояний:
Иммунодефицитные состояния у детей
Развитию иммунодефицита у детей, как и у взрослых, способствуют:
Дисбактериоз у матери является причиной дисбактериоза у ребёнка с последующим замедлением и неполноценным созреванием иммунной системы. Каждый курс антибиотикотерапии может усугубить это состояние.
Проявления иммунодефицита зависят от степени его выраженности, они сопровождаются частыми ОРВИ с инфекционными осложнениями, эпизодами лихорадки, болезненностью, увеличением лимфоузлов, болью в животе, рвотой и нарушением стула.
Симптомы вторичного иммунодефицита
Как проявляется вторичный иммунодефицит
Клинические проявления вторичного иммунодефицита разнообразны. Очень часто на первый план выходят симптомы основного заболевания, которое привело к развитию иммунодефицита. Но основные проявления проблем с иммунитетом, которые указывают на необходимость иммунологического обследования, всё же присутствуют. К ним относятся:
Все хронические инфекции и воспаления протекают на фоне ослабленной иммунной защиты. Поэтому любая хронизация инфекции будет указывать на несостоятельность иммунитета, который не может справиться с болезнью в ходе острого воспалительного процесса.
Патогенез вторичного иммунодефицита
В течение жизни организм подвергается воздействию различных повреждающих факторов, вызывающих вторичный иммунодефицит. Они приводят к угнетению реакций клеточного иммунитета, снижению лейкоцитов и интерферонов — белков иммунной системы, которые вырабатываются лейкоцитами и иммунными клетками и блокируют распространение вируса. Вследствие этого появляются хронические инфекционно-воспалительные процессы, часто рецидивирующие.
Опухоли, возникающие в организме с ослабленной иммунной защитой, истощают иммунитет по мере своего роста, а проводимое лечение (операция, лучевая и химиотерапия) усугубляют возникший иммунодефицит. В этом случае страдает клеточное звено иммунитета:
Классификация и стадии развития вторичного иммунодефицита
По причине возникновения выделяют:
По форме вторичный иммунодефицит может быть:
По продолжительности выделяют два типа вторичного иммунодефицита:
По локализации основного дефекта различают:
Установить локализацию повреждения иммунной системы, основываясь только на симптомах, без лабораторного исследования иммунного статуса, практически невозможно: сходная клиническая картина может наблюдаться при разных типах вторичного дефицита. Например, склонность к вирусным инфекциям может встречаться как при Т-клеточном дефиците, так и при дефиците системы интерферонов.
Осложнения вторичного иммунодефицита
Вторичный иммунодефицит, развивающийся на фоне инфекции и/или воспаления, становится причиной тяжёлых жизнеугрожающих состояний. Без своевременной коррекции иммунитета патологический круг замыкается: течение основной болезни ухудшается.
Наиболее частыми осложнениями вторичного иммунодефицита являются тяжёлые инфекционные заболевания: пневмония, сепсис, абсцесс и флегмона. Их основные проявления: высокая температура и признаки воспаления. При пневмонии наблюдается одышка, кашель и боль в грудной клетке. Сепсис является жизнеугрожающим состоянием, он развивается при попадании в кровь инфекции, сопровождается системной воспалительной реакцией и полиорганной недостаточностью. При абсцессах и флегмоне в организме присутствует очаг гнойного воспаления с выраженной болью, отёком и гиперемией (покраснением).
Диагностика вторичного иммунодефицита
Диагноз «вторичный иммунодефицит» ставится на основании истории болезни, физикального обследования и оценки статуса иммунной системы.
Чтобы назначить эффективных мер по коррекции иммунитета, важно выявить факторы, которые поспособствовали развитию иммунодефицита. Поэтому на консультацию к врачу-иммунологу стоит принести все имеющиеся обследования, а врач будет очень подробно расспрашивать о перенесённых заболеваниях, проведённом лечении, операциях и образе жизни пациента.
Как распознать вторичный иммунодефицит
При подозрении на вторичный иммунодефицит врач назначает анализ крови и иммунограмму — иммунологические тесты, которые оценивают компоненты иммунной системы с точки зрения количества и качества.
Схема обследования различных звеньев иммунной системы (иммунограмма):
На вторичный иммунодефицит могут указывать как пониженные, так и повышенные показатели иммунограммы.
При подозрении на дисбаланс ключевых нутриентов (витаминов, микроэлементов и т. д.) врач-иммунолог может назначить исследования:
В своём заключении врач-иммунолог может указать «вторичный иммунодефицит» как основной или сопутствующий диагноз. Всё зависит от клинической картины.
Лечение вторичного иммунодефицита
Лечение пациента с вторичным иммунодефицитом проводится совместно с врачом, который курирует пациента по поводу основного заболевания. Задача врача-иммунолога заключается в подборе иммунокорригирующей терапии.
«Коррекция иммунитета» в данном случае подразумевает восстановление ослабленной иммунной защиты, исправление дисбаланса её компонентов и иммунных реакций, ослабление патологических иммунных процессов и подавление аутоиммунных реакций.
Лечение вторичного иммунодефицита начинают с определения и устранения его причины. Например, при нарушении иммунитета, вызванном инфекционно-воспалительным процессом, устраняются очаги хронического воспаления.
Если вторичный иммунодефицит возник в результате витаминно-минеральной недостаточности, то назначаются комплексы, содержащие дефицитные компоненты. Например, при истощении лимфоузлов и старении вилочковой железы назначают витамины В6. При обострении или начале аутоиммунных и лимфопролиферативных заболеваний показаны витамины Е.
Важными минералами для иммунной системы являются цинк, йод, литий, медь, кобальт, хром, молибден, селен, марганец и железо. Эти микроэлементы помогают активировать ферменты, которые участвуют в иммунных реакциях. К примеру, цинк предотвращает гибель клеток иммунной системы.
Заместительное лечение вторичного иммунодефицита
Заместительная терапия помогает предотвратить инфекции. Для этого применяют:
Иммунотропное лечение вторичного иммунодефицита
При остром инфекционном воспалении иммуностимуляторы позволяют:
При хроническом инфекционном воспалении иммуномодуляторы:
На степень эффективности иммунокоррекции влияет кратность приёма и стадия заболевания. Срок действия иммуномодуляторов зависит от характера препарата, показателей иммунного статуса и вида заболевания, вызвавшего вторичный иммунодефицит.
Устранение дефицита одного звена иммунитета может привести к компенсации другого звена, так как иммунная система работает по принципу взаимосвязанных модулей.
Может быть назначен как один иммуномодулятор, так и несколько, то есть их комбинация. При комбинированной иммунокоррекцией последовательно или одновременно принимают несколько модуляторов, обладающих разными механизмами действия. Таких иммуномодулирующих препаратов сейчас довольно много.
Показаниями для комбинированной иммунотерапии являются:
ВАЖНО: Самостоятельно назначать себе иммунокорректоры нельзя, так как их бесконтрольное применение может спровоцировать развитие вторичного иммунодефицита.
Прогноз. Профилактика
При вторичном иммунодефиците работа иммунной системы нарушена слабее, чем при первичном. В большинстве случаев выявляется несколько факторов, подавляющих иммунный ответ.
Прогноз определяется тяжестью основного заболевания. Например, если иммунодефицит возник из-за нехватки витаминов или нарушения режима труда и отдыха, он намного легче компенсируется, чем иммунодефицит, спровоцированный опухолевым процессом, сахарным диабетом или ВИЧ-инфекцией.
У детского организма отдельные звенья иммунной системы ещё незрелы: Т-лимфоциты только начинают «знакомиться» с различными инфекциями, поэтому ребёнок часто болеет ОРВИ. Со временем нарабатываются «клетки памяти». По мере взросления формируется широкий «репертуар» Т-лимфоцитов, способных распознавать и быстро запустить иммунный ответ, в связи с чем заболеваемость снижается.
С возрастом иммунная система стареет: в ответ на новые антигены участвует меньше Т-клеток, ухудшается кооперация между клетками иммунной системы, фагоциты хуже поглощают вирусы и мёртвые клетки. Поэтому многие инфекционно-воспалительные заболевания у пожилых людей протекают значительно тяжелее и чаще дают осложнения.
Первичная профилактика вторичного иммунодефицита заключается в ведении здорового образа жизни, сбалансированном питании, отказе от курения. Всё это позволяет предупредить развитие различных заболеваний.
Вторичная профилактика направлена на своевременное лечение инфекционных и общесоматических заболеваний.
Людям с вторичным иммунодефицитом нужны «особые условия», которые не позволят усугубить нарушение иммунитета. Пациентам следует:
Вакцинотерапия
Вакцинация проводится в соответствии с национальным календарем прививок. Перед введением вакцины нужно скомпенсировать иммунодефицит: пропить курс витаминов, минералов и иммуномодуляторов по назначению врача. Это позволит сформировать иммунный ответ на прививку и снизить риск осложнений.
ИММУНОДЕФИЦИТЫ:диагностика и иммунотерапия
Целью настоящего обзора является анализ современных данных о диагностике и иммунотерапии иммунодефицитов. Иммунодефицит — это понижение функциональной активности основных компонентов иммунной системы, ведущее к нарушению защиты организма от микробов и пр
Целью настоящего обзора является анализ современных данных о диагностике и иммунотерапии иммунодефицитов. Иммунодефицит — это понижение функциональной активности основных компонентов иммунной системы, ведущее к нарушению защиты организма от микробов и проявляющееся в повышенной инфекционной заболеваемости. Иммунодефициты делятся на первичные и вторичные.
 |
Первичные иммунодефициты (ПИД) — это врожденные нарушения иммунной системы, связанные с генетическими дефектами одного или нескольких компонентов иммунной системы, а именно: комплемента, фагоцитоза, гуморального и клеточного иммунитета. Общей чертой всех видов ПИД является наличие рецидивирующих, хронических инфекций, поражающих различные органы и ткани и, как правило, вызываемых оппортунистическими или условно-патогенными микроорганизмами, т. е. низковирулентной флорой. ПИД часто бывают ассоциированы с анатомическими и функциональными нарушениями других систем организма и имеют некоторые характерные черты, позволяющие поставить предварительный диагноз у новорожденных без лабораторно-иммунологического обследования (см. табл.).
Таблица. Данные физикального обследования, позволяющие сделать предварительный диагноз ПИД [8]
Различные компоненты иммунной системы могут принимать неодинаковое участие в элиминации микробов из макрорганизма. Поэтому по характеру инфекционного процесса можно также предварительно судить о том, какой компонент иммунитета работает недостаточно. Так, при развитии в течение первых дней жизни ребенка гнойно-воспалительных процессов кожи и слизистых оболочек, вызываемых пиогенными кокками, есть повод думать о наличии врожденных дефектов фагоцитарной системы. Для них также характерно очень медленное заживление пупочной раны и отпадение пупочного канатика. Инфекционные процессы, связанные с дефектом антителообразования, развиваются, как правило, во втором полугодии жизни ребенка после исчезновения из кровяного русла материнских иммуноглобулинов. Чаще всего эти инфекции вызываются инкапсулированными пиогенными микроорганизмами (стрептококками, пневмококками, Haemophiluls influlenzae и др.), поражающими верхние и нижние отделы респираторного тракта. Упорные нейссериальные инфекции часто ассоциируются с врожденными дефектами в компонентах комплемента С5-С9. Частые инфекционные процессы, вызываемые вирусами и другими внутриклеточными возбудителями, дают основание предполагать наличие дефекта в Т-системе иммунитета. Об этом также может свидетельствовать кожно-слизистый кандидоз. Триада — хронические пневмонии, длительная, трудно поддающаяся лечению диарея и кандидоз — всегда служит основанием для предположения о наличии врожденных дефектов Т-лимфоцитов. Для комбинированных дефектов Т- и В-систем иммунитета характерно необычайно тяжелое течение инфекционных процессов, которые развиваются в первый месяц жизни ребенка. Без соответствующего лечения ребенок погибает, как правило, в течение первого года жизни.
Лабораторно-иммунологическое обследование проводится с целью идентификации конкретного нарушения иммунной системы и подтверждения клинического диагноза. Первичная диагностика может осуществляться с помощью панели скрининговых лабораторных тестов.
Применение панели скрининговых лабораторных тестов возможно практически в любой областной или городской больнице, где имеется клинико-диагностическая лаборатория. Однако углубленный анализ можно провести лишь в специализированном лечебно-профилактическом учреждении, имеющем современную лабораторию клинической иммунологии. У больного с подозрением на ПИД следует детально исследовать функциональную активность фагоцитов, Т- и В-систем иммунитета. Более подробно методические подходы к оценке иммунитета будут описаны в соответствующем разделе.
В настоящее время идентифицировано более 70 врожденных дефектов иммунной системы, и, вероятно, их число по мере совершенствования методов молекулярной иммунодиагностики будет расти. ПИД — это относительно редкие заболевания: их частота составляет в среднем 1/25000-1/100000. Исключением является селективный IgA-дефицит, встречающийся с частотой 1/500-1/700. Изучение ПИД представляет большой интерес для теоретической и прикладной иммунологии. Анализ молекулярно-генетических механизмов, лежащих в основе этих дефектов, дает возможность выявлять принципиально новые механизмы функционирования иммунной системы и, следовательно, разрабатывать новые подходы к иммунодиагностике и иммунотерапии заболеваний, связанных с нарушениями иммунной системы.
Вторичные иммунодефициты (ВИД). Значительный интерес для клинической иммунологии представляет и изучение ВИД, которые в количественном отношении среди иммунодефицитов являются, без сомнения, доминирующими. Под ВИД понимают такие нарушения иммунной системы, которые развиваются в позднем постнатальном периоде или у взрослых и, как принято считать, не являются результатом какого-то генетического дефекта. Среди ВИД условно можно выделить три формы: приобретенную, индуцированную и спонтанную. Наиболее ярким примером первой формы является синдром приобретенного иммунодефицита (СПИД), развивающегося в результате поражения лимфоидной ткани человека соответствующим вирусом. Индуцированные ВИД — это такие состояния, возникновение которых связано с какой-то конкретной причиной: рентгеновское облучение, кортикостероиды, цитостатики, травмы и хирургические операции, а также нарушения иммунитета, развивающиеся вторично по отношению к основному заболеванию (диабет, заболевания почек и печени, злокачественные процессы и т. д.). Индуцированные формы ВИД, как правило, являются транзиторными, и при устранении вызвавшей причины в большинстве случаев происходит полное восстановление иммунитета. В отличие от индуцированной, спонтанная форма ВИД характеризуется отсутствием явной причины, вызвавшей нарушение иммунологической реактивности. Так же как и при ПИД, эта форма иммунодефицита проявляется в виде хронических, рецидивирующих, инфекционно-воспалительных процессов бронхолегочного аппарата и околоносовых придаточных пазух, урогенитального и желудочно-кишечного трактов, глаз, кожи и мягких тканей, вызываемых, как и ПИД, оппортунистическими или условно-патогенными микроорганизмами с атипичными биологическими свойствами и часто с наличием множественной устойчивости к антибиотикам. В количественном отношении спонтанная форма является доминирующей формой ВИД.
Как уже отмечалось, изучение иммунного статуса при иммунодефицитах должно включать изучение количества и функциональной активности основных компонентов иммунной системы, играющих главную роль в противоинфекционной защите организма. К ним относятся фагоцитарная система, система комплемента, Т- и В-системы иммунитета. Методы, применяемые для оценки функционирования этих систем, условно разделены Петровым Р. В. с соавт. (1984) на тесты 1-го и 2-го уровней. По данным этих авторов, тесты 1-го уровня являются ориентировочными и направлены на выявление грубых дефектов в иммунной системе; тесты 2-го уровня являются функциональными и направлены на идентификацию конкретной “поломки” в иммунной системе. Мы относим к тестам 1-го уровня методы, направленные на идентификацию того продукта функционирования соответствующей системы иммунитета, который определяет ее антимикробный эффект. Тесты 2-го уровня являются дополнительными. Они существенно обогащают информацию о функционировании соответствующей системы иммунитета.
К тестам 1-го уровня для оценки фагоцитоза относится определение:
Процесс фагоцитоза состоит из нескольких этапов: хемотаксиса, адгезии, поглощения, дегрануляции, киллинга и разрушения объекта. Их изучение имеет определенную значимость в оценке фагоцитарного процесса, так как существуют иммунодефициты, связанные с наличием поломок практически в каждом этапе. Главным итогом работы нейтрофила и моноцита является киллинг и разрушение микроба, т. е. завершенный фагоцитоз. Для оценки киллинга можно рекомендовать определение образования активных форм кислорода в процессе фагоцитоза. Если нет возможности определять активные формы кислорода с помощью хемолюминесценции, об образовании супероксидного радикала можно судить по восстановлению нитросинего тетрозолия. Но в данном случае следует помнить, что киллинг микробов в фагоците осуществляется с помощью как кислородозависимых, так и кислородонезависимых механизмов, т. е. определение активных форм кислорода не дает полной информации об этом процессе.
К тестам 2-го уровня оценки фагоцитоза можно отнести определение:
К тестам 1-го уровня оценки B-системы иммунитета можно отнести определение:
Определение уровня иммуноглобулинов — это по-прежнему важный и надежный метод оценки B-системы иммунитета. Его можно считать главным методом диагностики всех форм иммунодефицитов, связанных с биосинтезом антител.
К тестам 2-го уровня оценки В-системы иммунитета можно отнести определение:
Определение субклассов IgG представляет определенную диагностическую ценность, так как при нормальном уровне IgG могут быть дефициты по субклассам иммуноглобулинов. У таких людей в ряде случаев наблюдаются иммунодефицитные состояния, проявляющиеся в повышенной инфекционной заболеваемости. Так, IgG2 является субклассом иммуноглобулина G, который преимущественно содержит антитела против полисахаридов инкапсулированных бактерий (Haemophiluls influlenzae, Steptococculs pneulmoniae). Поэтому дефицит, связанный с IgG2, а также с IgA, ведет к повышенной заболеваемости респираторными инфекциями. Нарушения в соотношении субклассов IgA и в соотношении каппа- и лямбда-цепей также могут быть причиной иммунодефицитных состояний. Важную информацию о состоянии гуморального иммунитета дает определение антител к бактериальным белковым и полисахаридным антигенам, так как степень защиты организма от данной конкретной инфекции зависит не от общего уровня иммуноглобулинов, а от количества антител к ее возбудителю. Особенно наглядно демонстрируют это данные, свидетельствующие о том, что развитие хронических синуситов и отитов зависит только от дефицита у таких больных IgG3-антител к Moraxella catarrhalis. Другим наглядным примером важности определения специфических антител могут служить данные, доказывающие, что у лиц, страдающих частыми инфекционными процессами дыхательных путей, при нормальном уровне всех классов иммуноглобулинов существенно понижен титр антител к Haemophiluls influlenzae.
Ценную информацию о состоянии гуморального иммунитета можно получить не только при определении уровня иммуноглобулинов, их субклассов или антител к определенным антигенам, но и путем изучения их функциональных свойств. К ним в первую очередь следует отнести такое свойство антител, как аффинность, от которого в значительной степени зависит прочность взаимодействия антител с антигеном. Продукция низкоаффинных антител может вести к развитию иммунодефицитного состояния. Нами было доказано, что у лиц, часто и длительно страдающих заболеваниями дыхательного тракта, при нормальном уровне иммуноглобулинов, несколько повышенном уровне антител к пептидогликану St.aulreuls, Str.pneulmoniae, Br.catarrhalis, аффинность антител к этим микробам существенно снижена.
Важным фунцинальным свойством является опсонизирующая активность иммуноглобулинов. Как уже отмечалось, нейтрофил — это центральная фигура в защите организма от внеклеточных микробов. Однако выполнение им этой функции в значительной степени зависит от опсонизирующей активности сыворотки крови, где иммуноглобулинам и комплементу принадлежит ведущая роль в этой активности. При исследовании 30 больных с бактериемией, вызванной грамотрицательными бактериями, было установлено, что нейтрофилы этих больных обладали пониженной способностью к киллингу E.coli. Это зависело только от неспособности сыворотки крови больных к опсонизации, так как добавление к нейтрофилам этих больных сыворотки здоровых доноров полностью восстанавливало способность нейтрофилов к киллингу E.coli.
К тестам 1-го уровня оценки T-системы иммунитета можно отнести определение:
К скрининговым лабораторным тестам относится определение:
При оценке B-системы иммунитета мы рекомендовали в качестве тестов 1-го уровня определение числа B-лимфоцитов, а также и уровня иммуноглобулинов. Так как последние являются главным конечным продуктом B-клеток, то это позволяет оценить B-систему иммунитета как с количественной, так и с функциональной стороны. Такой подход пока трудно осуществить в отношении T-системы иммунитета, так как главным конечным продуктом Т-лимфоцитов являются цитокины, а системы для их определения пока еще мало доступны практическим лабораториям клинической иммунологии. Тем не менее оценка функциональной активности T-системы иммунитета представляет задачу исключительной важности, так как она может быть понижена, иногда даже существенно, при нормальном количестве T-клеток и их субпопуляций. Методы оценки функциональной активности T-лимфоцитов достаточно сложны. Простейшим из них, на наш взгляд, является реакция бласт-трансформации с применением двух основных T-митогенов: фитогемагглютинина и конканавалина А. Пролиферативный ответ T-лимфоцитов на митогены понижен практически при всех хронических инфекционно-воспалительных процессах, злокачественных заболеваниях, особенно кроветворной системы; при всех видах иммунодепрессивной терапии, при СПИД и при всех первичных T-клеточных иммунодефицитах.
С помощью скрининг-тестов можно выявить следующие виды ПИД:
К тестам 2-го уровня для оценки T-системы иммунитета мы относим определение:
Без сомнения, определение продукции цитокинов лимфоцитами и макрофагами должно стать главным методическим приемом в иммунодиагностике заболеваний, связанных с нарушениями иммунной системы. Идентификация цитокинов в ряде случаев позволит более точно установить диагноз заболевания и механизм иммунного нарушения.
Важным является и определение таких провоспалительных цитокинов, как ФНО, ИЛ-1 и гамма-интерферон. Велика их роль в этиопатогенезе различных острых и хронических воспалительных процессов как инфекционной, так и аутоиммунной природы. Их повышенное образование является главной причиной септического шока. При сепсисе уровень ФНО в крови может достигать 1 нг/мл. Накапливаются данные о роли провоспалительных цитокинов в этиопатогенезе неспецифического язвенного колита, рассеянного склероза, ревматоидного артрита, инсулинзависимого диабета и др.
Мы считаем важным для иммунодиагностики изучение экспрессии активационных молекул и молекул адгезии на поверхности T-лимфоцитов. Как указывает само название, идентификация активационных молекул дает важную информацию о степени активации T-клеток. Нарушения экспрессии рецептора для ИЛ-2 наблюдаются при многих злокачественных заболеваниях крови — T-клеточной лейкемии, волосатоклеточной лейкемии, лимфогрануломатозе и др. — и аутоиммунных процессах: ревматоидном артрите, системной красной волчанке, апластической анемии, склеродермии, болезни Крона, саркоидозе, инсулинзависимом диабете и др.
Особым, на наш взгляд, является вопрос о применении кожных проб в диагностике T-клеточных иммунодефицитов. Как уже отмечалось, по рекомендации зарубежных специалистов и в соответствии с рекомендациями экспертов ВОЗ они применяются в качестве скринирующих или тестов 1-го уровня для оценки T-системы иммунитета. Это связано с двумя обстоятельствами. Во-первых, кожные пробы — это простейшие и в то же время информативные тесты, позволяющие оценить функциональную активность T-лимфоцитов. Положительные кожные тесты с некоторыми микробными антигенами с большой степенью вероятности позволяют исключить наличие у больного T-клеточного иммунодефицита. Во-вторых, рядом западных фирм разработаны системы для постановки кожных проб, которые включают основные антигены для определения T-клеточного иммунитета. Это позволяет в строго контролируемых условиях оценить функциональную активность T-системы иммунитета. К сожалению, такие системы в России отсутствуют и, следовательно, практически не применяются для оценки T-системы иммунитета.
Оценка иммунной системы у людей с признаками ВИД может встретить ряд трудностей, и прежде всего связанных с оценкой причинно-следственных отношений. Нередко те изменения, которые регистрируются при анализе параметров иммунной системы, являются следствием, а не причиной патологического процесса. Так, у лиц, часто и длительно болеющих (ЧДБ) респираторными инфекциями, уровень антител к основным бактериальным возбудителям этих инфекций резко повышен. Аналогичная ситуация наблюдается у больных СПИД, имеющих инфекционные осложнения со стороны респираторного тракта. Естественно, что повышение титров антител к возбудителям респираторных инфекций как у больных группы ЧДБ, так и у больных СПИД является следствием активации иммунной системы в результате инфекционно-воспалительного процесса в респираторном тракте. Еще одна трудность, с которой врач может столкнуться при оценке иммунного статуса у больных с хроническими инфекционно-воспалительными процессами, — это выбор адекватного методического подхода и выбор адекватного материала для исследования. Хотя достижения теоретической и клинической иммунологии трудно переоценить и врач-иммунолог располагает большим набором современных методик для определения состояния иммунной системы, все-таки следует признать, что мы все еще мало знаем о функционировании иммунной системы в целом. Недостаточно изучена и конкретная взаимосвязь между развитием тех или иных заболеваний и нарушением различных звеньев иммунитета. Поэтому нередко при использовании стандартных методов оценки фагоцитоза, Т- и В-систем иммунитета у больных с хроническими инфекционно-воспалительными процессами врач не получает убедительной информации о нарушении иммунитета. Так, например, при определении иммунного статуса по указанным выше параметрам у больных с хроническими заболеваниями придаточных околоносовых пазух мы не выявили существенных отклонений. Вместе с тем оказалось, что у таких больных имеется дефект по синтезу IgG3-антител к Branhamella catarrhalis, и это является главной причиной развития основного патологического процесса. Как уже отмечалось, у лиц, страдающих частыми инфекционными заболеваниями бронхолегочного аппарата, повышен титр антител к возбудителям этих заболеваний. Оказалось, что аффинность этих антител у значительной части больных существенно снижена. А низкоаффинные антитела малоэффективны в элиминации возбудителя из организма, и это может быть одной из причин хронизации инфекционного процесса. Можно привести много таких примеров. Во всех этих случаях клинически имеются отчетливые признаки нарушения иммунной системы, но они не всегда убедительно подтверждаются с помощью иммунолабораторных методов исследования.
Мы предлагаем рассматривать хронические, рецидивирующие, вялотекущие, трудно поддающиеся традиционному лечению инфекционно-воспалительные процессы самых различных локализаций, выявляемые у взрослых больных, как проявление вторичного иммунодефицитного состояния, вне зависимости от того, обнаружены или нет изменения в иммунной системе с помощью использованных в данной лаборатории тестов, т. е. рассматривать в данных случаях ВИД как чисто клиническое понятие. У нас нет никаких сомнений, что наличие хронического инфекционно-воспалительного процесса является следствием какой-то поломки в одном или нескольких компонентах иммунной системы, осуществляющих защиту организма от инфекции. И если эти поломки не выявлены, то это могло быть, как только что указывалось, следствием неадекватного методического подхода, использования неадекватного материала для исследования или невозможности идентифицировать имеющуюся поломку на данном этапе развития науки. Типичным примером последнего положения может служить LAD-синдром, заключающийся в нарушении экспрессии молекул адгезии на фагоцитарных клетках. Его обнаружение стало возможным только благодаря возникновению гибридомной технологиии и появлению моноклональных антител.
В то же время мы отдаем себе отчет в том, что в основе развития спонтанной формы ВИД должны лежать какие-то конкретные причины. Чтобы рассмотреть эти причины, уместно еще раз вспомнить, что иммунитет человека является сложной многокомпонентной системой и в защите организма от инфекции участвуют факторы как врожденной резистентности, так и приобретенного иммунитета. На ранних этапах развития инфекционного процесса — в первые 96 часов — защита организма от инфекционного агента осуществляется совокупностью неспецифических факторов иммунитета, как-то: системой комплемента, белками острой фазы, монокинами, фагоцитами, естественными киллерами и т. д. Возможно, что дефект одной из этих систем может какое-то время не проявляться клинически в виде повышенной инфекционной заболеваемости, так как все другие компоненты иммунитета находятся в нормальном функциональном состоянии и компенсируют этот дефект. Однако происходящие со временем и под влиянием различных неблагоприятных факторов изменения в этих компенсаторных компонентах, пусть даже не очень значительные, могут давать кумулятивный эффект, ведущий к фенотипическому проявлению первичного дефекта и развитию повышенной заболеваемости. Можно предположить, что в основе многих, а может быть практически и всех клинических форм ВИД, проявляющихся у взрослых в виде повышенной инфекционной заболеваемости, лежит первичная иммунологическая недостаточность какого-то компонента иммунной системы, скомпенсированная до определенного времени за счет нормальной или высокой функциональной активности других компонентов этой системы. Подтверждением такой возможности может служить общая вариабельная иммунная недостаточность (ОВИН), чаще всего проявляющаяся в хронических, рецидивирующих инфекциях бронхолегочного аппарата и придаточных пазух носа. Для этого заболевания является характерным понижение уровня всех классов иммуноглобулинов. У ОВИН имеется два пика: первый пик развивается между 6-10 годами, второй — между 26-30 годами, причем до развития заболевания эти больные являются практически здоровыми людьми. Имеется немало доказательств того, что дефект гуморального иммунитета у больных ОВИН имеет генетическое происхождение. Следовательно, этот дефект до определенного времени был компенсирован за счет нормальной или повышенной функциональной активности других компонентов иммунной системы, обеспечивающих защиту организма от инфекции. Помимо ОВИН имеется ряд болезней, относящихся к ПИД, но иногда проявляющихся клинически во взрослом возрасте. К ним относятся селективный IgA-дефицит, дефицит субклассов IgG, дефицит системы комплемента. Описаны случаи первичного проявления у взрослых форм ПИД, типичных только для детского возраста. К ним относятся дефицит аденозиндезаминазы, синдром Вискотта-Олдрича, X-сцепленная агаммаглобулинемия. Как правило, в этих случаях отсроченное наступление симптомов заболевания является результатом наличия у данного индивидуума умеренного генетического дефекта. Но нельзя исключить и компенсаторной коррекции первичного дефекта за счет других компонентов иммунитета. Их изменение со временем и позволяет клинически проявиться первичному, пусть даже легкому дефекту иммунной системы.
Иммуномодулирующая терапия является неэффективной или малоэффективной при ПИД. Основные методы их лечения — это антимикробная и заместительная терапия. За рубежом применяется реконструктивная терапия, заключающаяся в пересадке больным детям костного мозга. Также интенсивно разрабатываются методы генной терапии.
Применение иммуномодуляторов более оправданно и целесообразно при ВИД. Назначение последних должно всегда проводиться на основании клинического и иммунологического обследования. В зависимости от результатов этого обследования можно выделить две группы людей:
Главным критерием при назначении иммуномодуляторов является клиническая картина. Иммуномодуляторы можно (или целесообразно) использовать в комплексной терапии больных как первой, так и второй групп. Возникает вопрос, какие конкретно иммуномодуляторы следует назначать при наличии признаков ВИД? Особенно остро этот вопрос встает у больных без выявленных отклонений в иммунной системе. Для того чтобы ответить на этот вопрос, следует кратко разобрать основные механизмы антиинфекционной защиты, так как основным проявлением иммунодефицитов, как уже отмечалось, является повышенная инфекционная заболеваемость. Первоочередная цель применения иммуномодуляторов у больных с признаками ВИД — это повышение антиинфекционной резистентности организма.
Условно все микроорганизмы можно разделить на внеклеточные и внутриклеточные. Главными эффекторными клетками в борьбе с внеклеточными возбудителями являются нейтрофилы. Их поглотительная и бактерицидная функции резко усиливаются в присутствии комплемента и IgG, а также при их активации фактором некроза опухолей — (ФНО), интерлейкином-1 (ИЛ), ИЛ-6 и другими цитокинами, продуцируемыми макрофагами, NK-клетками и Т-лимфоцитами. Главными эффекторными клетками в борьбе с внутриклеточными возбудителями являются макрофаги, NK-клетки и Т-лимфоциты. Их микробоцидные и цитотоксические свойства резко повышаются под влиянием интерферонов, ФНО, и других цитокинов, продуцируемых после активации антигенами возбудителя этих же трех популяций клеток. Первой клеткой, с которой встречается возбудитель, преодолевший слизистые или кожные покровы, является тканевой макрофаг. Макрофаг, захвативший микроб, активируется и синтезирует ряд монокинов, которые повышают функциональную активность новых моноцитов/макрофагов, нейтрофилов и NK-клеток. Этот макрофаг, расщепив с помощью своей ферментной системы микроб, представляет его антигенные детерминанты Т- и В-лимфоцитам, инициируя тем самым развитие гуморального и клеточного ответов и продуцируя некоторые цитокины, необходимые для их развития.
На основании анализа этой упрощенной схемы антиинфекционной защиты (см. рисунок) можно сделать вывод, что для ее стимуляции наиболее целесообразным является применение таких иммуномодуляторов, которые преимущественно действуют на клетки моноцитарно-макрофагальной системы (ММС). При активации этой системы приводится в движение вся совокупность специфических и неспецифических факторов защиты организма от инфекции. Ранее все иммуномодуляторы мы разбили на три группы: экзогенные, эндогенные и химически чистые или полимерные. Препараты, оказывающие преимущественное воздействие на клетки ММС, имеются во всех этих трех группах иммуномодуляторов. К высокоэффективным лечебным средствам последнего поколения с преимущественным воздействием на клетки ММС относятся полиоксидоний, ликопид, миелопид, его фракция МП-3.
Подводя итог вышесказанному, мы считаем, что использование иммуномодуляторов в комплексе с другими лекарственными средствами поможет врачам-иммунологам более эффективно лечить больных с признаками ВИД.
Об иммунодефиците в целом
Сущность любого иммунного ответа заключается в распознавании и элиминации из организма чужеродных веществ антигенной природы, как экзогенно проникающих (микроорганизмы), так и эндогенно образующихся (вирусинфицированные клетки, клетки, модифицированные ксенобиотиками, старением, опухолевые клетки и др.). Защита организма от чужеродных веществ осуществляется гуморальными и клеточными факторами врожденного и приобретенного иммунитета, которые составляют единый функциональный комплекс, дополняя друг друга и находясь в постоянном контакте и взаимодействии.
В функционировании иммунной системы, как и в любой другой системе организма, могут возникнуть нарушения, которые ведут к развитию заболеваний, характерных, прежде всего, для этой системы. К таким нарушениям относятся [20]:
Обратите внимание!
Некоторые общие принципы иммунотерапии больных с признаками ВИД