впг герпес что такое
Что такое герпес простой? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
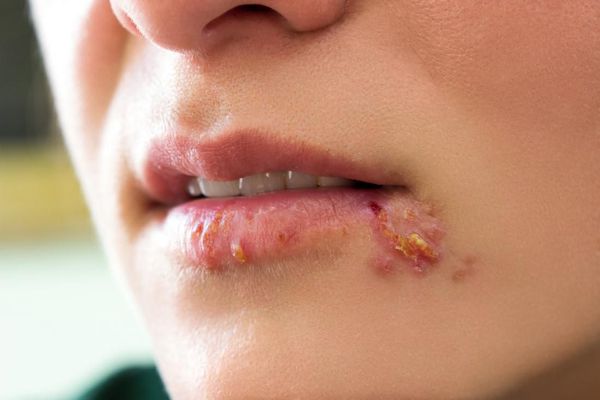
Простой герпес — это высококонтагиозное острое и хроническое инфекционное заболевание, при котором поражается кожа и слизистые оболочки. Его провоцируют вирусы простого герпеса I и II типов, вызывая типичную пузырьковую сыпь и изъязвления, как правило, локализованного характера. У людей с выраженным иммунодефицитом эти вирусы могут вызывать тяжёлые генерализованные формы болезни.
Заболевание входит в TORCH-комплекс, так как влияет на развитие плода: при первичном заражении или реактивации (реже) у беременных оно вызывает врождённую инфекцию.
Этиология
Семейство — Herpesviridae (от греч. herpes — ползучий)
Подсемейство — α-герпесвирусы (Alphaherpesvirinae)
Виды — вирус простого герпеса I, II (Herpes simplex virus I, II)
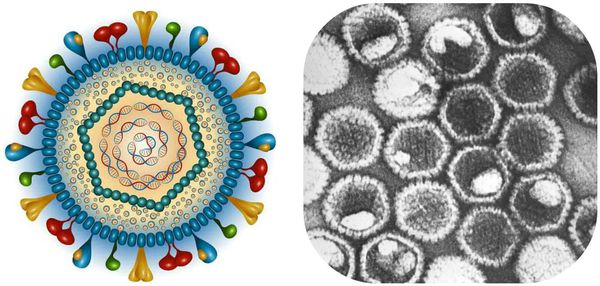
ДНК-содержащие вирусы. В их составе есть нуклеоид — вирусный геном-ДНК, который окружён капсидом сложного строения, покрытым оболочкой белково-липидного характера. Также вирусы содержат гликопротеиды gG1 и gG2, что позволяет провести серотипическое деление вируса герпеса на I и II тип.
Обладают специфической способностью прикрепляться к покровным тканям человека. Это сопровождается постоянной или периодической персистенцией — способностью к размножению в инфицированных клетках без проявлений патологического действия, т. е. простым неактивным носительством.
Эпидемиология
Данным вирусом инфицировано более 90 % населения планеты. После 30-40 лет им заражается почти 100 % людей, причём преимущественно I типом вируса.
Единожды инфицированный человек становится пожизненным носителем вируса одного или обоих типов. Данных об эпизодах самоизлечения нет.
В последнее время появились случаи носительства вируса простого герпеса с отсутствием специфических антител IgG к обоим типам вируса. Клиническое и эпидемиологическое значение этого феномена неизвестно. Возможно, такое явление перекрёстно связано с лицами, которые не поддаются заражению.
Источник инфекции — инфицированный человек. Он заразен в любую фазу болезни или носительства, но преимущественно при обострении.
Вирус может находиться в любой биологической жидкости организма — слюне, сперме, вагинальном секрете, отделяемом пузырьков и других.
Восприимчивость всеобщая. Риск заражения возрастает при травмировании кожи и слизистых оболочек здорового человека и попадании на них инфицированных биологических субстратов. Причём вирус может передаваться даже при отсутствии видимых поражений у инфицированного человека.
Большая часть случаев протекает в виде неактивного носительства. Как правило, первично человек приобретает I тип вируса простого герпеса (с детства), а II тип появляется в период половой зрелости. Однако всё относительно.
Основные способы передачи вируса:
В 20% случаев возможна обратная связь типов вирусов и способов их передачи.
Симптомы простого герпеса
Инкубационный период при приобретённой форме длится 2-14 дней. Чаще всего установить его не удаётся из-за отсутствия манифестации.
Простой герпес у детей обычно протекать по типу стоматита и гингивита — повышается температура, появляется лихорадка, общая интоксикация, очаговая гиперемия (покраснение) всех слизистых образований ротовой полости, болезненность при жевании, повышенное слюноотделение. Маленькие дети из-за болевых явлений отказываются от еды. В короткий промежуток времени на месте гиперемии появляются мелкие везикулярные высыпания, которые быстро вскрываются, оставляя после себя болезненные эрозии — афты. Увеличиваются и становятся болезненными регионарные лимфоузлы. С течением времени иммунитет укрепляется и симптомы постепенно регрессируют без каких-либо следов поражения. Рецидивы наблюдаются редко.
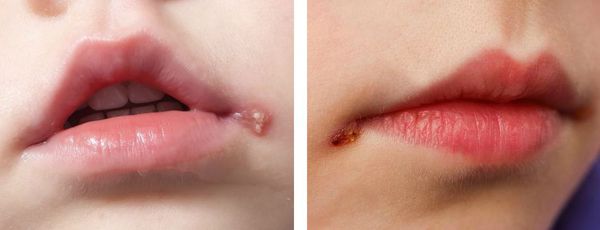
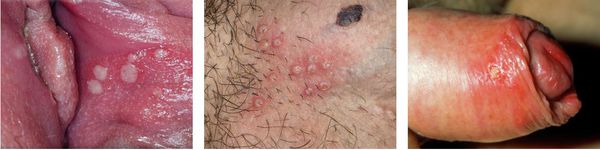
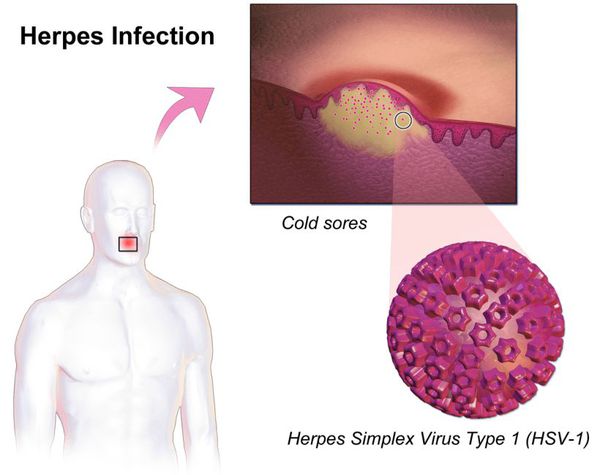
При поражении кожи (преимущественно у взрослых) везикулярные высыпания чаще появляются вокруг рта, крыльев носа, иногда на туловище и ягодицах. Сыпь представляет собой небольшие везикулы с серозным содержимым на слегка гиперемированном фоне кожи. Впоследствии они вскрываются и подсыхают, после чего образуются бесследно отпадающие корки.
Иногда пузырьки сливаются в достаточно большие пузыри. Нередко их содержимое нагнаивается, образуется мокнутий, и присоединяется вторичная стрептококковая или стафилококковая инфекция (стафило- и стрептодермии).
Общее самочувствие, как правило, не изменяется. Иногда может быть несколько увеличен и болезнен регионарный лимфоузел. В основном процесс редко продолжается более недели.
При серьёзных иммунодефицитах инфекция может принять более распространённое (генерализованное) течение. В таком случае возникает синдромом общей инфекционной интоксикации и затрагиваются внутренние органы: увеличивается печень и селезёнка, поражается нервная система (менингоэнцефалиты, энцефалиты и менингиты), а также лёгкие, почки и другие органы. При рецидивах хронической инфекции больные иногда ощущают слабый дискомфорт и пощипывание в области будущих высыпаний.
При генитальном герпесе высыпания появляются на коже и слизистых в области половых органов и промежности. Обычно они сопровождаются болезненностью, гиперемией окружающей ткани, увеличением и болезненностью паховых лимфоузлов. Частота рецидивирования зависит от индивидуальных особенностей иммунной системы.
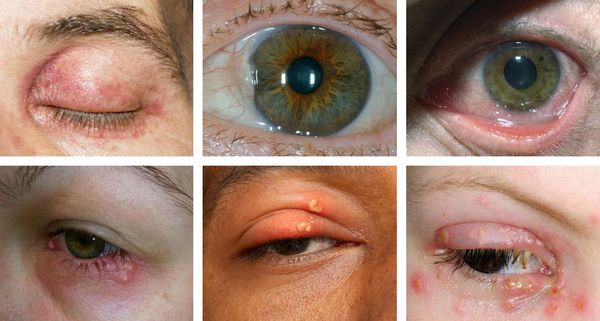
При офтальмогерпесе — герпесе глаз — чаще наблюдаются односторонние поражения из-за перехода первичного процесса на орган зрения, т. е. происходит вторичное поражение. Могут наблюдаться кератиты, блефароконъюнктивиты, иридоциклиты, увеиты, хориоретиниты, невриты зрительного нерва и другие проявления.
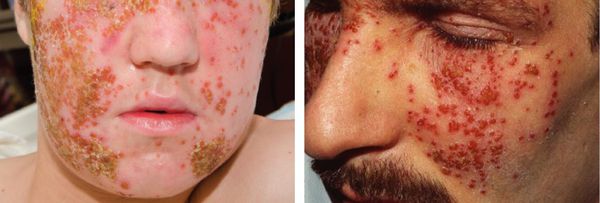
Весьма необычной является форма проявления простого герпеса, известная под названием герпетиформная экзема Капоши — герпетическая экзема. Как правило, она возникает у лиц, имеющих какое-либо кожное заболевание или предрасположенность к нему (дерматоз или «проблемная кожа»). При этом наблюдается интоксикация и высокая температура тела, повсеместно появляются герпетические пузырьки, достаточно обильные и близко расположенные, периодически сливающиеся, иногда с геморрагической пропиткой. В некоторых случаях происходит их нагноение, далее они вскрываются, подсыхают и образуют сплошную корку. При тотальной обработке высыпаний зелёнкой кожа больного приобретает вид кожи крокодила. Заболевание нередко протекает достаточно тяжело, может привести к летальному исходу.
При беременности инфицирование ребёнка происходит:
При первичном инфицировании беременной в первый триместр или при восходящем инфицировании плода зачастую развиваются пороки развития, несовместимые с жизнью, или происходит выкидыш, особенно при заражении II типом вируса герпеса, который является инфицирующим агентом чаще всего — до 80 % случаев.
Патогенез простого герпеса
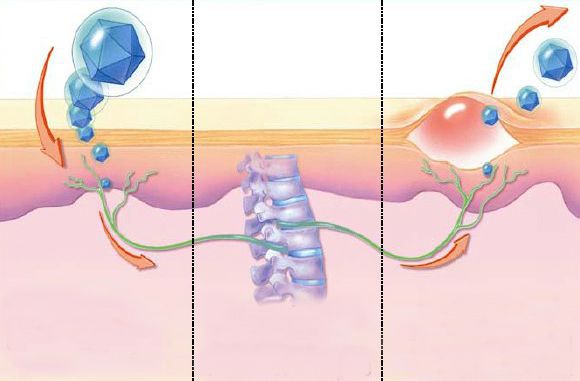
Ворота инфекции — повреждённая кожа и слизистые оболочки.
Вирус прикрепляется к поверхности клетки эпителия, проникает в неё и начинает размножаться. Это может привести к гибели самой клетки, а при массивном процессе — к явным воспалительным процессам, появлению характерной гиперемии, везикулёзных высыпаний и попаданию вируса в кровь и лимфу. В крови вирус обнаруживается на поверхности эритроцитов, лимфоцитов, тромбоцитов. В этот период вирус может попасть в различные органы и ткани, в т. ч. передаться плоду при первичном заражении матери во время беременности.
Вирус простого герпеса инфицирует чувствительные нервные окончания, паравертебральные нервные ганглии. Оттуда может произойти нейрогенное распространение вируса до кожи, в связи с чем появляются новые высыпания. Они далёки от места первичного внедрения:
Если иммунная система адекватна, то вирус исчезает из органов и тканей, но при этом пожизненно сохраняется в чувствительных нервных волокнах. Там он может передаваться из клетки в клетку, минуя межклеточное пространство, и в итоге оказывается недоступным для противодействия иммунной системы – т. н. «иммунное ускользание». После этого вирус может более никогда не иметь манифестных проявлений, но при иммунных нарушениях — Т-клеточном иммунодефиците, нарушении продукции интерферона и работы макрофагов — возможна его реактивация, гиперразмножение, выход из нейросенсорных депо и вновь поражение кожи и слизистых оболочек.
Предрасполагающими факторами реактивации вируса могут являться:
Одну из ключевых ролей в появлении симптомов простого герпеса играют макрофаги. Они «позволяют» или «не позволяют» осуществлять размножение вируса внутри себя (т. н. пермиссивность). В первом варианте развивается инфекция с выраженными симптомами, во втором — субклиническая картина заболевания.
Особую роль играет повышение чувствительности организма антигенами вируса. Оно проявляется в развитии местных аллергических реакций замедленного типа в местах высыпаний. При СПИДе данная реактивация приобретает генерализованный вторичный характер с поражением большинства внутренних органов — головного мозга, печени, лёгких, почек и других.
Классификация и стадии развития простого герпеса
В МКБ-10 (Международной классификации болезней) выделяют на две группы, связанных с вирусом простого герпеса:
По степени тяжести простой герпес бывает:
По форме возникновения заболевания различают:
По форме и распространённости инфекции выделяют четыре стадии простого герпеса:
По клинической картине и локализации высыпаний различают две формы простого герпеса:
Осложнения простого герпеса
Диагностика простого герпеса
Лабораторная диагностика:
Дифференциальная диагностика:
Лечение простого герпеса
Больные с осложнёнными формами простого герпеса подлежат госпитализации в инфекционный стационар. Остальные пациенты при отсутствии серьёзных сопутствующих состояний могут лечиться на дому амбулаторно.
Существует две стратегии этиотропного лечения:
Применение средств местного действия в виде мазей и кремов имеет ограниченный малоэффективный результат.
Высокоэффективное этиотропное лечение вполне может быть дополнено средствами повышения иммунной защиты организма (при наличии резервов организма) и витаминотерапией.
Прогноз. Профилактика
При неосложнённых формах болезни прогноз благоприятный, при генерализованных или формах с поражением ЦНС — серьёзный, возможен летальный исход или инвалидизация.
Важное значение в профилактике развития манифестной инфекции имеет ведение здорового образа жизни, правильное питание, предупреждение и лечение сопутствующих заболеваний, избегание переохлаждений и стрессов.
Специальных ограничительных мероприятий при заболевании не проводят. Больного следует обеспечить индивидуальной посудой, не допускать поцелуев с неинфицированными людьми.
При генитальном герпесе высокоэффективным мероприятием является использование презерватива. Определённое снижение риска распространения инфекции даёт регулярный приём противогерпетических средств уже инфицированным людям.
Если у беременной выявлен генитальный герпес при наличии частых рецидивов, высокой вирусной нагрузке области гениталий и родовых путей, то пациентке показан профилактический приём противогерпетических средств, начиная с 36 недели беременности и до родов (если планируются естественные роды). Или же выполняется плановое кесарево сечение.
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
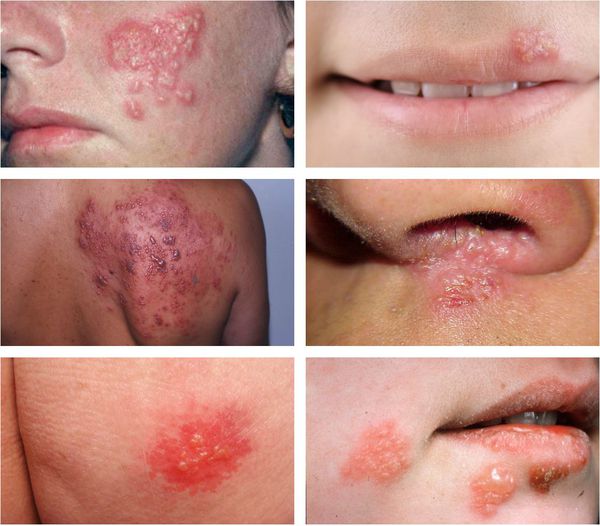
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
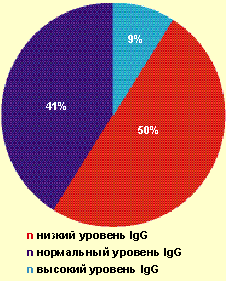 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
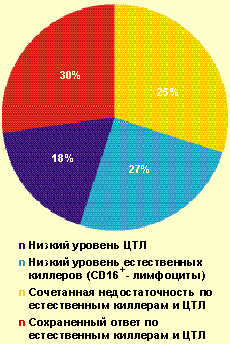 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва