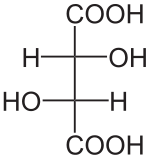
винная кислота l и dl в чем отличие
Виноградная кислота
Продажа
Как профессиональный поставщик химических реагентов, АО «Реахим» поставляет виноградную кислоту чистую на самых выгодных условиях. Если у Вас есть какие-либо вопросы или Вы хотите оформить заказ, оставьте свои контактные данные в форме. Мы свяжемся с Вами для уточнения цены на виноградную кислоту, времени и объема доставки.
Общее определение
Виноградная кислота – смесь 1:1 L-винной и D-винной кислоты. Слабая кислота, имеет вид бесцветных кристаллов или белого кристаллического порошка. Не имеет запаха и кислая на вкус.
Применение
DL-винная кислота широко применяется в качестве регулятора кислотности в пищевых продуктах и напитках, в том числе:
Помимо регулятора кислотности, используется как хелатирующий агент, синергист композитного разрыхлителя.
Получение
Есть несколько способов получения виноградной кислоты, один из них – способ, благодаря которому она стала известна: рацемизация винной кислоты.
Так же можно получить кислоту в результате реакции окисления фумаровой кислоты H4C4O4 (для этого применяется KMnO4 – перманганат калия) или восстановления глиоксиловой кислоты C2H2O3.
Идентификация
Название: Виноградная кислота / DL-Tartaric Acid
Синонимы: dl-винная кислота / (±)-tartaric acid; 2,3-dihydroxybutanedioic acid; 2,3-dihydroxysuccinic acid
Формула: С4H6О6
ТУ 6-09-3938-84
CAS: 133-37-9 / 138508-61-9
Физические данные
Физическое состояние: твердое
Цвет: без цвета, белый
Форма: кристаллы, кристаллический порошок
Запах: без запаха
Молекулярная масса: 150.09
Температура кипения: 399.3°С при 760 мм рт.ст.
Температура плавления: 200-206ºС с разложением при быстром нагревании в герметичной капиллярной трубке
Плотность: 1.886 г/см 3
pH 5% водного раствора: 2
Содержание сульфатов: не более 0.048%
Растворимость: легко растворяется в воде (133 г на 100 мл при 20ºС), умеренно растворяется в этаноле
Чистота: не ниже 99.5%
Пожар и взрыв
Температура вспышки: 210ºС
При высокой температуре виноградная кислота может быть горючей, для тушения пожара применяется распылитель воды, сухая химия или диоксид углерода.
Влияние на организм
Виноградная кислота не классифицируется как опасное вещество, однако при попадании в глаза может привести к повреждению роговицы или слепоте. На коже вызывает раздражение, покраснение, боль и даже волдыри, при проглатывании вызывает сильное раздражение желудочно-кишечного тракта.
Агрессивных побочных эффектов на организм виноградная кислота не оказывает, но повышенное содержание ее может вызвать жажду, рвоту, понос, боли в животе, желудочно-кишечное воспаление.
Допустимое потребление виноградной кислоты: 0-30 мг/кг массы тела.
Стабильность
Стабильная кислота при нормальной температуре и давлении.
Опасные продукты разложения: оксиды углерода (CO, CO2).
Несовместимость: окислительные средства, восстановители, щелочи.
Разлив и очищение
Для сбора разлива виноградной кислоты используются средства индивидуальной защиты и соблюдая меры предосторожности. Материал собирается, затем помещается в подходящий чистый сухой контейнер и плотно закрывается для утилизации.
Не допускать разлива в окружающую среду.
Профилактика
Избегать попадания на кожу и в глаза, не вдыхать пыль.
При работе избегать образования пыли. Помещение должно быть оборудовано вентиляцией для предотвращения образования пыли.
Безопасность
Символ опасности: Xi – раздражающее.
Коды риска:
Коды безопасности:
Защитное оборудование и одежда
Защита включает респиратор NIOSH/MSHA или европейский стандарт EN 149, защитные очки или химические защитные очки, перчатки, одежду.
Хранение
Виноградная кислота должна храниться в прохладном и сухом месте, удаленно от сильного света и тепла, источников возгорания. Не хранить контейнера из-под реагента, не добавлять в кислоту воду.
Упаковка и транспортировка
Ограничений на транспортировку виноградной кислоты по морю, воздуху или суше нет.
Упаковка: 100 г / 500 г / 2,5 кг / 25 кг в комплексном пакете с полиэтиленовым пакетом.
Разделение винта и спидов на d и l изомеры
Anonymous
Разделение винта и спидов на d и l изомеры
Anonymous
Я почитал, спасибо! И другим советую. Верить, конечно, нужно с оглядкой, но что-то здесь не чисто, с этими изомерами.
На Хае я тоже не зарегистрирован, и вряд ли смогу взять пропись, как они делали.
Я вот на это давно уже смотрю (это из британского патента 508757):
85 parts of racemic methamphetamine are introduced into a solution of 100 parts of d-tartaric acid in 1000 parts of methyl alcohol. After protracted standing about 100 parts of the precipitated salt are aspirated off and extracted with hot ethyl alcohol. Since the d-tartrate of dextrorotary methamphetamine is readily soluble in both methyl and ethyl alcohol whereas the d-tartrate of levorotary methamphetamine is sparingly soluble both in methyl alcohol and hot ethyl alcohol an extremely simple separation of the d-tartrates of the optical antipodes of the base is effected.
Конкретно смущает кусок фразы про «and extracted with hot ethyl alcohol». Откуда extracted? А конкретно радует про растворимость.
Все, l-изомер на руках. Дальше выпарить спирт до порошка или густой массы, перетереть с эфиром, отфильтровать. Это будет d-изомер.
Anonymous
«. «ПАРУ СТРОК О РАЗДЕЛЕНИИ РАЦЕМАТОВ ВИТАМИНОВ»
P.S. Надеюсь Гарин не обидится, что я выложил его процедуру здесь. Я просто считаю, что статья очень интересная. «
ЗЫ от меня: Выложено без изменений. Надеюсь автор не против, т.к. инф. общедоступна