валидация и верификация в лаборатории что это простыми словами
Такие слова, как «верификация» и «валидация», довольно часто можно услышать в различных телепередачах, но мало кто из людей знает, что они означают. Их звучание довольно сходное, и те, кто произносят эти слова, часто сами путаются в них. Из контекста слушатель догадывается, что дело и там, и там связано с проверкой чего-то. Что же в действительности означают эти слова, что у них общего и чем отличается валидация от верификации?
Происхождение термина
Философский и научный термин «верификация» пришел в наш язык из латыни (от лат. verus — «истинный», и facere — «делать»). Он означает проверку какого-либо предположения на соответствие заранее сформулированным требованиям, стандартам или спецификациям. Содержание термина существенно меняется в зависимости от контекста.
Верификация в науке
Для этого проводятся серии натурных или мысленных экспериментов, и если их результаты подтверждают гипотезу, она считается верифицированной и становится научной концепцией или даже теорией.
Верификация на производстве товаров и в предоставлении услуг
Наиболее широко процесс начал использоваться при производстве программного обеспечения и разработке сложных технических систем. Из этих отраслей метод распространился и в другие отрасли.
Подтверждение на основе представления объективных свидетельств того, что установленные требования были выполнены. (ИСО 9000:2000)
Производственная верификация заключается в сборе документальных доказательств того, что проектируемый и производимый продукт (или услуга) соответствует всем требованиям технического задания, производственных спецификаций и стандартов отрасли на каждом этапе производственного цикла. В случае сложных и продолжительных производственных процессов важно не откладывать сбор таких свидетельств на ночь перед отгрузкой продукции.
В производстве сложных систем и программных продуктов применяют следующие методы верификации:
Тестирование и анализ документов представляют собой наиболее широко и часто используемые подходы. Сопоставление научно-технической и проектной документации также весьма популярно, однако для многих передовых разработок трудно подобрать аналогичный проект.
Проведение альтернативных расчетов по независимому алгоритму позволяет получить базу для оценки точности расчетов, выполненных по проверяемому алгоритму. Один из наиболее часто используемых способов альтернативных расчетов – это калькулятор.
Верификация субъекта услуги
В этом случае происходит идентификация личности пользователя, какого-либо сетевого сервиса, например Twitter. В данном случае это означает проверку подлинности пользователя и подтверждения его личности. Аналогичные идентификации проводят и другие социальные медиа, сетевые торговые площадки и платежные системы.
Верификация заемщика в банке заключается не только в установлении его личности, но и в проверке его соответствия требованиям банка к пользователю данного продукта, таких как:
В русскоязычных медиа термин иногда используется в значении «проверка публикуемых фактов». Это чисто русский новояз, весь мир пользуется простым термином “fact cheking”, или «проверка фактов».
Валидация
Валидация на транспорте
Валидатором (от англ. valid – «действительный, правомерный») называют также специальное приспособление, с помощью которого проводят проверку электронных проездных документов. Таким образом определяют правомочность посадки пассажира в салон общественного транспорта. Часто валидатор совмещают с турникетом. Это позволяет экономить значительные средства на организации и проведении контроля оплаты проезда пассажирами. Применяют такие устройства также и для контроля прохода сотрудников на территорию предприятия.
Валидация в системе управления качеством
Формулировка в стандарте ИСО несколько невнятная и слишком похожа на определение «верификации».
«Валидация — подтверждение на основе представления объективных свидетельств того, что требования, предназначенные для конкретного использования или применения, выполнены».
Основное отличие
В чем основное отличие верификации и валидации?
Верификация – обязательный внутренний процесс проверки изделия или услуги на соответствие стандартам и спецификациям.
«-К пуговицам претензии есть?
-К лацканам претензии есть?
К рукавам претензии есть?
«-Костюм можно носить?
Основная задача верификации и валидации
Основная задача верификации состоит в том, что она подтверждает тот факт, что удалось произвести правильный продукт, абстрактно соответствующий всем утвержденным стандартам и спецификациям. Основная задача валидации заключается в том, чтобы подтвердить, что продукт может успешно использоваться конкретным потребителем в вот таких-то конкретных условиях.
Верификация проводится всегда, а вот валидация может и не проводиться.
Примеры верификации и валидации
Завод по производству лекарственных препаратов всегда будет проверять, соответствуют ли они техническим условиям и стандартам (верификация), а вот проверку, подойдут ли эти препараты определенному пациенту с таким-то набором симптомов, не будет (валидация).
Компания выпускает ботинки, предназначенные для загородных прогулок. Эти ботинки полностью соответствуют техническим условиям, и это проверяется для каждой пары (верификация). А вот подойдет ли эта обувь для высокогорных восхождений, предстоит определять отдельно (валидация).
Еще один пример, относящийся практически к любому предприятию. Отдел технического контроля осуществляет верификацию, а аудиторы проводят валидацию.
Верификация методик анализа
Что такое верификация?
Верификация [verification] – подтверждение лабораторией способности получать достоверные результаты (пригодные для решения конкретной задачи) по готовой валидированной методике
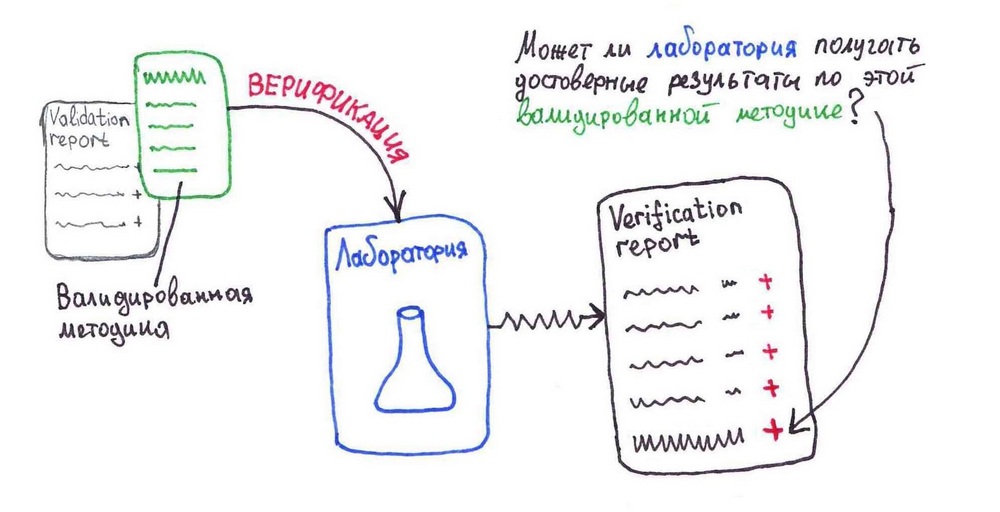
Отличие верификации от валидации
Валидация
доказываем, что МЕТОДИКА пригодна для решения конкретной аналитической задачи, т.е. позволяет получать достоверные результаты
Верификация
доказываем, что ЛАБОРАТОРИЯ в состоянии получить достоверные результаты по данной ВАЛИДИРОВАННОЙ методике
Из таблицы сразу видно, что лаборатория, которая проводила валидацию «автоматически» доказала достоверность результатов, получаемых в своей лаборатории (естественно, при успешной валидации)
Зачем делать верификацию?
Проведение верификации методик предусмотрено ISO 17025, ведущими фармакопеями и правилами GMP:
Лаборатория должна подтвердить, что она может правильно использовать стандартные методики, прежде чем приступить к испытаниям
п. 5.4.2 ГОСТ ИСО/МЭК 17025-2009
Лаборатория, которая использует методику испытаний и которая не выполняла ее первоначальную валидацию, должна верифицировать пригодность методики
Литература по верификации
Видео про верификацию (примеры)
Шаблон протокола верификации для химической лаборатории
Вопрос-ответ
Кто несет ответственность за верификацию? Ваш шаблон гарантирует что этого эксперимента достаточно?
Мы не аккредитованная лаборатория. Нам все равно надо делать верификацию?
Любая лаборатория, даже не аккредитованная, несет полную ответственность за выдаваемые результаты. Верификация позволяет убедиться самим, и подтвердить документально, что по данной методике лаборатория может выдавать достоверные результаты.
Верификация выгодна любому предприятию, т.к. существенно снижает риски получения недостоверных результатов, и позволяет выявить проблему на старте, а не через год работы.
Потери от недостоверных результатов анализа (выпуск некачественной и опасной продукции, работа технологов «впустую» и др.) обычно на порядки более существенны, чем затраты на организацию нормальной работы лаборатории.
Верификация гарантирует, что теперь у нас всегда будут достоверные результаты?
Чтобы быть уверенным что и дальше результаты выдаются достоверные, проводят контроль качества и множество других процедур.
В СССР никаких верификаций не делали, и нормально работали!
Делали. Только называлась это по другому: «внедрение методики», «постановка методики», «отработка методики». Эту процедуру, в соответствии современными международными рекомендациями, мы называем верификацией.
Вы гарантируйте, что к шаблону не будет вопросов?
Нет. Это просто пример-шаблон, чтобы доработать его под себя. Ответственность лежит на конкретной лаборатории.
По какому ГОСТу, нормативному документу составлен этот шаблон?
Шаблон составлен на основе нашего опыта внедрения методик, здравого смысла, с опорой на международные рекомендации Eurachem «A Laboratory Guide to Method Validation and Related Topics» и некоторые Российские документы из рекомендованного списка литературы.
А вот в ГОСТе, РМГ написано не так!
Любой ГОСТ в России доброволен к применению:
добровольность применения заинтересованным лицом документов в области стандартизации и обязательность соблюдения указанным лицом требований, содержащихся в этих документах, в случае объявления об их использовании, а также в случае определения обязательности исполнения требований стандартов в рамках контрактных (договорных) обязательств
Если лаборатория не обременена обязательствами, разумно опереться на Р 50.2.060, РМГ 76, РМГ 61, Eurachem «Laboratory guide to method validation» как на справочные документы, доработав шаблон под себя.
А почему не оценивается погрешность / неопределенность?
Шаблон содержит минимальный, наш взгляд, объем эксперимента, чтобы можно было убедиться в нормальной работе методики, и начать работать. Делать расчет неопределенности / погрешности на основе только 3 серий измерений на наш взгляд не совсем корректно.
Можно расширить объем эксперимента (количество серий), и рассчитать погрешность / неопределенность на основе оценок правильности и прецизионности (по ГОСТ Р ИСО 21748-2012, РМГ 61-2010, Р 50.2.060-2008, приложениям А и Б, РМГ 76-2014).
Кто утверждает критерии верификации? Где их брать?
Т.к верификации подвергаются только валидированные методики (для которых уже доказано, что методика позволяет получать результаты, пригодных для достоверного принятия управленческих решений по результатам анализа), разумно проверить выполнение базовых валидционных критериев (пусть в меньшем объеме): повторяемости, промежуточной прецзионности, правильности.
Для обоснования требований к верификационным критериям есть несколько подходов:
Валидация и верификация в лаборатории что это простыми словами
ГОСТ Р 56431-2015/
GHTF/SG3/N99-10:2004
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
СИСТЕМА МЕНЕДЖМЕНТА КАЧЕСТВА
Руководство по валидации процессов
Quality management system. Medical devices. Process validation guidance
Дата введения 2016-07-01
Предисловие
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью «МЕДИТЕСТ» (ООО «МЕДИТЕСТ») на основе собственного перевода на русский язык англоязычной версии документа, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 436 «Управление качеством медицинских изделий»
6 ПЕРЕИЗДАНИЕ. Март 2020 г.
Введение
«Системы менеджмента качества. Руководящие указания по валидации процессов» первоначально завершены в 1999 г. и переизданы под названием «GHTF/SG3/N99-10:2004 (издание 2)» после пересмотра из-за изменений в ИСО 13485, который применяют в некоторых регулирующих системах. Руководящие указания по валидации процессов были пересмотрены начиная с раздела 0 по 3.4, рисунок 1 и приложение В. Выполненный пересмотр можно разделить на две части: 1) редакционный пересмотр терминологии в соответствии с ИСО 13485 (т.е. термин «система качества» изменена на термин «система менеджмента качества», «управление проектированием» изменено на «управление проектированием и разработкой»); 2) изменения на рисунке 1 и далее по тексту для отражения новых требований по валидации процессов, установленных в 7.5.2 ИСО 13485.
Настоящий стандарт оказывает помощь изготовителям в понимании требований системы менеджмента качества в отношении валидации процессов и имеет общее отношение к процессам производства медицинских изделий (включая монтаж и обслуживание). В настоящем стандарте приведены общие предложения в отношении того, как изготовители могут подготовить и выполнить валидацию процессов.
Термин «валидация процесса» использован в области медицинских изделий для обозначения того, что процесс был подвергнут такому тщательному рассмотрению, что на практике обеспечен результат процесса (продукции, услуги или иного). Это существенно необходимо, если соблюдение предварительно установленных требований к продукции можно проверить только путем разрушающего контроля.
Несоответствия в процессах могут стать очевидными только после последующей обработки полуфабриката продукта или применения готовой продукции. Валидация процесса демонстрирует, что если процесс выполняют в установленных границах, то процесс производства продукции будет стабильным в соответствии с предварительно определенными требованиями (при проектировании и разработке).
Медицинская промышленность связана с широким спектром технологий и областей применения: начиная от простых инструментов до сложных хирургических установок с компьютерным управлением, от имплантируемых винтов до искусственных органов, от тест-полосок на наличие сахара в крови до диагностических систем и лабораторного испытательного оборудования. Эти изделия изготавливают в компаниях разного размера, структуры, объема производства, с использованием различных технологий и методов менеджмента. Эти факторы, особенно объем производства и количество технологических операций на единицу (например, этапов пайки или сварки), существенно влияют на то, как фактически применяется процесс валидации. С учетом такого разнообразия настоящий стандарт не предлагает подробных методов внедрения и поэтому не должен быть использован для оценки соответствия требованиям системы менеджмента качества. Настоящий стандарт предназначен для пояснения требований системы менеджмента качества посредством практических объяснений и примеров принципов валидации процессов. Изготовители могут и должны использовать настоящий стандарт по применению процессов валидации с учетом специфики технологии применительно к конкретной ситуации.
Настоящий стандарт дает общие предложения по тому, как изготовители могут подготовиться к валидации процессов и ее осуществлению. Отдельные регулирующие требования определяют ответственность изготовителей в отношении процессов, требующих валидации, и квалификации работников, задействованных в валидируемых процессах. Независимо от метода, используемого для валидации процесса, записи по всей деятельности при валидации и окончательный результат должны быть документированы.
Кроме того, что осуществление процесса валидации является обязательным требованием, изготовитель может валидировать процесс для улучшения качества в целом, устранения отходов, уменьшения затрат, повышения удовлетворенности потребителей или по другим причинам. В сочетании с должным управлением деятельности по проектированию и разработке валидированный процесс может привести к сокращению времени выпуска на рынок новой продукции.
Для управления многими процессами используют компьютеры. Несмотря на то что программные средства компьютеров могут считаться составной частью процесса, настоящий стандарт не охватывают валидацию программных средств.
Некоторые обязательные требования констатируют, что каждый процесс, который не может быть верифицирован последующим мониторингом или измерениями, должен быть валидирован. Настоящий стандарт предназначен для поддержки решений в отношении необходимости валидации.
1 Назначение и область применения
1.1 Назначение
Настоящий стандарт предназначен для содействия изготовителям в понимании требований системы менеджмента качества в отношении валидации процессов.
1.2 Область применения
Настоящий стандарт имеет общее отношение к производственным процессам (включая процессы монтажа и технического обслуживания) медицинских изделий. Специальные рекомендации для верификации выходных данных проектирования и валидации проекта включены в документы GHTF, касающиеся управления проектами.
2 Определения
В настоящем стандарте применимы следующие термины с соответствующими определениями. В отдельных стандартах могут встречаться термины, отличающиеся от приведенных.
2.1 установочная квалификация (installation qualification, IQ): Предоставление объективных свидетельств того, что все ключевые аспекты установки оборудования для процессов и вспомогательных систем соответствуют техническим требованиям изготовителя и что рекомендации поставщика оборудования должным образом учтены.
2.2 операционная квалификация (operational qualification, OQ): Предоставление объективных свидетельств того, что границы управления процессом и пределы выполняемых действий приводят к созданию продукции, удовлетворяющей всем установленным требованиям.
2.3 эксплуатационная квалификация (performance qualification, PQ): Предоставление объективных свидетельств того, что процесс при возможных условиях стабильно производит продукцию, которая удовлетворяет всем установленным требованиям.
2.4 валидация процесса (process validation): Предоставление объективных свидетельств того, что на выходе процесса стабильно получается результат или продукция, удовлетворяющие установленным требованиям.
2.5 протокол валидации процесса (process validation protocol): Документ, определяющий, как валидацию будут проводить, включая параметры испытаний, характеристики продукции, технологическое оборудование и контрольные точки, которые устанавливают приемлемые результаты испытаний.
2.6 верификация (verification:): Подтверждение на основании проверки и представления объективных свидетельств того, что установленные требования были выполнены.
3 Валидация процессов в рамках системы менеджмента качества
Валидация процессов является частью интегрированных требований системы менеджмента качества. Валидацию осуществляют в рамках системы, включающей управление проектированием и разработкой, управление процессами и корректирующие и предупреждающие действия.
Взаимосвязь управления проектированием и процесса разработки может быть очень тесной для некоторых технологий. Для других видов деятельности взаимосвязь может быть косвенной. Продукцию следует спроектировать продуманно, чтобы она выдерживала изменения технологического процесса, и применять воспроизводимый и стабильный технологический процесс для постоянного обеспечения безопасности продукции и функционирования надлежащим образом. Часто это приводит к интерактивным разработкам продукции и деятельности по процессам.
Ежедневную деятельность по мониторингу и измерению проводят в соответствии с планом управления процессом, который часто разрабатывают при валидации процесса.
Корректирующие действия часто выявляют недостаточную валидацию процесса/процессов. Во все корректирующие действия следует включать рассмотрение выполнения валидации и/или повторной валидации процессов.
3.1 Решение по валидации процессов
Модель, представленная на рисунке 1, может быть полезна для определения того, следует или нет валидировать процесс.
Приведенная модель описывает дерево принятия решения, которому изготовитель может следовать для принятия решения о необходимости валидации процесса. В этой модели рассмотрен самый простой процесс, однако многие реальные процессы могут быть более масштабными и/или состоять из совокупности подпроцессов.
Для каждого процесса следует установить технические требования, описывающие параметры процесса и требуемый результат. Изготовителю необходимо принять во внимание возможность верификации последующим мониторингом или измерениями результатов процесса А. При положительном ответе нужно убедиться, достаточна ли только верификация для исключения недопустимого риска и является ли решение рентабельным В. Если проведение верификации достаточно, то результат процесса следует верифицировать, а процессом следует управлять соответствующим образом С.
Если результат процесса нельзя верифицировать, то следует принять решение о валидации процесса D; альтернативой может стать перепроектирование продукции или процесса для уменьшения отклонений и улучшения продукции либо процесса Е. Изменение технологического процесса, кроме прочего, может привести к необходимости валидации процесса, даже если ранее для этого требовались только верификация и управление.
Риск или затраты могут быть также снижены путем изменения проекта (перепроектирование) продукции или процесса таким образом, что простая верификация окажется приемлемым решением Е.
3.2 Примеры
1 Процессы, которые следует валидировать:
— процессы, связанные с обеспечением чистоты помещений;
— процессы асептической расфасовки;
— процессы герметизации стерильных упаковок;
— процессы нанесения покрытий;
— процессы опрессовки пластмасс под давлением.
2 Процессы, которые могут быть удовлетворительно охвачены верификацией:
— процессы ручной резки;
— процессы проверки цвета, мутности, показателя рН для растворов;
— визуальный контроль печатных плат;
— процессы изготовления и испытания электропроводки.
3 Процессы, которые можно верифицировать, но для которых по коммерческим соображениям выбрана валидация:
— некоторые процессы очистки;
— некоторые процессы ручной сборки;
— процессы резки с программным управлением;
— некоторые процессы расфасовки.
Несмотря на то, что результат процесса может быть верифицирован, используемые компьютерные программные средства должны быть валидированы в отношении предназначенного применения.
Валидация и верификация в лаборатории что это простыми словами
ГОСТ Р ИСО 11064-7-2016
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ЭРГОНОМИЧЕСКОЕ ПРОЕКТИРОВАНИЕ ЦЕНТРОВ УПРАВЛЕНИЯ
Принципы верификации и валидации
Ergonomic design of control centres. Part 7. Principles for verification and validation
Дата введения 2017-12-01
Предисловие
1 ПОДГОТОВЛЕН Открытым акционерным обществом «Научно-исследовательский центр контроля и диагностики технических систем» (АО «НИЦ КД») на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 201 «Эргономика, психология труда и инженерная психология»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 2 ноября 2016 г. N 1583-ст
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5 (подраздел 3.5).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВЗАМЕН ГОСТ Р ИСО 11064-7-2010
6 ПЕРЕИЗДАНИЕ. Август 2019 г.
Введение
В настоящем стандарте установлены основные принципы, эргономические требования и рекомендации по проверке их выполнения для центров управления.
ISO 11064-1:2000 Эргономическое проектирование центров управления. Часть 1. Принципы проектирования центров управления (ISO 11064-1:2000 Ergonomic design of control centres. Part 1: Principles for the design of control centres).
ISO 11064-2:2000 Эргономическое проектирование центров управления. Часть 2. Принципы организации центров управления (ISO 11064-2:2000 Ergonomic design of control centres. Part 2: Principles for the arrangement of control suites).
ISO 11064-3:1999 Эргономическое проектирование центров управления. Часть 3. Расположение зала управления (ISO 11064-3:1999 Ergonomic design of control centres. Part 3: Control room layout).
Все стандарты серии ИСО 11064 обеспечивают выполнение общих принципов эргономического проектирования при изготовлении и обслуживании центров управления.
Настоящий стандарт будет полезен руководителям проектов, инженерам службы приемки, потребителям, поставщикам и регулирующим органам.
Пользователями настоящего стандарта являются также операторы центров управления и некоторые другие заинтересованные группы пользователей, потребности которых составляют основу эргономических требований, используемых разработчиками международных и национальных стандартов. Применение настоящего стандарта позволяет обеспечить пользователю условия работы, которые в наибольшей степени соответствуют его требованиям. Это способствует снижению количества ошибок и повышению производительности труда.
Применение настоящего стандарта особенно важно при выполнении проектов в области инжиниринга, поскольку способствует оптимальному применению верификации и валидации в процессе реализации проекта. Эффективная проверка выполнения основных эргономических требований и оперативная корректировка проекта позволяют сократить сроки разработки и внедрения нового проекта.
Общие рекомендации по инжинирингу центров управления приведены в приложении ДБ.
Международный стандарт, на основе которого подготовлен настоящий стандарт, разработан Техническим комитетом ISO/TC 159 «Эргономика».
1 Область применения
Применение требований настоящего стандарта очень важно при выполнении инжиниринговых разработок, связанных с созданием или модернизацией центров управления. Проверка эргономических принципов на ранних этапах разработки проекта позволяет сократить время проектирования и внедрения проекта.
Настоящий стандарт может быть применен ко всем типам центров управления, включая центры управления промышленными процессами, транспортными системами и диспетчерскими пунктами аварийных служб. Несмотря на то, что в настоящем стандарте рассмотрены в основном стационарные центры управления, многие приведенные принципы могут быть применены для мобильных центров управления, расположенных, например, на кораблях или на самолетах.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ISO 11064-1:2000, Ergonomic design of control centres: Part 1: Principles for the design of control centres (Эргономическое проектирование центров управления. Часть 1. Принципы проектирования центров управления)
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 процесс проверки (evaluation process): Действия всех видов верификации и валидации проекта, в том числе выбранные методы и регистрация полученных результатов.
3.2 индивидуальная модификация, HED (human engineering discrepancy, HED): Изменение некоторой общепринятой конструкции системы, учитывающее особенности действий или возможностей оператора и/или пользователя.
3.3 резолюция (заключение, выводы) (resolution): Решения по устранению несоответствий, выявленных в процессе проведения верификации и валидации.
3.4 осведомленность ситуации (situation awareness): Понимание оператором/пользователем фактического состояния управляемой системы и/или процесса в каждый момент времени.
3.5 достоверность (validity): Степень, с которой средство или методика измерений могут продемонстрировать способность измерять предназначенную величину.
3.6 валидация (validation): Подтверждение на основе объективных данных, что установленные требования в условиях намеченного использования или применения выполнены.
3.7 верификация (verification): Подтверждение на основе объективных данных, что установленные требования выполнены.
3.8 план верификации и валидации (V&V план) (verification and validation plan): План, специально разработанный для выполнения процедур проверки.
3.9 рабочая нагрузка (workload): Установленные требования к физической и ментальной нагрузке пользователей системы и/или обслуживающего персонала.
4 Требования и рекомендации по организации процесса верификации и валидации
В подразделах 4.1-4.10 представлены общие требования и рекомендации по проведению проверки эргономических требований. В приложении А приведен контрольный лист для проверки выполнения этих требований.
4.1 Основные требования к верификации и валидации
a) Верификация и валидация должны быть частью общего процесса проектирования в соответствии с ИСО 9241-210 и ИСО 11064-1 (см. рисунок 2).
b) Верификацию и валидацию следует проводить на всех этапах жизненного цикла проекта.
c) Испытания должны быть проведены на возможно более ранних этапах проектирования, чтобы можно было выполнить необходимые корректирующие действия.
Результаты предыдущих верификации и валидации могут быть повторно использованы в некоторых случаях. Окончательное решение о приемлемой форме проведения верификации и валидации должно быть индивидуальным в каждом конкретном случае. Дополнительная информация приведена в приложении В.
4.2 План верификации и валидации
a) План верификации и валидации должен быть подготовлен на ранних этапах проектирования до проведения верификации и валидации.