в вегетативной иннервации сердца преобладает симпатический компонент что это значит
В вегетативной иннервации сердца преобладает симпатический компонент что это значит
Возбуждение в вегетативной (автономной) нервной системе (ВНС) проводится к тканям и органам через периферические вегетативные ганглии. Нервные волокна, отходящие от расположенных в гипоталамусе и стволе мозга центров ВНС, образуют синапсы с расположенными в сером веществе ствола мозга и спинного мозга преганглионарными нейронами. Распространяясь далее,эти преимущественно миелинизированные преганглионарные нервные волокна покидают центральную нервную систему (ЦНС) и образуют синаптические соединения с мультиполярными нейронами в составе периферических вегетативных ганглиев. Немиелинизированные постганглионарные волокна обеспечивают иннервацию структур организма, образуя обширные сети (концевые сплетения).
Несмотря на то, что вегетативная нервная система (ВНС) анатомически и функционально состоит из симпатического и парасимпатического отделов, ее деятельность тесно связана с работой нейроэндокринной системы, а также с двигательной активностью организма. Большую часть ВНС сознание непосредственно не контролирует, однако ее деятельность тесно взаимосвязана с функционированием ЦНС (а именно, с работой корковых и подкорковых структур головного мозга).
а) Симпатическая нервная система. Симпатическая нервная система получила свое название из-за прямой зависимости ее деятельности от эмоций человека. В том случае, если человек испытывает гнев или страх, симпатическая система реагирует формированием реакции «борьбы или бегства», а при отсутствии угрозы для жизни — реакции «покоя и переваривания пищи». В момент физиологической реакции «борьбы или бегства» происходят учащение сердцебиения, расширение зрачков, повышение потоотделения. Кровь оттекает от кожи и желудочно-кишечного тракта (ЖКТ) и перенаправляется в скелетные мышцы, происходит закрытие сфинктеров пищеварительной и мочевыделительной систем.
Симпатическая иннервация — тораколюмбальная, так как тела преганлионарных нейронов этой системы расположены в сером веществе боковых рогов грудного (торакального) и двух (в некоторых случаях трех) верхних поясничных (люмбальных) сегментов спинного мозга. Аксоны этих нейронов выходят из спинного мозга в составе соответствующих передних корешков и затем направляются к ганглиям в составе паравертебральных симпатических стволов. Существует четыре анатомических варианта распространения преганглионарных нервных волокон.
1. Часть волокон образует синапсы с наиболее близко расположенными к ним ганглиями. Постганглионарные волокна возвращаются в состав спинномозговых нервов (двенадцати грудных и двух поясничных — T1-L2); функция этих волокон — симпатическая иннервация соответствующих кровеносных сосудов, потовых желез, а также пилоэректорных мышц (пучков гладкомышечных волокон волосяных фолликулов, поднимающих волосы).
2. Часть волокон распространяется вверх вдоль симпатических стволов и образует синапсы с верхним или средним шейными ганглиями либо со звездчатым (шейно-грудным) ганглием. (Звездчатый ганглий состоит из двух ганглиев — нижнего шейного и первого грудного; он расположен в передней части шеи над первым ребром.) Постганглионарные волокна отвечают за иннервацию головы, шеи, верхних конечностей и сердца. Важно отметить, что данные волокна также иннервируют мышцу, расширяющую зрачок.
3. Часть волокон распространяется вниз вдоль симпатических стволов и образует синапсы с расположенными в них поясничными или крестцовыми ганглиями. Постганглионарные волокна входят в состав пояснично-крестцового сплетения и осуществляют иннервацию кожи и кровеносных сосудов нижних конечностей.
4. Часть волокон остается преганглионарными, так как они проходят транзитом (не переключаясь, без образования синапсов) через симпатические стволы; эти волокна образуют грудные и поясничные внутренностные нервы. Грудные внутренностные нервы (обычно называемые внутренностными нервами) проходят транзитом через восемь нижних грудных ганглиев, прободают диафрагму и попадают брюшную полость, где образуют синапсы с чревным и брыжеечным превертебральными ганглиями, а также с почечными ганглиями.
По ходу ветвей аорты постганглионарные волокна достигают иннервируемых структур: ЖКТ, печени, поджелудочной железы и почек. Поясничные внутренностные нервы проходят транзитом через три верхних поясничных ганглия, встречаются перед бифуркацией брюшной аорты и в качестве подчревных нервов попадают в полость таза. Здесь они образуют синапсы с тазовыми ганглиями, отвечающими за иннервацию мочеполового тракта.
Онтогенетически мозговое вещество надпочечника развивается из нервного гребня. Вследствие этого его можно рассматривать как особый симпатический ганглий, получающий иннервацию от волокон в составе соответствующего грудного внутренностного нерва.
Симпатическая нервная система влияет на тонус гладких мышц кровеносных сосудов конечностей, вызывая их продолжительное сокращение (вазоконстрикцию). В связи с этим для восстановления нормального кровотока верхних или нижних конечностей осуществляют хирургическое прерывание симпатической иннервации соответствующей области.
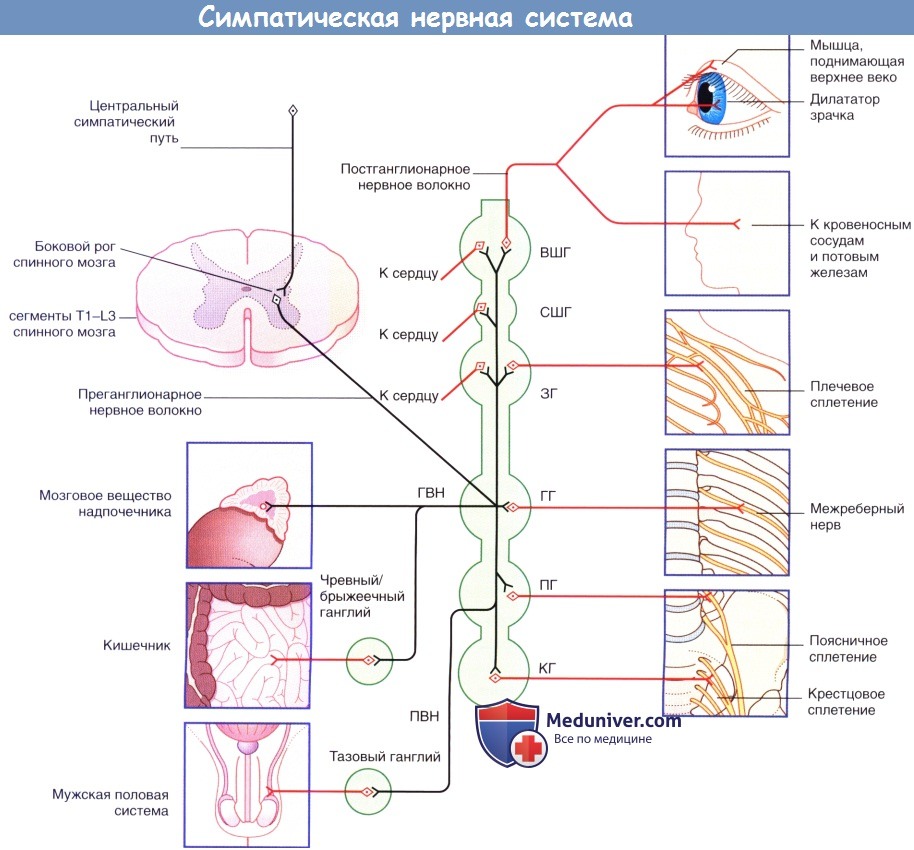
ПГ — поясничный ганглий; ПВП — поясничный внутренностный нерв; СШГ—средний шейный ганглий;
ВШГ—верхний шейный ганглий; КГ—крестцовые ганглии; ЗГ—звездчатый ганглий;
ГГ—грудные ганглии; ГВН—грудной внутренностный нерв.
б) Блокада звездчатого ганглия. Блокада звездчатого ганглия (введение в область ганглия местного анестетика) — процедура, которую применяют для оценки влияния прерывания симпатической иннервации на кровоснабжение верхней конечности. Инактивация в ходе процедуры как преганглионарных, так и постганглионарных нервных волокон приводит к ипсилатеральному симпатическому параличу верхней конечности, половины головы и шеи. Об успешности блокады звездчатого ганглия у пациента судят по:
(а) состоянию верхней конечности (должна быть сухой и теплой),
(б) наличию синдрома Горнера (сужение зрачка, происходящее за счет активации сфинктера зрачка и блокады иннервации его дилататора),
(в) наличию птоза (опущения) верхнего века на фоне паралича гладкомышечных волокон, входящих в состав мышцы, поднимающей верхнее веко.
Доказано, что правый звездчатый ганглий оказывает большее влияние на частоту сердечных сокращений, чем левый (при его блокаде происходит большее снижение пульса).
Кроме того, возможно осуществление функциональной симпатэктомии путем пересечения симпатического ствола ниже уровня звездчатого ганглия. Такая симпатэктомия не является анатомической, поскольку в ходе процедуры ганглионарная иннервация верхней конечности (иннервация от среднего шейного и звездчатого ганглиев) остается интактной. В то же время симпатэктомия ниже уровня звездчатого ганглия—функциональная, так как после нее ганглионарные нейроны, иннервирующие верхнюю конечность, лишаются симпатической импульсации. Пересечение симпатического ствола на уровне второго ребра позволяет избежать появления синдрома Горнера: преганглионарные волокна, иннервиру ющие голову и шею, направляются к звездчатому ганглию от первого грудного спинномозгового нерва.
Существуют два относительных показания к проведению односторонней или двухсторонней функциональной симпатэктомии: синдром Рейно (болезненное побледнение пальцев в ответ на воздействие низких температур) и гипергидроз (заболевание, проявляющееся в пубертатном периоде и характеризующееся избыточным потоотделением участков кожи с повышенным количеством потовых желез,—ладоней, ступней, паха).
Симпатическая иннервация глаза подробнее рассмотрена в отдельной статье на сайте.

Обратите внимание на умеренно выраженные птоз века и миоз (сужение зрачка).
На стороне синдрома сохранена (но замедлена) реакция суженного зрачка на свет.
в) Поясничная симпатэктомия. Ранее для лечения нейропатических болей и улучшения кровоснабжения нижней конечности применяли поясничную симпатэктомию (процедура, в ходе которой преганглионарную иннервацию прерывали путем хирургического пересечения верхнего конца поясничного симпатического ствола). При этом обычно иссекали второй и третий поясничные симпатические ганглии. Однако у мужчин билатеральная поясничная симпатэктомия приводит к нарушению нервных путей, отвечающих за неэрегированное состояние (состояние покоя) полового члена, что может привести к персистирующим болезненным эрекциям (приапизм).
В настоящее время существует недостаточно доказательств того, что поясничная симпатэктомия эффективна у большинства пациентов; в связи с этим процедуру проводят лишь в редких случаях. Для лечения резистентной к стандартной терапии артериальной гипертензии все чаще применяют абляцию симпатических нервов почечных артерий (эндоваскулярно через катетер).
Учебное видео анатомии вегетативной нервной системы (ВНС)
Редактор: Искандер Милевски. Дата публикации: 13.11.2018
В вегетативной иннервации сердца преобладает симпатический компонент что это значит
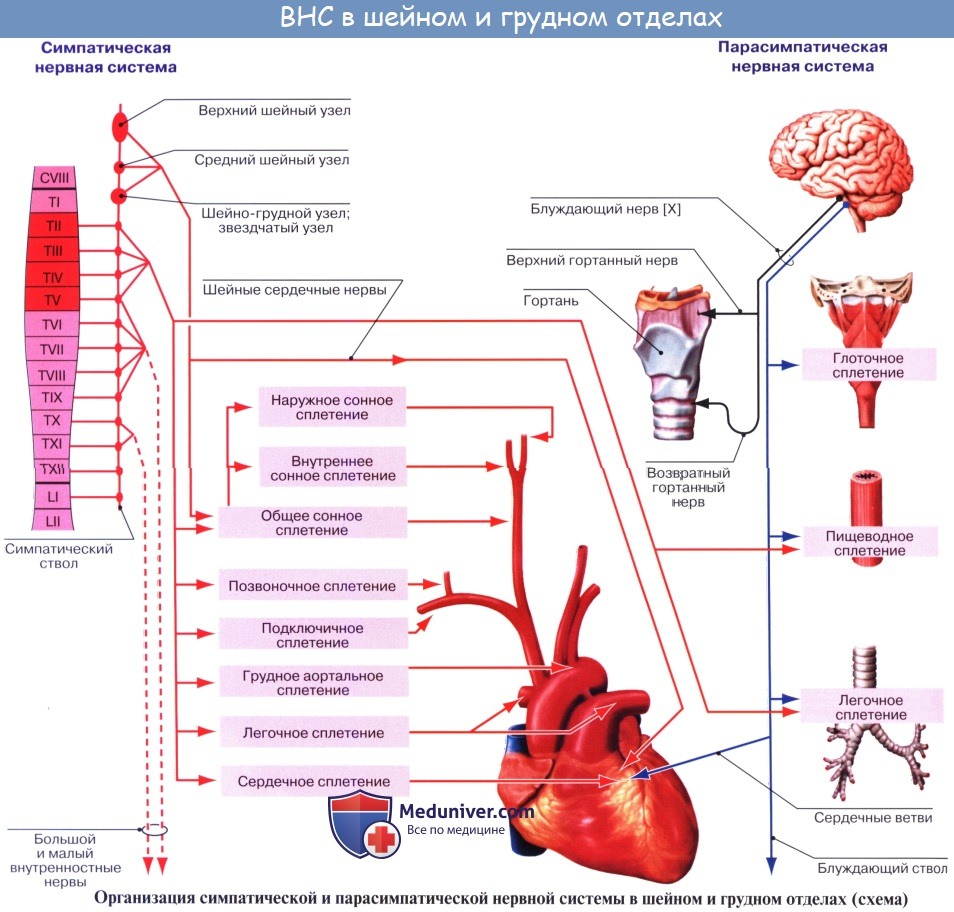
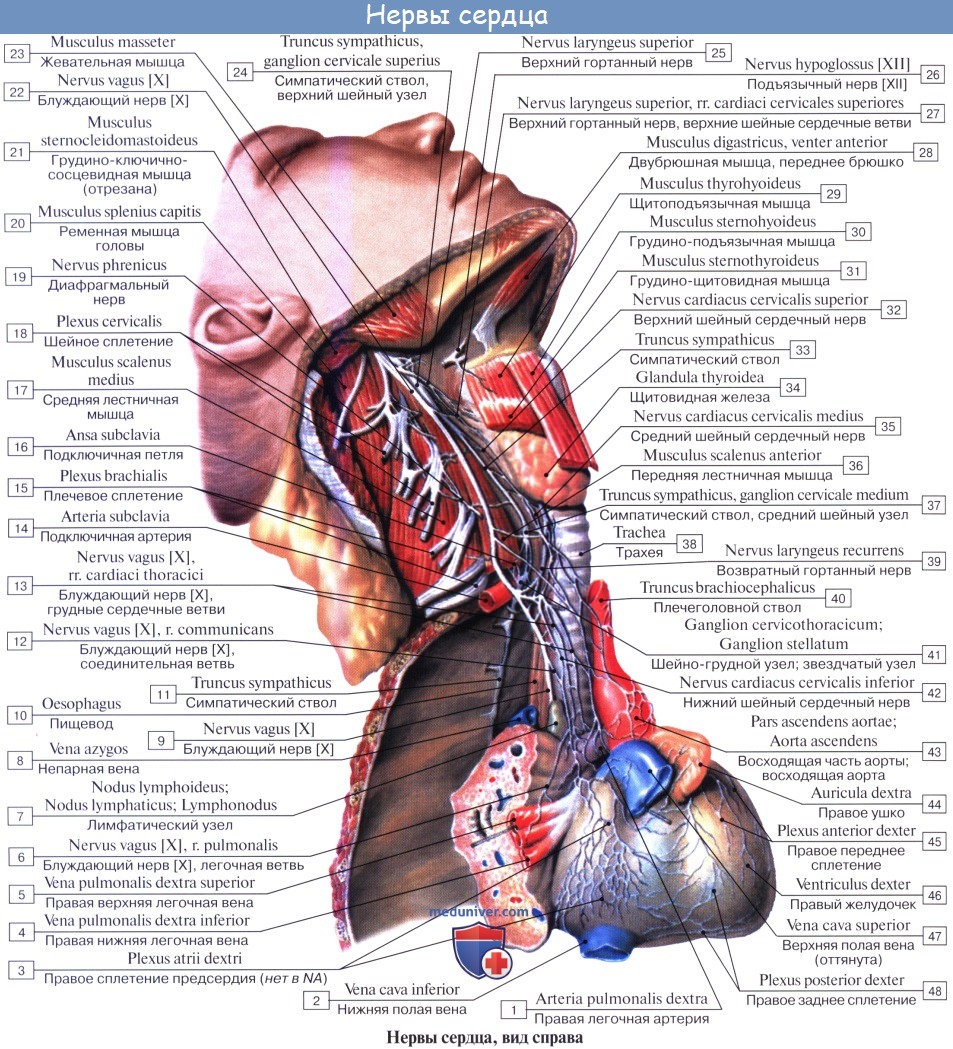
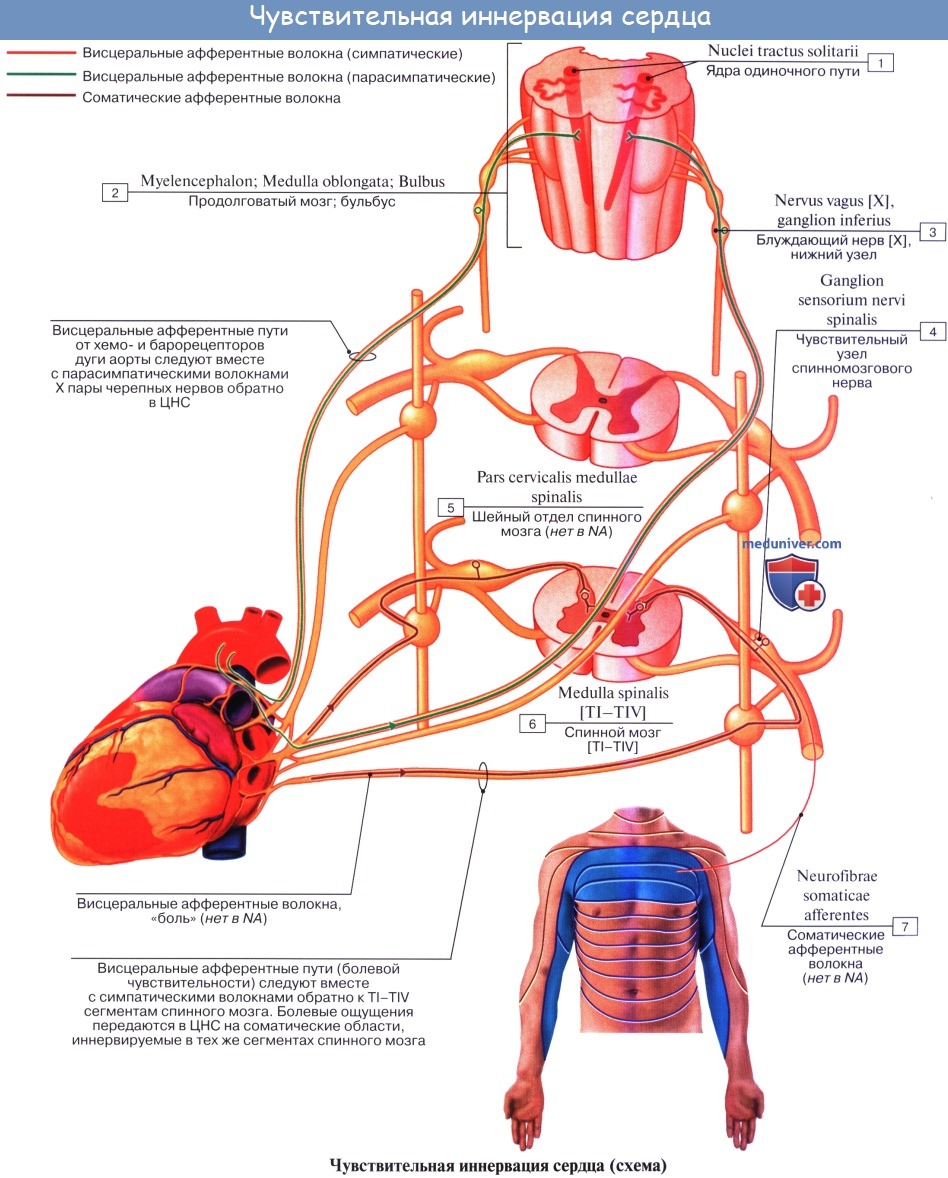
Афферентные пути от сердца идут в составе n. vagus, а также в среднем и нижнем шейных и грудных сердечных симпатических нервах. При этом по симпатическим нервам проводится чувство боли, а по парасимпатическим — все остальные афферентные импульсы.
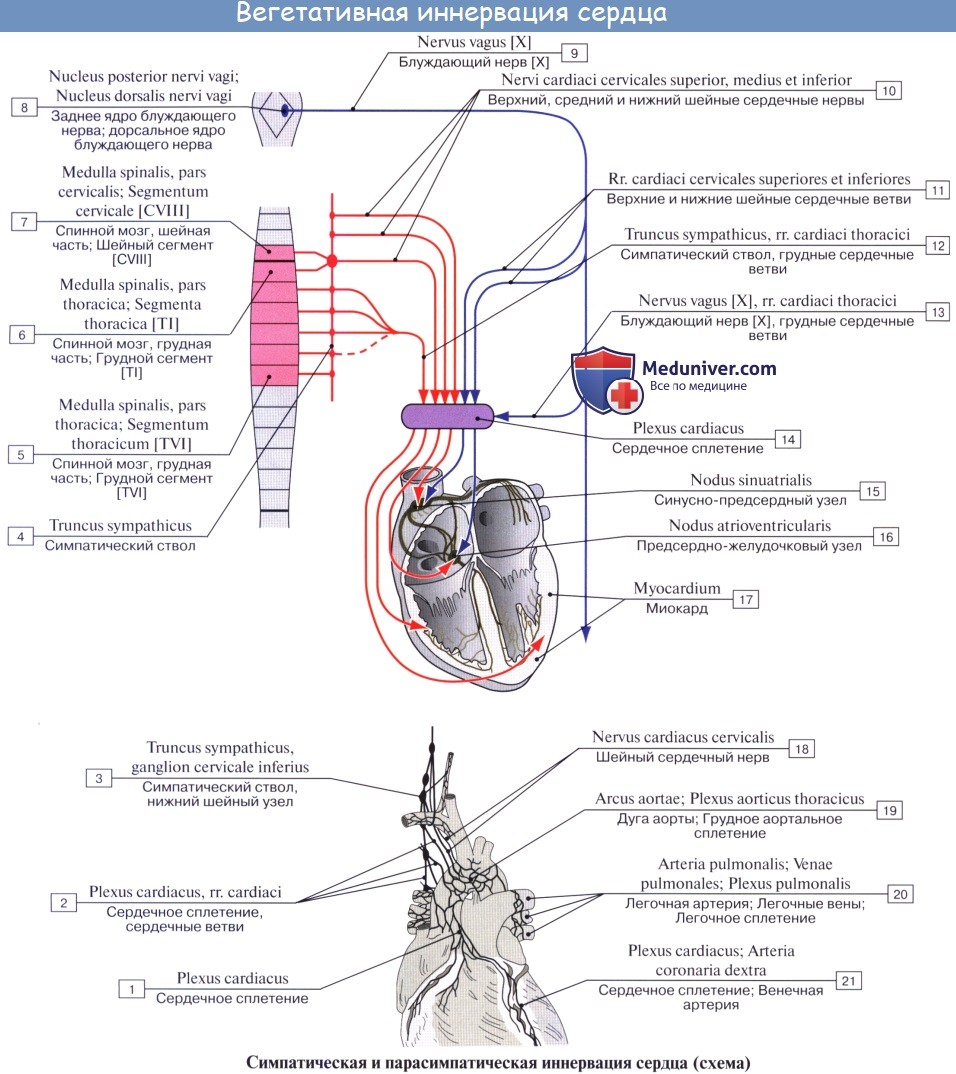
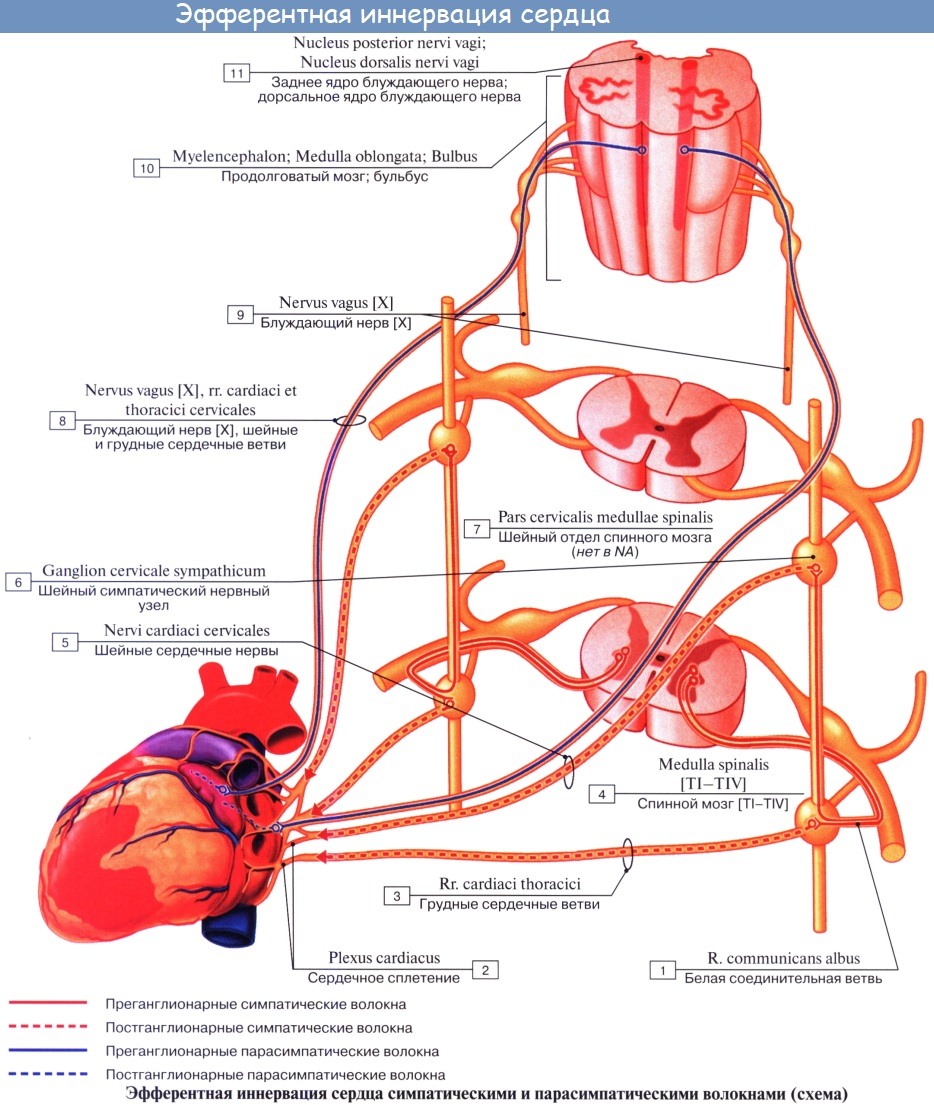
Эфферентная парасимпатическая иннервация. Преганглионарные волокна начинаются в дорсальном вегетативном ядре блуждающего нерва и идут в составе последнего, его сердечных ветвей (rami cardiaci n. vagi) и сердечных сплетений (см. иннервацию сердца) до внутренних узлов сердца, а также узлов околосердечных полей. Постганглионарные волокна исходят от этих узлов к мышце сердца.
Функция: торможение и угнетение деятельности сердца; сужение венечных артерий.
Функция: усиление работы сердца (это установил И. П. Павлов в 1888 г., назвав симпатический нерв усиливающим) и ускорение ритма (это впервые установил И. Ф. Цион в 1866 г.), расширение венечных сосудов.
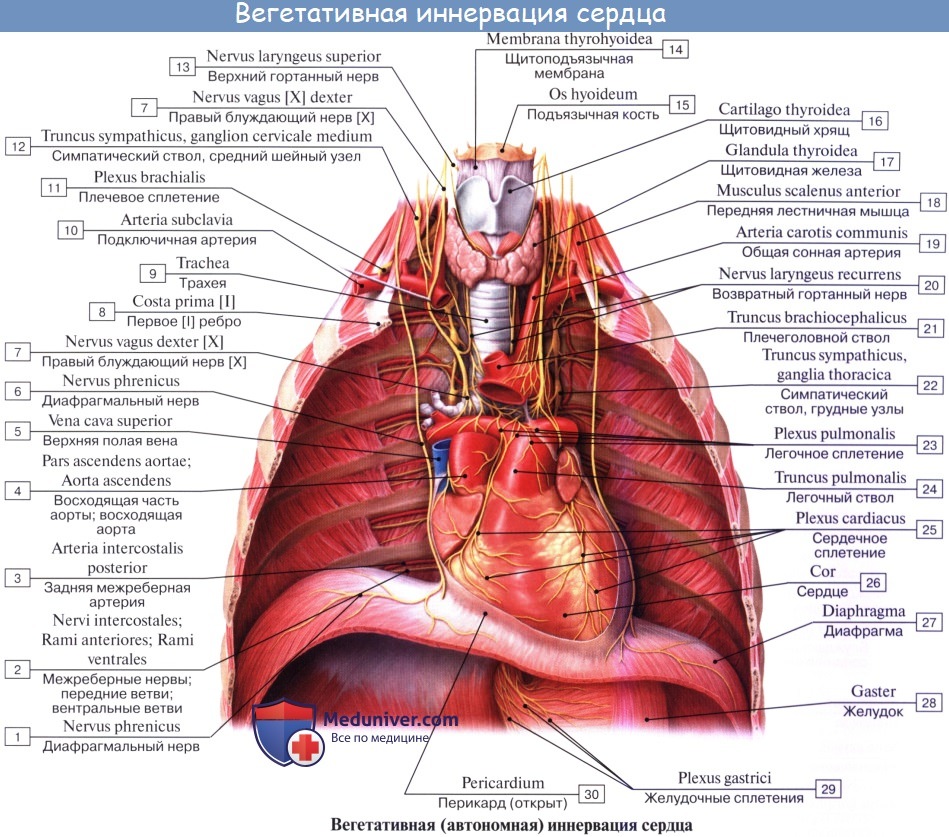
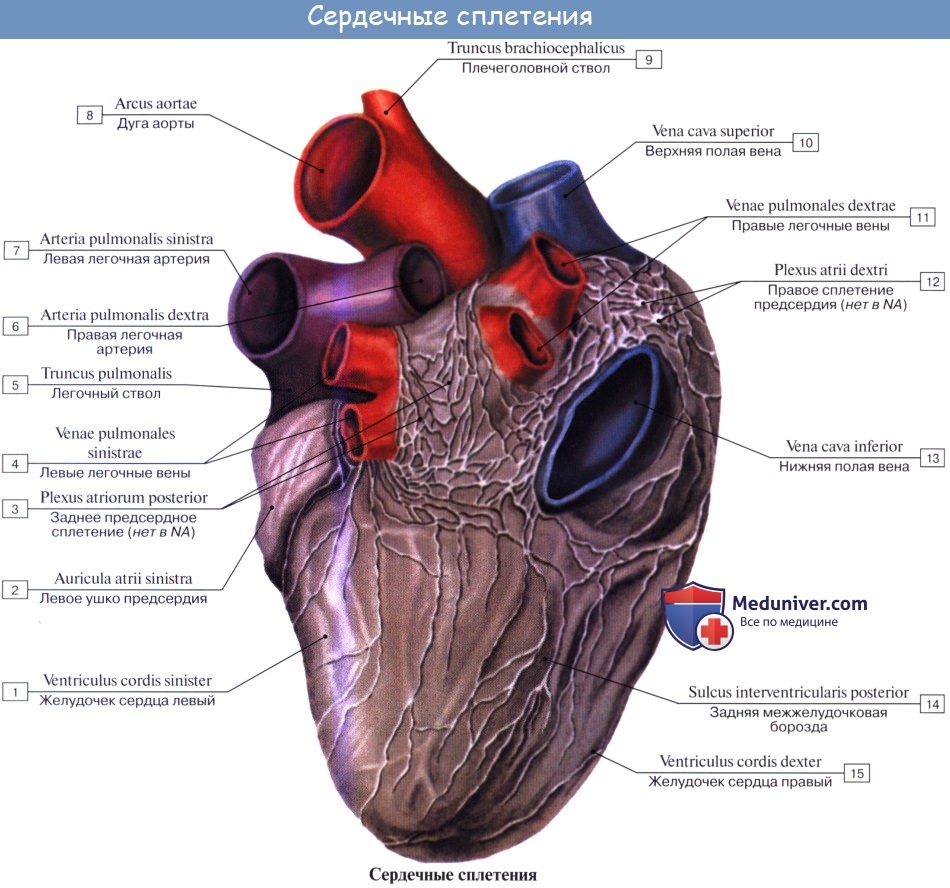
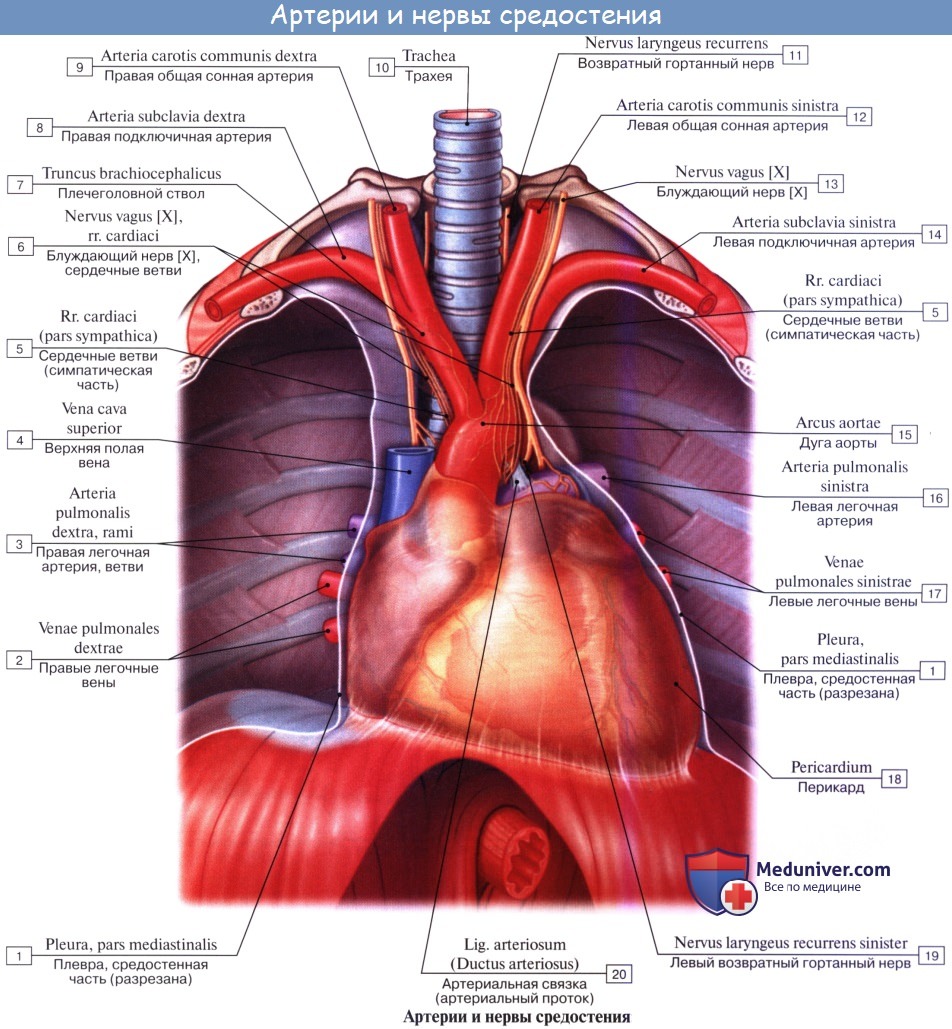
Сердечные, легочные сплетения и сплетения грудной части аорты ясно видны на сердце и окружающих его сосудах. Эти сплетения получают вегетативные волокна от блуждающего нерва и симпатического ствола.
Правый и левый блуждающие нервы сначала входят в переднюю часть верхнего средостения, потом разветвляются на пучки, которые входят в заднее средостение. Симпатические волокна направляются к сердечным сплетениям в виде шейных сердечных нервов (идущих от третьего шейного узла) и грудных сердечных ветвей (идущих от грудного узла).
Большинство вегетативных волокон в сплетениях очень тонки, но на рисунке для наглядности они изображены более толстыми. Диафрагмальный нерв не иннервирует сердце, но разветвляется на соматосенсорные ветви в перикарде (перикардиальные ветви не показаны) в среднем средостении на пути к диафрагме.

Учебное видео иннервации сердца (нервов сердца)
Редактор: Искандер Милевски. Дата последнего обновления публикации: 28.8.2020
Вегетативная дисфункция сердца
Вегетативная дисфункция сердца является частью симптомокомплекса, называемого соматоформной дисфункцией вегетативной нервной системы. Так как ВНС обеспечивает стабильность работы практически всех внутренних органов, то и симптомы расстройства ее чрезвычайно разнообразны.
Симптомы вегетативной дисфункции сердца
Симптоматику вегетативной дисфункции выявить достаточно просто, однако для окончательного установления диагноза врачу нужно точно ответить на следующие вопросы: являются ли данные симптомы признаком самостоятельной болезни или же проявлением другого, соматического, неврологического, психического заболевания? Могут ли они означать наличие патологии ССС (сердечно-сосудистой системы): гипертония, ИБС, клапанные пороки, воспаление миокарда?
При установке диагноза вегетативной дисфункции учитывают:
Выделяют основные и дополнительные диагностические признаки вегетативной дисфункции. Достоверным можно считать диагноз при наличии двух и больше основных и 2-х дополнительных признаков.
Основные признаки:
Дополнительные признаки:
Также есть признаки, наличие которых со стопроцентной вероятностью исключает диагноз вегетативной дисфункции. Выявляются они при осмотре и дополнительном обследовании. Это отеки ног, влажные хрипы в легких, аускультативные шумы в диастолу, увеличение сердца (гипертрофия, дилатация), изменения на ЭКГ (блокада левой ножки п.Гиса, АВ-блокада II-III степени, очаговые изменения, смещение сегмента ST, нарушения ритма кроме единичной экстрасистолии), изменения в анализах крови.
Причины ВСД
В основе заболевания — нарушение нейрогуморальной регуляции вегетативной нервной системы, отвечающей за стабильность и слаженность деятельности всех внутренних органов и организма в целом. Это отдел нервной системы, не подчиняющийся сознанию и управлению волей человека.
Диагностика и лечение вегетативной дисфункции сердца
Вегетативная дисфункция является диагнозом исключения. После того как будет исключен ряд сердечно-сосудистых заболеваний благодаря лабораторным, инструментальным методам (ЭКГ, ЭхоКГ, Холтер-ЭКГ и др.) следует проводить дифдиагностику с нервно-психическими заболеваниями и только в последнюю очередь думать о вегетатике.
Лечение же непосредственно расстройства вегетативной нервной системы следует начинать с оздоровления образа жизни: регулярные физические нагрузки, спорт (приоритетно плавание), исключение вредных привычек, полноценный ночной сон, оптимальное питание, нормализация массы тела, закаливание.
Из медикаментов используются адаптогены, дневные транквилизаторы, ноотропы, сосудистые препараты, антиоксиданты, витамины.
К кому обратиться?
В случае преобладания кардиальной симптоматики для правильной диагностики и при необходимости лечения нужна консультация врача-кардиолога. Лечение вегетативных расстройств является компетенцией неврологов и психиатров.
Вегетативные расстройства: в чем отличия и как с этим жить?
Часто мы сталкиваемся с плохим самочувствием и пытаемся понять, в чем причина этого состояния. И когда уже проведено множество лабораторных и инструментальных тестов и ничего не найдено, мы задумываемся: «С чем это может быть связано? Ведь я действительно чувствую себя плохо». Если никаких поражений органов нет, самое время обратиться к неврологу. Синдром вегетативной дистонии, вегетативная недостаточность, вегетативные кризы – неврологические заболевания, которые мы затронем в этой статье.
Синдром вегетативной дистонии
Синдром вегетативной дистонии – это все формы нарушения вегетативной регуляции, чаще это вторичные проявления различных патологий.
Существуют 3 формы СВД:
Вегетативная недостаточность
Вегетативная недостаточность – синдром, связанный с нарушением иннервации внутренних органов, сосудов и эндо- и экзокринных желез.
В большинстве случаев она представляет из себя прогрессирующую вегетативную недостаточность. В свою очередь ПНВ включает в себя первичные нарушения:
Ко вторичным нарушениям можно отнести:
Могут наблюдаться различные симптомы:
Диагностика данного заболевания проводится путем физикального осмотра, проверки неврологического статуса и медикаментозных проб.
Вегетативный криз
Вегетативный криз (паническая атака) – ряд клинических проявлений, характерных для эмоциональных расстройств и расстройств вегетативной нервной системы, в зависимости от преобладания симпатической и/или парасимпатической иннервации. Обязательное присутствие тревоги, ощущение страха (вплоть до страха за свою жизнь), хотя видимой угрозы не существует, страх сойти с ума, нанесение увечья близким или себе.
Вегетативные кризы разделяют на:
Важно проведение дифференциальной диагностики с соматическими заболеваниями: гипо-, гипертиреоз, сахарный диабет, феохромоцитома, нарушение сердечного ритма и проводимости, гастрит, язвенная болезнь, эпилепсия, нейроэндокринные опухоли.
Соматоформные расстройства
Состояния наблюдаются при постоянном наличие клинических симптомов с требованием дообследования, в то время как выявленные симптомы не объясняют характер и тяжести психосоматичекой симптоматики.
Соматоформное расстройство ВНС («органные неврозы»)
Пациент предъявляет жалобы, которые возникают при нарушении функции органов, преимущественно или полностью иннервируемых вегетативной нервной системой. Соматоформные расстройства связаны с нарушением работы нервной системы и психоэмоциональные расстройства.
СРВНС включает в себя:
Диагноз ставится на основании отсутствия соматической патологии и заключения невролога и психиатра.
Лечение данного расстройства включает в себя проведение психотерапии, назначения лекарственных препаратов, иглорефлексотерапию, массаж, лечебную физкультуру, физиотерапию.
Лечение должно быть подобрано специально для каждого пациента после проведения осмотра и беседы. Важно чтобы лечение подходило самому пациенту. В случае, если пациент настроен и готов избавиться от недуга, то лечение займет меньше времени. Сроки лечения не могут быть определены точно, так как каждый случай индивидуален, но мы имеем все возможности добиться стойкой ремиссии.
Для записи к нашему специалисту позвоните по телефону +7 495 221-05-00 или оставьте заявку на сайте. Администратор подробно проконсультирует вас и запишет на осмотр специалиста в любое удобное вам время. Стоимость услуг вы узнаете непосредственно на консультации у врача.
Не стоит стесняться данных расстройств и бояться обращаться к врачу за помощью. Главное справиться с этим состоянием и иметь возможность жить полноценной жизнью.
ПРОБЛЕМЫ ЭЛЕКТРОКАРДИОЛОГЧЕСКОЙ ОЦЕНКИ ВЛИЯНИЯ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ НА СЕРДЦЕ
 |  | Ключевые слова вегетативная нервная система, вариабельность сердечного ритма, реполяризация желудочков, электрокардиография |


autonomic nervous system, heart rate variability, ventricular repolarization, electrocardiography
 |  | Аннотация Рассматривается корреляция показателей вариабельности сердечного ритма и «симпатико-парасимпатического» балланса, роль ряда электрокардиологических критериев как маркеров неоднородности реполяризации желудочков. |  |  | Annotation The correlation of the heart rate variability indices with «sympatico-parasympathetic» balance, the role of a number of electrocardiological criteria as markers of inhomogeneity of ventricular repolarization are considered. |