в мазке у ребенка кокки что это
«Мазок на флору»: о чём расскажет анализ?
Исследование «Мазок на флору» относится к микроскопическому виду анализа. Тест назначают при подозрении на инфекционный процесс репродуктивных органов.
Для проведения анализа необходимо получить мазок. У мужчин биотопом является уретра, у женщин — цервикальный канал, влагалище, уретра. Исходя из места локализации патологического процесса, врач может направить женщину сдать мазок только из влагалища или цервикального канала. Однако чаще требуются все три локуса сразу.
| Взятие мазка — процедура безболезненная и безопасная. Все беременные женщины также сдают мазок минимум три раза: первый визит, 30 и 36 неделя, при условии нормально протекающей беременности. Полученный мазок переносится на стекло, высушивается и окрашивается, после чего врач-лаборант исследует препарат под микроскопом и описывает его. Бланк результата содержит информацию о микрофлоре, лейкоцитах, эпителиальных клетках и патологических агентах. |  |
Микрофлора
В процессе анализа врач описывает её тип, обильность. В норме должна преобладать палочковая флора. Палочки являются представителями лактобактерий, поддерживают определенный уровень pH. Основная роль палочек — защита влагалища от болезнетворных микроорганизмов и стимулирование местных реакций иммунитета. Когда в мазке присутствует иные бактерии, например, кокковые, число палочек снижается. Такое состояние указывает на дисбиоз и требует обязательной коррекции.
Лейкоциты
Лейкоциты в мазке позволяют судить о наличии воспалительной реакции. Число лейкоцитов в графе «результаты» указывается через дефис. Первая и вторая цифры соответствуют минимальному и максимальному числу, обнаруженному в полях зрения микроскопа. Для каждого локуса есть свои референтные показатели. В цервикальном канале допустимо не больше 25 клеток в поле зрения, в уретре — не более 5, во влагалище — не более 10.
Увеличение абсолютного число лейкоцитов говорит о воспалении, поэтому необходимо получить консультацию гинеколога или уролога.
Эпителий
Эпителиальные клетки в препарате располагаются пластами или разрозненно в виде отдельных клеток. В мазке их число должно быть единичным. В случае увеличения количества клеток эпителия, врач указывает: умеренно — означает, что в одном поле зрения находятся до 10 эпителиальных клеток, много — до 20, обильно — свыше 25.
Изменение размера и морфологии клеток эпителия, могут косвенно говорить о воспалительной реакции или о проблемах гормонального характера. Клетки эпителия, покрытые по всей поверхности кокками, носят название «ключевых клеток». Обнаружение их в мазке является морфологическим критерием бактериального вагиноза.
Слизь
Значения «мало», «умеренно», «отсутствует» являются вариантом нормы. Если слизь присутствует в большем количестве, то это признак дисбиотических нарушений во влагалище.
Патологические элементы
В мазке врач может идентифицировать мицелий и споры дрожжеподобных грибков, трихомонады, актиномицетов, сперматозоиды и др. Но определить точную видовую принадлежность возбудителя не сможет из-за ограничений метода. Например, в урогенитальном тракте человека обитают несколько представителей рода Neisseriaceae, которые похожи между собой, поэтому отличить в стандартном микроскопе не представляется возможным.
Диагностическая чувствительность микроскопии при диагностике гонококковой инфекции в России составляет 30%, а трихомонадной инфекции — 44–68%. Микроскопия носит описательный характер, для точного определения вида возбудителя необходимо использовать молекулярно-биологические методы (ПЦР, NASBA) и культуральный метод.
Гинекологический мазок «на флору»: на что смотреть, и как понять
Большинству женщин мазок «на флору» знаком, как самый «простой» гинекологический анализ. Однако исследование куда «полезнее», чем может казаться. И всего несколько (а то и одно) отклонений способны подсветить значимые проблемы, еще до появления каких-либо симптомов. Так как же понять полученные результаты? Рассказываем по пунктам.
1. Эпителий
Как известно, любой живой объект в природе имеет ограниченный срок жизни, по истечении которого он погибает «от старости».
Эпителий в гинекологическом мазке – это и есть слущенные «старые» клетки слизистой оболочки влагалища, цервикального или уретры (в зависимости от оцениваемого локуса). Которые могут присутствовать в материале в умеренных количествах.
Превышение нормативных пределов («много» или «обильно») может указывать на:
Уменьшение или отсутствие эпителия в мазке – на атрофические изменения, недостаток эстрадиола или избыток андрогенов.
Кроме того, ввиду зависимости эпителия от уровня половых гормонов, его количество в материале может сильно меняться в зависимости от дня цикла, начиная с единичного «в поле зрения» в самом начале – до умеренного и даже большого количества ближе к овуляции и во время нее.
А появление в мазке так называемых «ключевых клеток» (эпителий, «облепленный» мелкими кокковыми бактериями) – является маркером бактериального вагиноза.
2. Лейкоциты
«Норма» лейкоцитов в мазке также сильно зависит от стадии цикла и уровня половых гормонов, а также исследуемого локуса.
Так, за «максимум» для:
Повышение показателя – очевидно, свидетельствует о воспалении, а полное отсутствие может иметь место в норме в самом начале цикла.
Слизь
Результат «отсутствует», «мало» или «умеренно» для этого показателя является нормой, что тоже связано с индивидуальными особенностями гормонального фона и циклом.
А вот «много» слизи в мазке – может свидетельствовать о том, что мазок взят в середине цикла, дисбиотических изменениях или избытке эстрогенов. Поэтому требует внимания специалиста или, как минимум, контроля в динамике.
Флора
Преобладающей флорой женских половых путей в норме у женщин репродуктивного возраста, как известно, являются лактобактерии (или палочки Дедерлейна). Количество которых может быть от умеренного до обильного, в том зависимости, в том числе, от фазы менструального цикла.
Патологические элементы
Присутствия мицелия грибов, трихомонад, диплококков (в том числе и возбудитель гонореи), лептотрикса, мобилункуса и прочих патогенных микроорганизмов в нормальном мазке не допускается, даже в минимальном количестве. А их выявление – серьезный повод незамедлительно обратиться за лечением.
Вульвовагиниты у девочек и возрастные нормы микрофлоры
Анатомические особенности строения гениталий и постепенное формирование биоценоза половых путей у девочек допубертатного возраста часто связаны с развитием воспалительных заболеваний влагалища и вульвы. Наиболее распространённым вариантом является сочетанное поражение — вульвовагинит.
Нормальные показатели микрофлоры влагалища и вульвы у растущих девочек связаны с возрастом, — таким образом, критерии выявления патологии основываются на изученности состояния биоценоза пациенток из разных возрастных групп. При классификации в зависимости от возраста, выделяют вульвовагиниты периода младенчества (0–12 мес), детства (1–8 лет), препубертатного (с 8 лет до менархе) и пубертатного периода (с менархе).
В процессе формирования микрофлоры ключевую роль играет взаимодействие гормональной и иммунной систем пациентки, — в частности, крайне важно состояние местного иммунитета. Также весьма значимы функциональное состояние яичников и наличие лактофлоры.
Инфицированию влагалища и вульвы у девочек способствует ряд факторов, среди которых ведущие позиции занимают анатомо-физиологические особенности гениталий, различные экстрагенитальные заболевания, а также экзогенные патологические факторы. Кроме того, нужно учитывать, что вульвовагинитам более подвержены пациентки, живущие в неблагоприятных социально-бытовых условиях и не соблюдающие правила личной гигиены.
У девочек до рождения и в раннем периоде после него слизистая влагалища состоит, в основном, из 3–4 слоёв плоского эпителия промежуточного типа. Вместе с тем, из плацентарного кровотока или с молоком матери эпителиальные клетки получают дозы эстрогенов и прогестерона, под действием которых могут продуцировать гликоген, а следовательно — поддерживать жизнедеятельность молочнокислых бактерий. После 3–4 ч неонатального периода во влагалище обнаруживаются лактобациллы, бифидобактерии и коринебактерии, а также единичные кокковые элементы. В этот период усиливается десквамация эпителия и происходит помутнение шеечной слизи.
С течением времени лактофлорой накапливается молочной кислота, а значит, кислотно-щелочной баланс среды влагалища у девочки смещается к кислому (рН=4,0–4,5). Наряду с лактобактериями, слизистую оболочку влагалища защищают бифидобактерии. Они препятствуют воздействию патогенных и условно-патогенных микроорганизмов, а также их токсинов, кроме того — стимулируют образование интерферона и выработку лизоцима. Главным же образом высокой резистентности у новорождённых девочек способствует доза иммуноглобулинов класса G (IgG), полученных ими от матери через плаценту.
Уровень эстрогенов в организме девочки падает в промежутке 10 дней после рождения. В этот период происходит так называемый половой криз и появление менструальноподобных выделений примерно у 10% новорождённых. Эпителиальные клетки теряют способность к пролиферации и синтезу гликогена.
К концу первого месяца жизни влагалищный эпителий составляют базальные и парабазальные клетки. Реакция влагалищного содержимого становится щелочной, а уровень рН возрастает до 7,0–8,0. Пропадают лактобактерии и бифидобактерии, эпителий становится тонким и уязвимым, во влагалище начинает преобладать кокковая и бациллярная флора.
С двух месяцев жизни и до наступления менархе во влагалище без патологии преобладают эпидермальный стафилококк (84%), дифтероиды (80%), бактероиды и пептококки (76%), пептострептококки (56%), эубактерии (32%), gardnerella vaginalis (32% у девочек школьного возраста), микоплазма (9%, главным образом, у пациенток до 9 лет).
Новые изменения в структуре влагалищного эпителия происходят после 9 лет: усиление пролиферации, созревание, накопление гликогена. К 10 годам pH-показатели среды вновь смещаются к кислым в связи с заселением лактобациллами.
К 12 годам лактофлора преобладает в мазках у здоровых девочек, а к 13–14 годам pH влагалищной среды окончательно становится кислым в связи с размножением лактобацилл и созреванием эпителия под воздействием эстрогенов. Если в «нейтральном» периоде частота вульвовагинитов лидирует в структуре гинекологической заболеваемости, составляя, по разным данным, 82–85%, то после 10 лет она падает до 30–40%, а первое место у пациенток пубертатного занимают расстройства менструации.
Вся изложенная информация более подробно представлена в учебном пособии «Воспалительные заболевания половых органов у девочек и девушек» авторства Ольги Евгеньевны Баряевой (Иркутский государственный медицинский университет).
Воспалительные заболевания гениталий у девочек
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В структуре гинекологических заболеваний детского возраста воспалительные поражения гениталий занимают ведущее место. Клиническое значение указанной патологии определяется не только ее частотой, но и тем, что она может явиться причиной серьезных нарушений репродуктивной системы в дальнейшем.
У девочек допубертатного «нейтрального» периода (в среднем до 10 лет) наружные половые органы и влагалище наиболее подвержены воспалительным процессам с развитием вульвитов и вагинитов. При этом самым распространенным является сочетанное поражение, трактуемое как вульвовагинит.
Сказанное определяется прежде всего физиологическими особенностями и этапностью становления биоценоза половых путей растущей девочки.
Микрофлора вульвы и влагалища девочек в норме в зависимости от возраста
Биоценоз половых путей растущей девочки изучен достаточно хорошо, что дало возможность выработать критерии для оценки его состояния в норме и при патологии. Формирование естественной микрофлоры влагалища у здоровой девочки – сложный многофакторный процесс, в основе которого лежит взаимодействие гормональной системы с иммунологическими особенностями организма. При этом доминирующее значение имеет функциональное состояние яичников, наличие лактофлоры и состояние местного иммунитета.
У новорожденной девочки влагалище стерильно, но уже через 12 часов после рождения слизистая заселяется бактериями, среди которых преобладают лактобациллы (палочка Додерлейна). Последние расщепляют гликоген влагалищного эпителия с образованием молочной кислоты, что формирует кислую реакцию влагалищной среды, которая и защищает слизистую от контаминации экзогенными микроорганизмами.
К 20–му дню жизни материнские гормоны (прогестерон, эстрогены), обеспечивающие пролиферацию вагинального эпителия и его высокую степень насыщения гликогеном, выводятся из организма. Мазок принимает атрофический характер – эпителий истончается, лактобактерии исчезают, реакция среды становится слабо–щелочной или нейтральной. При этом влагалище заселяется кокковой и бациллярной флорой.
Обследование здоровых девочек с 2–х месячного возраста до менархе показало преобладание следующих микроорганизмов:
Наибольшая частота вульвовагинитов приходится на «нейтральный» период и составляет, по данным различных авторов, 82–85% в структуре гинекологической заболеваемости.
После 9 лет повышается эстрогенная секреция и вновь происходят изменения во влагалищном эпителии в виде усиления пролиферации, созревания, накопления гликогена, и к 10 годам начинается заселение лактобациллами, со смещением рН среды в кислую сторону.
К 12 годам в мазке преобладает лактофлора. Повышение эстрогенной стимуляции приводит к дальнейшему созреванию эпителия, размножению лактобацилл и к 13–14 годам рН влагалищной среды становится кислой.
Частота вульвовагинитов после 10 лет снижается до 30–40%, уступая в пубертатном периоде заболеваниям, именуемым расстройствами менструальной функции.
В основу большинства классификаций вульвовагинитов у девочек положен этиологический принцип. Наиболее удобной для использования в практической работе является классификация, приведенная в таблице 1.
Имеют значение неблагоприятные социально–бытовые условия, несоблюдение правил личной гигиены.
Однако ведущая роль принадлежит причинному инфекционному фактору. В большинстве случаев (в 72%) у девочек до 10 лет этиологическим фактором вульвовагинитов является бактериальная флора, представленная:
В возрасте от 10 до 15 лет среди вульвовагинитов чаще встречаются микотические, что может быть обусловлено кислой реакцией влагалищной среды, благоприятной для грибов, а также наличием взаимосвязи с предшествующей антибактериальной терапией. Согласно литературным данным, наиболее часто встречаются:
Следует обратить внимание на возрастание этиологической роли стрептококковой инфекции в развитии вульвовагинитов у девочек–подростков.
Несмотря на различие этиологических факторов вульвовагинитов, клинические проявления в основном идентичны (табл. 2).
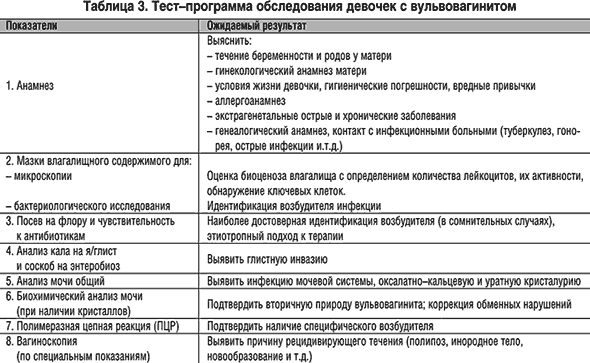
Необходимые исследования для установления и подтверждения диагноза включают как общие, так и специальные методы обследования девочек (табл. 3).
При наличии клиники вульвовагинита в мазке:
– лейкоцитов больше 15 в п/зрения;
– слущенного эпителия – много;
– флора – смешанная, кокковая, палочковая, специфическая – в значительном количестве (табл. 4).
Лечение вульвовагинитов у девочек нередко является сложной задачей, требует комплексной терапии и предполагает дифференцированную тактику. При тяжелых проявлениях воспаления, частых рецидивах, кроме соблюдения личной гигиены и проведения местного противовоспалительного лечения, необходима терапия основного заболевания, санация очагов хронической инфекции, повышение защитных сил организма (табл. 5).
Лечение вульвовагинитов у девочек нередко является сложной задачей, требует комплексной терапии и предполагает дифференцированную тактику. При тяжелых проявлениях воспаления, частых рецидивах, кроме соблюдения личной гигиены и проведения местного противовоспалительного лечения, необходима терапия основного заболевания, санация очагов хронической инфекции, повышение защитных сил организма (табл. 5).
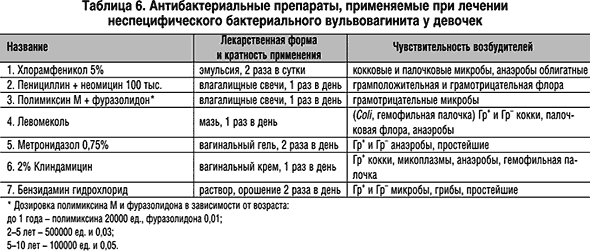
Местная антибиотикотерапия применяется при рецидивирующем характере течения и только при идентифицированной патогенной микрофлоре с определением ее чувствительности к антибактериальным препаратам (табл. 6). При тяжелых вульвовагинитах показано парентеральное введение антибактериальных препаратов. Учитывая частоту анаэробов, участвующих в развитии вагинитов, а также тяжесть анаэробной инфекции, многие авторы рекомендуют широкое использование в его лечении метронидазола, эффективного в отношении Trichomonas vaginalis, бактероидов, фузобактерий. При наружном применении препарат обладает также антиоксидантным и противовоспалительным дерматопротективным действием. Метронидазол действует синергически с другими антибиотиками. Внутрь детям старше 15 лет назначают по 250–500 мг 2–3 раза в сут. Детям до 15 лет назначают в дозе 20–40 мг/кг в сут., в 3 приема. Свечи и вагинальные таблетки назначают по 1 шт. (500 мг) на ночь. Внутривенное введение показано при тяжелом течении инфекций, а также при отсутствии возможности приема препарата внутрь. Для детей старше 12 лет разовая доза при внутривенной инфузии составляет 500 мг, интервал между введениями 8 ч. Длительность курсов лечения и частота их проведения определяются индивидуально.
На заключительном этапе этиотропного лечения с целью коррекции вагинальных дисбиотических процессов применяются местно и энтерально такие препараты, как, бифидумбактерии, лактобактерин, биовестин–лакто.
Лечение микотического вульвовагинита у девочек
Микотический вульвовагинит в большинстве случаев является частным проявлением кандидоза, развитию которого способствуют тяжелые соматические и инфекционные заболевания, нарушение обмена, гиповитаминозы, нерациональное использование антибиотиков широкого спектра действия, иммунодефицитные состояния. В связи с этим обязательным условием эффективного лечения кандидоза гениталий является сведение к минимуму или устранение указанных факторов, что достигается:
1) лечением основного заболевания;
2) диетотерапией с ограничением продуктов, богатых углеводами;
3) витаминотерапией и иммунокорригирующими средствами;
4) десенсибилизирующей терапией.
Особенностью кандидозного вульвовагинита является упорное течение, склонность к рецидивированию. Поэтому специфическое лечение, как правило, должно быть длительным, курсовым. Количество курсов – не менее 2–3, перерыв между курсами 7–10 дней.
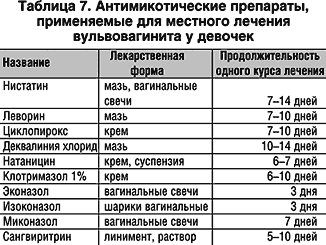
При микотическом поражении гениталий у девочек нередко возникают ассоциации с бактериями, простейшими. В этих случаях целесообразно применение препаратов, обладающих не только антимикотической активностью, но и проявляющих антибактериальное воздействие на грамположительные и грамотрицательные микроорганизмы, а также имеющих антипаразитарное действие (табл. 7, 8).
К таким препаратам (из указанных выше) относятся:
Изоконазол – активен в отношении дрожжеподобных грибов, грамположительных микробов (стафилококки, микрококки, стрептококки).
– активен в отношении дрожжеподобных грибов, грамположительных микробов (стафилококки, микрококки, стрептококки).
Миконазол – выражена активность в отношении грибов рода Кандида и грамположительной микрофлоры
Сангвиритрин – обладает широким спектром антимикотической и антимикробной активности, действуя на грамположительные и грамотрицательные микроорганизмы. Активен в отношении антибиотикорезистентных штаммов микробов.
В последние годы стали применяться комбинированные препараты для лечения микотических и смешанных вульвовагинитов. Литературные данные свидетельствуют об их высокой эффективности, позволяющей добиться полного клинического и микробиологического выздоровления при отсутствии побочных реакций. В то же время сведений о применении комбинированных препаратов в педиатрической практике фактически нет, имеются лишь отдельные наблюдения.
В перерывах между курсами специфической антимикотической местной терапии проводят неспецифическую терапию широко известными средствами:
Вышеперечисленные средства способствуют удалению мицелия гриба, нарушают процесс прикрепления гриба к слизистым, тормозят его размножение.
Эффективность лечения микотического вульвита увеличивается при сочетанном применении антимикотических средств местно и энтерально. Общее лечение становится обязательным при неэффективности местного, в частности, при рецидивировании процесса и его генерализации.
Кетоконазол – высокоэффективный антимикотический препарат. Однако при лечении возможны серьезные побочные реакции, обладает кумулятивным эффектом. В связи с этим применение препарата ограничено.
Натамицин – малотоксичен, к нему чувствительны большинство патогенных дрожжеподобных грибов, особенно Candida albicans. По данным сотрудников кафедры педиатрии РМАПО, препарат эффективен, хорошо переносится больными, в т.ч. детьми первого года жизни, побочных реакций не отмечено.
С целью восстановления биоценоза влагалища и коррекции местного иммунитета после проведенной комплексной терапии микотического вульвовагинита целесообразно назначение эубиотиков (ацилакт, лактобактерин и др.) в свечах ректально и вагинально.
Исходя из вышеизложенного, тактика лечения вульвовагинитов у девочек должна быть строго дифференцирована и определяться как этиологическим фактором, так и состоянием макроорганизма в целом. Внедрение в практику современных антибактериальных и антимикотических препаратов позволяет не только повысить эффективность терапии воспалительных заболеваний гениталий у девочек, но и снизить число рецидивов, профилактировать хронизацию процесса, избежать отдаленных последствий перенесенного воспаления гениталий.
1. Кохреидзе Н.А., Кравченко М.Е.. Становление вагинальной микрофлоры в возрастном аспекте // Ж. Детская больница, 2002, 3: 45–47.
2. Буданов П.В., Баев О.Р. Диагностика и варианты комплексного нарушения микроценоза влагалища // Вопросы гинекологии, акушерства и перинатологии, 2002; т.1, 2: 73–76.
3. Лебедев В.А., Давыдов А.И. Урогенитальный хламидиоз // Вопросы гинекологии, акушерства и перинатологии, 2002; т.1, 2: 25–30.
4. Коколина В.Ф., Бижанова Д.А. Диагностика и лечение вульвовагинитов // Ж. Педиатрия, 1993№ 6: 57–59.
5. Коколина В.Ф., Зубакова О.В. Диагностика и лечение урогенитальных инфекций в гинекологии детского и подросткового возраста. Методическое пособие. М. 1998.
6. Кобозева Н.В., Кузнецова М.Н., Гуркин Ю.А. Гинекология детей и подростков // Ленинград «Медицина». 1988, 126–146.
7. Кулаков В.И., Прилепская В.Н. Практическая гинекология // Москва, 2001, 177–253.
8. Серов В.Н. с соавт. Значение генитальных инфекций в формировании распространенных гинекологичесих заболеваний и их современное лечение // Информационное письмо, Москва, 1997.
Микрофлора полости рта
Последнее обновление: 11.11.2021
От состояния микрофлоры полости рта зависит не только здоровье зубов и десен, но и работа органов пищеварения, иммунной и других систем и органов. Давайте разберемся, что представляет собой эта часть организма, что влияет на состояния полости рта и как быстро восстановить нормальную работу микрофлоры.
Что представляет собой микрофлора полости рта?
Удивительно, но во рту здорового человека живет примерно 160 видов микроорганизмов. Вам, наверное, приходилось слышать о том, что «рот — это самое грязное место в организме». Отчасти это утверждение верно: ротовая полость — один из наиболее заселенных отделов тела человека.
Микроорганизмы попадают в ротовую полость с пищей и водой, а также из воздуха. Именно во рту наблюдаются самые благоприятные условия для развития бактерий. В этой части тела всегда стоит равномерная влажность и температура (примерно 37 °С). Обилие питательных веществ, достаточное содержание кислорода, наличие складок в полости рта, межзубных промежутков и десневых карманов, слабощелочная pH провоцируют размножение различных бактерий.
Микроорганизмы неравномерно распределяются в полости рта. Максимальное их количество наблюдается на поверхности зубов и на спинке языка. В одном грамме зубного налета содержится примерно 300 миллиардов микробов, а в слюне — примерно 900 миллионов на 1 миллилитр.
Можно очень долго перечислять все виды бактерий, заселяющих микрофлору полости рта. Важно понимать, что каждый человек уникален, и для оценки «нормальности» микрофлоры нужно знать особенности конкретного организма.
Например, в одном случае большое количество лактобактерий в полости рта будет сохранять зубы, а в другом — образование большого количества молочной кислоты в процессе их жизнедеятельности задержит рост других важнейших микроорганизмов. Снижается число стафилококков, дизентерийных и брюшнотифозных палочек, активизируются кариозные процессы, и микрофлору полости рта придется восстанавливать.
Нарушение микрофлоры полости рта: причины
Дисбактериоз ротовой полости могут спровоцировать самые разные заболевания и проблемы. Нарушение условно-патогенной микрофлоры полости рта чаще всего вызывают такие проблемы, как:
Стадии дисбактериоза
В зависимости от степени развития заболевания стоматологи различают четыре стадии дисбактериоза:
Для запущенных форм дисбактериоза характерны такие симптомы, как:
Методы восстановления микрофлоры полости рта
Лечение дисбактериоза зависит, в первую очередь от характера возбудителя, который определяется на основании экспертизы в стоматологии.
К сожалению, зачастую постановка диагноза при дисбактериозе бывает затрудненной, так как на начальном этапе болезнь никак не проявляет себя. При малейших подозрениях на заболевание стоматолог направляет пациента на мазок с поверхности слизистых, анализы крови и мочи.
В зависимости от диагностированной причины дисбактериоза стоматолог может назначить следующие методы лечения заболевания:
В редких случаях назначаются противогрибковые средства и антибиотики.
Как правило, длительность лечения дисбактериоза составляет 2-4 недели и зависит от состояния здоровья пациента, количества очагов воспаления и имеющихся осложнений заболевания.
Надежным помощником в борьбе с дисбактериозом станет пробиотический комплекс АСЕПТА PARODONTAL*, источник лактобактерий для восстановления микрофлоры полости рта. Этот уникальный комплекс с запатентованными штаммами лактобактерий и витамином D обладает способностью эффективно восстанавливать микрофлору полости рта. Комплекс нормализует бактериальную флору в ротовой полости, устраняет неприятный запах изо рта и препятствует образованию биопленок патогенных микроорганизмов.
Для улучшения эффективности назначенной терапии стоматологи рекомендуют отказаться от вредных привычек (хотя бы на время лечения), пересмотреть рацион, уделив внимание растительной пищи и обязательно ухаживать за полостью рта после каждого приема пищи.
Возможные осложнения дисбактериоза
Каждому пациенту важно внимательно следить за состоянием микрофлоры полости рта. Отсутствие лечения дисбактериоза может привести к таким неприятным заболеваниям, как:
Кроме того, научно доказана тесная взаимосвязь состояния микрофлоры полости рта с состоянием сердечнососудистой системы. В 2008 году в США была доказано, что заболевания периодонта как источник хронического воспаления являются независимым фактором риска возникновения ишемической болезни сердца (ИБС).
Итак, теперь вам известна роль нормальной микрофлоры полости рта в организме человека. Относитесь к себе внимательно, и ваш здоровый организм будет радовать вас каждый день.
Клинические исследования
Проведенные в 10-ом отделении Cтоматологии и челюстно-лицевой хирургии Стоматологического факультета Международного университета Каталонии, доказали, что применение лактобактерий помогает снизить болевые ощущения и трудности с приемом пищи после удаления зубов у взрослых пациентов.
Эффективность применения комплексной терапии в лечении заболеваний пародонта. (кафедра пародонтологии СФ ГБОУ ВПО МГМСУИМ.А.И.Евдокимова. Москва.)
Немерюк Д.А.- доцент, к.м.н., Дикинова Б.С.- аспирант кафедры пародонтологии СФ Царгасова М.О.- аспирант кафедры пародонтологии СФ Яшкова В.В.- аспирант кафедры пародонтологии СФ
кафедра пародонтологии СФ ГБОУ ВПО МГМСУИМ.А.И.Евдокимова. Москва