в чем сущность коррозии металлов
Коррозия металлов. Виды коррозии металлов
Определение коррозии
Материалы из металлов под химическим или электрохимическим воздействием окружающей среды подвергаются разрушению, которое называется коррозией.
Коррозия металлов вызывается окислительно-восстановительными реакциями, в результате которых металлы переходят в окисленную форму и теряют свои свойства, что приводит в негодность металлические материалы.
Можно выделить 3 признака, характеризующих коррозию:
Виды коррозии металлов
Наиболее часто встречаются следующие виды коррозии металлов:
С точки зрения механизма коррозионного процесса можно выделить два основных типа коррозии: химическую и электрохимическую.
Химическая коррозия металлов
Химическая коррозия металлов — это результат протекания таких химических реакций, в которых после разрушения металлической связи, атомы металла и атомы, входящие в состав окислителей, образуют химическую связь.
Электрический ток между отдельными участками поверхности металла в этом случае не возникает. Такой тип коррозии присущ средам, которые не способны проводить электрический ток – это газы, жидкие неэлектролиты.
Виды химической коррозии
Химическая коррозия металлов бывает газовой и жидкостной.
Газовая коррозия металлов – это результат действия агрессивных газовых или паровых сред на металл при высоких температурах, при отсутствии конденсации влаги на поверхности металла. Это, например, кислород, диоксид серы, сероводород, пары воды, галогены. Такая коррозия в одних случаях может привести к полному разрушению металла (если металл активный), а в других случаях на его поверхности может образоваться защитная пленка (например, алюминий, хром, цирконий).
Жидкостная коррозия металлов– может протекать в таких неэлектролитах, как нефть, смазочные масла, керосин и др. Этот тип коррозии при наличии даже небольшого количества влаги, может легко приобрести электрохимический характер.
При химической коррозии скорость разрушения металла пропорциональна скорости химической реакции и той скорости с которой окислитель проникает сквозь пленку оксида металла, покрывающую его поверхность. Оксидные пленки металлов могут проявлять или не проявлять защитные свойства, что определяется сплошностью.
Фактор Пиллинга-Бэдворса
Сплошность такой пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе) по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла
где Vок — объем образовавшегося оксида
VМе — объем металла, израсходованный на образование оксида
Мок – молярная масса образовавшегося оксида
ρМе – плотность металла
n – число атомов металла
AMe — атомная масса металла
ρок — плотность образовавшегося оксида
Оксидные пленки, у которых α 2,5 условие сплошности уже не соблюдается, вследствие чего такие пленки не защищают металл от разрушения.
Ниже представлены значения сплошности α для некоторых оксидов металлов
| Металл | Оксид | α | Металл | Оксид | α |
| K | K2O | 0,45 | Zn | ZnO | 1,55 |
| Na | Na2O | 0,55 | Ag | Ag2O | 1,58 |
| Li | Li2O | 0,59 | Zr | ZrO2 | 1.60 |
| Ca | CaO | 0,63 | Ni | NiO | 1,65 |
| Sr | SrO | 0,66 | Be | BeO | 1,67 |
| Ba | BaO | 0,73 | Cu | Cu2O | 1,67 |
| Mg | MgO | 0,79 | Cu | CuO | 1,74 |
| Pb | PbO | 1,15 | Ti | Ti2O3 | 1,76 |
| Cd | CdO | 1,21 | Cr | Cr2O3 | 2,07 |
| Al | Al2O2 | 1,28 | Fe | Fe2O3 | 2,14 |
| Sn | SnO2 | 1,33 | W | WO3 | 3,35 |
| Ni | NiO | 1,52 |
Электрохимическая коррозия металлов
Электрохимическая коррозия металлов – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
При таком типе коррозии атом удаляется из кристаллической решетки результате двух сопряженных процессов:
Сам процесс отвода электронов с катодных участков называется деполяризацией, а вещества способствующие отводу – деполяризаторами.
Наибольшее распространение имеет коррозия металлов с водородной и кислородной деполяризацией.
Водородная деполяризация
Водородная деполяризация осуществляется на катоде при электрохимической коррозии в кислой среде:
2H + +2e — = H2 разряд водородных ионов
Кислородная деполяризация
Кислородная деполяризация осуществляется на катоде при электрохимической коррозии в нейтральной среде:
O2 + 4H + +4e — = H2O восстановление растворенного кислорода
Все металлы, по их отношению к электрохимической коррозии, можно разбить на 4 группы, которые определяются величинами их стандартных электродных потенциалов:
Виды электрохимической коррозии
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
А: Fe – 2e — = Fe 2+
K: O2 + 4H + + 4e — = 2H2O
Катодом является та поверхность, где больше приток кислорода.
Методы защиты от коррозии металла
Основной способ защиты от коррозии металла – это создание защитных покрытий – металлических, неметаллических или химических.
Металлические покрытия
Например, при нанесении слоя цинка на железо, при нарушении целостности покрытия, цинк выступает в качестве анода и будет разрушаться, а железо защищено до тех пор, пока не израсходуется весь цинк. Цинковое покрытие является в данном случае анодным.
Катодным покрытием для защиты железа, может, например, быть медь или никель. При нарушении целостности такого покрытия, разрушается защищаемый металл.
Неметаллические покрытия
Такие покрытия могут быть неорганические (цементный раствор, стекловидная масса) и органические (высокомолекулярные соединения, лаки, краски, битум).
Химические покрытия
В этом случае защищаемый металл подвергают химической обработке с целью образования на поверхности пленки его соединения, устойчивой к коррозии. Сюда относятся:
оксидирование – получение устойчивых оксидных пленок (Al2O3, ZnO и др.);
азотирование – поверхность металла (стали) насыщают азотом;
воронение стали – поверхность металла взаимодействует с органическими веществами;
цементация – получение на поверхности металла его соединения с углеродом.
Изменение состава технического металла и коррозионной среды
Изменение состава технического металла также способствует повышению стойкости металла к коррозии. В этом случае в металл вводят такие соединения, которые увеличивают его коррозионную стойкость.
Изменение состава коррозионной среды (введение ингибиторов коррозии или удаление примесей из окружающей среды) тоже является средством защиты металла от коррозии.
Электрохимическая защита
Электрохимическая защита основывается на присоединении защищаемого сооружения катоду внешнего источника постоянного тока, в результате чего оно становится катодом. Анодом служит металлический лом, который разрушаясь, защищает сооружение от коррозии.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором. Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
Примеры задач с решениями на определение защитных свойств оксидных пленок, определение коррозионной стойкости металлов, а также уравнения реакций, протекающих при электрохимической коррозии металлов приведены в разделе Задачи к разделу Коррозия металлов
Коррозия металлов
Коррозия – это самопроизвольный окислительно-восстановительный процесс разрушения металлов и сплавов вследствие взаимодействия с окружающей средой.
Различают два вида коррозии – химическую и электрохимическую. Х
Химическую коррозию, обусловленную взаимодействием металлов с газами, называют газовой. Основной вклад в газовую коррозию металла вносит кислород воздуха. Различные металлы обладают различной устойчивостью по отношению к О2. Некоторые металлы (Al, Cr, Zn, Pb, Sn) образуют на воздухе плотные пленки оксидов, не разрушающиеся при изгибе или нагревании. Такие пленки защищают металл от дальнейшего доступа к нему газов и жидкостей, и процесс коррозии резко замедляется. Оксидные пленки других металлов (например, Fe) представляют собой рыхлые, пористые, механически непрочные образования. Они не предохраняют металл от доступа к нему газов и жидкостей. Поэтому такие металлы корродируют особенно быстро.
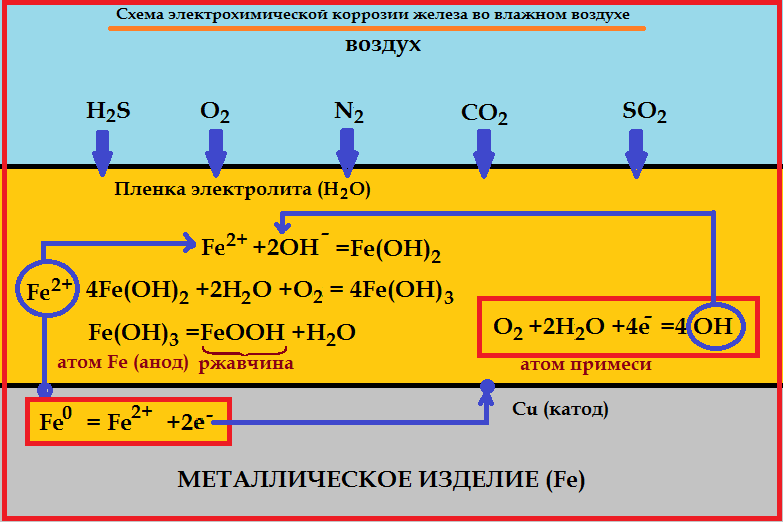
Процесс химической коррозии Fe схематически можно представить следующими уравнениями:
2Fe + O2=2FeO
Fe(OH)3= t H2O+FeOOH (ржавчина)
Однако наибольший вред приносит не химическая, а электрохимическая коррозия, связанная с переходом электронов от одних участков металла к другим. Химическая коррозия сопровождает электрохимическую и усиливает ее.
Сущность электрохимической коррозии
Металлы обычно содержат примеси других металлов и неметаллов. При соприкосновении таких металлов с электролитом (которым может служить Н2О, адсорбированная из воздуха, поскольку в ней как правило имеются ионы растворенных веществ) на поверхности металла возникает множество микрогальванических пар. В этих парах атомы более активного металла (обычно Fe) играют роль анода, а атомы менее активного – роль катода.
На катоде идет процесс восстановления молекул О2 в нейтральной и щелочной средах, или ионов Н + – в кислой среде.
Скорость электрохимической коррозии тем больше, чем дальше друг от друга расположены металлы в ряду напряжений, и чем выше температура окружающей среды.
Чистые металлы устойчивы к коррозии. Однако, так ка абсолютно чистым металлов нет, а также вследствие того, что гальваническая пара может быть образована отдельными участками одного и того же металла, находящимися в различных условиях (под разными электролитами или под одним и тем же электролитом разной концентрации), то электрохимическая коррозия имеет место всегда при соприкосновении металла с электролитом (атмосферной влагой).
Роль катода при электрохимической коррозии могут выполнять не только менее активные металлы, но и примеси неметаллов, способных принимать электроны.
Коррозия – процесс поверхностный и при отсутствии трещин внутри металла развиваться не может. Поэтому одним из способов защиты от коррозии является нанесение на поверхность металла металлических и неметаллических покрытий.
В качестве металлических покрытий используются пленки Au, Ag, Ni, Cr, Zn и других металлов, которые мало подвергаются коррозии из-за своей индифферентности или по причине образования прочных оксидных пленок. Некоторые из этих металлов (Au, Ag, Ni, Cr), помимо защитной, выполняют и эстетическую – придают изделиям приятный внешний вид.
Различают два вида металлических покрытий – анодное и катодное. Покрытие называется
Примером анодных покрытий для изделий из железа являются пленки из Cr, Zn, примером катодных – пленки из Ni, Sn, Ag, Au. Катодные покрытия не защищают металлы в случае нарушения их целостности (трещины, царапины), так как при наличии электролита возникает гальваническая пара, роль растворимого анода в которой играет защищаемый металл.
Неметаллические покрытия также делятся на два вида: неорганические и органические. В качестве органических покрытий используются пленки лаков, красок, пластмасс, резины, битума, в качестве неорганических – эмали.
Протекторная защита заключается в соединении защищаемого изделия проводником с протектором – пластиной из более активного металла (Al, Mg, Zn). В процессе коррозии протектор служит анодом и разрушается, предохраняя от коррозии металлическое изделие или конструкцию.
Электрохимическая (катодная) защита заключается в соединении защищаемого изделия с катодом внешнего источника тока, вследствие чего изделие становится катодом. Анодом служит вспомогательный, обычно стальной, электрод (кусок металла), который и разрушается в процессе коррозии.
Химия вокруг нас
Коррозия металлов
Слово коррозия происходит от латинского corrodere, что означает разъедать. Хотя коррозию чаще всего связывают с металлами, но ей подвергаются также камни, пластмассы и другие полимерные материалы и дерево. Например, в настоящее время мы являемся свидетелями большого беспокойства широких слоев людей в связи с тем, что от кислотных дождей катастрофически страдают памятники (здания и скульптуры), выполненные из известняка или мрамора.
Таким образом, коррозией называют самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды. Процессы физического разрушения к коррозии не относят, хотя часто они наносят неменьший вред памятникам культуры. Их называют истиранием, износом, эрозией.
Металлы составляют одну из основ цивилизации на планете Земля. Среди них как конструкционный материал явно выделяется железо. Объем промышленного производства железа примерно в 20 раз больше, чем объем производства всех остальных металлов, вместе взятых. Широкое внедрение железа в промышленное строительство и транспорт произошло на рубеже XVIII. XIX вв. В это время появился первый чугунный мост, спущено на воду первое судно, корпус которого был изготовлен из стали, созданы первые железные дороги. Однако начало практического использования человеком железа относят к IX в. до н.э. Именно в этот период человечество из бронзового века перешло в век железный. Тем не менее история свидетельствует о том, что изделия из железа были известны в Хеттском царстве (государство Малой Азии), а его расцвет относят к XIV. XIII вв. до н.э.
В природе, хотя и очень редко, но встречается самородное железо. Его происхождение считают метеоритным, т.е. космическим, а не земным. Поэтому первые изделия из железа (они изготавливались из самородков) ценились очень высоко – гораздо выше, чем из серебра и даже золота.
Несмотря на широкое внедрение в нашу сегодняшнюю жизнь полимерных материалов, стекла, керамики, основным конструкционным материалом продолжает оставаться железо и сплавы на его основе. С изделиями из железа мы на каждом шагу встречаемся в быту и знаем, как много хлопот доставляют его ржавление и сама ржавчина. Ржавлением называют только коррозию железа и его сплавов. Другие металлы корродируют, но не ржавеют. Хотя корродируют практически все металлы, в повседневной жизни человек чаще всего сталкивается с коррозией железа.
Строгие расчеты показывают, что большинство металлов имеет склонность к коррозии. Поэтому удивительно не то, что металлы корродируют, а то, что изделия из них могут существовать длительное время. Скорость, с которой протекает коррозия, не поддается теоретическому вычислению. Как правило, она определяется опытным путем. Скорость прежде всего зависит от характера образующихся продуктов коррозии и прочности их сцепления с металлом.
Сущность процессов коррозии
Коррозия металлов чаще всего сводится к их окислению и превращению в оксиды. В частности, коррозия железа может быть описана упрощенным уравнением
Гидратированный оксид железа Fе2O3·H2О и является тем, что люди называют ржавчиной. Это рыхлый порошок светло-коричневого цвета. Многие металлы при коррозии покрываются плотной, хорошо скрепленной с металлами оксидной пленкой, которая не позволяет кислороду воздуха и воде проникнуть в более глубокие слои и потому предохраняет металл от дальнейшего окисления. Например, алюминий – очень активный металл и теоретически с водой должен был бы взаимодействовать в соответствии с уравнением
Однако его поверхность покрывается плотной пленкой оксида Al2O3, которая защищает металл от воздействия воды и кислорода. По этой причине вода в алюминиевом чайнике при нагревании кипит, но не действует на металл и потому чайник служит довольно долгое время. Однако в воздухе часто содержатся оксиды серы, азота, углерода и другие, а в воде – растворенные газы и соли. Поэтому процесс коррозии и его продукты часто не столь простые. Например, бронзовые статуи, коррелируя, покрываются слоем зеленой патины, состав которой отвечает основному сульфату меди (II) (CuOH)2SO4. Следует отметить, что по недоразумению патину долго считали основным карбонатом меди (II).
Коррозия металлов бывает сплошной и местной. Сплошная коррозия не представляет особой опасности для конструкций и аппаратов особенно в тех случаях, когда потери металлов не превышают технически обоснованных норм. Ее последствия могут быть сравнительно легко учтены. Значительно опаснее местная коррозия, хотя потери металла здесь могут быть и небольшими. Один из наиболее опасных видов местной коррозии – это точечная. Она заключается в образовании сквозных поражений, т.е. в образовании точечных полостей – так называемых питтингов. Местной коррозии благоприятствуют морская вода, растворы солей, в частности галогенидных (хлорид натрия, магния и др.). Опасность местной коррозии состоит в том, что, снижая прочность отдельных участков, она резко уменьшает надежность конструкций, сооружений, аппаратов.
Особенно большие неприятности связаны с хлоридом натрия (в некоторых странах используют отход производства – хлорид кальция), разбрасываемым в зимнее время на дорогах и тротуарах для удаления снега и льда. В присутствии солей они плавятся и образующиеся растворы стекают в канализационные трубопроводы. Соли и особенно хлориды являются активаторами коррозии и приводят к ускоренному разрушению металлов, в частности транспортных средств и подземных коммуникаций. Подсчитано, что только в США применение для этой цели солей приводит к потерям на сумму 2 млрд долларов в год в связи с коррозией двигателей и 0,5 млрд на дополнительный ремонт дорог, подземных магистралей и мостов. Для работников коммунального хозяйства городов привлекательность хлорида натрия заключается в его дешевизне. К сожалению, пока не известно другое дешевое и эффективное средство. В настоящее время выход лишь один – вовремя убирать снег и вывозить его на свалки. Экономически он более чем оправдан.
По своей сущности коррозию делят на химическую и электрохимическую. Ржавление железа или покрытие патиной бронзы – химическая коррозия. Если эти процессы происходят на открытом воздухе в комнатных и особенно в природных условиях, то такую коррозию часто называют атмосферной. В промышленном производстве металлы нередко нагреваются до высоких температур и в таких условиях химическая коррозия ускоряется. Многие знают, что при прокатке раскаленных кусков металла образуется окалина. Это типичный продукт химической коррозии. Окалина получается и при простой разливке на воздухе расплавленного металла в изложницы.
Установлено, что коррозии железа способствует наличие в нем серы. Современных людей поражает устойчивость к коррозии некоторых античных предметов, изготовленных из железа. Одной из причин этого является низкое содержание в нем серы. Обычно в железо она попадает из каменного угля при доменной выплавке из руд. В далеком прошлом для этой цели использовался не каменный, а древесный уголь, который практически не содержит серы. Сера в железе обычно содержится в виде сульфидов FeS и др. В процессе коррозии сульфиды железа разлагаются с выделением сероводорода H2S, который является катализатором коррозии железа.
Особенно разнообразные процессы химической коррозии встречаются в различных химических производствах. В атмосфере водорода, метана и других углеводородов, оксида углерода (II), сероводорода, хлора, в среде кислот, щелочей, солей, а также в расплавах солей и других веществ протекают специфические реакции с вовлечением материала аппаратов и агрегатов, в которых осуществляется химический процесс. Задача специалистов при конструировании реактора – подобрать металл или сплав, который был бы наиболее устойчив к компонентам химического процесса.
Строго отделить химическую коррозию от электрохимической трудно, а иногда и невозможно. Дело в том, что электрохимическая коррозия часто связана с наличием в металле случайных примесей или специально введенных легирующих добавок.
Многие неопытные химики в разное время были озадачены тем, что иногда реакция
описанная во всех учебниках, не идет. Более опытные химики знают, что в такой ситуации в раствор нужно добавить немного сульфата меди (П) (медного купороса). В этом случае на поверхности цинка выделится медь
и водород начнет бурно выделяться. При объяснении данного явления в 1830 г. швейцарским химиком А. де-ля Ривом была создана первая электрохимическая теория коррозии.
Вскоре после открытия итальянцем Л. Гальвани электрохимического явления его соотечественник А. Вольта сконструировал (1800) источник электрического тока (гальванический элемент), что открыло человечеству эру электричества. В одном из вариантов источник состоял из чередующихся медных и цинковых дисков, разделенных пористым материалом, пропитанным раствором соли (вольтов столб). В зависимости от числа дисков получается ток различной силы. При осаждении на поверхности цинка металлической меди получается коротко-замкнутый элемент. В нем цинк является анодом, а медь – катодом. Поскольку медь находится в контакте с цинком и оба эти металла окружены раствором электролита, гальванический элемент оказывается «включенным». Цинк в виде иона Zn 2+ переходит в раствор серной кислоты, а оставшиеся от каждого атома два электрона перетекают на более электроположительный металл – медь:
медному катоду подходят ионы водорода, принимают электроны и превращаются в атомы водорода, а затем и в молекулы водорода:
Таким образом, потоки движения ионов разделены и при избытке кислоты процесс протекает до тех пор, пока не растворится весь цинк.
Сущность первой электрохимической теории состояла в том, что примеси в металлах создают микрогальванические элементы, в которых происходит перетекание электронов от анодных участков к катодным. Поскольку катодный и анодный процессы разделены на поверхности, то разделены и противоположные потоки ионов, атомов и молекул. Разделенные потоки не мешают друг другу и по этой причине процесс коррозии протекает быстрее, чем в случае отсутствия микрогальванических элементов. Конечно, в настоящее время теории электрохимической коррозии выглядят гораздо более совершенными. Они основаны на многочисленных экспериментальных фактах и выражены в математической форме. Здесь мы не имеем возможности углубляться в детали.
Коррозия металлов наносит большой экономический вред. Человечество несет огромные материальные потери в результате коррозии трубопроводов, деталей машин, судов, мостов, морских конструкций и технологического оборудования. Коррозия приводит к уменьшению надежности работы оборудования: аппаратов высокого давления, паровых котлов, металлических контейнеров для токсичных и радиоактивных веществ, лопастей и роторов турбин, деталей самолетов и т.д. С учетом возможной коррозии приходится завышать прочность этих изделий, а значит, увеличивать расход металла, что приводит к дополнительным экономическим затратам. Коррозия приводит к простоям производства из-за замены вышедшего из строя оборудования, к потерям сырья и продукции (утечка нефти, газов, воды), к энергетическим затратам для преодоления дополнительных сопротивлений, вызванных уменьшением проходных сечений трубопроводов из-за отложения ржавчины и других продуктов коррозии. Коррозия также приводит к загрязнению продукции, а значит, и к снижению ее качества. Затраты на возмещение потерь, связанных с коррозией, исчисляются миллиардами рублей в год. Специалисты подсчитали, что в развитых капиталистических странах стоимость потерь, связанных с коррозией, составляет 3. 4% валового национального дохода.
За долгий период интенсивной работы металлургической промышленности выплавлено огромное количество металла и переведено в изделия. Этот металл постоянно корродирует. Сложилась такая ситуация, что потери металла от коррозии в мире уже составляют около 30% от его годового производства. Считается, что 10% прокорродировавшего металла теряется (в основном в виде ржавчины) безвозвратно. Возможно, в будущем установится баланс, при котором от коррозии будет теряться примерно столько же металла, сколько его будет выплавляться вновь. Из всего сказанного следует, что важнейшей проблемой является изыскание новых и совершенствование старых способов защиты от коррозии.
Способы защиты от коррозии
Проблема защиты металлов от коррозии возникла почти в самом начале их использования. Люди пытались защитить металлы от атмосферного воздействия с помощью жира, масел, а позднее и покрытием другими металлами и прежде всего легкоплавким оловом (лужением). В трудах древнегреческого историка Геродота (V в. до н.э.) уже имеется упоминание о применении олова для защиты железа от коррозии.
Задачей химиков было и остается выяснение сущности явлений коррозии, разработка мер, препятствующих или замедляющих ее протекание. Коррозия металлов осуществляется в соответствии с законами природы и потому ее нельзя полностью устранить, а можно лишь замедлить. Имеется способ уменьшения коррозии металлов, который строго нельзя отнести к защите, – это легирование металлов, т.е. получение сплавов. Например, в настоящее время создано большое число нержавеющих сталей путем присадок к железу никеля, хрома, кобальта и др. Такие стали, действительно, не покрываются ржавчиной, но их поверхностная коррозия хотя и с малой скоростью, но имеет место. Оказалось, что при добавлении легирующих добавок коррозионная стойкость меняется скачкообразно. Установлено правило (правило Таммана), согласно которому резкое повышение устойчивости к коррозии железа наблюдается при введении легирующей добавки в количестве 1/8 атомной доли, т.е. один атом легирующей добавки приходится на восемь атомов железа. Считается, что при таком соотношении атомов происходит их упорядоченное расположение в кристаллической решетке твердого раствора, что и затрудняет коррозию. Одним из наиболее распространенных способов защиты металлов от коррозии является нанесение на их поверхность защитных пленок: лака, краски, эмали, других металлов. Лакокрасочные покрытия наиболее доступны для широкого круга людей. Лаки и краски обладают низкой газо- и паропроницаемостью, водоотталкивающими свойствами и поэтому препятствуют доступу к поверхности металла воды, кислорода и содержащихся в атмосфере агрессивных компонентов. Покрытие поверхности металла лакокрасочным слоем не исключает коррозию, а служит для нее лишь преградой, а значит, лишь тормозит коррозию. Поэтому важное значение имеет качество покрытия – толщина слоя, сплошность (пористость), равномерность, проницаемость, способность набухать в воде, прочность сцепления (адгезия). Качество покрытия зависит от тщательности подготовки поверхности и способа нанесения защитного слоя. Окалина и ржавчина должны быть удалены с поверхности покрываемого металла. В противном случае они будут препятствовать хорошей адгезии покрытия с поверхностью металла. Низкое качество покрытия нередко связано с повышенной пористостью. Часто она возникает в процессе формирования защитного слоя в результате испарения растворителя и удаления продуктов отверждения и деструкции (при старении пленки). Поэтому обычно рекомендуют наносить не один толстый слой, а несколько тонких слоев покрытия. Во многих случаях увеличение толщины покрытия приводит к ослаблению адгезии защитного слоя с металлом. Большой вред наносят воздушные полости, пузыри. Они образуются при низком качестве выполнения операции нанесения покрытия.
Для снижения смачиваемости водой лакокрасочные покрытия иногда, в свою очередь, защищают восковыми составами или кремнийорганическими соединениями. Лаки и краски наиболее эффективны для защиты от атмосферной коррозии. В большинстве случаев они непригодны для защиты подземных сооружений и конструкций, так как трудно предупредить механические повреждения защитных слоев при контакте с грунтом. Опыт показывает, что срок службы лакокрасочных покрытий в этих условиях невелик. Намного практичнее оказалось применять толстослойные покрытия из каменноугольной смолы (битума).
В некоторых случаях пигменты красок выполняют также роль ингибиторов коррозии. К числу таких пигментов относятся хроматы стронция, свинца и цинка (SrCrO4, PbCrO4, ZnCrO4).
Часто под лакокрасочный слой наносят слой грунтовки. Пигменты, входящие в ее состав, также должны обладать ингибиторными-свойствами. Проходя через слой грунтовки, вода растворяет некоторое количество пигмента и становится менее коррозионноактивной. Среди пигментов, рекомендуемых для грунтов, наиболее эффективным признан свинцовый сурик Рb3O4.
Вместо грунтовки иногда проводят фосфатирование поверхности металла. Для этого на чистую поверхность кистью или напылителем наносят растворы ортофосфатов железа (III), марганца (II) или цинка (II), содержащих и саму ортофосфорную кислоту H3PO4. В нашей стране для этой цели применяют 3%-ный раствор смеси кислых солей Fe(H2PO4)3 и Мn(H2PO4)2 с добавками KNO3 или Cu(NO3)2 в качестве ускорителей. В заводских условиях фосфатирование ведут при 97. 99°C в течение 30. 90 мин. В образование фосфатного покрытия вносят вклад металл, растворяющийся в фосфатирующейся смеси, и оставшиеся на его поверхности оксиды.
Для фосфатирования поверхности стальных изделий разработано несколько различных препаратов. Большинство из них состоит из смесей фосфатов марганца и железа. Возможно, наиболее распространенным препаратом является «мажеф» – смесь дигидрофосфатов марганца Mn(H2PO4)2, железа Fe(H2PO4)2 и свободной фосфорной кислоты. Название препарата состоит из первых букв компонентов смеси. По внешнему виду мажеф – это мелкокристаллический порошок белого цвета с соотношением между марганцем и железом от 10:1 до 15:1. Он состоит из 46. 52% P2O5; не менее 14% Mn; 0,3. 3,0% Fe. При фосфатировании мажефом стальное изделие помещается в его раствор, нагретый примерно до 100°C. В растворе происходит растворение с поверхности железа с выделением водорода, а на поверхности образуется плотный, прочный и малорастворимый в воде защитный слой фосфатов марганца и железа серо-черного цвета. При достижении толщины слоя определенной величины дальнейшее растворение железа прекращается. Пленка фосфатов защищает поверхность изделия от атмосферных осадков, но мало эффективна от растворов солей и даже слабых растворов кислот. Таким образом, фосфатная пленка может служить лишь грунтом для последующего нанесения органических защитных и декоративных покрытий – лаков, красок, смол. Процесс фосфатирования длится 40. 60 мин. Для ускорения фосфатирования в раствор вводят 50. 70 г/л нитрата цинка. В этом случае время фосфатирования сокращается в 10. 12 раз.
В производственных условиях используют также электрохимический способ – обработку изделий переменным током в растворе фосфата цинка при плотностях тока 4 А/дм 2 и напряжении 20 В и при температуре 60. 70°C. Фосфатные покрытия представляют собой сетку плотносцепленных с поверхностью фосфатов металлов. Сами по себе фосфатные покрытия не обеспечивают надежной коррозионной защиты. Преимущественно их используют как основу под окраску, обеспечивающую хорошее сцепление краски с металлом. Кроме того, фосфатный слой уменьшает коррозионные разрушения при образовании царапин или других дефектов.
Для защиты металлов от коррозии используют стекловидные и фарфоровые эмали – силикатные покрытия, коэффициент теплового расширения которых должен быть близок к таковому для покрываемых металлов. Эмалирование осуществляют нанесением на поверхность изделий водной суспензии или сухим напудриванием. Вначале на очищенную поверхность наносят грунтовочный слой и обжигают его в печи. Далее наносят слой покровной эмали и обжиг повторяют. Наиболее распространены стекловидные эмали – прозрачные или заглушенные. Их компонентами являются SiO2 (основная масса), B2O3, Na2O, PbO. Кроме того, вводят вспомогательные материалы: окислители органических примесей, оксиды, способствующие сцеплению эмали с эмалируемой поверхностью, глушители, красители. Эмалирующий материал получают сплавлением исходных компонентов, измельчением в порошок и добавлением 6. 10% глины. Эмалевые покрытия в основном наносят на сталь, а также на чугун, медь, латунь и алюминий.
Эмали обладают высокими защитными свойствами, которые обусловлены их непроницаемостью для воды и воздуха (газов) даже при длительном контакте. Их важным качеством является высокая стойкость при повышенных температурах. К основным недостаткам эмалевых покрытий относят чувствительность к механическим и термическим ударам. При длительной эксплуатации на поверхности эмалевых покрытий может появиться сетка трещин, которая обеспечивает доступ влаги и воздуха к металлу вследствие чего и начинается коррозия.
Для защиты чугунных и стальных водяных труб от коррозии используют цементные покрытия. Поскольку коэффициенты теплового расширения портландцемента и стали близки, а стоимость цемента невысокая, то он довольно широко применяется для этих целей. Недостаток портландцементных покрытий тот же, что и эмалевых, – высокая чувствительность к механическим ударам.
Широко распространенным способом защиты металлов от коррозии является покрытие их слоем других металлов. Покрывающие металлы сами корродируют с малой скоростью, так как покрываются плотной оксидной пленкой. Покрывающий слой наносят различными методами: кратковременным погружением в ванну с расплавленным металлом (горячее покрытие), электроосаждением из водных растворов электролитов (гальваническое покрытие), напылением (металлизация), обработкой порошками при повышенной температуре в специальном барабане (диффузионное покрытие), с помощью газофазной реакции, например 3CrCl2 + 2Fe – [1000°C] → 2FeCl3 + 3Cr (в сплаве с Fe).
Имеются и другие методы нанесения металлических покрытий, например, разновидностью диффузионного способа защиты металлов является погружение изделий в расплав хлорида кальция CaCl2, в котором растворены наносимые металлы.
В производстве широко используют химическое нанесение металлических покрытий на изделия. Процесс химического металлирования является каталитическим или автокаталитическим, а катализатором является поверхность изделия. Раствор, используемый для металлизации, содержит соединение наносимого металла и восстановитель. Поскольку катализатором является поверхность изделия, выделение металла и происходит именно на ней, а не в объеме раствора. В автокаталитических процессах катализатором является металл, наносимый на поверхность. В настоящее время разработаны методы химического покрытия металлических изделий никелем, кобальтом, железом, палладием, платиной, медью, золотом, серебром, родием, рутением и некоторыми сплавами на основе этих металлов. В качестве восстановителей используют гипофосфит и боргидрид натрия, формальдегид, гидразин. Естественно, что химическим никелированием можно наносить защитное покрытие не на любой металл. Чаще всего ему подвергают изделия из меди.
Металлические покрытия делят на две группы: коррозионностойкие и протекторные. Например, для покрытия сплавов на основе железа в первую группу входят никель, серебро, медь, свинец, хром. Они более электроположительны по отношению к железу, т.е. в электрохимическом ряду напряжений металлов стоят правее железа. Во вторую группу входят цинк, кадмий, алюминий. По отношению к железу они более электроотрицательны, т.е. в ряду напряжений находятся левее железа.
В повседневной жизни человек чаще всего встречается с покрытиями железа цинком и оловом. Листовое железо, покрытое цинком, называют оцинкованным железом, а покрытое оловом – белой жестью. Первое в больших количествах идет на кровли домов, а из второго изготавливают консервные банки. И то и другое получают главным образом протягиванием листа железа через расплав соответствующего металла. Для большей стойкости водопроводные трубы и арматуру из стали и серого чугуна часто подвергают оцинковыванию также окунанием в расплав данного металла. Это резко повышает срок их службы в холодной воде. Интересно, что в теплой и горячей воде срок службы оцинкованных труб может быть даже меньше, чем неоцинкованных.
Испытания показали, что оцинкованная жесть при толщине покрытия в 0,03 мм, что соответствует 0,036 г/см 2 при покрытии с двух сторон, на крышах домов служит примерно 8 лет. В промышленной атмосфере (в атмосфере больших городов) она же служит всего лишь четыре года. Такое уменьшение срока службы связано с воздействием серной кислоты, содержащейся в воздухе городов.
Покрытия из цинка и олова (так же как и других металлов) защищают железо от коррозии при сохранении сплошности. При нарушении покрывающего слоя (трещины, царапины) коррозия изделия протекает даже более интенсивно, чем без покрытия. Это объясняется «работой» гальванического элемента железо – цинк и железо – олово. Трещины и царапины заполняются влагой и образуются растворы. Поскольку цинк более электроотрицателен, чем железо, то его ионы будут преимущественно переходить в раствор, а остающиеся электроны будут перетекать на более электроположительное железо, делая его катодом (рис. 2)
Рис. 2. Схема коррозии оцинкованного железа
К железу-катоду будут подходить ионы водорода (вода) и разряжаться, принимая электроны. Образующиеся атомы водорода объединяются в молекулу H2. Таким образом, потоки ионов будут разделены и это облегчает протекание электрохимического процесса. Растворению (коррозии) будет подвергаться цинковое покрытие, а железо до поры до времени будет защищено. Цинк электрохимически защищает железо от коррозии. На этом принципе основан протекторный метод защиты от коррозии металлических конструкций и аппаратов. Английское слово «претект» – означает защищать, предохранять. При протекторной защите к конструкции, к аппарату через проводник электрического тока присоединяется кусок более электроотрицательного металла. Его можно поместить прямо в паровой котел.
При наличии влаги, а точнее в присутствии электролита начнет действовать гальванический элемент. В нем будет растворяться более электроотрицательный металл, а конструкция или аппарат оказываются катодно защищенными. Защита будет действовать до тех пор, пока полностью не растворится анод – более электроотрицательный металл.
Вероятно, впервые катодную защиту применил знаменитый английский ученый Дэви (1824). Для защиты медной облицовки морских судов он рекомендовал использовать «жертвенные» аноды из железа, которые присоединялись снаружи к корпусу судна. Скорость коррозии медной облицовки в морской воде при этом, действительно, значительно снизилась. Однако вместо одной неприятности появилась другая. Ионы меди Cu 2+ являются биоцидными (ядовитыми) для микроорганизмов. Поскольку медный корпус оказался защищенным и ионы меди перестали переходить в морскую воду, то корпус оказался беззащитным от микроорганизмов. Они стали поселяться на корпусе судна, что приводило к обрастанию ракушками. В результате скоростные характеристики судна значительно снизились. Периодическая очистка днища судна от ракушек стоила больших затрат.
С протекторной защитой весьма сходна катодная защита металлов от коррозии. Можно сказать, что катодная защита является модификацией протекторной защиты. В данном случае конструкция или корпус корабля присоединяются к катоду источника постоянного тока и тем самым защищаются от растворения.
Рис. 3. Схема коррозии белой жести
Считают, что нанесение олова на поверхность металлов (лужение) было освоено уже в бронзовом веке. Этому способствовала низкая температура плавления олова. В прошлом особенно часто проводили лужение медной и латунной посуды: тазов, котлов, кувшинов, самоваров и др. Продукты коррозии олова безвредны для человека, поэтому луженая посуда широко применялась в быту. В XV в. во многих странах Европы (Германии, Австрии, Голландии, Англии и Франции) широко использовалась столовая посуда, изготовленная из олова. Имеются сведения, что в рудных горах Богемии оловянные ложки, чашки, кувшины, тарелки начали изготавливать уже в XII в.
Луженое железо до сих пор в больших количествах идет на изготовление тары для хранения пищевых продуктов (консервные банки). Однако в последние годы для этой цели все шире применяется алюминиевая фольга. Посуда из цинка и оцинкованного железа не рекомендуется для хранения пищевых продуктов. Несмотря на то, что металлический цинк покрыт плотной оксидной пленкой, он все же подвергается растворению. Хотя соединения цинка относительно мало ядовиты, в больших количествах они могут оказать вредное действие.
Говоря о металлической таре, уместно отметить, что патент на способ сохранения пищевых продуктов в жестяных банках был выдан парижскому повару Н.Ф. Апперу в 1810 г. Он запаивал продукты в банках из белой жести, а затем нагревал в кипящей соленой воде.
Современная техника включает детали и конструкции из различных металлов и сплавов. Если они находятся в контакте и попадают в раствор электролитов (морская вода, растворы любых солей, кислот и щелочей), то может образоваться гальванический элемент. Более электроотрицательный металл становится анодом, а более электроположительный – катодом. Генерирование тока будет сопровождаться растворением (коррозией) более электроотрицательного металла. Чем больше разность электрохимических потенциалов контактирующих металлов, тем больше скорость коррозии. Почти все книги, особенно популярные, по коррозии металлов описывают случай, произошедший в 20-х годах текущего столетия в США. Один из американских миллионеров, не жалея денег, решил построить самую шикарную яхту. Ее днище было обшито дорогим монель металлом (сплав 70% никеля и 30% меди), а киль, форштевень и раму руля изготовили из стали. В морской воде в подводной части яхты образовался гальванический элемент с катодом из монель металла, а анодом из стали. Он настолько энергично работал, что яхта еще до завершения отделочных работ вышла из строя, ни разу не побывав в море. Интересно, что яхте было дано имя «Зов моря».
Иногда зубные коронки, изготовленные из различных металлов (золота и стали) и близко расположенные друг к другу, доставляют их носителям неприятнейшие болевые ощущения. Поскольку слюна является электролитом, эти коронки образуют гальванический элемент. Электрический ток протекает по десне и вызывает зубную боль.
Пассивация металлов
Каждый школьник знает, что серная кислота взаимодействует с железом в соответствии с уравнением
Несколько иначе идет реакция железа с HNO3:
Вероятно, многие обратили внимание на то, что серную и азотную кислоты перевозят по железной дороге в стальных цистернах. Об этом свидетельствуют надписи, например «Осторожно, серная кислота». Как это согласуется с теми знаниями, которые отражены в школьных учебниках? Все дело в том, что по железной дороге перевозят не разбавленные, а концентрированные кислоты. Зачем же перевозить воду? Разбавить кислоту можно и на месте потребления.
Оказывается, что в отличие от разбавленных концентрированная серная, так же как и концентрированная азотная кислоты, не взаимодействует с железом. Правильнее сказать, что кратковременное взаимодействие происходит, но оно быстро прекращается. Специалисты говорят, что в крепких растворах этих кислот железо пассивируется. Еще в 1836 г. знаменитый английский химик М. Фарадей высказал предположение, что причиной пассивации является образование на поверхности металла плотной оксидной пленки. В свое время на это предположение не обратили должного внимания. Лишь через 100 лет эти взгляды возродил и развил известный русский ученый В.А. Кистяковский. После него этот взгляд на пассивацию оформился в виде теории. Согласно ей при пассивации на поверхности металла образуется сплошная и плотная оксидная (реже хлоридная, сульфатная, фосфатная) пленка толщиной в несколько десятков нанометров. Например, на поверхности железа образуется оксидная пленка нестехиометрического состава Fe8O11, Fe3O4.
Имеется и другой взгляд на причину пассивации металлов, согласно которому она обусловлена слоем адсорбированного кислорода или какого-либо другого окислителя. Считают, что при адсорбции происходит насыщение валентности поверхностных атомов металла, что и приводит к снижению его химической активности.
Первая теория наиболее распространена, хотя не исключено, что в разных случаях процессы пассивации согласуются то с одной, а то с другой теорией.
Металлы можно перевести в пассивное состояние не только под действием окислителей, но и электрохимически, подав на них положительный потенциал.
Способность металлов пассивироваться широко используют для их защиты от коррозии. Например, известно, что хранение лезвий безопасных бритв в растворах солей хромовых кислот позволяет дольше сохранять их острыми. В ином случае под действием влажного воздуха железо, особенно на острие лезвия, окисляется и покрывается рыхлым слоем ржавчины.
Пассивируя металл, т.е. создавая оксидные или солевые пленки, можно проводить окраску или тонирование металлов. Толщина таких пленок соизмерима с длиной волны видимого света, поэтому цвет тонированной поверхности зависит от толщины покрытия и цвета металла. Для химического оксидирования с целью окраски широко используют персульфатный раствор, а для электрохимического – изделие делают анодом. В последнем случае говорят, что окрашивание проводят путем анодирования. Тонированию чаще всего подвергают изделия из меди и ее сплавов, а также из алюминия, олова, никеля.
Тонирование может также обусловливаться сульфидной пленкой. Приводим распространенный состав тонирующего раствора: CuSO4 (10. 12 г/л), Pb(NO3)2 (10. 12 г/л), Na2S2O3 (100. 180 г/л), сегнетова соль (15. 20 г/л). Тонирование изделий при комнатной температуре в этом растворе позволяет получить следующую цветовую гамму: желтый (5 мин), коричневый (7 мин), красный (10 мин), фиолетовый (13 мин), синий (17 мин), зеленый (20 мин). Электрохимический метод тонирования отличается более широкой цветовой гаммой и лучшей воспроизводимостью цветов по сравнению с химическим.
Издавна известен процесс воронения и синения сталей. По существу, это термический способ их оксидирования. Его проводят на воздухе при температуре 350. 360°C. Поверхность изделий предварительно покрывают тонким слоем 15. 20%-ного раствора асфальтового лака в бензине и подсушивают на воздухе. Такой же эффект может быть получен при оксидирующей обработке изделий в кипящем растворе щелочи в присутствии нитратов и нитритов щелочных металлов.
К сказанному можно добавить, что оксидирование металлов в промышленных масштабах осуществляют не только для их противокоррозионной защиты и декорировки изделий, но и для придания электроизоляционных свойств поверхностному слою и увеличению коэффициента отражения зеркал. Оксидный слой также используют в качестве грунта под окраску и лакировку.
Ингибиторы коррозии металлов
Применение ингибиторов – один из эффективных способов борьбы с коррозией металлов в различных агрессивных средах (в атмосферных, в морской воде, в охлаждающих жидкостях и солевых растворах, в окислительных условиях и т.д.). Ингибиторы – это вещества, способные в малых количествах замедлять протекание химических процессов или останавливать их. Название ингибитор происходит от лат. inhibere, что означает сдерживать, останавливать. Ингибиторы взаимодействуют с промежуточными продуктами реакции или с активными центрами, на которых протекают химические превращения. Они весьма специфичны для каждой группы химических реакций. Коррозия металлов – это лишь один из типов химических реакций, которые поддаются действию ингибиторов. По современным представлениям защитное действие ингибиторов связано с их адсорбцией на поверхности металлов и торможением анодных и катодных процессов.
Первые ингибиторы были найдены случайно, опытным путем, и часто становились клановым секретом. Известно, что дамасские мастера для снятия окалины и ржавчины пользовались растворами серной кислоты с добавками пивных дрожжей, муки, крахмала. Эти примеси были одними из первых ингибиторов. Они не позволяли кислоте действовать на оружейный металл, в результате чего растворялись лишь окалина и ржавчина.
Ингибиторами, не зная того, давно пользовались и на Руси. Уральские оружейники для борьбы с ржавчиной готовили «травильные супы» – растворы серной кислоты, в которые добавлялись мучные отруби. Одним из наиболее простых ингибиторов атмосферной коррозии металлов является нитрит натрия NaNO2. Его используют в виде концентрированных водных растворов, а также растворов, загущенных глицерином, оксиэтилцеллюлозой или карбоксиметилцеллюлозой. Нитрит натрия используют для консервирования изделий из стали и чугуна. Для первой применяют. 25%-ные водные растворы, а для второго – 40%-ные. После обработки (обычно окунанием в растворы) изделия заворачивают в парафиновую бумагу. Лучшим действием обладают загущенные растворы. Срок хранения изделий, обработанных загущенными растворами, увеличивается в 3. 4 раза по сравнению с водными растворами.
По данным 1980 г., число известных науке ингибиторов коррозии превысило 5 тыс. Считают, что 1 т ингибитора дает в народном хозяйстве экономию около 5000 руб.
Работа по борьбе с коррозией имеет важнейшее народнохозяйственное значение. Это весьма благодатная область для приложения сил и способностей.