в чем разница между металлами и неметаллами
Разница между металлами и неметаллами
Химики разделили все простые вещества на металлы и неметаллы. Они сильно различаются по строению, физическим и химическим свойствам. Многие из них легко отличить визуально, например медь – металл, а бром – неметалл. Однако чтобы не допустить ошибку при классификации элементов, лучше опираться на знание четких признаков, свойственных металлам и неметаллам.
Определение
Элементы, отдающие электроны с внешнего энергетического уровня, называют металлами. Металлы – это, как правило, твердые вещества (особняком стоит ртуть, которая при нормальных условиях является жидкостью).
Элементы, принимающие электроны на внешний энергетический уровень, являются неметаллами. Они находятся в различных агрегатных состояниях. Кислород и азот – это газы, бром – жидкость, а к твердым веществам относятся, например, мышьяк, углерод и бор.
Сравнение
Все металлы наделены металлическим блеском, они превосходные проводники электрического тока и тепла. Большинство из них пластичны, при физическом воздействии металлы легко меняют форму. Неметаллы, наоборот, плохие проводники тепла и электрического тока.
Строение металлов и неметаллов – главная отличительная характеристика. Неметаллы – обладатели большего числа неспаренных электронов, размещающихся на внешних уровнях. Металлы имеют металлическую кристаллическую решетку. А неметаллам присущи молекулярные (к примеру, кислороду, хлору и сере) и атомарные (углероду, образующему алмаз) кристаллические решетки.
У металлов маленькая электроотрицательность, а значит и окислительно-восстановительный потенциал невелик. Они, как правило, принимают электроны и окисляются, проявляя восстановительные свойства. Неметаллы, наделенные большой электроотрицательностью и значительным окислительно-восстановительным потенциалом, могут выступать как в качестве окислителей, так и в качестве восстановителей (такое возможно в присутствии наиболее мощного окислителя).
У металлов есть весьма интересное свойство – амфотерность. Амфотерным металлам присущи свойства и металлов, и неметаллов. Например, цинк, находясь в состоянии высшей степени окисления, ведет себя как неметалл.
Металлы и неметаллы – в чем разница и как понять, когда металлические свойства усиливаются, а когда ослабевают
Одни отдают электроны, другие принимают.
Металлы – это такие элементы, которые стараются отдавать свои электроны. Неметаллы – наоборот, стараются их принимать. Вам надо понять, почему это происходит, и что значат фразы типа «металлические свойства усиливаются, а неметаллические ослабевают». Сейчас я вам это объясню.
Почему металлические свойства слабеют «слева направо»
Протоны и нейтроны находятся в ядре. Поэтому заряд ядра всегда плюсовой. А электроны крутятся вокруг ядра и притягиваются к нему, потому что у них заряд минусовой.
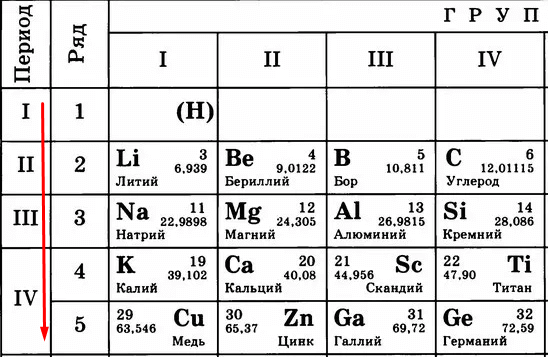
Электроны крутятся по электронным уровням – как планеты по орбитам вокруг Солнца.
Атомный номер показывает, сколько в атоме протонов. Как видите, это количество постоянно увеличивается.
Чем больше протонов, тем сильнее они «тянут» к себе электроны. Сравните:
Вывод – чем больше становится протонов, тем сильнее они удерживают электроны. Тем сложнее становится эти электроны отдавать. Поэтому слева направо, с увеличением порядкового номера (и, соответственно, числа протонов) металлические свойства слабеют, а неметаллические усиливаются.
На заметку – про радиус атома
Чем сильнее протоны притягивают электроны, тем ближе эти электроны становятся к протонам. Поэтому радиус атома уменьшается, атом как бы сжимается из-за увеличения заряда.
Почему неметаллические свойства слабеют «сверху вниз»
Идем дальше. Период в таблице показывает количество уровней (тех самых орбит), по которым летают электроны.
Чем больше период, тем больше этих орбит и тем дальше оказываются электроны от ядра. Сравните:
Кому сложнее удерживать электроны на последнем уровне? Меди, конечно, потому что эти электроны в два раза дальше от ядра, чем, например, у лития. Их проще становится отдать, чем пытаться удерживать.
Следовательно, «сверху вниз» количество уровней, по которым движутся электроны, растет, удерживать их становится сложнее, поэтому металлические свойства усиливаются, а неметаллические – слабеют.
Если смотреть на таблицу «сверху вниз» радиус ядра растет, потому что уровней становится больше.
Да, заряд атома тоже растет, но все-таки расстояние перевешивает. Чем больше уровней, тем труднее становится держать электроны, даже несмотря на то, что заряд увеличивается.
Из этих двух положений следует, что в правом углу таблицы Менделеева будут сосредоточены неметаллы, а в левом – металлы.
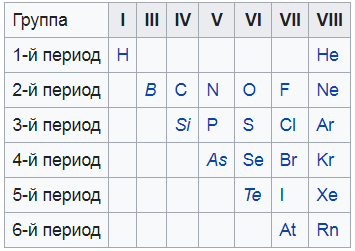
Я нашел вам вот такую картинку, на ней показаны все неметаллы. То, что выделено курсивом – это так называемые металлоиды – вроде и не совсем металлы, и в то же время не неметаллы. Нечто среднее.
Это основа основ. Надеюсь, я объяснил понятно и вы разобрались. Если нет – перечитайте еще раз, задайте вопросы мне в комментариях. Только когда разберетесь – читайте дальше.
Свойства металлов
Эти свойства проявляются в разной мере, но все-таки присущи всем металлам:
На сегодняшний день металлов известно 87.
Свойства неметаллов
У них почти все наоборот:
Неметаллов на данный момент 22.
Это первая статья по химии на нашем сайте. Напишите, что не так, что нравится и не нравится. Я буду думать, как сделать материал лучше.
И еще – есть идея записывать видеоролики с объяснениями. Лично вам удобнее разбираться в чем-то, читая текст, или просматривая видео?
Буду рад каждому вашему отзыву и комментарию.
Металлы и неметаллы: сравнительная характеристика
Все химические элементы условно можно разделить на неметаллы и металлы. Знаете ли вы, по каким признакам они отличаются? Как определить их положение в таблице химических элементов? На эти и другие вопросы вы найдете ответы в нашей статье.
Положение неметаллов и металлов: таблица Менделеева
По внешним признакам и физическим свойствам не всегда можно выяснить, к какой группе относится химический элемент. Свойства металлов и неметаллов можно определить по расположению в периодической таблице.

Энергетический уровень
Отличия неметаллов и металлов первоначально обусловлены строением их атомов. Начнем с количества электронов на внешнем энергетическом уровне. У атомов металлов оно варьирует от одного до трех. Как правило, они обладают большим радиусом, поэтому атомы металлов достаточно легко отдают наружные электроны, так как имеют сильные восстановительные свойства.
У неметаллов число электронов на внешнем уровне больше. Это объясняет их окислительную активность. Неметаллы присоединяют недостающие электроны, полностью заполняя энергетический уровень. Самые сильные окислительные свойства проявляют неметаллы второго и третьего периода VI-VII групп.
Заполненный энергетический уровень содержит 8 электронов. Самой большой окислительной способностью обладают галогены с валентностью I. Среди них лидирует фтор, так как у этого элемента нет свободных орбиталей.
Строение металлов и неметаллов: кристаллические решетки
У некоторых неметаллов формируется атомная кристаллическая решетка, частицы которой соединены ковалентными связями. Вещества с таким строением твердые и нелетучие. К примеру, фосфор, кремний и графит.
Физические свойства
Металлическая связь обусловливает ковкость и пластичность. По этим показателям лидирует золото, из которого можно раскатать лист толщиной в человеческий волос.
Что такое полуметаллы
В периодической таблице между металлами и неметаллами находится ряд химических элементов, которые занимают промежуточное положение. Их называют полуметаллами. Атомы полуметаллов связаны ковалентной химической связью.
Итак, типичные неметаллы и металлы обладают противоположными свойствами, но деление это достаточно условно, поскольку ряд веществ сочетает в себе и те и другие признаки.
Металлы и неметаллы
Содержание:
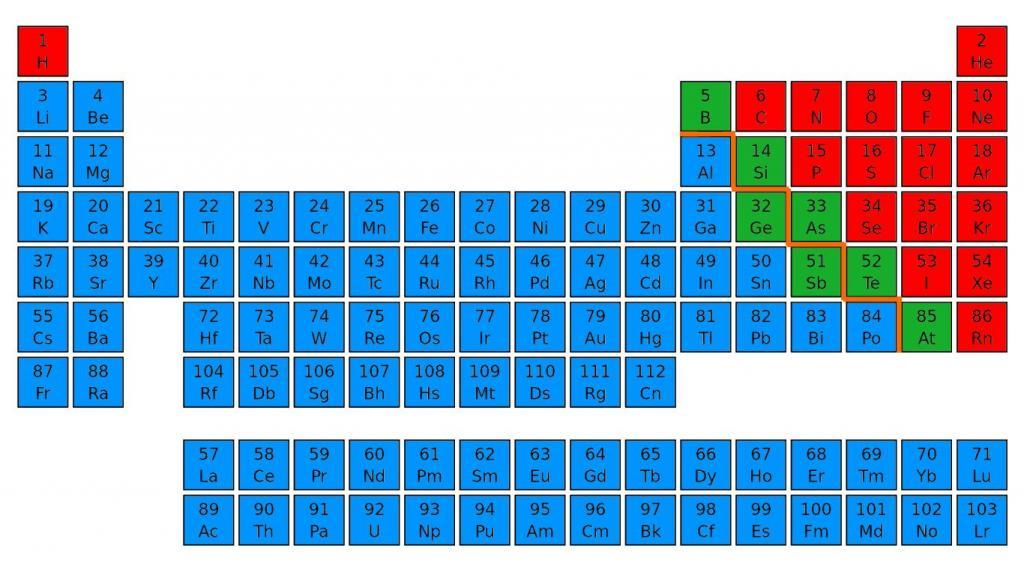
Неметаллы – это все элементы (и простые вещества), не являющиеся металлами. В нашей периодической таблице символы неметаллов красные, а металлов – синие.
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Металлы и неметаллы
Весь естественный мир состоит из химических элементов И даже далекие галактики состоят из тех же химических элементов что и наша Земля.
Химические элементы делятся на металлы и неметлллы
Все металлы (кроме ртути) твердые при нормальных условиях. Однако твердость их различна.
Некоторые неметллы в свободном виде при комнатной температуре являются газами, другие — твердые, и один — жидкий.
Металлы и неметаллы отличаются в первую очередь строением. Изобразим строение атома натрия и хлора
Сравните строение их внешних уровней. Легко заметить, что у металлов небольшое число электронов поэтому они легко отдают наружные электроны и проявляют восстановительные свойства. Склонность металла отдавать электроны зависит от его строения прежде всего, от размера атомов: чем больше атомные радиусы, тем легче металл отдает электроны.
В периодической системе свойства металлов и неметаллов изменяются в периодах и группах (рис. 36).
Наблюдаются раличия и в радиусах атомов этих элементов (рис. 37),
Аналогично существует различие в образовании химической связи у металлов и неметаллов:
Существуют различия и в кристаллических решетках простых веществ. У металлов только металлическая кристаллическая решетка, а неметаллам характерны атомные и молекулярные кристаллические решетки:
Безусловно, различия в строении атомов, видах химических связей и кристаллическом строении приводят к различиям в физических свойствах металлов и неметаллов (табл. 14).
Используя полученные знания in курса химии, на практике сравните физические свойства меди и серы.
Химические элементы делятся на металлы и неметаллы. Металлы — твердые вещества <кроме ртути). Неметаллы находятся в различных агрегатных состояниях.
Строение металлов и неметаллов — главная отличительная характеристика. Металлы имеют металлическую кристаллическую решетку. А неметаллам присущи молекулярные и атомные кристаллические решетки. Металлы проявляют восстановительные. а неметаллы окислительные свойства.
Сравнение химических свойств ii способов получения металлов и неметаллов
Атомы металлов, не обладая склонностью принимать электроны, могут только их отдавать пли обобщать. Все металлы в тон или иной степени проявляют восстановительные свойства.
Казалось бы, что самым активным из металлов должен быть фракций. Однако самый из долгоживущих изотопов фракция имеет период полураспада 22.3 мин. Его равновесное содержание в земной коре только 340 г. Кроме него имеется еще один вид с периодом полураспада 3.0 млн. Его равновесное содержание в земной коре составляет лишь 0.5 г.
Вследствие этого из применяемых металлов все-таки самым активным считается цезий.
Его легкость отдачи своего наружного электрона нашла применение в фотоэлементах.
Сравнительная активность металлов определяется схим рядом активности (приводится в сокращении):
Расположение лития на первом месте в этом ряду объясняется легкостью образования гидратной оболочки в водных растворах кислот и солей.
Из расположения металлов в этом ряду видно, что самыми активными металлами являются металлы с одним внешним электроном, а самыми устойчивыми — плашка и золото. Химические свойства металлов (рис. 37).
1. С неметаллами (не со всеми ):
Наиболее активные металлы легко реагируют с галогенами и кислородом. а с азотом реагируют только литий, кальций и магний.
Реагируя с кислородом, большинство металлов образует оксиды, а наиболее активные —пероксиды 
2. С оксидами менее активных мешаное :
3. С растворами кислот
В этом случае возможность реакции легко определяется по ряду напряжении (реакция протекает, если металл в ряду напряжений стоит до водорода).
4. С растворами солей :

Для определения возможности протекания реакции здесь также используется ряд напряжений.
5. Краме того, наиболее активные металлы (щелочные и щелочно-земельные ) реагируют с водой :
Большинство металлов в промышленности получают восстанавливая их оксиды:
В лаборатории этого часто используют водород. Наиболее активные металлы как в промышленности, так и в лаборатории получают с помощью электролиза.
В лаборатории менее активные металлы могут быть восстановлены из растворов их солен более активными металлами.
Неметаллы. В отличие от металлов, неметаллы обладают склонностью присоединять электроны, т, е. могут проявлять окислительные свойства. Самый активный неметалл — фтор. Он бурно взаимодействует почти со всеми веществами и с большинством из них — с горением и со взрывом. Контакт фтора с водородом приводит: к воспламенению и взрыву даже при очень низких температурах 
Неметаллы могут окислять:
2. Другие неметаллы :
3. Многие сложные вещества :
Фтор — самый сильный окислитель. Ненамного уступают ему кислород и хлор (обратите внимание на их положение в системе элементов).
В значительно меньшей степени окислительные свойства проявляют бор. графит, алмаз, кремний и другие простые вещества, образованные элементами, примыкающими к границе между металлами и неметаллами. Атомы этих элементов менее склонны присоединять электроны. Именно эти вещества (особенно графит и водород) способны проявлять восстановительные свойства:
Неметаллы получают из природных соединении, например, путем электролиза пли сложных окислительно-восстановительных процессов.
Металлы проявляют в химических реакциях свойства восстановителем. а неметаллы — свойства окислителей.
Сравнительная активность металлов определяется электрохимическим рядом активности. Метаны и неметаллы взаимодействуют с простыми и сложными веществами. Все металлы — восстановители, при взаимодействии с другими веществами отдают свои элекроны и окисляются. Самые сальные восстановители — щелочные металлы, А неметаллы при взаимодействии с другими веществами присоединяют электроны и восстанавливаются. Самый сильный окислитель — фтор.
Соединения металлов и неметаллов
После того как мы сравнили строение п свойства простых веществ металлов и неметаллов, можно приступить к более полном классификации и сравнению свойств важнейших соединений металлов и неметаллов.
Общие формулы водородных соединений по группам периодической системы химических элементов приведены в таблице 15.
С кислородом неметаллы образуют кислотные оксиды, В одних оксидах они проявляют максима льнуло степень окисления, равную номеру группы (например. 




Характеристики кислородных соединений неметаллов
1. Свойства высших оксидов в периодах слева направо постепенно изменяются от основных к кислотным
2. В группах сверху вниз кислотные свойства высших оксидов постепенно ослабевают. Об этом можно судить по свойствам кислот, соответствующих этим оксидам.
Кислородные соединения металлов представлены в таблице 16
Как видите. важнейшие классы химических веществ различаются по разным классификационным признакам. Но по какому бы признаку мы ни выделяли класс веществ. все вещества этого класса обладают общими химическими свойствами. Соединения металлов и неметаллов могут взаимодействовать между собой, так как их свойства противоположны.
Между всеми соединениями металлов и неметаллов существует генетическая связь, с которой вы уже знакомы (рис. 38).
С кислородом неметаллы образуют кислотные оксиды, а металлы — основные оксиды. Соединения металлов и неметаллов могут взаимодействовать между собой, так как их свойства противоположны. Между всеми соединениями металлов и неметаллов существует генетическая связь.
Биологическая роль металлов и неметаллов в жизнедеятельности живых организмов
Хорошо известно, что организмы в своем составе содержат различные химические элементы. В то же время организм человека нуждается в регулярном поступлении элементов извне, т. е. в химически сбалансированной пище. так как недостаток или избыток любого из элементов отрицательно сказывается на здоровье человека.
По современным представлениям из 118 известных элементов незаменимыми являются 22. Углерод, водород, азот и кислород не входят в этот список — они слишком широко природе.
К этой группе относятся водород, углерод, кислород, азот, натрий, магний, фосфор, сера, хлор, калий, кальций, Оиэло 96% от массы тела человека приходится на водород (H), кислород (О), углерод (С), азот (N). Они поступают в организм преимущественно в связанном виде с пищей, водой, воздухом и участвуют в большинстве химических реакции, протекающих в организме. Кроме того, эти элементы входят в состав белков, жиров и углеводов (рис. 39). К. этой же группе химических элементов относятся кальций (Са). фосфор (Р). калий (К), натрий (Na),
хлор (Сl). магний (Mg) и сера (S). На их долю в сумме приходится около 4% от массы организма.
Их роль сводится к:
— участию в пластических процессах и построении тканей (например, Р и Са — основные структурные компоненты костей);
— поддержанию кислотно-щелочного равновесия и водно-солевого обмена;
— поддержанию солевого состава крови и участию в структуре формирующих ее элементов:
— участию в структуре и функции большинства ферментативных систем и процессов, протекающих в организме.
В связи с этим их часто называют «следовыми» химическими элементами.
В организме каждого взрослого человека присутствует небольшое количество микроэлементов. Несмотря на их малое содержание, микроэлементы чрезвычайно важны.
В таблице 18 приведен список важнейших из них. Кроме того, исследования на животных показали, что в следовых количествах незаменимыми являются кобальт (Со) никель (Ni) мышьяк (As) и кадмий
Макроэлементы сконцентрированы. как правило, в соединительных тканях (мышцы, кости, кровь), входя в состав органических соединений. Они определяют пластический материал основных несущих тканей, а также обеспечивают поддержку основных свойств внутренней среды организма в целом (гомеостаз): значение pH. осмотическое давление, кислотно-щелочное равновесие, устойчивость коллоидных систем в организме.
Микроэлементы неравномерно распределены между тканями н часто обладают сродством к определенному типу тканей и органон. Так, цинк аккумулируется в поджелудочной железе, молибден — в почках, барии — в сетчатке плаза, стронций — в костях, йод — в щитовидной железе (рис. 40. табл. 18).
Знаешь ли ты?
Снижение содержания цинка в плазме крови — обязательное следствие инфаркта миокарда.
Уменьшение содержания лития в крови — показатель гипертонического заболевания.
То, что, например, мышьяк, общеизвестный ял. незаменим для жизни, может вас удивить. Но нет ничего необычного в том, что одни и те же вещества могут приносить и пользу, и вред — все зависит от дозы. Даже поваренная соль может стать ядовитой, если попадет в организм в стишком больших количествах. Пороговое содержание различных элементов для организма человека представлен о в таблице 19.
Наша пища должна быть сбалансирована по необходимым химическим элементам. Правильное питание — залог здоровья каждого человека,
Знаешь ли ты?
Суточное потребление йода жителями Японии в несколько раз выше (за счет продуктов моря), чем в Центральной Азми.
В Казахстане снижено потребление йода, но превышено потребление калия, натрия.
Жители Индии потребляют с гнилей в 3 раза больше магния, марганца. железа, в 2 раза больше мели и калия, чем жители Англии.
В то же время англичане потребляют с пищей в 2 раза больше хрома и кальция.
В Англии потребление с пищей алюминия — в 20 раз, лития — в 10 раз, молибдена — в 3 раз,з ниже, чем в США. а хрома — в б раз. калышя — в 3 раза выше, чем в Германии
В состав клеток живых организмов, в т. ч. и человека, входят органические и неорганические вещества.
Реакции, происходящие каждый день
Невидимые чернила:
Китайский император использовал для своих тайных надписей невидимые чернила из рисового отвара, который после высыхания не оставлял никаких видимых следов. Однако если такое письмо слегка смочить слабым спиртовым раствором йода, то появляются синие буквы. Рис содержит крахмал, а крахмал выдает себя полностью при наличии йода.
Услуги по химии:
Лекции по химии:
Лекции по неорганической химии:
Лекции по органической химии:
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.