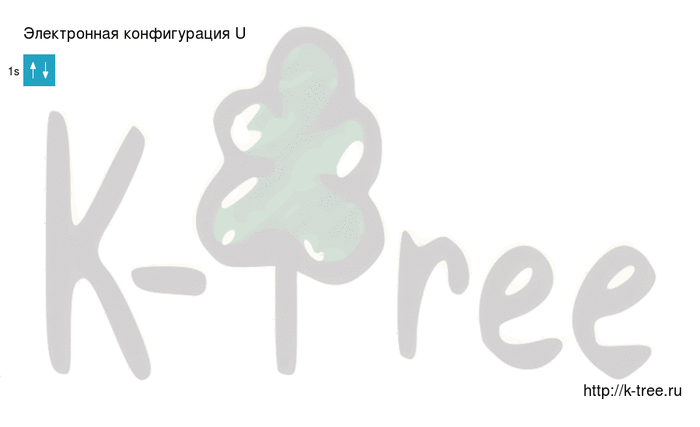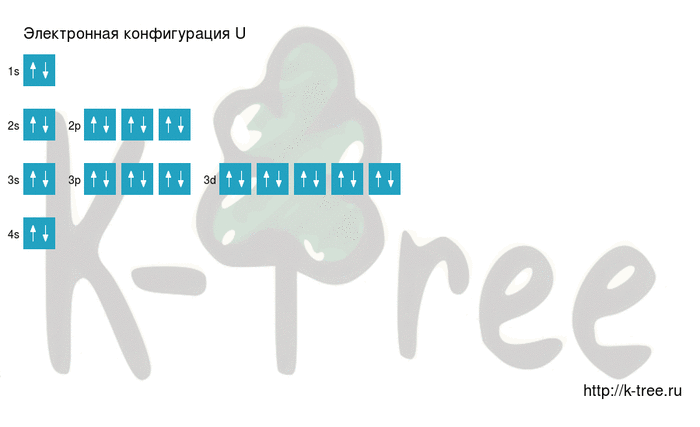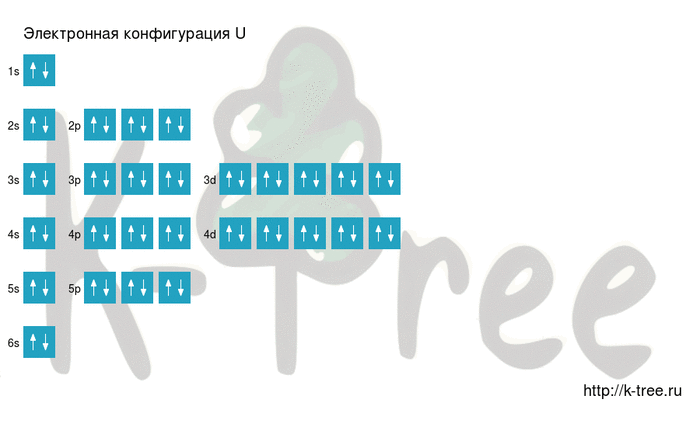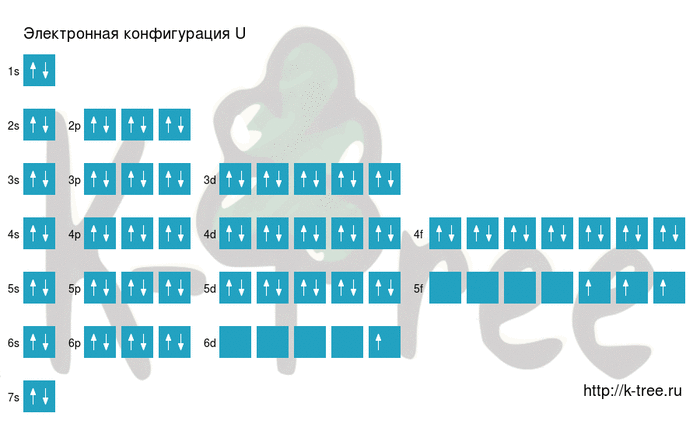уран в таблице менделеева номер
Химический элемент Уран
Использование и свойства элемента Уран
Изображение основано на общем астрологическом символе планеты Уран.
Радиоактивный серебристый металл.
Уран не имеет известной биологической роли. Это токсичный металл.
Уран встречается в естественных условиях в нескольких минералах, таких как уранит (урановая обманка), браннерит и карнотит. Он также встречается в фосфатных породах и монацитовых песках. Мировая добыча урана составляет около 41 тысячи тонн в год.Извлеченный уран превращается в очищенный оксид, известный как желтый кек. Металлический уран можно получить путем восстановления галогенидов урана металлами группы 1 или группы 2 или путем восстановления оксидов урана кальцием или алюминием.
История химического элемента Уран
В средние века минеральная урановая обманка (оксид урана, U 3 O 8 ) иногда обнаруживалась в серебряных рудниках, а в 1789 году ее исследовал Мартин Генрих Клапрот из Берлина. Он растворил его в азотной кислоте и выпал в осадок желтое соединение, когда раствор был нейтрализован. Он понял, что это оксид нового элемента, и попытался получить сам металл, нагревая осадок с древесным углем, но безуспешно.
Эжену Пелиго в Париже выпало выделить первый образец металлического урана, что он и сделал в 1841 году, нагревая тетрахлорид урана с калием.
Открытие радиоактивности урана произошло только в 1896 году, когда Анри Беккерель в Париже оставил образец урана на неэкспонированной фотографической пластинке. Это заставило его помутнеть, и он пришел к выводу, что уран испускает невидимые лучи. Была обнаружена радиоактивность.
Уран как радиоактивный элемент таблицы Менделеева
Как был открыт Уран
Вообще, такой химический элемент как уран был известен очень давно. Известно, что ещё до нашей эры природная окись урана использовалась для изготовления жёлтой глазури для керамики. Открытие этого элемента произошло можно считать в 1789 году, когда немецкий химик, по имени Мартин Генрих Клапрот, восстановил из руды черный металлоподобный материал. Этот материал Мартин решил назвать Ураном, чтобы поддержать название новой открытой планеты с одноименным названием(в этом же году была открыта планета Уран). В 1840 году было выявлено, что этот материал открытый Клапротом, оказался оксидом Урана не смотря на характерный металлический блеск. Эжен Мелькиор Пелиго из оксида синтезировал атомарный Уран и определил его атомный вес равный 120 а.е., а в 1874 году Менделеев удвоил это значение, поместив его в самую дальнюю клетку своей таблицы. Только через 12 лет решение Менделеева о удвоении массы было подтверждено опытами немецкого химика Циммермана.
Где и как добывают Уран
Уран является довольно распространенным элементом, но он распространен в виде урановой руды. Чтоб вы понимали, содержание ее в земной коре составляет 0.00027% от общей массы Земли. Урановая руда как правило входит в состав кислых минеральных пород с высоким содержанием кремния. Основными видами урановых руд являются настуран, карнотит, казолит и самарскит. Крупнейшие запасы урановых руд с учётом резервных месторождений являются такие страны как Австралия, Россия и Казахстан, причем из всех перечисленных Казахстан занимает лидирующую позицию. Добыча урана является очень не простой и дорогостоящей процедурой. Далеко не все страны могут позволить себе добывать и синтезировать чистый уран. Технология производства выглядит следующим образом: руда или минералы добываются в шахтах, сравнимо золоту или драгоценным камням. Добытые породы дробят и смешивают с водой для того, чтобы отделить урановую пыль от остальных. Урановая пыль очень тяжёлая и поэтому она выпадает в осадок быстрее остальных. Следующим шагом является очищение урановой пыли от других пород путем кислотного или щелочного выщелачивания. Процедура выглядит примерно так: урановую смесь нагревают до 150 °С и подают чистый кислород под давлением. В результате образуется серная кислота которая очищает уран от других примесей. Ну и на заключительном этапе отбирают уже чистые частицы урана. Помимо урановой пыли там попадаются и другие полезные минералы.
Опасность радиоактивного излучения урана
Все прекрасно знают такое понятие как радиоактивное излучение и то, что оно наносит непоправимый вред здоровью, который приводит к летальному исходу. Уран как раз является одним из таких элементов, который при определенных условиях может выпускать радиоактивное излучение. В свободной форме в зависимости от его разновидности он может испускать альфа и бета лучи. Альфа лучи не представляют большой опасности для человека если облучение является внешним так как у этого излучения малая проникающая способность, но при попадании внутрь организма они наносят непоправимый вред. Для сдерживания внешних альфа лучей хватит даже листа писчей бумаги. С бета излучением дела обстоят серьезнее, но не намного. Проникающая способность бета излучения выше, чем у альфа излучения, но для сдерживания бета излучения потребуется 3-5 мм ткань. Вы скажете как так? Уран же является радиоактивным элементом, который используется в ядерном оружии! Все верно, он используется в ядерном оружии, которое наносит колоссальный урон всему живому. Просто при детонировании ядерной боеголовки, основной урон живым организмам наносят гамма излучения и поток нейтронов. Данные виды излучений образуются в результате термоядерной реакции при взрыве боеголовки, которая выводит частицы урана из стабильного состояния и уничтожает все живое на земле.
Разновидности урана
Как говорилось выше, у урана есть несколько разновидностей. Разновидности подразумевают собой наличие изотопов, чтоб вы понимали изотопы подразумевают собой одинаковые элементы, но с разными массовыми числами.
Итак существуют два вида:
Как вы уже догадались природный тот который добывают из земли, а искусственный люди создают самостоятельно. К природным относят изотопы урана с массовым числом 238, 235 и 234. Причем U-234 является дочерним от U-238, то есть первый получается от распада второго в природных условиях. Вторая группа изотопов, которую создают искусственно, имеет массовые числа от 217 до 242. Каждый из изотопов имеет разные свойства и характеризуется разным поведением при определенных условиях. В зависимости от потребностей учёные ядерщики пытаются найти всевозможные решения проблем, ведь каждый изотоп имеет разную энергетическую ценность.
Периоды полураспада
Как уже говорилось выше, каждый из изотопов урана обладает разной энергетической ценностью и разными свойствами, одним из которых является полураспад. Для того чтобы понимать что это такое нужно начать с определения. Периодом полураспада называется время за которое число радиоактивных атомов уменьшается в двое. Период полураспада влияет на многие факторы, в пример можно привести его энергетическую ценность или полное очищение. Если в пример взять последнее то можно посчитать за какой промежуток времени произойдет полная очистка от радиоактивного заражения земли. Полураспады изотопов урана:
| Массовое число | Период полураспада | Основной тип излучения |
| U-233 | 15.9*10⁴ лет | альфа |
| U-234 | 24.5*10⁴ лет | альфа |
| U-235 | 71000*10⁴ лет | альфа |
| U-236 | 2390*10⁴ лет | альфа |
| U-237 | 6.75 суток | бета |
| U-238 | 447000*10⁴ лет | альфа |
| U-239 | 23.54 минуты | бета |
| U-240 | 14 часов | бета |
Как можно увидеть из таблицы период полураспада изотопов варьируется от минут до сотен миллионов лет. Каждый из них находит себе применение в разных областях жизнедеятельности людей.
Применение
Уран U
Уран в таблице менделеева занимает 92 место, в 9 периоде.
| Символ | U |
| Номер | 92 |
| Атомный вес | 238.0289100 |
| Латинское название | Uranium |
| Русское название | Уран |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
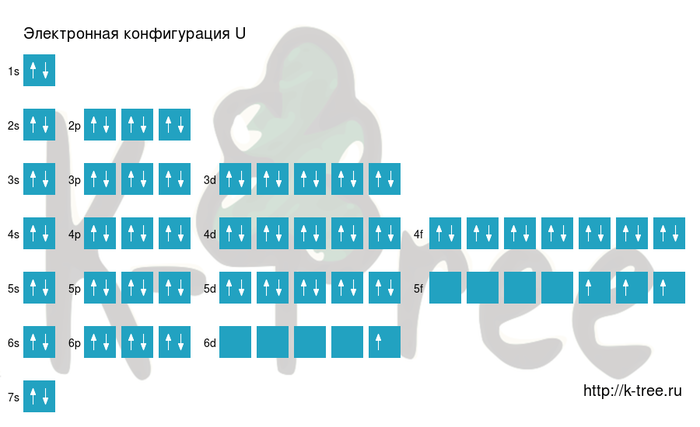
Электронная схема урана
U: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 3 6d 1
Короткая запись:
U: [Xe]6s 2 4f 14 5d 10 6p 6 7s 2 5f 3 6d 1
Порядок заполнения оболочек атома урана (U) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Уран имеет 92 электрона, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
6 электронов на 5p-подуровне
2 электрона на 6s-подуровне
14 электронов на 4f-подуровне
10 электронов на 5d-подуровне
6 электронов на 6p-подуровне
2 электрона на 7s-подуровне
3 электрона на 5f-подуровне
1 электрон на 6d-подуровне
Степень окисления урана
Атомы урана в соединениях имеют степени окисления 6, 5, 4, 3, 2.
Ионы урана
Валентность U
Атомы урана в соединениях проявляют валентность VI, V, IV, III, II.
Валентность урана характеризует способность атома U к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа U
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Уран в таблице менделеева номер
Этот элемент был открыт на территории Германской империи в 1789 году. Он назван в честь планеты Уран, которая была обнаружена на 8 лет раньше. Однако радиоактивность урана была открыта лишь в 1896 году.
Уран — последний элемент в таблице Менделеева. Он ещё и самый тяжёлый элемент, существующий в естественном виде на Земле. Именно при расщеплении его атома получается электричество.
Электричество, которое производится из урана, является альтернативой горючим ископаемым, таким как нефть и уголь. Сегодня 16% электричества в мире получается из урана.
Уран и производство электричества
Символ урана в периодической таблице — U. Уран состоит в основном из двух изотопов — 235U и 238U. Уран на 99,7 % состоит из изотопа 238U и только оставшиеся 0,7 % — это изотоп 235U.
Именно изотоп 235U, который составляет столь малый процент урана, позволяет получить энергию посредством расщепления ядра атома. Для производства электричества концентрация изотопа 235U должна составлять 3–4 %. Поэтому химики обогащают уран.
Обогащение урана можно провести двумя способами: с помощью ультрацентрифугирования или газовой диффузии. Оба метода разделяют изотопы и в результате концентрация 235U повышается.
Ядерная энергия считается чистой, потому что она не выделяет парниковые газы и её отходы достаточно малы. Другим преимуществом этой энергии то, что её легко транспортировать и она не требует много места для хранения.
Обогащённый уран прессуют в таблетки размером 1х1 см. Энергоотдача такой таблетки очень высока: две таблетки способны обеспечить энергией семью из 4 человек на 1 месяц.
Таким образом, уран является отличной альтернативой нефти и углю: чтобы произвести столько же электроэнергии, сколько производит 1 килограмм урана, потребуется 10 тонн нефти и 20 тонн угля. Это помимо негативных эффектов, которые последние оказывают на окружающую среду. К тому же нефть и уголь требуют много места.
Недостатки ядерной энергии
Одним из основных недостатков является риск аварий и их последствия для окружающей среды. Зоны, заражённые радиоактивностью урана, становятся непригодными для жилья.
Нахождение и применение урана
После того, как урановую руду извлекают из земли, её измельчают, перерабатывают и делают небольшие урановые таблетки. Таблетки урана подвергаются высоким температурам, чтобы они стали более прочными.
После того как топливо закладывается в реактор, начинается процесс ядерного деления. Деление происходит в результате бомбардировки нейтронами атомного ядра урана.
Когда нейтрон сталкивается с атомом урана, последний расщепляется на два других атома. Происходит выделение большого количества энергии и других нейтронов. Они сталкиваются с атомами и порождают цепную реакцию.
Выделяемая энергия становится теплотой, которая нагревает воду в реакторе. Пар от горячей воды активирует турбины, а те, в свою очередь, запускают электрогенераторы. Такие генераторы и производят электроэнергию.
Характеристики урана
Ядерная (атомная) энергетика России
В России функционируют 10 атомных электростанций.
Основные залежи урана в России находятся рядом с городом Краснокаменском. Там же находятся основные горно-химическое объединения и крупнейшее уранодобывающее предприятие.
По объёму добытого урана Россия занимает 5 место. А вот по запасам урана — 3 место.
Уран в мире
Самые большие запасы урана находятся в Австралии. Затем идут Казахстан, Россия, Канада, ЮАР, Нигер и Бразилия.
Что касается производства электроэнергии с помощью атомных электростанций, то Канада, Казахстан и Австралия занимают лидирующие позиции. Эти три страны вместе производят более чем половину ядерной энергии в мире.
Смотрите таблицу с данными по производству и запасам урана каждой из перечисленных стран.
| Страна | Запасы урана (тысяч тонн / в год) | Производство обогащённого урана (тонн / в год) |
| Австралия | 1 661 | 7 743 |
| Казахстан | 629 | 7 994 |
| Россия | 487 | 3 239 |
| Канада | 468 | 10 485 |
| Нигер | 421 | 3 355 |
| Бразилия | 276 | 238 |
Уран и ядерные бомбы
Для производства электроэнергии уран обогащают для того, чтобы содержание изотопа 235U составило 3 или 4 %.
Для производства же атомной бомбы его содержание должно быть 90 %.
Бомба, сброшенная США на Хиросиму (город в Японии) в конце Второй мировой войны, называлась «Малыш» (от англ. Little boy). Она содержала 64 кг обогащённого урана. Разрушительная сила этой бомбы была равна 15 000 тоннам тротилового эквивалента.
«Малыш» произвёл тепловую волну, температура которой достигла 4000 градусов, а её скорость равнялась 440 метрам в секунду.
Взрыв стал причиной гибели 80 000 человек. Тысячи людей подверглись радиации.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
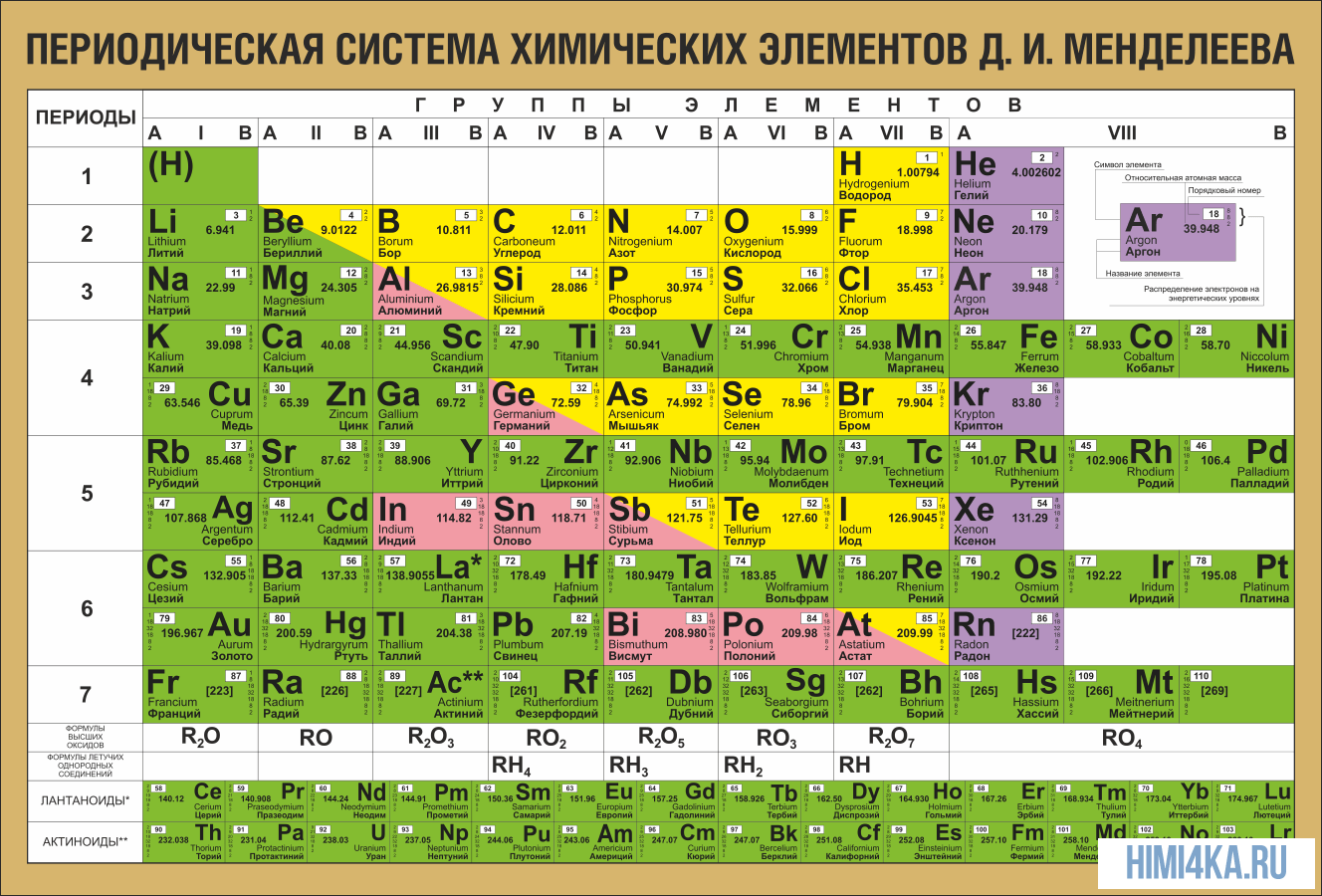
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.
Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
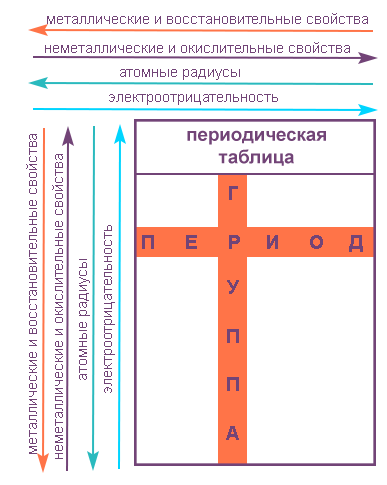
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
| Неметаллы |
| Водород H 1 |
| Углерод C 6 |
| Азот N 7 |
| Кислород O 8 |
| Фосфор P 15 |
| Сера S 16 |
| Селен Se 34 |
| Флеровий Fl 114 |
| Унунсептий Uus 117 |
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Хотите ещё проще? Мы создали новый курс, где максимум за 7 дней вы овладете химией с нуля. Подробннее по ссылке