гемафагоцитарный лимфогистиоцытоз что это
Гемофагоцитарный лимфогистиоцитоз
Гемофагоцитарный лимфогистиоцитоз – группа врожденных и приобретенных заболеваний, возникающих вследствие нарушений регуляции иммунного ответа и характеризующихся гиперпродукцией гистиоцитов, а также цитотоксических T-лимфоцитов. Клиническая симптоматика проявляется фебрильной лихорадкой, увеличением печени и селезенки, периферических лимфатических узлов, поражением нервной системы, костного мозга и других органов. Диагностика основана на данных клинического, лабораторного (цитопения, коагулопатия, билирубинемия и др.) и инструментального обследования. Лечение: иммуносупрессивная терапия, кортикостероиды, воздействие на причинные факторы.
МКБ-10
Общие сведения
Гемофагоцитарный лимфогистиоцитоз (гемофагоцитарный синдром) – врожденное или приобретенное нарушение регуляции иммунного ответа, при котором происходит аномальная активация цитотоксических T-лимфоцитов, моноцитов и макрофагов с аккумуляцией в органах-мишенях и развитием в них выраженного патологического процесса (воспаления, повреждения тканей, фагоцитоза форменных элементов крови). При врожденной, генетически детерминированной форме заболевания болеют преимущественно дети раннего возраста и в 60-80% случаев – на первом году жизни.
Вторичный (приобретенный) гемофагоцитарный лимфогистиоцитоз встречается во всех возрастных категориях, развивается на фоне затяжного течения различных инфекционных заболеваний, аутоиммунных процессов и новообразований. Впервые признаки гемофагоцитарного синдрома были описаны еще в 1939 году, а заболевание тогда было названо гистиоцитарным медуллярным ретикулезом. Семейная наследственная форма лимфогистиоцитоза была впервые описана в 1959 году. Распространенность заболевания колеблется от 1 случая на 50 тысяч новорожденных до 1-2 случаев на 1 миллион детей в возрасте до 15 лет.
Причины гемофагоцитарного лимфогистиоцитоза
Врожденный гемофагоцитарный лимфогистиоцитоз возникает вследствие генетического дефекта механизмов клеточной цитотоксичности из-за мутаций гена перфорина. В норме регуляция иммунного ответа обеспечивается своевременным ограничением активности эффекторов иммунной системы в процессе ликвидации угрозы для организма со стороны проникших инфекционных агентов и других негативных воздействий. В этой регуляции важную роль играют механизмы клеточной цитотоксичности.
При первичном гемофагоцитарном лимфогистиоцитозе регулятивная роль цитотоксических гранул клеток и цитотоксических T-лимфоцитов в отношении клеток-мишеней нарушается, происходит чрезмерная активация иммунных клеток, в избытке продуцируются провоспалительные цитокины (интерфероны, фактор некроза опухоли и др.). Активированные вследствие «цитокинового шторма» T-лимфоциты и макрофаги инфильтрируют, а затем повреждают органы и ткани. Важным фактором патогенеза заболевания является развитие патологического гемофагоцитоза зрелых форменных элементов крови. Такой фагоцитоз происходит и в норме, помогая организму избавиться от старых клеток. В данном же случае макрофаги начинают фагоцитировать полноценные, нормально функционирующие форменные элементы крови, приводя к выраженной цитопении, коагулопатии и другим проявлениям заболевания.
Приобретенный (вторичный) гемофагоцитарный лимфогистиоцитоз развивается на фоне некоторых инфекционных заболеваний, опухолей, аутоиммунных процессов, при трансплантации органов и тканей, причем характерные нарушения регуляции иммунного ответа могут быть как следствием основного заболевания, так и осложнением, связанным с проведением иммуносупрессивной терапии и возникновением вторичной инфекции.
Симптомы гемофагоцитарного лимфогистиоцитоза
Клинические проявления гемофагоцитарного лимфогистиоцитоза чрезвычайно вариабельны. Наиболее часто наблюдается длительная лихорадка, рефрактерная к проводимой антибактериальной и противовирусной терапии. Озноб, признаки общей интоксикации (слабость, потливость, нарушения сна, отказ от приема пищи, тошнота и рвота, боли в мышцах) продолжаются в течение длительного времени, приобретая волнообразное течение с периодическими временными улучшениями самочувствия.
Характерным проявлением заболевания является увеличение печени и селезенки, имеющее прогрессирующий характер. К ранним симптомам первичного гемофагоцитарного лимфогистиоцитоза относится появление кожной сыпи, увеличение периферических лимфатических узлов, а также развитие неврологических расстройств в виде повышенной возбудимости, двигательных нарушений и расстройств чувствительности, судорожного синдрома, признаков повышения внутричерепного давления у детей раннего возраста. Встречаются при гемофагоцитарном лимфогистиоцитозе и симптомы, свидетельствующие о наличии анемии, коагулопатии – бледность и желтушность кожных покровов, периферические отеки, признаки кровотечения из пищеварительного тракта (черный кал, примесь крови в каловых массах и др.).
При вторичном гемофагоцитарном синдроме сочетаются клинические признаки поражения иммунной системы и проявления основного заболевания (вирусной инфекции, злокачественного новообразования, аутоиммунного заболевания).
Диагностика гемофагоцитарного лимфогистиоцитоза
Диагноз устанавливается в результате тщательного изучения анамнеза, клинической картины заболевания, результатов лабораторных и инструментальных исследований. Необходимы осмотры врача-гематолога, аллерголога-иммунолога, онколога, инфекциониста, ревматолога и других специалистов. Разработаны международные диагностические критерии гемофагоцитарного лимфогистиоцитоза, к которым относятся:
Наличие хотя бы пяти из этих признаков свидетельствует о гемофагоцитарном лимфогистиоцитозе. Для установления наследственной формы заболевания необходимо генетическое исследование, в результате которого обнаруживаются мутации генов PRF1, UNC13D, Munc18-2, STX11.
Приобретенные формы гемофагоцитарного синдрома диагностируются на основании вышеописанных международных критериев и проведения уточненной диагностики основного заболевания, для чего зачастую необходимо выполнять сложные лабораторные и инструментальные исследования (эндоскопические, УЗИ, КТ, МРТ, ПЭТ).
Дифференциальный диагноз гемофагоцитарного лимфогистиоцитоза проводится с:
Лечение гемофагоцитарного лимфогистиоцитоза
Современная тактика лечения наследственной формы гемофагоцитарного лимфогистиоцитоза включает проведение химиотерапии с использованием иммуносупрессивных средств (дексаметазона, этопозида, циклоспорина A), а также трансплантации стволовых клеток. Прогноз заболевания значительно улучшается при своевременном проведении трансплантации от гистосовместимого родственного донора.
При вирусных, бактериальных и паразитарных инфекциях, вызвавших появление гемофагоцитарного синдрома, проводится этиотропная антимикробная терапия, инфузии высокодозного иммуноглобулина, а также иммуносупрессивная терапия с введением циклоспорина A и кортикостероидов. Иногда показано проведение трансплантации костного мозга. При опухолях, наряду с лечением основного заболевания, в терапевтическую схему включаются иммуносупрессивные средства в индивидуально подобранных дозах. При аутоиммунных процессах лечение включает сочетание иммуноглобулина, пульс-терапии с использованием кортикостероидов, а также циклоспорина A.
Гемофагоцитарный лимфогистиоцитоз
Гемофагоцитарный лимфогистиоцитоз (семейный гемофагоцитарный ретикулез) — это заболевание крови, при котором иммунная система производит избыточное количество иммунных клеток (лимфоцитов), называемых Т-клетками, природных клеток-киллеров, В-лимфоцитов и макрофагов (гистиоцитов).
Кроме того, в крови увеличивается количество белков иммунной системы, называемых цитокинами. Такая сверхповышенная активность вызывает лихорадку и повреждает печень и селезенку, поскольку происходит быстрое и неконтролируемое увеличение этих органов.
Что такое семейный гемофагоцитарный ретикулез, признаки расстройства. Первичный и вторичный гемофагоцитарный лимфогистиоцитоз
В ходе развития семейного гемофагоцитарного ретикулеза разрушаются кровеносно-продуцирующие клетки костного мозга. Этот процесс называется гемофагоцитоз. В результате этого процесса больные имеют крайне низкие показатели эритроцитов в крови — анемию, а также пониженное количество клеток крови, принимающих участие в процессе свертывания — тромбоцитов. Снижение количества тромбоцитов может привести к аномальным кровотечениям и появлениям кровоподтеков, синяков, сосудистых звездочек.
Данное заболевание передается по наследству. У новорожденных с данным расстройством проявляются характерные внешние признаки лимфогистиоцитоза, например, задержка срастания костей черепа, раздражительность, ригидность затылочных мышц, нарушение мышечного тонуса, паралич, слепота и даже судороги и кома.
В дополнение к неврологическим проблемам семейный гемофагоцитарный лимфогистиоцитоз может вызвать аномалии развития сердца, почек и других органов и тканей. Все больные с этим заболеванием также имеют повышенный риск развития рака кроветворных клеток (лейкемии и лимфомы).
Первичный гемофагоцитарный лимфогистиоцитоз является гетерогенным наследственным заболеванием, передающимся по аутосомно-рецессивному признаку.
Вторичная форма заболевания происходит после сильной иммунологической активации, например, во время поражения организма системной инфекцией, иммунодефицитом или злокачественной опухолью. Обе формы характеризуются подавлением активации Т-лимфоцитов и макрофагов, и неизменно приводят к клиническим и гематологическим нарушениям и смерти при отсутствии лечения.
Заболевание было открыто более 60 лет назад шотландскими педиатрами Джеймсом Фаркухаром и Альбертом Клоре, которые окончили Эдинбургский университет. Специалисты отметили семейное повторение расстройства, поражавшего и мальчиков, и девочек примерно в одном и том же возрасте — 2 месяца. Общими симптомами была высокая температура, цитопения, гепатоспленомегалия и, несмотря на лечение антибиотиками, быстрый летальный исход.
Признаки и симптомы гемофагоцитарного лимфогистиоцитоза, как правило, становятся очевидными еще в младенчестве, хотя иногда они появляются на более позднем этапе жизни. Появляются они обычно при избыточном ответе иммунной системы на инфекцию, но могут возникать и спонтанно. Примерно у 65% больных наблюдаются видимые поражения кожи, например, эритродермия, пурпура, макулы и папулы по всему телу, жидкие выделения из мелкой сыпи и папул.
Без лечения большинство детей с гемофагоцитарным лимфогистиоцитозом живут всего несколько месяцев.
Причины гемофагоцитарного лимфогистиоцитоза
Основными причинами развития гемофагоцитарного лимфогистиоцитоза являются:
Примечательно, что данные причины характерны для вторичного лимфогистиоцитоза. Другие причины вторичного лимфогистиоцитоза это:
Первичный лимфогистиоцитоз является наследственным заболеванием и развивается в основном у детей младше 18 месяцев. В крови накапливается большое количество цитокинов и активированных Т-клеток и макрофагов. Клетки костного мозга атакуют мозг и/или селезенку, лейкоциты и тромбоциты. Заболевание диагностируется, когда у ребенка обнаруживается мутация в одном из HLH-ассоциированных генов.
В обеих формах заболевания клинические появления и результаты анализов схожи.
Симптомы гемофагоцитарного лимфогистиоцитоза
Для постановки диагноза «гемофагоцитарный лимфогистиоцитоз» необходимо зафиксировать у больного следующие симптомы:
Могут присутствовать респираторные симптомы: кашель, одышка. У взрослых больных налицо изменение психических функций, увеличение лимфатических узлов, отказ печени.
Методы лечения гемофагоцитарного лимфогистиоцитоза
Быстрая диагностика и раннее лечение важны для повышения вероятности выживания. Такое редкое заболевание, как лимфогистиоцитоз, нуждается в стационарном лечении, особенно в случае заболевания новорожденных и детей младше полутора лет.
Американская ассоциация гистиоцитоза рекомендует следующие методы лечения:
Пациенты с лимфогистиоцитозом могут быть разделены на группы высокого риска и низкого риска. Группы высокого риска могут получать препарат этопозид по специальной схеме приема. Группа низкого риска проходит лечение при помощи следующих препаратов: циклоспорин, кортикостероиды.
Пациенты с гемофагоцитарным лимфогистиоцитозом могут подвергаться повышенному риску развития синдрома обратимой задней энцефалопатии.
Хирургическое лечение
Основным видом хирургического лечения является ТКМ (трансплантация гемопоэтических стволовых клеток). Она выполняется, когда находится подходящий донор, и состояние пациента в целом стабильное. Если больной страдает от неконтролируемого гиперспленизма, проводится спленэктомия — удаление селезенки.
Гистиоцитозы из мононуклеарных фагоцитов, отличных от клеток Лангерганса
Этот подвид заболевания относится к группе гистиоцитозов, условно разделяющихся на:
Подгруппы определяются, исходя из внешних различий и особых окрашиваний ткани под микроскопом.
Как и другие формы гистиоцитоза, форма заболевания, происходящая из мононуклеарных фагоцитов, отличных от клеток Лангерганса, вызывает такие симптомы, как появление на коже красно-коричневых пятен, сыпи на голове и за ушами, повреждение внутренних органов — печени, почек, легких.
Лечение проводят при помощи кортикостероидов, антибактериальных препаратов, нитразина и ультрафиолетового облучения (ПУВА-терапии).
Избавление от лишнего веса на 60% снижает риск тяжелой формы COVID-19
Почему нельзя пить воду прямо из бутылки и на что указывает изменение вкуса воды?
Прикованный к постели мужчина осуществил операцию, которая вернула его к нормальной жизни
Фактор, который может увеличить риск развития болезни Паркинсона на 90%
Небольшие изменения, которые помогут улучшить здоровье в 2022 году
Учеными найден способ нейтрализации Омикрона
Гемофагоцитарный лимфогистиоцитоз
. или: ГЛГ HLH — Hemophagocytic lymphohistiocytosis Вирус-ассоциированный гемофагоцитарный синдром, гемофагоцитарный гистиоцитоз, семейный эритрофагоцитарный лимфогистиоцитоз
Гемофагоцитарный лимфогистиоцитоз – это редкое и тяжелое, часто жизнеугрожающее гематологическое заболевание (заболевание крови), характеризующееся значительным увеличением количества гистиоцитов (тканевых макрофагов – клеток иммунной системы, которые в норме из крови переходят в окружающие ткани и уже в них осуществляют свои функции – поглощение и удаление инородных частиц и бактерий). При гемофагоцитарном лимфогистиоцитозе макрофаги начинают поглощать другие клетки крови (эритроциты (красные клетки крови), лейкоциты (белые клетки крови), тромбоциты (клетки крови, участвующие в процессах ее свертываемости)) и клетки внутренних органов. В результате такой неправильной активности макрофагов работа внутренних органов нарушается, они не могут полноценно выполнять свои функции. Возникает иммунная дисрегуляция – нарушение взаимодействия между клетками иммунной системы и другими клетками организма, а также внутри иммунной системы. Развивается обширный воспалительный процесс, который затрагивает многие системы органов и тканей. Заболевание встречается редко – примерно 1 случай на 50000 новорожденных.
Симптомы гемофагоцитарного лимфогистиоцитоза
Клиническая картина очень разнообразна. Заболевание может начинаться как обычная инфекция, в процесс могут вовлекаться различные органы и ткани. Среди наиболее часто встречающихся симптомов выделяют несколько.
Формы
Выделяют первичный и вторичный гемофагоцитарный лимфогистиоцитоз.
Причины
Врач аллерголог-иммунолог поможет при лечении заболевания
Диагностика
Лечение гемофагоцитарного лимфогистиоцитоза
Осложнения и последствия
Профилактика гемофагоцитарного лимфогистиоцитоза
Причины возникновения первичного гемофагоцитарного лимфогистиоцитоза до конца неясны, поэтому комплекс профилактических мероприятий не разработан.
Профилактика развития вторичного гемофагоцитарного лимфогистиоцитоза заключается в лечении основного заболевания. Например, при наличии:
ИНФОРМАЦИЯ ДЛЯ ОЗНАКОМЛЕНИЯ
Необходима консультация с врачом
Певцова Анастасия Владимировна, врач-методист, акушер-гинеколог, медицинский редактор.
Ельчанинова Ольга Николаевна, редактор.
Что делать при гемофагоцитарном лимфогистиоцитозе?
У вас гемофагоцитарный лимфогистиоцитоз?
аллерголог-иммунолог назначит правильное лечение при гемофагоцитарном лимфогистиоцитозе
Гемофагоцитарный лимфогистиоцитоз у детей
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «07» декабря 2017 года
Протокол № 34
Гемофагоцитарный лимфогистиоцитоз – редкое наследственное или приобретенное заболевание, характеризующееся неконтролируемой активацией макрофагов, и, как следствие, нерегулируемым фагоцитозом клеток крови и их предшественников [1].
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| D76.1 | Гемофагоцитарный лимфогистиоцитоз |
| D76.2 | Гемофагоцитарный синдром, связанный с инфекцией |
Дата разработки/пересмотра протокола: 2017 год.
Пользователи протокола: врачи-педиатры, ВОП, онкологи/гематологи, ревматологи.
Категория пациентов: дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
К ГФС относятся два различных состояния, которые по начальным клиническим симптомам трудно отличить друг от друга [1].
Семейно-наследственный (первичный) гемофагоцитарный лимфогистиоцитоз – аутосомно-рецессивное заболевание, в генезе которого важную роль играет мутация в гене перфорина, которая встречается в 20–40% случаев СГЛГ.
Вторичный гемофагоцитарный лимфогистиоцитоз – синдром макрофагальной активации с гемофагоцитозом, который развивается в результате иммуной активации системы мононуклеарных фагоцитов.
Вторичные гемофагоцигарные синдромы развиваются как осложнение основного заболевания при широком круге патологических процессов [1,2,3]. В зависимости от природы основного заболевания принято выделять гемофагоцитарный синдром, связанный с [3]:
· инфекцией;
· опухолью;
· первичным иммунодефицитом;
· системной аутоиммунной патологией;
· наследственными дефектами метаболизма.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Физикальное обследование [3,4]:
Осмотр больного: необходимо обратить внимание на температуру тела, рост, вес, окружность головы, сыпь на коже головы и туловища, геморрагические элементы на коже, активные кровотечения, желтушность, бледность, альбинизм, лимфаденопатию, тонзиллит, пороки развития скелета, одышку, тахипноэ, размеры печени, селезенки, периферические отеки, неврологическую симптоматику (парезы/параличи черепных нервов, уровень сознания, менингеальные знаки).
Клиническая симптоматика [2]:
· упорная лихорадка более 38,5°С в течение 7 суток и более, рефрактерная к антимикробной терапии;
· спленомегалия более 3 с, из-под реберной дуги.
Лабораторные исследования 5:
· ОАК + лейкоформула ручным методом: анемия (Hb 9 ), нейтропения ( 9 ), ускорение СОЭ. Возможны 2-х или 3-х ростковые цитопении
· Биохимический анализ крови: повышение уровня триглицеридов (уровень триглицеридов натощак ³2,0 ммоль/л или ³3,0 стандартных отклонения от средней возрастной нормы), ферритина (>500 мкграмм/л), возможны гипопротеинемия, повышение трансаминаз
· Коагулограмма: гипофибриногенемия (£1,5 г/л или 3,0 стандартные отклонения), снижение протромбинового времени (ПВ) и протромбинового комплекса (ПТИ), удлинение международного нормализованного времени (МНО)
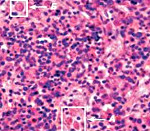
· цитологическое исследование миелограммы или морфологическое исследование биоптата лимфоузла или селезенки: наличие гемофагоцитирующих макрофагов. При стандартном окрашивании пунктата костного мозга выявляется инфильтрация активированными моноцитами/макрофагами, не несущими признаков злокачественного перерождения. Моноцитарный компонент сопровождается, как правило, инфильтратом из малых лимфоцитов. Часто удается обнаружить феномен гемофагоцитоза, т.е. макрофаги с явлением фагоцитоза клеточных элементов: эритроцитов, реже тромбоцитов и лейкоцитов. На поздних этапах отмечается выраженное обеднение костного мозга с формированием картины аплазии кроветворения.
· Иммунограмма: низкая или полное отсутствие активности натуральных киллеров (NK-клеток), повышен уровень растворимого рецептора интерлейкина-2 (IL-2) CD25 >2400 U/ml. Исследование дегрануляции НК-клеток на основе экспрессии CD 107а на активированных НК-клетках. Исследование экспрессии перфорина, SAP, XIAP в НК и Т-клетках методом проточной цитометрии.
· Молекулярно-генетическое исследование для дифференциации СЛГЛ и ЛГЛ: мутации гена перфорина (10q21).
· HLA типирование пациента и его семьи
Диагноз ГЛГ является правомочным при наличии мутации гена порфирина при молекулярно-генетическом исследовании и/или при выполнении 5 из 8 условий [2]:
1) лихорадка
2) спленомегалия
3) 2-х или 3-х ростковая цитопения
4) гипертриглицеридемия и/или гипофибриногенемия
5) гемофагоцитоз в пунктате костного мозга или в биопсийном материале лимфоузла или селезенки
6) гиперферритинемия
7) снижение или полное отсутствие активности NK- клеток
8) увеличение уровня растворимого рецептора IL-2 CD25
Инструментальные исследования [3,6]:
· УЗИ органов брюшной полости и забрюшинного пространства – позволяет оценить размеры печени, селезенки, и увеличение лимфоузлов брюшной полости, наличие свободной жидкости в брюшной полости.
· МРТ головного мозга в режиме Т1и, Т2, FLAIR, с контрастированием гадолинием.
Диагностический алгоритм: (схема 1)
Дифференциальный диагноз
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Острый лейкоз | Гиперпластический, анемический, геморрагический синдромы, лихорадка и другие симптомы интоксикации | Исследование миелограммы | Наличие бластной метаплазии в костном мозге более 25% |
| Миелодиспластический синдром | Гиперпластический, анемический, геморрагический синдромы, лихорадка и другие симптомы интоксикации | Исследование миелограммы | Как правило, гиперклеточный костный мозг, дисплазия ростков кроветворения, наличие бластной метаплазии |
| Приобретенная апластическая анемия | Симптомы интоксикации, лихорадка, 2-х или 3-х ростковая цитопения | Исследование миелограммы | костный мозг малоклеточный, ростки кроветворения угнетены, костный мозг полиморфный, бластные клетки |
| Инфекционный мононуклеоз | Лимфопролиферативный синдром, лимфоцитоз, моноцитоз, возможны позитивные IgM, IgG, DNA-EBV | Исследование миелограммы. | Отсутствует гемофагоцитозвмиелограмме |
| Сепсис | Упорная лихорадка, выраженные симптомы интоксикации, возможны 2-х и 3-х ростковые цитопении, коагулопатия | Исследование миелограммы, уровня прокальцитонина | В миелограмме раздражение или угнетение костного мозга, без признаков гемофагоцитоза. Уровень прокальцитонина резко повышен. |
| Синдром Вискотта-Олдрича | Геморрагический синдром, инфекционные осложнения, тромбоцитопения | Сбор анамнеза, Исследование иммунного статуса, миелограмма. Молекулярно-генетические исследования | Сочетание иммунодефицита, тромбоцитопении и атопического дерматита. В миелограмме отсутствует гемофагоцитоз7 Мутация в WASP |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Азитромицин (Azithromycin) |
| Амикацин (Amikacin) |
| Ампициллин (Ampicillin) |
| Амфотерицин B (Amphotericin B) |
| Ацикловир (Acyclovir) |
| Валацикловир (Valacyclovir) |
| Ванкомицин (Vancomycin) |
| Вориконазол (Voriconazole) |
| Ганцикловир (Ganciclovir) |
| Гентамицин (Gentamicin) |
| Дексаметазон (Dexamethasone) |
| Декстроза (Dextrose) |
| Имипенем (Imipenem) |
| Иммуноглобулин G человеческий нормальный (Immunoglobulin G human normal) |
| Каспофунгин (Caspofungin) |
| Кларитромицин (Clarithromycin) |
| Левофлоксацин (Levofloxacin) |
| Линезолид (Linezolid) |
| Меропенем (Meropenem) |
| Метотрексат (Methotrexate) |
| Метронидазол (Metronidazole) |
| Микафунгин (Micafungin) |
| Натрия хлорид (Sodium chloride) |
| Нистатин (Nystatin) |
| Омепразол (Omeprazole) |
| Офлоксацин (Ofloxacin) |
| Преднизолон (Prednisolone) |
| Ранитидин (Ranitidine) |
| Сульбактам (Sulbactam) |
| Сульфаметоксазол (Sulphamethoxazole) |
| Триметоприм (Trimethoprim) |
| Флуконазол (Fluconazole) |
| Цефепим (Cefepime) |
| Цефоперазон (Cefoperazone) |
| Цефтазидим (Ceftazidime) |
| Цефтриаксон (Ceftriaxone) |
| Цефуроксим (Cefuroxime) |
| Циклоспорин (Cyclosporine) |
| Ципрофлоксацин (Ciprofloxacin) |
| Эртапенем (Ertapenem) |
| Этопозид (Etoposide) |
Группы препаратов согласно АТХ, применяющиеся при лечении
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
посиндромная терапия с целью обеспечения транспортабельности больного в специализированное отделение.
Немедикаментозное лечение [3,6,7]: режим и диета зависит от тяжести состояния пациента.
· Режим – палатный.
· Диета – Стол №11, стол №1Б, стол №5П (с исключением острых, жирных, жареных блюд, обогащенная белком).
Медикаментозное лечение.
Терапия на догоспитальном этапе зависит от наличия того или иного синдрома, имеющего место у больного:
· анемический синдром требует заместительной терапии одногруппной лейкофильтрованной эритроцитарной взвесью при снижении Нв ниже 80г/л;
· геморрагический синдром – остановка кровотечение, заместительная терапия одногруппнымлейкофильтрованным, вирусинактивированнымтромбоконцентратом. При дефиците плазменных факторов свертывания и ДВС синдроме трансфузия СЗП;
· симптоматическая терапия – адекватная антибактериальная, противогрибковая терапия.
Перечень основных лекарственных средств: нет
Перечень дополнительных лекарственных средств
Хирургическое вмешательство: нет.
Дальнейшее ведение:
Профилактические мероприятия: своевременная терапия инфекционно-септических осложнений в случае вторичного ЛГЛ, медико-генетическая консультация в случае СГЛГ.
Мониторинг состояния пациента:
· контроль основных витальных функций – АД, пульс, частота дыхания, степени сознания;
· контроль показателей гемограммы – эритроциты, Нв, лейкоциты, тромбоциты ежедневно;
· контроль коагулограммы ежедневно.
Индикаторы эффективности лечения
· Ясное сознание;
· Стабильная гемодинамика;
· Отсутствие кровотечения;
· стабильные показатели гемограммы (Нв>80г/л, тромбоциты ³30´10 9 /л);
· сохранный диурез.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента
Тактика лечения программная химиотерапия, иммуносупрессивная терапия с последующей трансплантацией гемопоэтических стволовых клеток [2,3,7,8,9,10].
Немедикаментозное лечение:
· Режим: пациенты в изолированные (боксированные) палаты:
— ламинарный поток воздуха,
— изоляция инфекционных больных в палаты с отрицательным давлением;
— личная гигиена и правильная обработка рук (согласно «Руководство ВОЗ по гигиене рук в медико-санитарной помощи”, Женева, 2006 г.) [8];
— при агранулоцитозе туалет полости рта поролоновыми щетками, полоскания антисептиками;
· Диета – низко бактериальная пища, усиленное питание – высококалорийная диета с полуторным по сравнению с возрастными нормами количеством белков, витаминизированная, богатая минеральными веществами. Для детей с различными нарушениями питания включение в питание различных лечебных смесей.
· обеспечение венозного доступа с установкой центрального венозного катетера (из тефлона). Смена катетера по леске запрещается. Применение катетеров из полиэтилена запрещается. Уход за центральным катетером осуществляется обученным медицинским персоналом.;
Медикаментозное лечение [2]:
· Терапия состоит из инициального 8-недельного курса комбинированной иммуносупрессивной и химиотерапии, затем продолженная иммуносупрессивная и химиотерапия до подбора донора для ТГСК и проведения ТГСК. Инициальная терапия включает длительную терапию дексаметазоном, циклоспорин и этопозид, а для некоторых пациентов (с поражением ЦНС) – интратекальная терапия метотрексатом и преднизолоном.
· сопроводительная антибактериальная, противогрибковая, противовирусная терапия, заместительная терапия, направленная на профилактику и лечение инфекционных осложнений. Лечение сопутствующих инфекционных и других осложнений осуществляется согласно Протоколам терапии соответствующих нозологий 19.
Схема инициальной терапии (1-8 недели):
· Дексаметазон назначается перорально в 3 приема (при невозможности перорального приема внутривенно). Доза дексаметазона в 1,2 недели 10мг/м 2 /день, в 3,4 недели – 5мг/м 2 /день, в 5,6 недели – 2,5 мг/м 2 /день, в 7,8 недели – 1,25 мг/м 2 /день/
· Этопозид назначается внутривенно капельно 1-3 часа, разводится на 0,9% хлорида натрия или 5% растворе глюкозы из расчета 0,4мг/мл раствора. В случае инициальнойнейтропении (абсолютное количество нейтрофилов
| Возраст | 1-2 года | 2-3 года | >3 лет | |
| Метотрексат | 6 мг | 8 мг | 10 мг | 12 мг |
| Преднизолон | 4 мг | 6 мг | 8 мг | 10 мг |
Схема продолженной терапии(9-24 недели, 25-40 недели): 
· Дексаметазон 10мг/м 2 /день пульс-терапия по 3 дня каждые 2 недели перорально в 3 приема;
· Этопозид 150мг/м 2 внутривенно капельно 1-3 часа, вводится каждые 2 недели, разводится на 0,9% хлорида натрия или 5% растворе глюкозы из расчета 0,4мг/мл раствора;
· Циклоспорин назначается под контролем функции почек внутрь в 2 приема, доза зависит от уровня циклоспорина в сыворотке крови. Необходимый уровень циклоспорина, который рекомендуют поддерживать 200 микрограмм/мл.
Предлагаются 4 стратегии лечения, и лечение может быть редуцировано и остановлено, если нет реактивации:
1) продолжить продолженную терапию до 40 недель;
2) продлить интервал между каждой инфузиейэтопозида и пульс-терапиейдексаметазона от 2 до 4 недель, продолжить терапию циклоспорином как ранее. Таким образом, пациенты получают альтернирующую терапию каждую вторую неделю (не еженедельно) введениями этопозида и пульс-терапиейдексаметазона;
3) исключить из терапии этопозид, продолжить терапию дексаметазоном и циклоспорином А, в дозах и интервалах, рекомендуемых для продолженной терапии на 9-40 неделях;
4) исключить из терапии этопозид, продолжить терапию дексаметазоном или циклоспорином А в монотерапии.
Перечень основных лекарственных средств:
Хирургическое лечение:
Процедура Аллогенной трансплантации гемопоэтических стволовых клеток – является обязательной для первичных форм ЛГЛ, для прогрессирующих и персистирующих форм ЛГЛ, не имеющих генетической верификации. В случае разрешающихся форм ЛГЛ, не имеющих генетической верификации, АллоТГСК проводится при реактивации заболевания после окончания продолженной терапии. В случае отсутствия совместимого донора как альтернатива возможна гаплоидентичная АллоТГСК [21,22] (УДА).
Дальнейшее ведение
· соответствует наблюдению пациентов после АллоТГСК [21].
Индикаторы эффективности лечения [2]:
Клинический ответ (оценивается на 2-4 неделе терапии):
· отсутствие лихорадки;
· редукция размеров селезенки;
· тромбоциты ³100´10 9 /л;
· нормальный уровень фибриногена;
· редукция уровня ферритина (на 25%).
Оценка ответа в решающие точки и в дальнейшем на терапии через 8 недель (резолюция):
Неактивное заболевание:
· нет лихорадки;
· нет спленомегалии;
· нет цитопении (Нв³90г/л, тромбоциты³100´10 9 /л, абсолютное количество нейтрофилов ³0,5´10 9 /л);
· нет гипертриглицеридемии ( 9 /л;
· гипертриглицеридемия (³3 ммоль/л или ³265 мг/дл);
· гипофибриногенемия£1,5 г/л;
· повышение уровня ферритина;
· CD25³2400 U/ml.
· развитие новых ЦНС симптомов достаточно рассматривать как единственный критерий реактивации заболевания
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
· при ранее установленном диагнозе повторная госпитализация на очередной курс терапии.
Показания для экстренной госпитализации:
· при подозрении на ГЛГ для первичной диагностики и лечения, а также в случае реактивации заболевания при уже установленном диагнозе.
Информация
Источники и литература
Информация
| п/о | перорально |
| АллоТГСК | аллогенная трансплантация гемопоэтических стволовых клеток |
| АЧТВ | активированное частично тромбопластиновое время |
| ВИЧ | вирус иммунодефицита человека |
| ВВИГ | внутривенные иммуноглобулины |
| ВОЗ | всемирная организация здравоохранения |
| ВПГ | вирус простого герпеса |
| ГЛГ | Гемофагоцитарный лимфогистиоцитоз |
| ГФС | Гемофагоцитарный синдром |
| ИФА | иммуноферментный анализ |
| ИТ | интратекальная терапия |
| КТ | компьютерная томография |
| ЛДГ | лактатдегидрогеназа |
| МНН | международное непатентованное название |
| МНО | международное нормализованное время |
| МРТ | магнитно-резонансная томография |
| ОАК+тромбоциты | общий анализ крови с подсчетом лейкоформулы и тромбоцитов |
| ОАМ | общий анализ мочи |
| ПЦР | полимеразная цепная реакция |
| ПВ | протромбиновое время |
| ПТИ | протромбиновый индекс |
| ПДФ | продукты деградации фибринолиза |
| РКИ | Рандомизированные клинические исследования |
| РК | Республика Казахстан |
| СГЛГ | семейный гемофагоцитарныйлимфогистиоцитоз |
| СОЭ | скорость оседания эритроцитов |
| ТГСК | трансплантация гемопоэтических стволовых клеток |
| УЗИ | ультразвуковое исследование |
| УД | уровень доказательности |
| ЦНС | центральная нервная система |
| ЦНС | центральная нервная система |
| ЦсА | циклоспорин А |
| ЭБВ | Эбштейн-Барр вирус |
| ЭКГ | электрокардиография |
| ЭхоКГ | эхокардиография |
| Hb | гемоглобин |
| HLA | Human leukocytes antigen (система человеческих лейкоцитарных антигенов) |
| IL | Интерлейкин |
| CD | кластеры дифференцировки (моноклональные антитела) |
| NK | натуральные киллеры |
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола
1) Манжуова Лязат Нурбапаевна –кандидат медицинских наук, заведующий отделением онкогематологии, РГП на ПХВ«Научный центр педиатрии и детской хирургии».
2) Омарова Кулян Омаровна – профессор, доктор медицинских наук, РГП на ПХВ«Научный центр педиатрии и детской хирургии».
3) Булабаева Гульнара Ержановна – заведующая отделением онкогематологии РГП на ПХВ «Научный центр педиатрии и детской хирургии».
4) Нургалиев Даир Жванышевич – доктор медицинских наук, заведующий отделением гематологии АО «Национальный научный центр материнства и детства», г. Астана.
5) Сарсекбаев Ергали Семгалиевич – врач отделения ТГСК РГП на ПХВ«Научный центр педиатрии и детской хирургии».
6) Калиева Шолпан Сабатаевна – кандидат медицинских наук, PHD, доцент, заведующая кафедрой клинической фармакологии и доказательной медицины РГП на ПХВ «Карагандинский государственный медицинский университет».
Указание на отсутствие конфликта интересов:нет.
Список рецензентов:
1) Ташенова Гульнара Талиповна – доктор медицинских наук, заведующий кафедрой детских болезней №2, Казахский научный медицинский университет имени С.А.Асфендиарова.