гайро или орнидазол что лучше
Бактериальный вагиноз
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагиналь
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагинального эпителия осуществляется на клеточном и молекулярном уровнях и постоянно контролируется со стороны ряда систем макроорганизма. Результатом этого взаимодействия являются создание и поддержание высокой колонизационной резистентности вагинального эпителия к внедрению патогенных и условно-патогенных микроорганизмов [1–6].
Бактериальный вагиноз выделен из категории неспецифических вагинитов в отдельную нозологическую форму. К нему относят патологические состояния во влагалище, сопровождающиеся нарушениями качественного и количественного состава нормальной микрофлоры и не связанные с бактериальными инфекциями, передаваемыми половым путем (ИППП), грибами или простейшими.
Согласно современным представлениям, бактериальный вагиноз — инфекционный невоспалительный синдром полимикробной этиологии, который связан с дисбиозом вагинального биотопа. Нарушение микроэкологии влагалища при бактериальном вагинозе характеризуется резким снижением количества или отсутствием лактобактерий, продуцирующих перекись водорода и увеличением количества Gardnerella vaginalis, грамотрицательных анаэробных бактерий (Bacteroides spp., Mobiluncus spp., Fusobacterium spp., Peptostreptoicoccus spp., M. hominis, U. urealyticum).
Гарднереллы, как и лактобациллы, обладают выраженной способностью к адгезии на поверхности вагинальных эпителиоцитов. Gardnerella vaginalis могут продуцировать токсические биопродукты, к которым относятся муколитические ферменты и гемолизин, являющийся лейкотоксическим фактором. Гемолизин, воздействуя на эритроциты, вызывает образование многочисленных пор в эритроцитарной мембране, а также оказывает влияние на лейкоциты, вызывая их структурные и функциональные нарушения. Этим и объясняется отсутствие существенной лейкоцитарной инфильтрации, т. е. активности лейкоцитов в присутствии Gardnerella vaginalis.
Определенную роль в патогенезе бактериального вагиноза играют представители семейства Mycoplasmataceae — Mycoplasma hominis и Ureaplasma urealyticum. 70% выделенных штаммов Ureaplasma urealyticum относятся к биовару Parvo, 23,3% — к биовару Т960. Большинство пациенток, у которых была выделена Ureaplasma urealyticum, относящаяся к биовару Parvo, имели в прошлом раннее начало половой жизни, частую смену половых партнеров, наличие одновременно нескольких половых партнеров, большое количество беременностей и абортов, а также сопутствующие гинекологические заболевания и ИППП.
При обследовании половых партнеров пациенток с бактериальным вагинозом морфотипы ассоциированных с бактериальным вагинозом микроорганизмов выявлялись у 25% мужчин, при этом клинические проявления (баланопостит) наблюдались только у 3,1% [2].
В результате субмикроскопического исследования вагинального экссудата пациенток с бактериальным вагинозом определены структурно-функциональные особенности микробных клеток, участвующих во взаимодействии друг с другом, при этом клетки организма-хозяина представлены преимущественно плоским эпителием. Установлена грамвариабельность Gardnerella vaginalis вне зависимости от характера микробных ассоциаций. Анализ электронограмм продемонстрировал, что структурная организация Gardnerella vaginalis, адгезированных на поверхности эпителиальных клеток, не зависела от сочетания бактериального вагиноза с другими инфекционными агентами.
При сочетании бактериального вагиноза с Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum наблюдали значительное количество микроорганизмов в межклеточном пространстве и бактерий, морфологически идентичных микоплазмам [2].
Пациентки предъявляют жалобы на обильные выделения из половых путей белого или серого цвета, часто с неприятным запахом, особенно после полового акта или во время менструации. При длительно текущем процессе выделения приобретают желтовато-зеленую окраску, становятся более густыми, нередко напоминают творожистую массу, обладают свойством пениться; слегка тягучие и липкие, они равномерно распределяются по стенкам влагалища. Количество белей варьирует от умеренных до весьма обильных, составляя в среднем 20 мл в сутки. Жалобы на зуд и дизурические расстройства встречаются редко: они могут совсем отсутствовать или появляться периодически. Эти симптомы обнаруживаются у 16–23% пациенток с нарушениями микрофлоры влагалища. Характерным признаком бактериального вагиноза является отсутствие воспалительного процесса стенок влагалища. Нередко женщины с бактериальным вагинозом жалуются на обильное менструальное кровотечение, боли в низу живота. В то же время у части пациенток какие-либо субъективные ощущения отсутствуют.
Диагностика бактериального вагиноза основана на данных анамнеза, оценке субъективных и объективных симптомов заболевания, результатах лабораторных тестов — микроскопического исследования материала, аминного теста и рН вагинального экссудата [3].
При сборе анамнеза выясняют:
Диагноз бактериального вагиноза устанавливается на основании наличия трех критериев из нижеперечисленных:
Обследование пациентки следует проводить не ранее, чем через 72 ч после последнего полового контакта (без использования презерватива); оно не проводится также во время менструации. В течение 3 нед до обследования женщина не должна получать терапию системными и местнодействующими антибактериальными препаратами [3].
При микроскопическом исследовании нативного и окрашенного по Граму вагинального мазка определяются следующие признаки:
Оценка общей микробной обсемененности вагинального отделяемого проводится по 4-балльной системе — по числу микробных клеток, обнаруживаемых в одном поле зрения при иммерсионной микроскопии:
1 балл (+) — до 10 микробных клеток в поле зрения, незначительное их количество (скудный рост);
2 балла (++) — от 11 до 100 микробных клеток в поле зрения, умеренное их количество;
3 балла (+++) — от 100 до 1000 микробных клеток в поле зрения, большое их количество;
4 балла (++++) — более 1000 микробных клеток в поле зрения, массивное их количество.
Так как Gardnerella vaginalis может быть обнаружена у здоровых женщин, культуральное исследование и ПЦР-диагностику для идентификации Gardnerella vaginalis не проводят. Культуральное исследование проводят при наличии показаний для определения видового и количественного состава вагинального микроценоза и исключения возбудителей ИППП.
При культуральном исследовании могут быть обнаружены изменения, характерные для бактериального вагиноза: общая микробная обсемененность превышает 10 9 КОЕ/мл; при использовании только аэробных условий культивирования рост микроорганизмов отсутствует или наблюдается рост сопутствующих условно-патогенных микроорганизмов (чаще в небольшом титре); полимикробный характер микрофлоры с абсолютным преобладанием облигатно-анаэробных видов и Gardnerella vaginalis; отсутствие роста лактобацилл или резкое снижение их титра ( 4 КОЕ/мл).
На основании проведенных исследований в настоящее время рекомендуется в план ведения пациенток включать:
Целью лечения является уменьшение выраженности клинических симптомов, нормализация лабораторных показателей, предотвращение развития возможных осложнений в период беременности, а также в послеродовом периоде и при выполнении инвазивных гинекологических процедур.
Результаты лабораторных исследований в норме следующие.
Лечение
Основное направление терапии — применение местных или системных антибактериальных препаратов с антианаэробным эффектом.
Показано применение клиндамицина. Препарат является 7-дезоксипроизводным линкомицина, ингибирует синтез белков в микроорганизмах, оказывает бактериостатическое или бактерицидное действие в зависимости от концентрации в макроорганизме и чувствительности микроорганизма. Препарат эффективен в отношении грамположительных микроорганизмов (стафилококков, стрептококков, пневмококков, палочки дифтерии), гарднерелл, микоплазм. Устойчивость микроорганизмов к клиндамицину вырабатывается медленно. При приеме внутрь клиндамицин всасывается лучше, чем линкомицин. После внутримышечного введения максимум его концентрации в крови отмечается через 2–2,5 ч. Препарат хорошо проникает в жидкости и ткани организма, выводится с мочой и желчью. При нарушении функции почек и печени выведение клиндамицина замедляется. При бактериальном вагинозе можно назначать одну из лекарственных форм клиндамицина: крем 2%-ный 5 г в аппликаторе (разовая доза) интравагинально 1 раз в день (на ночь) в течение 6 дней; овули 100 мг интравагинально на ночь в течение 3 дней; капсулы 300 мг внутрь 2 раза/сут в течение 7 дней.
Клиндамицин разрешенн к применению у беременных в виде 2%-го крема 5 г (разовая доза) интравагинально 2 раза/сут в течение 5 дней.
Также при бактериальном вагинозе можно назначать метронидазол. Он обладает широким спектром действия в отношении простейших, подавляет развитие Trichomonas vaginalis, Entamoeba histolytica и лямблий. В отношении анаэробных бактерий препарат высокоэффективен. Метронидазол хорошо всасывается при приеме внутрь, проникает в органы и ткани, проходит через плаценту и гематоэнцефалический барьер, накапливается в печени. Период полувыведения препарата составляет 8–10 ч, полностью выводится из организма через 1–2 сут после введения. Метронидазол в основном выводится с мочой в неизмененном виде и в виде метаболитов, частично — с калом. При применении метронидазола могут отмечаться потеря аппетита, сухость и неприятный вкус во рту, тошнота, рвота, диарея, головная боль, крапивница, зуд. Эти явления проходят после окончания лечения или отмены препарата. Возможна лейкопения. Препарат противопоказан при беременности и кормлении грудью, нарушениях кроветворения, остром течении заболеваний центральной нервной системы. Во избежание развития тяжелых побочных реакций следует предупреждать пациентов о недопустимости приема алкоголя и содержащих его продуктов как в ходе терапии метронидазолом, так и в течение 24 ч после ее окончания. При бактериальном вагинозе можно применять одну из следующих схем лечения с использованием метронидазола:
Также используют и другие производные метронидазола:
Ранее было проведено сравнительное изучение эффективности местнодействующих пробиотиков. Поскольку не было выявлено достоверных отличий в результатах лечения у пациенток, получавших и не получавших эти средства, в настоящее время их не рекомендуют при лечении бактериального вагиноза [3].
При сочетании бактериального вагиноза с ИППП, одновременно применяют антибактериальные препараты в соответствии с нозологической формой заболевания [2]. При неосложненной гонорейной инфекции назначают цефтриаксон однократно внутримышечно в дозе 250 мг (препарат является цефалоспориновым антибиотиком III поколения; после внутримышечного введения пик концентрации в крови отмечается через 1,5 ч; из организма выводится медленно). При обнаружении хламидий и/или микоплазм показано применение антибиотиков — макролидов, тетрациклинов.
Высокий терапевтический эффект, хорошая переносимость способствовали значительному распространению применения макролидов. Их антимикробный эффект обусловлен нарушением синтеза белка в рибосомах микробной клетки. Как правило, макролиды оказывают бактериостатическое действие, но в высоких концентрациях способны вызывать и бактерицидный эффект. Кроме антибактериального действия, макролиды обладают умеренной иммуномодулирующей и противовоспалительной активностью. Представителем III поколения макролидов является джозамицин (Вильпрафен). Этот антибиотик быстро абсорбируется из желудочно-кишечного тракта (ЖКТ), хорошо проникает через биологические мембраны и накапливается в тканях. Максимальная концентрация достигается через 1–2 ч после приема. Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2,41 мг/л; связывание с белками плазмы не превышает 15%. Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2–4 дня регулярного приема. Концентрация джозамицина в полиморфонуклеарных лейкоцитах человека, моноцитах и альвеолярных макрофагах примерно в 20 раз выше, чем в других клетках организма. Препарат биотрансформируется в печени до менее активных метаболитов. Джозамицин выводится главным образом с желчью, выведение же с мочой составляет менее 20%. Препарат назначается по 500 мг 2 раза в день в течение 10 дней.
Из группы тетрациклинов при ИППП наиболее эффективен доксициклин; в последние годы широко применяется Юнидокс Солютаб. Препарат отличается от Доксициклина гидрохлорида нейтральной реакцией, оказывает меньшее раздражающее действие на слизистую оболочку пищеварительного тракта и обладает улучшенными противомикробными и фармакокинетическими свойствами. Юнидокс Солютаб блокирует рибосомальную полимеразу и тормозит синтез белка в микроорганизмах.
Таблетки Юнидокс Солютаб обладают контролируемой растворимостью. Их можно не только принимать внутрь целиком или по частям, но и быстро приготовить из них сироп, суспензию (растворив таблетку в 20 мл воды) или раствор (растворив таблетку в 100 мл воды), которые обладают приятным вкусом. Таблетки растворяются в воде в течение 5–10 с, в биологических жидкостях — в течение 1 мин, превращаясь в равномерную суспензию.
Юнидокс Солютаб всасывается полностью. Биодоступность препарата составляет 95%. Через 2 ч после приема (200 мг в первый день и 100 мг в последующие дни) уровень в сыворотке составляет от 1,5 до 3 мг/мл. Препарат на 80–90% связывается с белками плазмы, хорошо проникает в ткани, накапливается в ретикулоэндотелиальной системе. Период полувыведения составляет 16–18 ч, после приема повторных доз — 22–23 ч.
Ранее были отмечены преимущества, заключающиеся в отсутствии побочных эффектов по типу эзофагитов, встречающихся при применении обычных форм Доксициклина гидрохлорида, способности накапливаться в высоких концентрациях в репродуктивных органах и активно воздействовать на инфекционный агент.
Юнидокс Солютаб назначают в дозе 200 мг в течение 10 дней.
Лабораторный контроль эффективности терапии следует проводить непосредственно по окончании этиотропного лечения: при микроскопии вагинальных мазков, окрашенных по Граму, необходимо констатировать степень эрадикации микроорганизмов, ассоциированных с бактериальным вагинозом; при посеве вагинального отделяемого — выявлять случаи колонизации факультативно анаэробными условно-патогенными микроорганизмами.
При сочетании бактериального вагиноза с урогенитальным хламидиозом и/или микоплазмозом лабораторный контроль необходимо повторить через 3 нед по окончании терапии.
По вопросам литературы обращайтесь в редакцию.
И. В. Хамаганова, доктор медицинских наук, профессор
РГМУ, Москва
Гайро : инструкция по применению
Лекарственная форма
Таблетки, покрытые пленочной оболочкой 500 мг
Состав
Одна таблетка содержит,
вспомогательные вещества: целлюлоза микрокристаллическая, лактозы моногидрат, кремния диоксид коллоидный безводный, повидон (К-30), натрия лаурилсульфат, тальк, магния стеарат, натрия кроскармеллоза,
состав пленочной оболочки Опадри II зеленый: поливинил частично спиртовогидролизированный E1203, тальк E553b, титана диоксид Е171, макрогол/полиэтиленгликоль Е1521, лецитин Е322, хинолиновый желтый Е104, бриллиантовый синий Е133
Описание
Двояковыпуклые, продолговатой формы таблетки, покрытые пленочной оболочкой, зеленого цвета с линией разлома на одной стороне и гладкой поверхностью – на другой
Фармакотерапевтическая группа
Препараты для лечения амебиаза и других протозойных инфекции. Нитроимидазола производные. Орнидазол
Фармакологические свойства
После приема внутрь орнидазол быстро всасывается в желудочно-кишечном тракте. В среднем, всасывается 95% препарата. Максимальные концентрации в плазме крови достигаются в пределах 3-х часов.
Связывание с белками крови составляет около 13%. Активное вещество проникает в спинномозговую жидкость, в грудное молоко, проходит через гематоэнцефалический барьер (ГЭБ) и плаценту. Концентрация препарата в плазме крови варьирует в пределах 6-36 мг/л. Орнидазол метаболизируется в печени путем гидрооксилирования, окисления и глюкуронирования с образованием 2-гидроксиметил и альфа-гидроксметил метаболитов. Оба метаболита менее активны в отношении Trichomonas vaginalis и анаэробных бактерий, чем неизмененный орнидазол.
Период полувыведения составляет около 13 часов. После однократного приема, 85 % дозы выводится через почки в течение первых пяти дней, главным образом, в виде метаболитов.
Гайро – противопротозойное средство, производное 5-нитроимидазола. Механизм действия заключается в биохимическом восстановлении 5-нитрогруппы орнидазола внутриклеточными транспортными протеинами анаэробных микроорганизмов и простейших. Восстановленная 5-нитрогруппа орнидазола взаимодействует с ДНК- микроорганизмов и ингибирует синтез нуклеиновой кислоты, что ведет к гибели бактерий.
Показания к применению
— трихомониаз (мочеполовые инфекции у женщин и мужчин, вызванные Trichomonas vaginalis)
— амебиаз (все кишечные инфекции, вызванные Entamoeba histolytica, в том числе амебная дизентерия, а также все некишечные формы амебиаза, в особенности, амебный абсцесс печени)
— профилактика анаэробных инфекций при хирургических вмешательствах, особенно на толстой кишке или органах малого таза
Способ применения и дозы
Таблетки принимают внутрь после еды.
При лечении трихомониаза у взрослых применяются две схемы комбинированной терапии
1 вагинальная таблетка (Гайро) перед сном
500 мг (1 таб.) утром 500мг (1 таб.) вечером внутрь
500 мг (1 таб.) утром 500 мг (1 таб.) вечером внутрь+1вагинальная таб. (Гайро) перед сном
При других формах амебиаза взрослым назначают внутрь по 500мг 2 раза/сут. (1 таб. утром и 1 таб. вечером).
Курс лечения 5-10 дней.
Для профилактики назначают 500мг перед операцией и по 500мг 2 раза/сут после операции в течение 1-5 дней.
Побочные действия
— головокружение, головная боль, сонливость
— желудочно-кишечные расстройства (в т. ч тошнота), диспепсия
— лейкопения (при длительном лечении)
— дрожание, ригидность, нарушение координации движений, судороги и нарушение сознания, нарушения вкуса, атаксия
— отклонение от нормы показателей функции печени
— реакции гиперчувствительности, (кожная сыпь, зуд)
— симптомы сенсорной или смешанной периферической нейропатии, (чувство жжения, онемения конечностей, парестезии)
Противопоказания
— повышенная чувствительность к орнидазолу и другим производным нитроимидазола в анамнезе, а также другим компонентам препарата
— беременность и период лактации
— заболевания центральной нервной системы (эпилепсия, поражение головного мозга, рассеянный склероз)
— детский и подростковый возраст до 18 лет
Лекарственные взаимодействия
При совместном применении Гайро с другими производными
5-нитроимидазола могут наблюдаться периферическая невропатия, депрессия и эпилептоформные судороги.
Гайро не ингибирует альдегиддегидрогеназу и поэтому не взаимодействует с алкоголем.
Одновременное применение с индукторами микросомальных ферментов (барбитураты, бензодиазепины, рифампицины и т.д.) сокращает период полураспада орнидазола в сыворотке. Ингибиторы микросомальных ферментов (циметидин, макролиды и т.д.) увеличивают период полураспада орнидазола.
Гайро усиливает действие противосвертывающих средств, что требует коррекции их дозы.
Не рекомендуется комбинация Гайро с нейротоксичными и
Особые указания
Больные с нарушением функции печени. У больных с циррозом печени период полувыведения орнидазола удлиняется (22 часа вместо 14 часов) и снижен клиренс (35 вместо 51 мл/мин) по сравнению со здоровыми лицами. Интервал дозирования у больных с тяжелой недостаточностью функции печени должен быть удвоен.
Следует соблюдать осторожность у больных с заболеваниями ЦНС, например, с эпилепсией или рассеянным склерозом.
При трихомониазе следует проводить одновременное лечение полового партнера во избежание повторного инфицирования.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами. С учетом возможных побочных эффектов, таких как головокружение, необходимо соблюдать осторожность при управлении транспортным средством и работе с движущими механизмами
Передозировка
Симптомы: эпилептиформные судороги, депрессия, периферический неврит.
Лечение: симптоматическое (при судорогах диазепам).
Форма выпуска и упаковка
По 10 таблеток помещают в контурную ячейковую упаковку из пленки поливинилхлорида и фольги алюминиевой.
По 1 контурной ячейковой упаковке вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку картонную.
10 пачек картонных помещают в пачку картонную.
Условия хранения
Хранить в сухом, защищенном от света месте при температуре ниже 30°С.
Проблемы терапии трихомониаза и возможные пути решения
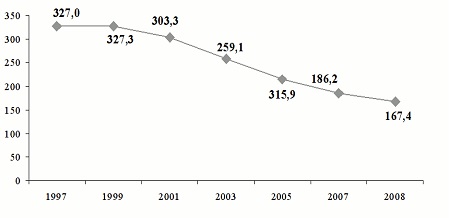
Из числа инфекций, передающихся преимущественно половым путем, ведущее место занимает мочеполовой трихомониаз. По данным Ивановой М.А., Виноградовой С.А. с соавторами за период с 1997 по 2008 гг. наибольшую долю в структуре заболеваемости ИППП занимал трихомониаз. Пик заболеваемости трихомониазом был отмечен в1995 г. (344,3 на 100 тыс. населения). С2000 г. вновь началось снижение показателей с 319,7 (в2000 г.) до 167,4 на 100 000 населения в2008 г.
Рис. 3. Динамика заболеваемости урогенитальным трихомониазом в Российской Федерации за 1997-2008 гг. (на 100 000 соотв. населения)
Превышение среднероссийского показателя сегодня отмечается в Сибирском (293,7 на 100 000 населения) и Уральском (181,4 на 100 000 населения) федеральных округах.
Распространенность трихомониаза велика и до конца не учтена. Еще в1962 г. И.И. Ировец сообщал, что трихомониазом поражено до 10% населения Земли.
По суммарным данным ВОЗ, в мире ежегодно заболевают 180-200 млн человек. Среди проституток, а также женщин с белями процент больных МТ достигает 70-80%; при скрининговом обследовании различных контингентов выявлялось до 5—30% женщин, больных трихомониазом, и до 6-15% мужчин — носителей трихомонад.
Значимость трихомонадной инфекции обусловлена не только ее широкой распространенностью, но и способностью вызывать ряд тяжелых осложнений.
Необходимо также учитывать тот факт, что трихомонады могут фагоцитировать и резервировать различные патогенные и условно-патогенные микроорганизмы, способствуя распространению других ИППП).
Клиническая картина мочеполового трихомониаза, по мнению ряда авторов, претерпевает патоморфоз, характеризуясь, обилием стертых и малосимптомных форм.
В ходе практической работы и при обзоре литературных данных нами отмечены возможные основные причины неудачного лечения трихомониаза и увеличение количества рецидивов заболевания:
Вот уже 50 лет метронидазол используется в лечении трихомониаза и анаэробных инфекций. По литературным данным, неэффективность лечения трихомониаза метронидазолом составляет до 44%.
Некоторые авторы приводят более впечатляющие результаты; так, по данным дерматовенерологической клиники Новосибирского мединститута, в 1995-1996 гг. рецидивы после полноценного лечения нитроимидазолами достигали 47%.
Уже опубликованы сообщения о более чем 100 резистентных к метронидазолу штаммах из США, порядка 20 устойчивых штаммов описаны европейскими учеными, в том числе российскими.
Описывается также перекрестная устойчивость к тинидазолу и орнидазолу, что свидетельствует о формировании устойчивости ко всей группе 5-нитроимидазолов. В то же время за неимением альтернативных схем лечения предпринимаются попытки лечить трихомониаз, вызванный устойчивыми к метронидазолу штаммами, увеличивая дозировки применяемых схем метронидазола, однако такие попытки редко оказываются успешными.
Известно, что устойчивость – это результат мутации и формирования новых резистентных штаммов. Все чаще появляются публикации, связывающие устойчивость T. vaginalis с ее инфицированием РНК-вирусами. Инфицированные изоляты близки друг к другу при оценке молекулярного строения. Эти изоляты чаще всех остальных оказываются резистентными к группе препаратов 5-нитроимидазолов.
Наиболее сложным вопросом терапии современного трихомониаза является выбор эффективного этиотропного средства. Несмотря на многочисленные публикации результатов изучения эффективности противотрихомонадной терапии, выбор конкретных препаратов на отечественном рынке остается весьма ограниченным.
Таким образом, несмотря на рекомендации, приведенные в отдельных публикациях, отсутствие доказательных данных об эффективности и безопасности препаратов, не принадлежащих к группе 5-НИ, в терапии трихомонадной инфекции, в т. ч. ее рефрактерных форм, не позволяет рекомендовать их использование у пациентов с данной патологией, за исключением случаев, когда другие терапевтические альтернативы исчерпаны.
Обобщение собственного опыта, отечественных и зарубежных дерматовенерологов показывает, что для более успешного лечения трихомониаза необходимо соблюдать следующие положения:
В Европейском руководстве по заболеваниям, передаваемым половым путем, отмечено, что при персистирующих и рецидивирующих симптомах, связанных с урогенитальным трихомониазом, часто у пациенток, у которых первый курс не дает эффекта, эффективным бывает второй курс стандартного лечения метронидазолом. Перед повторным курсом метронидазола необходимо провести эмпирическое лечение эритромицином или амоксициллином для снижения уровня b-гемолитических стрептококков, поскольку некоторые микроорганизмы, присутствующие во влагалище, могут снижать эффективность метронидазола, захватывая активную нитрогруппу. Это и есть так называемая относительная резистентность к терапии, когда излечение наступает после повторного назначения того же метронидазола после устранения, с помощью антибиотиков, кокковой флоры, являющейся истинной причиной неэффективности первого курса терапии.
Если повторно проведенное лечение вновь оказывается неэффективным, то согласно Европейскому руководству по заболеваниям, передаваемым половым путем, эффективного лечения не существует.
необходимости в местном лечении, так как достаточно общего лечения для ликвидации воспалительных явлений и эрадикации возбудителя
Что касается иммунокоррекции при трихомониазе, то следует отметить, что недостаточно изучен иммунопатогенез, роль клеточных, цитокиновых факторов иммунитета и интерферонового статуса.
А в тоже время назначаемые довольно часто иммунотропные и иммуномодулирующие препараты из разных фармокологических групп имеют как ни странно одинаковые показания в терапии хронических форм трихомониаза. Анализ практических и литературных данных позволил нам выделить следующие основные принципы применения иммуномодуляторов:
Перед назначением ИМ целесообразно выявить у больного клинические и лабораторные признаки нарушений иммунитета;
Таким образом, в решении задач излеченности и уменьшения количества рецидивов трихомониаза, мы видим в своевременном выявлении и профилактике вышеназванных причин неудачного лечения и в необходимости применения комплексной терапии, включая оптимальное этиотропное, патогенетическое, физиотерапевтическое, адекватное иммунотропное и местное лечение.