буллезный эпидермолиз что это фото
Синдром бабочки
Заболевание, связанное с генетической аномалией, из-за которой кожа человека не выполняет своей защитной функции, называют синдромом бабочки. Выбор наименования объясняет состояние кожи – она становится ранимой, словно крылья бабочки, которая не полетит после прикосновения к ней человеческих пальцев.
Буллезный эпидермолиз – это
Буллезным эпидермолизом называют заболевание кожи, при котором механические воздействия, даже легкие прикосновения к телу становятся причиной образования волдырей, пузырей и эрозии на коже.
Исследования показали, что это заболевание передается по наследству, но доминантность или рецессивность этой болезни не установлена из-за множества разновидностей синдрома бабочки, одни из которых передаются потомству при разных условиях, в другие передаются через поколение или без точной периодичности.
Чрезмерная нежность кожного покрова приводит к тому, что человек не может вести нормальный образ жизни: любое касание к швам на одежде, предметам мебели, тактильные контакты с другими людьми приводят к разрыву эпидермиса или образованию пузырей. Капилляры, расположенные близко к поверхности кожи, лопаются. Из-за чего возникают необильные кровотечения, которые трудно остановить из-за большой площади поражения.
Кроме того, обработка таких ран тоже представляет определенную сложность, потому что любые контакты только усугубляют состояние раны. В особенно тяжелых случаях можно спастись только если купить спрей с антисептиком. Промыть раны или протереть их ватным диском с обеззараживающим раствором нельзя.
Причины возникновения синдрома бабочки
При прикосновении к коже происходит выброс ферментов, которые разрушают эти белки. Это и становится причиной начала образования пузырьков разного размера. При легкой степени заболевания эти пузыри не разрушают кожу сильно глубоко, но при тяжелых течениях возникают волдыри, разрушающие полностью все слои эпидермиса.
Другой тип синдрома бабочки связывают с мутацией двух других генов: LAMB3 и LAMA3. В редких случаях вместе с ними изменениям подвергаются и другие. Наследование этого типа описывается как рецессивное. От атак со стороны ферментов в этом случае страдают другие белки – разновидность коллагена и ламинина. Их прямое назначение заключается в поддержке структуры самых нижних слоев кожи, поэтому их повреждение отличается специфической клинической картиной – такое течение болезни наиболее сложно переносимо из-за очень глубокого поражения эпидермиса.
Рассматривая дистрофический тип синдрома бабочки, следует отметить, что это менее тяжелое заболевание. Оно обусловлено поражением такого типа коллагена, которые содействует крепости соединительной ткани в слоях кожи. Его разрушение ведет к некоторым высыпаниям и эрозийными повреждениями. Но именно это заболевание считают одним из самых опасных, потому что разрушения этого типа коллагена отражается на поражении других органов, в частности – слизистой оболочки, выстилающей органы дыхания и весь желудочно-кишечный тракт. Рубцы, образовывающие после заживления волокон, часто перерождаются в онкологические заболевания.
Подводя итог, можно отметить, что причина хрупкости кожи, независимо от типа буллезного эпидермолиза, связана напрямую с разрушением белков из-за нарушений ферментарной активности непосредственно в тканях. Болезнь разбили на типы, чтобы объяснять и систематизировать локализацию образования пузырей.
Симптомы буллезного эпидермолиза
Главным характерным симптомом заболевания является появление пузырей на поверхности кожи при малейшем ее касании. Однако следует отметить, что разные типы синдрома бабочки по-разному отражаются на коже.
Существует разновидность буллезного эпидермолиза, при котором волдыри появляются только на определенных участках конечностей. Также существует такой тип болезни, который вызывает лишь мелкую сыпь, но из-за площади ее поражения тяжесть течения не становится легче.
Как правило, генетические нарушения выявляются с младенческого возраста. Что очень усугубляет состояние ребенка. Он, не понимая сложности ситуации, и не контролируя еще свои движения, может сам себе наносить увечья. Основное число заболевших тяжелыми формами синдрома бабочки не доживают и до 5 лет.
Выжившие становятся инвалидами. Они могут приспособиться к жизни, сильно при этом ограничивая себя – исключая тактильные контакты, посещения общественных мест, а часто даже выход из дома. У таких больных, как правило, прогрессирующий кариес, который к определенному возрасту вовсе лишает зубов из-за истончения эмали зубов. Ногти у них не просто становятся ломкими – они выпадают. Кожа и кутикула не способны их удерживать.
Осложнения буллезного эпидермолиза
В связи с тем, что заболевание напрямую связано с поражением кожных покровов широкой площади, первым и самым главным осложнением является присоединение инфекции. В отрытые раны легко занести болезнетворную флору, которая может стать причиной нагноений.
При обширных поражениях глубоких слоев возникает болевой шок. Лечение буллезного эпидермолиза в основном направлено на симптоматику и снижение риска возникновения сепсиса. Раны обрабатываются щадящими анисептическими растворами, а внутрь, в зависимости от возраста больного, могут приниматься препараты группы нестероидных (или стероидных) противовоспалительных средств, обладающих обезболивающим действием.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Помочь тем, кого нельзя обнять
Автор
Редактор
Статья на конкурс «био/мол/текст»: «Мальчик, который остался без кожи». Это не название очередного фильма ужасов. Это документальный фильм режиссера Патрика Коллертона, запечатлевшего последние месяцы жизни 36-летнего Джонни Кеннеди, страдавшего редким генетическим заболеванием — дистрофическим буллезным эпидермолизом. Фильм привлек внимание пяти миллионов зрителей по всей Великобритании и помог собрать 500 000 фунтов стерлингов на благотворительность для международной ассоциации DEBRA, чья деятельность направлена на изучение и лечение буллезного эпидермолиза. Жизнь людей с этим диагнозом и их родных — это путь, который осилит не каждый: он тяжел как физически, так и морально, и требует мужества и невероятной воли к жизни. Детей, страдающих этим недугом, называют детьми-бабочками, сравнивая хрупкость их кожи с хрупкостью крыла бабочки. Что же такое буллезный эпидермолиз и каковы прогнозы на будущее?
Обратите внимание!
Эта работа опубликована в номинации «лучшая обзорная статья» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Я знаю только один способ быть в ладу с собственной совестью: этот способ — не уклоняться от страдания.
Антуан де Сент-Экзюпери
Что такое буллезный эпидермолиз?
Буллезный эпидермолиз (БЭ) — группа редких генетически и клинически гетерогенных заболеваний, характеризующихся образованием пузырей и эрозий на коже и слизистых оболочках в результате незначительной механической травмы [1].
Кожа человека состоит из трех слоев: наружного — эпидермиса, среднего — дермы — и самого нижнего — подкожно-жировой клетчатки (гиподермы) (рис. 1).
Рисунок 1. Строение кожи человека. Рисунок с сайта lechenie-simptomy.ru.
Эпидермис кожи человека состоит из пяти различных слоев эпителиальных клеток, или кератиноцитов, самый нижний из которых — базальный эпителий — прикрепляется к дерме с помощью множества разных белков (рис. 2). Эти белки не только определяют стабильность соединения клеток базального эпителия с дермой, но и их собственную прочность. Мутации в генах, кодирующих эти белки, приводят к снижению прочности этого соединения, делая кожу чрезвычайно чувствительной к механическим воздействиям. Даже самое легкое надавливание — трение швов одежды, нежные объятия матери — может привести к образованию пузырей и причинить нестерпимую боль (рис. 3) [1].
Рисунок 2. Белки, участвующие в патогенезе различных типов наследственного БЭ. ПБЭ — простой БЭ; ПогрБЭ — пограничный БЭ; ДБЭ — дистрофический БЭ; СК — синдром Киндлера; БМ — базальная мембрана. Рисунок из [1], с изменениями.
Рисунок 3. Микроструктура образца кожи больного БЭ. При БЭ соединение между эпидермисом и дермой непрочное. В результате механического воздействия эпидермис отслаивается от дермы. В месте повреждения увеличивается проницаемость капилляров, и жидкая часть крови (плазма), а также клетки, участвующие в воспалении (лейкоциты), выходят в рану — образуется воспалительный экссудат. В месте отслоения формируется пузырь, который увеличится в размерах, если его вовремя не проткнуть стерильной иглой. Рисунок с сайта dermaamin.com, с изменениями.
Как правило, заболевание заметно сразу после рождения ребенка или в первые месяцы его жизни. Каждый новый день — настоящее испытание для больных БЭ и их опекунов: смена повязок, защищающих хрупкую кожу от повреждений и закрывающих уже существующие раны, обработка ран антисептиками — эти жизненно важные, чрезвычайно болезненные и изнурительные процедуры являются практически единственной составляющей современного лечения БЭ. При тяжелых формах заболевание поражает помимо кожных покровов слизистые оболочки и даже внутренние органы. БЭ относится к так называемым орфанным, то есть редким, заболеваниям. Частота встречаемости различных типов БЭ варьирует от 1:30 000 до 1:1 000 000 и зависит от популяции [2].
Классификация
В зависимости от уровня, на котором происходит повреждение кожи, выделяют четыре типа БЭ: простой, пограничный, дистрофический и синдром Киндлера.
Простой БЭ относится к так называемому интраэпидермальному типу БЭ, то есть повреждения затрагивают только эпидермис. Простой БЭ развивается в результате мутаций в генах белков, обеспечивающих прочность клеток базального слоя эпителия (рис. 2). Пузыри образуются ближе к поверхности кожи. Это самая легкая форма БЭ, при которой происходит полноценное заживление ран. Пограничный и дистрофический БЭ относятся к субэпидермальным типам БЭ, поскольку затрагивают не только эпидермис, но и дерму. При этих типах БЭ поврежденными оказываются белки, участвующие непосредственно в соединении двух слоев кожи (рис. 4). Полноценного заживления ран не происходит — на месте нормальной кожи в конечном счете образуются рубцы. Пограничный БЭ, в свою очередь, подразделяется на два типа: Герлиц и не-Герлиц, первый из которых летален. Дистрофический же БЭ в зависимости от типа наследования подразделяется на доминантную и рецессивную формы. Синдром Киндлера относится к смешанному типу БЭ, поскольку пузыри образуются на разных уровнях [1].
Рисунок 4. Иммунофлуоресцентное картирование образца кожи пациента с рецессивным дистрофическим БЭ. Для картирования использовали антитела к коллагену VII (зеленый цвет). а — Пониженное количество коллагена VII в биоптате от пациента с рецессивным дистрофическим БЭ. б — Кожа здорового донора. Ядра клеток окрашены йодидом пропидия (красный цвет). Рисунок из [3], с изменениями.
Диагностика
Для того чтобы подтвердить диагноз БЭ, необходимо провести тщательное обследование пациента. Самым важным этапом диагностики является исследование биоптата поврежденных участков кожи. Для этого используют такие методы, как световая, флуоресцентная и электронная микроскопия, а также генетический анализ.
Исследование с помощью световой микроскопии позволяет отличить интраэпидермальный тип БЭ от субэпидермальных. Для более точного определения уровня повреждения используют электронную и флуоресцентную микроскопии. С помощью электронной микроскопии можно отличить рецессивную форму дистрофического БЭ от доминантной (рис. 5). Так, при рецессивном дистрофическом БЭ наблюдается значительное снижение или полное отсутствие продукции коллагена VII типа, в то время как при доминантном дистрофическом БЭ дефектный белок вырабатывается в нормальном или слегка сниженном количестве. Однако из-за трудоемкости методов электронной микроскопии в настоящее время на первый план выходит микроскопия флуоресцентная. С помощью окрашивания флуоресцентными антителами этот метод позволяет визуализировать белки, участвующие в патогенезе заболевания, а также оценить их продукцию и распределение (рис. 4) [3].
Рисунок 5. Ультраструктура образца поврежденного участка кожи пациента с рецессивным дистрофическим БЭ. Звездочками обозначены места разрывов, расположенные сразу под темной пластинкой базальной мембраны (бесклеточного слоя, отделяющего дерму от эпидермиса), на которую указывают «галочки». Стрелками обозначены участки с единичными фибриллами коллагена VII. Изображение получено методом электронной микроскопии. Рисунок из [3].
Но только генетический анализ (ДНК-диагностику) можно назвать оптимальным методом для определения типа наследования и специфических мутаций, имеющихся у больных БЭ, а также наиболее точным методом различения клинических форм простого, пограничного и дистрофического БЭ [4].
Существует также пренатальная (до рождения) диагностика БЭ, материалом для которой служит ДНК из околоплодной жидкости, забираемая в первом триместре беременности (до 11 недель) [4].
Лечение
К сожалению, в настоящее время БЭ неизлечим. Основная терапия направлена на предотвращение образования новых пузырей и эрозий, лечение ран и предотвращение их инфицирования. Главные задачи лечения — защита хрупкой кожи пациентов от механических воздействий (использование специальных повязок) и обработка уже существующих ран (применение антисептиков, наложение повязок).
Но наука не стоит на месте, и ученые всего мира отчаянно ищут лекарство от страшного недуга. Наиболее проработаны три перспективных вида терапии БЭ: протеиновая, клеточная и генная. Рассмотрим эти подходы подробнее.
Протеиновая терапия
При этом подходе в организм пациента вводится достаточное количество нормального белка. Исследования показали, что внутридермальное введение мышам с рецессивным дистрофическим БЭ очищенного человеческого коллагена VII приводит к формированию нормальных коллагеновых фибрилл в зоне соединения эпидермиса с дермой. При внутривенном введении очищенного белка наблюдается системное отложение коллагена VII в коже. Также было показано, что подобная терапия не только улучшает функциональное состояние кожи, но и способствует заживлению ран. Основываясь на результатах доклинических исследований, компания Lotus Tissue Repair, впоследствии вошедшая в состав Shire Pharmaceuticals, начала проведение расширенных доклинических исследований внутридермальных и внутривенных инъекций коллагена VII на модели рецессивного дистрофического БЭ у собак, а также первую стадию клинических исследований [3, 5].
Клеточная терапия
При этом способе лечения в организм пациента вводится необходимое и достаточное количество клеток, содержащих нормальный ген, кодирующий нужный белок.
Одним из перспективных видов клеточной терапии является внутридермальная инъекция аллогенных (полученных от здоровых доноров) фибробластов. Так, было показано, что подобный подход восстанавливает синтез коллагена VII и стабилизирует соединение эпидермиса с дермой в мышиной модели рецессивного дистрофического БЭ. Следующий шаг на пути к реализации этого вида терапии уже предпринят: нескольким пациентам с рецессивным дистрофическим БЭ были введены аллогенные фибробласты. И хотя спустя две недели после инъекции введенные клетки не обнаруживались, уровень продукции коллагена оставался повышенным как через две недели, так и через три месяца. Ученые считают, что основной терапевтический эффект инъекции аллогенных фибробластов заключается в увеличении продукции эпидермального фактора роста HB-EGF, а также в увеличении экспрессии гена коллагена VII в кератиноцитах и фибробластах реципиента. Однако механизм этого явления пока не установлен [3, 6].
Аллогенная трансплантация костного мозга также может быть перспективным способом лечения БЭ. Так, на мышиной модели рецессивного дистрофического БЭ было показано, что трансплантация костного мозга приводит к облегчению симптомов болезни. Вслед за обнадеживающими результатами были начаты клинические испытания подобного метода терапии. Однако пока результаты неутешительны: пять из двадцати пациентов умерли от прогрессии заболевания или осложнений после трансплантации [3, 6].
Генная терапия
Наконец, последний и, пожалуй, самый перспективный подход — генная терапия (рис. 6). В этом случае пациентам пересаживаются аутологичные (сделанные из собственных клеток) трансплантаты, в клетках которых с помощью методов генетического редактирования дефектный ген заменяется нормальным. И хотя подобная процедура не приводит к полному исцелению, она способна временно устранить симптомы БЭ, а также является относительно простой в техническом отношении.
Рисунок 6. Редактирование собственной ДНК в лечении БЭ. а — Принцип генной терапии. На первом этапе культивируют эпидермальные стволовые клетки из биоптатов кожи пациента с БЭ. Затем стволовые клетки подвергают процедуре генетического редактирования, в результате которой дефектный ген замещается нормальным. После того как пласт из генетически отредактированных кератиноцитов будет проверен на безопасность, его трансплантируют пациентам. б — Трансплантаты, сформировавшиеся из «правильных» кератиноцитов пациента с рецессивным дистрофическим БЭ. Рисунок из [7].
Первые успехи генной терапии были достигнуты в Италии в 2006 году, когда в эпидермальные стволовые клетки пациента с пограничным БЭ с помощью ретровирусной конструкции был доставлен нормальный ген LAMB3, кодирующий одну из субъединиц белка ламинина-332. Из «исправленных» клеток были созданы эпидермальные трансплантаты, которые затем были пересажены на ноги пациента. В результате из них образовалась полноценная в функциональном отношении кожа. Исследование показало, что выживание даже небольшого числа стволовых клеток в подобных трансплантатах приводит к успешному восстановлению нормальных функций кожи. Спустя восемь лет продукция целевого белка LAMB3 в коже пациентов всё еще сохранялась. Не было обнаружено ни пузырей, ни признаков воспаления, опухолевого роста или какого-либо иммунного ответа в области трансплантата. В июле 2014 года в Австрии провели вторую подобную операцию. Профессор Альфред Лэйн из Стэнфордского университета (Калифорния) вместе с сотрудниками начал клинические испытания подобной технологии, нацеленной на восстановление синтеза коллагена VII в эпидермальных стволовых клетках пациента с рецессивным дистрофическим БЭ. Спустя 30 дней после операции в областях трансплантации не было отмечено никаких отклонений, а уровень продукции коллагена VII был гораздо выше исходного [7].
Конечно, и в случае генной терапии существует множество сложностей. Так, замена гена с использованием вирусных конструкций и невирусных систем редактирования ДНК (ZFN, TALEN и CRISPR/Cas9)* связана с риском встраивания гена не в то место генома, которое являлось мишенью. Оценить последствия такого встраивания довольно сложно. Поэтому такой подход требует большой осторожности.
* — Методы ZFN, TALEN и CRISPR/Cas9 основаны на сайт-специфическом действии нуклеаз in vivo. Эти системы обычно состоят из двух модулей, один из которых распознает целевую олигонуклеотидную последовательность, а другой режет цепи ДНК: «А не замахнуться ли нам на. изменение генома?» [8], «CRISPR-системы: иммунизация прокариот» [9], «Мутагенная цепная реакция: редактирование геномов на грани фантастики» [10]. — Ред.
Другая проблема подобной терапии — возможный риск развития иммунного ответа на экспрессируемый новый белок. Особенно велик риск для тех пациентов, чьи клетки несли мутации, полностью исключающие синтез определенного белка. В то же время известно, что у некоторых пациентов с БЭ есть участки кожи, на которых не образуются пузыри и продуцируется повышенный уровень белка. Это явление названо обратным мозаицизмом, или естественной генной терапией, и может предотвращать развитие иммунной реакции на синтезируемый в результате генной терапии белок. Более того, такие «самоизлечившиеся» клетки можно использовать для клеточной терапии, и тогда потребность в генной коррекции исчезнет. Однако до сих пор попытки создать трансплантаты на основе таких клеток у больных с пограничным БЭ не увенчались успехом из-за малого числа подобных клеток в пересаживаемом материале [11].
Заключение
С тех пор как в 1886 году немецкий врач Кебнер впервые употребил термин «буллезный эпидермолиз», многое стало известно о патогенезе этого заболевания. Тем не менее до сих пор основным инструментом терапии является правильный уход за такими больными. Всё дело в том, что разработка и производство лекарств для лечения орфанных заболеваний представляет собой наукоемкий и дорогостоящий процесс, увы, невыгодный с коммерческой точки зрения из-за малого потребительского рынка. К сожалению, государство не в состоянии самостоятельно обеспечить решение этой проблемы. В 1978 году в Великобритании была основана ассоциация DEBRA, в настоящее время насчитывающая более 40 стран-участниц. Деятельность ассоциации направлена в первую очередь на медицинскую и социальную помощь пациентам с БЭ и их родным. Помимо этого, ассоциация финансирует исследования в области БЭ и занимается привлечением общественного внимания к данной проблеме. Представителем ассоциации в России является фонд «Б.Э.Л.А. Дети-бабочки». Именно благодаря совместным усилиям государства и ассоциации DEBRA стало возможным проведение масштабных исследований БЭ. В результате многолетней работы ученых всего мира появилось несколько перспективных подходов к терапии БЭ, а некоторые из них сейчас проходят первую фазу клинических испытаний. И хотя впереди еще несколько этапов тщательных исследований, первые положительные результаты дают надежду пациентам с этим редким генетическим заболеванием.
Содержание
Дерматология в России
Зарегистрируйтесь!
Если Вы врач, то после регистрации на сайте Вы получите доступ к специальной информации.
Если Вы уже зарегистрированы, введите имя и пароль (форма в верхнем правом углу или здесь).
Наследственный буллезный эпидермолиз: новости исследований
Введение – буллезный эпидермолиз, что это?
При некоторых формах буллезного эпидермолиза бывают поражены только небольшие участки кожи, при других – большие по площади участки поражения, на всей коже, часто с вовлечением слизистых оболочек и ногтей. Определенные виды буллезного эпидермолиза вызывают поражение внутренних органов. Наиболее часто страдает желудочно-кишечный тракт в виде непроходимости пищевода, нарушения глотания, сужения пищевода, поносов, запоров, поражений прямой кишки, желудка, ногтей, сращение пальцев, сердца (кардиомиопатия), мышц (дистрофия), глаз (выворот век), повреждение роговицы, зубов (кариес, плохая эмаль) и пр.
Данное заболевание встречается редко. Так, за период 1986-1990 года в Соединенных Штатах было зарегистрировано 19 случаев на 1 млн. новорожденных. Но, несмотря на редкость его возникновения, оно требует активной диагностики, лечения, наблюдения.
Почему возникает буллезный эпидермолиз?
Форма заболевания зависит от пути наследования (доминантного или рецессивного). Простой буллезный эпидермолиз доминантно наследуется, пограничный – рецессивно, а дистрофические формы – как рецессивно, так и доминантно.
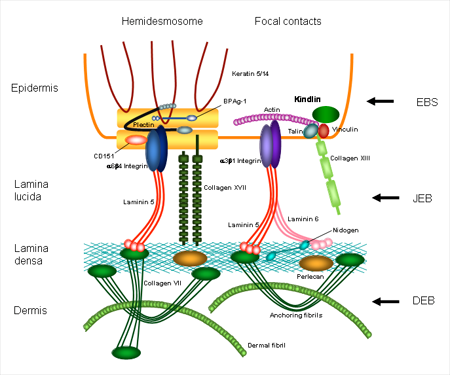
В настоящее время уже известны участки повреждения генов и белки, которые ими кодируются. При простом буллезном эпидермолизе повреждения затрагивают белки кератин 5, кератин 14, плектин, альфа-6,бета-4 интегрин. При пограничной форме заболевания изменения выявляются в белках ламинин 332, коллаген 17 типа, альфа-6,бета-4 интегрин. При дистрофическом буллезном эпидермолизе поражается коллаген 7 типа, при синдроме Киндлера – киндлин – 1. Каждый из этих белков принимает участие в связи верхних и нижних слоев кожи.
Схема «Строение кожи»
Для формирования более полной картины возникновения заболевания приводим данные о значении, функции этих белков в формировании структуры кожи, а также рассмотреть строение тех уровней кожи, на которых могут происходить патологические изменения.
Все перечисленные белки обеспечивают прочность кожи.
Таким образом, происходит нарушение структуры и функции связывающей слои кожи между собой сложного комплекса клеток, волокон и веществ. И если хотя бы один из компонентов этого комплекса оказывается дефектным, прочность кожи страдает.
Классификация
Существует 4 основных типа наследственного буллезного эпидермолиза
Клинические проявления
При буллезном эпидермолизе бывают: легкая травмируемость кожи, пузыри, эрозии, милиумы (крошечные прочные белые горошинки, иногда сгруппированные, утолщение ногтей или их отсутствие, образование атрофических рубцов, утолщение кожи ладоней и подошв, нарушение пигментации (темные или светлые), пятна в местах травмирования псоле заживления,поредение или отсутствие волос, снижение или увеличение потоотделения, пузыри во рту, кариес, сращение пальцев, затруднение глотания, рвота, запоры, снижение массы тела, медленный рост.
Стоит отметить, что несмотря на широкий спектр представленных клинических проявлений, существуют признаки, по которым можно поставить диагноз, не прибегая к другим исследованиям. Так, травмируемость кожи значительно выше при пограничном и дистрофическом буллезном эпидермолизе, чем при простой форме. Характерным признаком пограничного типа заболевания является дефект эмали.
Простой буллезный эпидермолиз
Данный тип буллезного эпидермолиза делится на 2 большие группы:
При локализованной форме (ранее известная как болезнь Вебера-Кокейна) пузыри образуются на кистях и стопах. Первые клинические признаки появляются в период полового созревания. Но при данной форме заболевания в младенчестве на слизистой оболочке полости рта могут возникать бессимптомные пузыри и эрозии. Поэтому периодически необходимо осматривать слизистую оболочку рта младенцев.
Генерализованные формы разделяются на 2 подгруппы – герпетиформный буллезный эпидермолиз (Dowling-Meara) и негерпетиформный буллезный эпидермолиз (Кебнера). При первой форме заболевания пузыри располагаются в виде групп, а при второй форме такой особенности нет. Еще одно важное отличие этих двух подтипов то, что при буллезном эпидермолизе Кебнера, как правило, кисти и стопы не поражаются, а при Dowling-Meara, наоборот, пузыри есть, практически всегда, как на кистях руках, так и на стопах. При буллезном эпидермолизе Dowling – Meara характерен значительный риск развития рака кожи, при буллезном эпидермолизе Кебнера риск развития рака минимален.
Милиумы, образование рубцов, а также повреждение ногтей обычно не характерны для простого буллезного эпидермолиза.
Пограничный буллезный эпидермолиз
Дистрофический буллезный эпидермолиз
Синдром Киндлера
При данной форме заболевания пузыри формируются к моменту рождения ребенка. Пузыри располагаются на разных уровнях эпидермиса – от нижних до верхних. Со временем развивается светочувствительность и атрофия и пигментация кожи с характерным испещренным видом (пойкилодермия). Часто возникают поражения ногтей и атрофические рубцы. Внекожные осложнения затрагивают желудочно-кишечный тракт (кишечник, желудок, пищевод) и мочеполовую систему.
Диагностика
В зависимости от периода проведения диагностических мероприятий их можно подразделить на пренатальные (до рождения ребенка) и постнатальные (после рождения ребенка).
Существует два основных метода постнатальной диагностики буллезного эпидермолиза – иммунофлюоресцентное генетическое картирование (IAM) и электронная микроскопия (TEM).
Для осуществления этих видов исследований у пациента осуществляется забор образцов кожи. Для проведения IAM и TEM образцы кожи получают при помощи биопсии. Осуществляют забор неповрежденного и поврежденного участков кожи. При IAM определяют наличие специфических белков кожи. Для этого используют специальные моноклональные антитела, которые избирательно связываются только с определенным белком кожи. Если данный белок отсутствует, то моноклональные антитела остаются несвязанными, окрашивания специальным светящимся составом не происходит.
При электронной микроскопии определяются конкретные компоненты кожи, отсутствие которых способно вызвать развитие буллезного эпидермолиза – кератиновые филаменты, полудесмосомы, якорные фибриллы и пр.
Также значительную роль играет анализ ДНК, проводимый с целью выявления генетической мутации и способа наследования. Но данный метод исследования используется только при наличии изменений, найденных при IAM и TEM, так как анализу необходимо подвергнуть слишком много генов, которые могут быть повреждены.
В пренатальной диагностике используется материал, полученный из околоплодных вод при сроке беременности более 17 недель. Поврежденный ген определяется путем анализа ДНК.
Лечение
Заключение
Проблема буллезного эпидермолиза остается открытой. Масштабы данной проблемы плохо изучены из-за недостаточной информированности пациентов и их родителей, а также медицинского персонала, работающего с новорожденными. Не существует единого подхода в диагностике и лечении буллезного эпидермолиза и его осложнений, что также оказывает неблагоприятное воздействие на ситуацию.
Гольченко В., Альбанова В.И. (по материалам зарубежных публикаций)