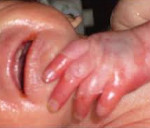
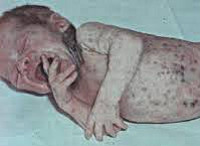
внутриутробный сепсис что это
Внутриутробные инфекции у новорождённых: диагностика, лечение, профилактика.
Почему и откуда берутся внутриутробные инфекции (ВУИ), в чём опасность внутриутробных инфекций у новорождённых, как их выявить и как с ними бороться, как защитить будущего ребёнка от заражения внутриутробно и во время родов (в интранатальный период)? Это вопросы, которые чаще всего беспокоят женщин, планирующих стать мамами, а также в период вынашивания ребёнка. Постараюсь в доступной форме ответить на эти и другие вопросы, волнующие будущих мамочек.
Какие инфекционные заболевания при беременности могут повлиять на развитие ребёнка?
Внутриутробные инфекции представляют собой группу заболеваний эмбриона, плода и новорожденного, которые развиваются в результате заражения в дородовом периоде или в родах, т. е. в анте-или интранатальный период. Инфицирование матери в период беременности нередко приводит к выкидышам и врождённым порокам развития у новорождённого. Возбудителями внутриутробных инфекционных заболеваний могут быть вирусы, бактерии, а иногда и паразиты, вызывающие явные либо скрытые инфекции у матери. Поэтому ещё на этапе планирования беременности врачу и будущей матери нужно обратить внимание на:
Что покажет УЗИ плода?
Ультразвуковое исследование (УЗИ) плода в период его вынашивания помогает специалисту своевременно обнаружить наличие различных патологий в развитии будущего ребёнка. Это, к примеру, маловодие или многоводие, большой живот, увеличенные какие-то внутренние органы, например, печень, селезёнка. В ходе ультразвуковой диагностики также могут быть обнаружены отложения кальцинатов в кишечнике, в печени, в головном мозге. В нашем медицинском лечебно-диагностическом центре «Целитель» в Махачкале опытные специалисты ультразвуковой диагностики проведут качественное исследование, которое позволит подтвердить или исключить патологию с высокой достоверностью.
Обнаруженные в ходе исследования ультразвуковые маркеры внутриутробной инфекции являются реальным подспорьем в оценке состояния плода и прогнозирования дальнейшей тактики ведения беременности. Если возможно, то врачи примут на ранних этапах меры для устранения обнаруженных отклонений. Если же это состояние, которое не совместимо с жизнью, то принимается решение о том, что лучше прервать беременность.
Клинические проявления внутриутробной инфекции?
При наличии внутриутробной инфекции околоплодные воды, которые отходят при рождении младенца, мутного цвета, имеют неприятный запах. Могут быть при этом даже загрязнены меконием (первые выделения из кишечного тракта), что указывает на угрожающее состояние заражения плода. На это врачам обязательно нужно обращать внимание. После этого опытные детские врачи осматривают плаценту, её полнокровие, есть ли какие-то кровоизлияния.
А что касается самого ребёнка, то в первую очередь нужно посмотреть на сроки, на вес. Обратить внимание на цвет кожи. Имеет ли место затяжная, длительная желтушность кожных покровов или, наоборот, бледность кожи, которая может указывать на анемию. Могут быть какие-то кожные высыпания, характерные для пиодермии, стрептодермии. У малыша может быть врождённая пневмония, врождённый миокардит, врождённые менингиты и энцефалиты. Исследуются печень, селезёнка на предмет увеличения этих органов. Также проводится анализ крови, где тоже можно увидеть изменения клинической картины.
Если мы видим соответствующие факторы риска, к примеру, 2 или 3 признака из тех, что перечислены выше, то этот ребёнок уже должен попасть в «группу риска» по внутриутробным инфекциям и его надо тщательным образом обследовать.
Чем опасны внутриутробные инфекции?
Существуют, так называемые, персистирующие инфекции, т. е. хронические, длительно текущие. Но они не всегда передаются от матери ребёнку. Поэтому не нужно особо беспокоиться, что вот, если у мамы есть инфекционная болезнь, то она на 100% передастся плоду. Частота передачи инфекции ребёнку в данном случае не такая высокая, как в случае первичного внутриутробного инфицирования.
Наибольшую угрозу для будущего ребёнка представляет мать, впервые заболевшая во время беременности, особенно в первом его триместре. Вот этот период наиболее опасен. Поэтому хочется призвать всех женщин – прежде, чем планировать рождение ребёнка, сдайте анализы на наличие антител к таким инфекциям со сходными эпидемиологическими признаками, как:
Почему? Потому что это группа инфекционно-воспалительных заболеваний, которую у будущей матери можно предотвратить, если она за 3 месяца до зачатия сделает вовремя вакцину.
Помимо этого, есть также ранние исходы инфекций. Это: миокардиты, пневмония, гипотрофия, анемия. Есть поздние, когда внутриутробная инфекция может проявиться позже. Бывает, что проходит 5-6 лет, и у малыша в этом возрасте может обнаружиться:
Об этом тоже нужно помнить и не забывать.
Диагностика и лечение внутриутробных инфекций?
В первую очередь опытный доктор в целях выявления у женщины инфекций, опасных для ребёнка, назначит общий анализ крови и общий анализ мочи. Также обязательно надо будет сделать УЗИ щитовидной железы и проверить гормональный статус женщины.
Общий принцип лечения внутриутробных инфекционных заболеваний в настоящее время включает в себя противовирусный, антибактериальный курс, проведение симптоматической и патогенетической терапии новорожденных. Если возникнут какие-то проблемы у вас или вашего ребёнка, лечащий врач должен будет подобрать индивидуальную схему лечения, наиболее эффективную в данном конкретном случае.
Профилактика ВУИ
Очень важно для женщины, планирующей беременность предпринять все возможные меры для исключения возможности врождённых инфекций у новорождённого. Прежде всего нужно встать на учёт у гинеколога в срок до 12 недель. Необходимо прислушаться к рекомендациям специалистов и провести полное обследование состояния здоровья будущей матери, включая сдачу следующих анализов:
Нужно также провести лечение имеющихся хронических очагов инфекции (кариес, тонзиллит, мочеполовые инфекционные заболевания) и не забывать о плановой вакцинации – прививках от кори, краснухи, гриппа.
Помимо этого, чтобы исключить заражения инфекциями, передающимися половым путём, желательно обследоваться и половому партнёру, ну и конечно же не допускать случайных сексуальных связей.
«Желаю вам родить живого, здорового, ребёнка. Чтобы он дальше по жизни только радовал вас своими успехами сначала в учёбе, а потом и дальше по работе. А для этого мы должны быть, во-первых, готовы и, во-вторых, мы должны полностью обследоваться. Т. е. женщина, решившая стать матерью, априори должна быть здорова.»
Улуханова Лала Уджаговна, доктор медицинских наук, профессор, врач-педиатр, гастроэнтеролог, инфекционист, нефролог, пульмонолог в Махачкале, специалист высшей квалификационной категории.
Сепсис новорожденных
Сепсис новорожденных – генерализованная гнойно-септическая инфекция, характеризующаяся наличием первичного очага и циркуляцией инфекции в крови. Сепсис новорожденных проявляется признаками инфекционного токсикоза (температурной реакцией, вялостью, диспепсией, землистой окраской кожных покровов) и образованием гнойных метастатических очагов в различных органах (мозговых оболочках, легких, костях, печени и пр.). Диагноз сепсиса у новорожденных устанавливается на основании клинических критериев и выделения возбудителя при бактериологическом посеве крови. Лечение сепсиса новорожденных включает системную антибиотикотерапию, санацию первичного и метастатических гнойных очагов, посиндромную терапию.
Общие сведения
Причины сепсиса новорожденных
В настоящее время доминирующее место (около 50%) среди возбудителей сепсиса новорожденных принадлежит грамположительной флоре (главным образом, стафилококкам, гемолитическому стрептококку группы А). Чуть реже (до 40% случаев) выявляется грамотрицательная микрофлора (кишечная палочка, синегнойная палочка, клебсиелла и др.); в 10% этиологическими агентами выступает смешанная флора (часто ассоциация стафилококка с грибами Candida).
Входными воротами инфекции могут являться кожа и слизистые, пупочная ранка, желудочно-кишечный тракт, мочевые пути. Первичными очагами инфекции, приводящими к развитию сепсиса новорожденных, чаще выступают омфалит, пиодермии, конъюнктивит, отит, фарингит, бронхит, инфекции мочевыводящих путей, энтерит, дисбактериоз и пр. В группе риска по развитию сепсиса новорожденных находятся дети с недоношенностью, внутриутробной гипоксией, внутриутробными инфекциями, внутричерепной родовой травмой; пребывающие в ОРИТ, длительно находящиеся на ИВЛ; получающие парентеральное питание, инфузионную и трансфузионную терапию; перенесшие катетеризацию пупочной и центральной вен, хирургические вмешательства в первые дни жизни.
Со стороны матери факторами, способствующими бактериальной контаминации новорожденного, выступают бактериальный вагиноз, кольпиты, эндометрит. Большое значение имеет степень и характер иммуносупрессии у новорожденного, которые могут быть связаны с неполноценным питанием или приемом лекарств беременной, наследственным иммунодефицитом или ВИЧ-инфекцией. В отдельных случаях причиной вспышек сепсиса новорожденных становится несоблюдение санитарного режима в родильных или детских отделениях.
Классификация сепсиса новорожденных
По времени развития выделяют внутриутробный и постнатальный (ранний неонатальный и поздний неонатальный) сепсис новорожденных. Внутриутробный сепсис предполагает антенатальное или интранатальное инфицирование плода; при этом первичный гнойно-септический очаг располагается вне организма ребенка (чаще всего в его роли выступает плацентит, хорионит, хориоамнионит и т. д.). В случае постнатального сепсиса первичный гнойно-воспалительный очаг всегда располагается в организме самого новорожденного.
Ранний неонатальный сепсис новорожденных развивается в первые 4-ро суток жизни ребенка. Клинические течение заболевания обычно молниеносное, с быстрым развитием полиорганнной недостаточности, летальным исходом в 5-20% случаев. Поздний неонатальный сепсис новорожденных манифестирует на 5-й день и позднее. Характеризуется медленно прогрессирующим течением, возникновением вторичных септических очагов, 5-10%-ной летальностью.
Течение сепсиса новорожденных может быть молниеносным (3-7 дней), острым (до 4-8 недель), подострым (до 1,5-3 месяцев), затяжным (более 3 месяцев). С учетом локализации первичного септического очага и входных ворот различают: пупочный, кожный, легочный, ринофарингеальный, отогенный, риноконъюнктивальный, кишечный, урогенный, катетеризационный и др. виды сепсиса новорожденных. Сепсис новорожденных может протекать в форме септицемии или септикопиемии.
Симптомы сепсиса новорожденных
Септицемия или сепсис новорожденных без метастазов обычно развивается на фоне предшествующего мокнущего пупка, конъюнктивита, гнойничковой сыпи, опрелостей, стоматита. Предвестниками сепсиса новорожденных могут выступать вялость или беспокойство, снижение аппетита, обильные частые срыгивания, плохая прибавка в весе. В период разгара развивается температурная реакция (гипер- или гипотермия), отечный синдром или эксикоз, гипотрофия. Характерным признаком сепсиса новорожденных является грязновато-серый (землистый) оттенок кожных покровов, желтушность, мраморность кожи, сыпь.
Вследствие токсического поражения различных органов возникают гепатоспленомегалия, пневмопатия (тахипноэ, цианоз), кардиопатия (тахикардия или брадикардия, артериальная гипотензия), диспепсия, мочевой синдром (олигурия, анурия, ОПН), геморрагический синдром, надпочечниковая недостаточность. Чаще всего септицемия осложняется присоединением пневмонии, которая выступает как самостоятельное интеркуррентное заболевание.
Септикопиемия или сепсис новорожденных с гнойными метастазами характеризуется возникновением на фоне интоксикации вторичных очагов отсева в мозговых оболочках, легких, костях, печени, других органах. Чаще всего септикопиемия протекает с развитием гнойного менингита, абсцедирующей пневмонии, остеомиелита; реже – с формированием абсцесса печени, гнойного артрита, панофтальмита, медиастинита, флегмоны желудка или кишечника. В восстановительном периоде происходит санация пиемических очагов, стихание токсикоза, постепенное восстановление нарушенных функций.
Молниеносная форма сепсиса новорожденных протекает с развитием септического шока: стремительным ухудшением состояния ребенка, снижением температуры тела, брадикардией, кровоточивостью, отеком легких, острой почечной недостаточностью. Летальный исход при молниеносном течении сепсиса новорожденных наступает в течение 3-5 суток.
Диагностика сепсиса новорожденных
Диагноз сепсиса новорожденного может быть заподозрен неонатологом или педиатром на основании лихорадки свыше 3 дней или прогрессирующей гипотермии; гиперлейкоцитоза, сменяющегося лейкопенией; повышением содержания в крови маркеров инфекционного процесса (СРБ, интерлейкина-8, прокальцитонина).
Факт бактериемии при сепсисе новорожденных подтверждается путем посева крови на стерильность. Важное значение имеет выявление первичного гнойного очага и метастатических очагов, микробиологического исследование отделяемого из них (бактериологическое исследование мазка с конъюнктивы, мочи на микрофлору, соскоба/отделяемого с кожи на микрофлору, мазка из глотки, кала на дисбактериоз и т. п.).
Дифференциальная диагностика сепсиса новорожденных осуществляется с локализованными гнойно-воспалительными заболеваниями (пневмонией, медиастинитом, перитонитом, менингитом, энтероколитом), генерализованными вирусными инфекциями (цитомегалией, герпесом, энтеровирусной инфекцией) и микозами (кандидозом, аспергиллезом) и др. Для этого используются дополнительные лабораторные методы – ПЦР, ИФА, микроскопия.
Лечение сепсиса новорожденных
Терапия при сепсисе новорожденных проводится одновременно в нескольких направлениях и включает санацию септического и пиемических очагов, подавление циркуляции возбудителя в крови, коррекцию нарушенных функций.
Основу этиологического лечения сепсиса новорожденных составляет антибиотикотерапия: эмпирическая комбинированная до уточнения характера микрофлоры) и целенаправленная после получения антибиотикограммы. Противомикробные препараты вводятся внутривенно, в максимальных возрастных дозировках в течение 10-15 суток с последующей сменой. Чаще всего в клинической практике для лечения сепсиса новорожденных в различных сочетаниях используются цефалоспорины, аминогликозиды, аминопенициллины, карбапенемы и др.
С целью местного лечения гнойных очагов производится вскрытие фурункулов и абсцессов, перевязки с антибактериальными и ферментными препаратами; назначается УВЧ, СВЧ, электрофорез.
Патогенетическая терапия сепсиса новорожденных включает иммунокоррекцию (плазмаферез, гемосорбцию, введение иммуноглобулинов), проведение дезинтоксикационной терапии (внутривенной инфузии глюкозо-солевых растворов и свежезамороженной плазмы), адекватную кислородотерапию и т. д. При сепсисе новорожденных обязательно проводится мониторинг состояния жизненно-важных функций: АД, ЧСС, ЭКГ, КОС и газового состава крови, биохимических показателей (сахара крови, креатинина, электролитов), гематокрита.
В остром периоде сепсиса целесообразно пребывание новорожденных в кувезе, кормление материнским молоком, тщательный уход. В восстановительном периоде к лечению подключается гимнастика, массаж, лечебные ванны.
Прогноз и профилактика сепсиса новорожденных
Прогноз сепсиса новорожденных серьезный: летальность составляет от 30-40% до 60% среди глубоко недоношенных детей. У выздоровевших детей в отделенном периоде могут отмечаться частые ОРВИ, пиелонефрит, анемия, перинатальная энцефалопатия.
Современный взгляд на проблему внутриутробной инфекции
Рассмотрена проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода, факторы риска внутриутробных инфекций, патогенетические механизмы возникновения, развития и воздействия ВУИ, подходы к диагностике и лечению.
The issue of fetal intrauterine infecting and intrauterine infection (IUI) was considered, as well as the risk factors of intrauterine infections, pathogenic mechanisms of their occurrence, development and effect of IUI, and approaches to the diagnostics and treatment.
Проблема внутриутробной инфекции особо актуальна в современных условиях в связи с распространенностью и тяжестью воспалительных процессов. Проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода является одной из ведущих в акушерской практике и в перинатологии в связи с высоким уровнем инфицирования беременных, рожениц и родильниц, опасностью нарушения развития плода и рождения больного ребенка. Наличие инфекции у матери является фактором риска ВУИ плода, но не всегда означает его заболевание [1, 5–7, 13].
Внутриутробная инфекция — группа инфекционно-воспалительных заболеваний плода и детей раннего возраста, которые вызываются различными возбудителями, но характеризуются сходными эпидемиологическими параметрами и нередко имеют однотипные клинические проявления. Заболевания развиваются в результате внутриутробного (анте- и/или интранатального) инфицирования плода. При этом в подавляющем большинстве случаев источником инфекции для плода является мать. Истинная частота врожденных инфекций до настоящего времени не установлена, но, по данным ряда авторов, распространенность данной патологии в человеческой популяции может достигать 10%. В структуре перинатальной смертности ВУИ составляет более 30% [1, 5–7].
Кроме этого, ВУИ относятся к тяжелым заболеваниям и во многом определяют уровень младенческой смертности.
Согласно данным многих авторов, причиной внезапной смерти грудных детей является инфекционное заболевание, протекающее без ясной симптоматики. В числе причин или фоновых состояний скоропостижной смерти могут быть ВУИ [2].
Под внутриутробным инфицированием понимают процесс внутриутробного проникновения микроорганизмов к плоду, при котором отсутствуют признаки инфекционной болезни плода. Как правило, инфекционный процесс затрагивает плаценту, в которой развивается плацентит, хориоамнионит и т. д. Диагноз внутриутробного инфицирования у новорожденного устанавливается на основании выделения возбудителя из клеток крови, ликвора и других источников, выявления IgM и низкоавидных IgG в пуповинной крови, а также при морфологическом исследовании плаценты [1, 5–7].
Внутриутробное инфицирование не означает неизбежного развития инфекционного заболевания. Для выявления ВУИ необходимо наличие данных лабораторного исследования в сочетании с клинической картиной инфекционного заболевания. Под ВУИ подразумевают не только процесс распространения инфекционных агентов в организме плода, но и вызванные ими морфофункциональные нарушения различных органов и систем, характерные для инфекционной болезни (сепсис, пневмония, менингит, гепатит и т. д.), возникшей анте- или интранатально и выявляемой пренатально или после рождения [10, 11].
Инфекционно-воспалительные заболевания во время беременности имеют особенности: инфицирование плода и новорожденного может быть вызвано как острой инфекцией матери, так и активацией хронической, персистирующей инфекции во время беременности; большая часть заболеваний беременных, приводящих к внутриматочной инфекции, протекает в латентной или субклинической форме; активация персистирующей инфекции возможна при любом нарушении гомеостаза в организме беременной (стресс, острые респираторные вирусные инфекции, переохлаждение и др.) [1, 2].
Зачастую ВУИ ассоциируются с наличием инфекций TORCH — то есть синдромом комплекса. Данный термин образован первыми буквами латинских названий наиболее часто верифицируемых врожденных инфекций: T — токсоплазмоз (Тoxoplasmоsis), R — краснуха (Rubella), С — цитомегалия (Cytomegalia), Н — герпес (Herpes) и О — другие инфекции (Оther). К последним относят сифилис, листериоз, вирусные гепатиты, хламидиоз, ВИЧ-инфекцию, микоплазмоз и др. [9, 11].
Принимая во внимание, что источником инфекции для плода всегда является его мать, особое значение приобретают следующие факторы риска внутриутробных инфекций:
Патогенетические механизмы возникновения, развития и воздействия ВУИ разнообразны и зависят от многих факторов:
Влияние инфекции на эмбрион и плод заключается в воздействии комплекса следующих факторов:
Таким образом, реализуется ли внутриутробное инфицирование в ВУИ или нет, зависит от ряда факторов, которые мы представили выше.
Учитывая неспецифичность клинических проявлений ВУИ во время беременности, диагностика данной патологии в большинстве случаев затруднена и возможна лишь в результате сочетания клинических и лабораторно-диагностических методов обследования.
Клинический метод исследования позволяет выявить различные осложнения гестационного периода, такие как невынашивание беременности и синдром задержки роста плода (СЗРП). Кроме этого, немаловажное значение имеет наличие проявлений инфекции у матери (отит, гайморит, пиелонефрит, цистит и т. д.).
Методы, позволяющие оценить состояние фетоплацентарной системы:
Микробиологические и серологические исследования:
Исследование хориона (биопсия хориона): бактериологический метод, ПЦР-диагностика.
Исследование околоплодных вод (амниоцентез): бактериологический метод, ПЦР-диагностика.
Исследование пуповинной крови плода (кордоцентез): бактериологический метод, ПЦР-диагностика и специфический иммунный ответ (IgM) плода.
Морфологическое исследование плаценты, данные аутопсии.
Клиническая оценка состояния новорожденного («незрелость» при доношенном сроке беременности, манифестация инфекционного заболевания, врожденные пороки развития) [1, 9, 11, 14, 15].
Предположительный диагноз внутриутробного инфицирования и ВУИ помогают поставить косвенные методы:
К прямым методам диагностики внутриутробного инфицирования и ВУИ относятся: выявление возбудителя в материале, полученном при биопсии хориона, амниоцентезе (ПЦР, бактериологический метод), кордоцентезе (ПЦР, бактериологический метод и определение уровня специфических IgM).
Характер течения беременности при внутриутробной инфекции зависит от срока воздействия возбудителя.
На ранних этапах зародыша (1–3 недели беременности) из-за отсутствия механизмов взаимодействия инфекционного агента и плодного яйца реализации воспалительной реакции чаще всего не происходит. Контакт с инфекцией может закончиться альтернативным процессом и гибелью плодного яйца. Повреждение эмбриона инфекцией на 4–12 неделях беременности связано с вирусной инфекцией, проникновением микроорганизмов через хорион. Плод еще не имеет защитных механизмов. Нарушение закладки органов и систем вызывает тератогенный и эмбриотоксический эффект [13, 15].
В I триместре беременности специфических клинических признаков наличия ВУИ нет, косвенно о ней свидетельствуют некоторые эхографические признаки:
Инфекционные фетопатии возникают с 16-й недели, когда происходит генерализация инфекции у плода. Могут возникать такие пороки развития, как фиброэластоз эндокарда, поликистоз легких, микро- и гидроцефалия (ранние фетопатии) [12–15].
В III триместре плод реагирует на внедрение возбудителя локальной реакцией. Могут возникнуть энцефалит, гепатит, пневмония, интерстициальный нефрит. Влияние вирусов чаще всего проявляется признаками незрелости, дисэмбриогенетическими стигмами, затяжным адаптационным периодом, значительной потерей массы тела в раннем постнатальном периоде. Данные эхографии во II и III триместрах беременности, указывающие на развитие инфекции у плода:
После верификации диагноза ВУИ лечебные мероприятии проводят с помощью этиотропной, антимикробной терапии: препараты пенициллинового ряда и макролиды. Целесообразность назначения антимикробных препаратов не вызывает сомнения, если ВУИ обусловлено наличием патогенных возбудителей (бледная спирохета, токсоплазма, хламидии, гонококк и т. д.) [8, 14].
В настоящее время одним из наиболее дискутабельных вопросов в акушерстве является выяснение истинной этиологической роли генитальных микоплазм (Mycoplasma hominis, Mycoplasma genitalis, Ureaplasma urealyticum) в развитии патологии матери и плода. Инфицирование плода генитальными микоплазмами происходит преимущественно интранатально: в 18–55% — у доношенных новорожденных и в 29–55% — у недоношенных [3, 16, 20].
Актуальность проблемы урогенитального микоплазмоза обусловлена не только значительным распространением этой инфекции в популяции, но и неоднозначностью ее оценки как эпидемиологами, так и клиницистами [16].
По данным различных исследователей, микоплазмы являются возможной причиной развития конъюнктивитов, врожденных пневмоний, респираторного дистресс-синдрома, хронических заболеваний легких, менингита и неонатального сепсиса. Вопрос о терапии микоплазменной инфекции до настоящего времени остается открытым. В схемах терапии предусматривается 7–10-дневные курсы макролидов [1, 3, 21, 22].
Во время беременности противовирусная терапия при генитальном герпесе, цитомегаловирусной инфекции, вирусе ветряной оспы проводится с помощью этиотропных препаратов (ацикловир) начиная со II триместра гестационного периода. Целью лечения является профилактика рецидивирования и антенатального инфицирования [14, 17, 19].
Трихомонадная инфекция относится к группе негонококковых воспалительных заболеваний мочеполовых органов. Лечение трихомониаза во время беременности осуществляется с помощью метронидазол-содержащих препаратов начиная со II триместра гестационного периода [8].
Появление новых методов диагностики, разработка и внедрение новых лекарственных средств не изменяют ситуацию с внутриутробными инфекциями, оставляя это по-прежнему актуальной проблемой в акушерстве. Все это обуславливает неуклонный рост инфекции в человеческой популяции, высокий процент рецидивов инфекции даже у пациентов, получавших курс антибиотикотерапии в соответствии с действующими инструкциями и схемами лечения. Проблема осложняется тем, что в настоящее время отсутствует единая концепция механизма рецидивирования, недостаточно изучена роль микст-инфекции в возникновении, течении и персистировании инфекции, не учитываются особенности гормонального и иммунного статуса больного, не сформированы диагностические критерии контроля излеченности патологического процесса. Это все вместе взятое является стимулом для продолжения исследований, направленных на решение данных проблем. Несмотря на то что роль вирусных и бактериальных инфекций в этиологии и патогенезе многих патологических процессов не вызывает сомнений, вопрос о значении инфекций в качестве моновозбудителя на сегодняшний день окончательно не решен. Актуальным по-прежнему остается вопрос разработки алгоритма лабораторной диагностики заболеваний.
Только совершенствование диагностических подходов, разработка оптимальных алгоритмов и методов обследования и предупреждение распространения резистентных штаммов путем адекватного отношения к каждому пациенту индивидуально (обязательное проведение посевов на определение чувствительности к антибиотикам до назначения терапии) может изменить данную ситуацию.
Исследование выполнено за счет гранта Российского научного фонда (проект № 15-15-00109).
Литература
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва