вилочковая железа где находится и за что отвечает у женщин
Заболевания вилочковой железы
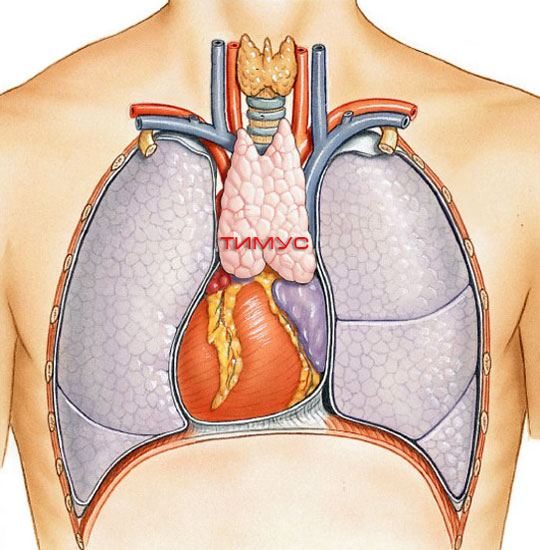
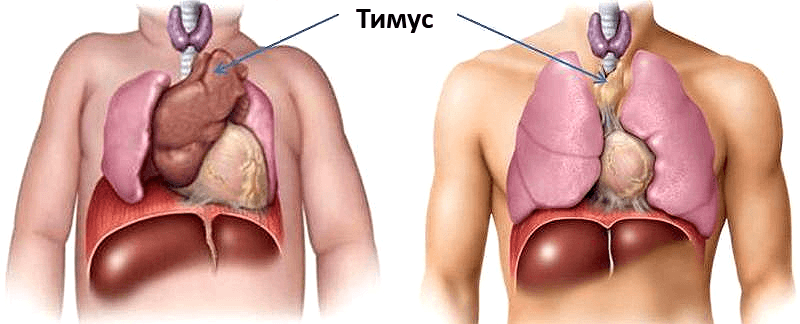
11.05.2011 Вилочковая железа или тимус является важным органом иммунной системы, который в детском возрасте отвечает за формирование первичного иммунитета. Он расположен сразу за грудиной в переднем отделе средостения (средостение — пространство в грудной полости, ограниченное легкими с двух сторон) и частично распространяется на шею. У взрослых в 20-25 лет функционирование вилочковой железы прекращается, и она постепенно превращается в жировую клетчатку.
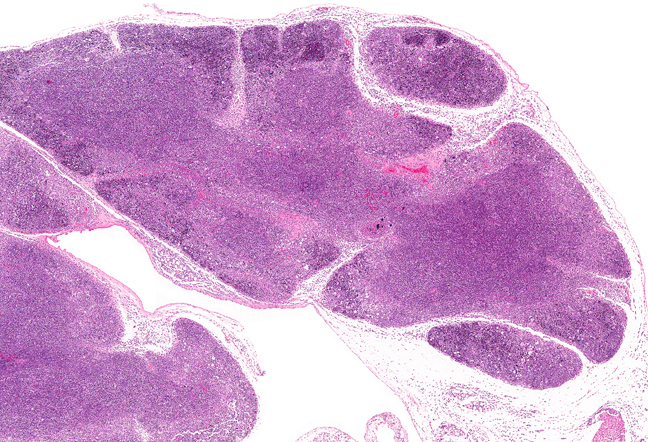
В тимусе могут появляться опухоли, кисты, метастазы рака других органов, лимфомы. Тимомы — наиболее часто встречающиеся опухоли вилочковой железы. Они могут прорастать в окружающие ткани или нет. По гистологическому строению тимомы относят к опухолям с неопределенным поведением.
Часто пациенты не предъявляют никаких жалоб, и тимомы оказываются случайной находкой при КТ исследовании грудной клетки. У некоторых пациентов появляются ряд симптомов (см. новообразования средостения).
Однако особым свойством заболеваний вилочковой железы, выделяющих их среди других новообразований, являются так называемые «паратимические синдромы». К ним относятся гипогаммаглобулинемия, гипоплазия красного костного мозга, дерматомиозит, системная красная волчанка, апластическая анемия, ревматоидный артрит и другие аутоиммунные заболевания. Однако наиболее распространенным из них является неврологическое заболевание – аутоиммунная миастения, которая встречается более чем у 40% больных тимомами.
Миастения — заболевание, которое характеризуется аутоиммунным поражением нервно-мышечного соединения, приводящим к затруднению или к полной блокаде передачи сигнала от нерва к мышечному волокну. Оно проявляется слабостью и патологической утомляемостью различных групп скелетной мускулатуры. Вилочковая железа у больного миастенией вырабатывает аутоантитела, блокирующие ацетилхолиновые рецепторы и, тем самым, передачу сигнала о движении от нерва к мышце.
Миастенический криз (развивается у 10-15% больных) — крайняя степень миастении, характеризующаяся быстрым усугублением двигательных расстройств, приводящих к нарушению дыхания и глотания. Если в это время не оказать больному экстренную помощь, возникает реальная угроза для жизни.
Некоторые лекарственные препараты могут провоцировать обострение миастении. К ним относятся некоторые антибиотики, β-адреноблокаторы, ботулотоксин, антагонисты кальция, курареподобные миорелаксанты, соли магния, лидокаин, прокаинамид, хинин, хинидин, рентгеноконтрастные средства, D-пеницилламин, дифенин, гормоны щитовидной железы, а также глюкокортикоиды.
При подозрении на миастению необходима консультация невропатолога и госпитализация в специализированную клинику, владеющую всем комплексом диагностических (в том числе КТ и МРТ) и лечебных возможностей, включая хирургическое лечение — удаление вилочковой железы (тимэктомия).
Для лечения тимом используют хирургический метод. Часто операцию можно выполнить торакоскопически, однако при больших размерах новообразования (более 8 см) используют стернотомию. При прорастании опухоли в соседние ткани и органы лечение следует продолжить лучевой терапией.
Вилочковая железа (тимус): где располагается и за что отвечает в организме
Одним из основных органов человека, который непосредственно влияет на нормальный образ жизни, является вилочковая железа, или тимус. Именно его здоровье обеспечивает наличие у организма защитных сил, которые помогают обеспечить иммунитет и защитить тело от вредоносных бактерий.
Как только тимус прекращает свою работу, то разнообразные вирусы, бактерии и иные патогены могут беспрепятственно бродить по организму, разрушая ткани и заражая его тяжелыми инфекционными болезнями. В этой статье будет рассказано о том, за что отвечает вилочковая железа, а также где именно она находится в организме.
Что такое вилочковая железа?
Даже сейчас многие врачи продолжают спорить по поводу вилочковой железы. Тимус то стараются отнести к эндокринной, то к лимфоидной системе, но при этом ни один из врачей не умаляет важнейшей роли самой железы, а именно обеспечения защитной функции организма.
В раннем возрасте, до того как ребенку исполнится год, функции тимуса особенно важны, поскольку в этот период только этот орган обеспечивает всю защиту малыша от вредоносных микроорганизмов. К счастью, по мере взросления ряд иных органов также берет на себя эту функцию.
Форма тимуса
Вилочковая железа, или тимус, свое название получила именно из-за оригинального внешнего вида, напоминающего вилку с двумя зубцами. Однако таким образом выглядит только здоровый орган, а по мере своего заболевания он начинает напоминать раздувшийся парус или бабочку. Орган растет до тех пор, пока ребенку не исполнится 10 лет, а по достижении совершеннолетия начинает уменьшаться.
Вся зобная железа покрыта соединительной тканью, образующей капсулу, которая под собой содержит Т-лимфобласты, вырабатывающиеся в тимусе. Эти специфические клетки и обеспечивают работу иммунной системы, борясь с чужеродными микроорганизмами, но при этом не влияя на собственное тело человека.
Размеры вилочковой железы
При атрофии нижние и боковые участки тимуса замещаются жировой тканью. Доподлинно неизвестно, почему же это так происходит, но многие врачи соглашаются с тем, что открытие данной загадки поможет повернуть вспять процесс старения.
Расположение органа
Расположение органа, как у детей, так и у взрослых, не меняется, кроме тех случаев, когда это вызвано аномалиями. В этих случаях отдельные доли могут прорасти в ткани щитовидной железы, в зоны миндалин или в шейную область. Однако такие нарушения встречаются всего в 25 % случаев, и обычно у женского пола. При этом также было замечено, что в случаях эктопии тимуса практически все больные диагностируются наличием врожденного сердечного порока.
Функции органа
Самой важной функцией тимуса, без сомнения, является продуцирование иммунных клеток, которые обеспечивают организму защиту. Однако, помимо этого, орган выполняет еще несколько очень важных действий:
Выработка гормонов
Также важным вопросом в данной теме является то, какие гормоны вырабатывает тимус и какова их роль в организме. При помощи тимозина и тимопоэтина преобразившиеся лимфоциты обеспечивают организму максимальный уровень защиты. А гормон тимулин улучшает уровень регенерации, ведь увеличивается уровень фагоцитоза.
Помимо этого, гормоны тимуса обеспечивают для организма ноотропный эффект, а также стабилизируют работу центральной нервной системы и уменьшают раздражительность, так что человек психически становится намного более стабильным.
Патологии тимуса
Самой опасной разновидностью патологии вилочковой железы является врожденная аномалия. В таких случаях орган начинает вырабатывать лимфоциты, которые направлены не на уничтожение чужеродных микроорганизмов, а клеток собственного тела. Также очень опасны аутоиммунные патологии хронического типа, поскольку из-за них организм начинает сильно ослабевать, а потому бактерии и различные вирусы могут беспрепятственно размножаться в теле больного человека. В таких случаях людям приходится всю жизнь сидеть на препаратах, которые предназначены для улучшения слабого иммунитета.
Помимо этого, нарушение работы тимуса может возникнуть:
Заболевания
В тех случаях, когда в детстве ребенок очень часто болеет, врачи назначают исследование вилочковой железы (тимуса), поскольку в малом возрасте только этот орган обеспечивает организму защиту. В тех случаях, когда имеются тяжелые поражения у данного органа, то его вообще рекомендуется удалить, а при умеренных или слабых повреждениях проблема может решиться при помощи курса лечения иммуномодуляторами, которые помогут возвратить иммунитет на должный уровень.
Но, на самом деле, заболевает тимус намного реже, чем иные органы, причем происходит это обычно у людей пожилого возраста, хотя в некоторых случаях может проявиться и у младенцев. Основными видами заболеваний тимуса являются:
Симптомы
Лечение болезней вилочковой железы
Лечить любые заболевания тимуса очень сложно, а к тому же и долго. К примеру, хронические аутоиммунные болезни вообще нельзя излечить, а только понизить уровень их негативного воздействия при помощи иммуномодуляторов и витаминов группы В. Это позволяет немного улучшить защитные функции организма и обеспечивает защиту от иных инфекционных заболеваний.
Именно поэтому очень важно следовать рекомендациям врача и принимать все назначенные препараты, поскольку это поможет понизить риски разрушения еще здоровых клеток органа. Помимо того, врачи также рекомендуют следовать профилактическим мерам и принимать витамины, особенно в осенне-зимний период, когда как никогда нужно укреплять иммунитет.
Заключение
Тимус является невероятно важным органом, который обеспечивает правильную защиту организма и нормальный иммунитет. Его по праву можно назвать одним из основных, поскольку в большинстве случаев он помогает вести человеку нормальный образ жизни. Поэтому любые нарушения в нем могут привести к длительному и сложному лечению.
Наивные Т-клетки — ключ к долголетию
Наивные Т-клетки — ключ к долголетию
Автор
Редактор
Статья на конкурс «био/мол/текст»: Наивные Т-лимфоциты могут поведать о том, что вы хотели бы скрыть. Впервые было осуществлено секвенирование профиля Т-клеточных рецепторов периферической крови человека. Успехи в развитии технологий секвенирования нового поколения дают возможность проследить за динамикой колебаний численности и разнообразия наивных Т-клеток по мере старения организма. Вместе с этими знаниями появляется ответ на вопрос, почему женщины живут дольше мужчин, и приходит мысль о том, что увеличить продолжительность жизни можно, используя собственные Т-клетки. «Иммунологические часы» несложно обмануть, пойдя на хитрость.
Обратите внимание!
Эта работа опубликована в номинации «лучшая статья по иммунологии» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Всегда ли можно дать сорокалетнему мужчине его сорок? А пятидесятилетнему? А скольким тридцатилетним женщинам вы бы не дали двадцати? Определять возраст человека по внешней составляющей не самая лёгкая задача. Однако, людям, перешагнувшим определённый порог, различный для мужчин и женщин, когда репродуктивная функция начинает стремительно угасать, становится сложнее скрывать свой возраст.
Для внутренних процессов человеческого организма характерны совершенно иные темпы изменений. «Возрастной порог» нашей иммунной системы расположен гораздо ближе к детству, чем к старости. Уже с первого года жизни в тимусе ребёнка начинают происходить драматические изменения: функциональная ткань органа заменяется на соединительную, уменьшаясь каждый год на 3% до 35–45 лет, а после 45 — на 1% (рис. 1). В 70 лет соединительная ткань занимает 90% тимуса [1]. Наиболее активно тимус функционирует в пренатальный период и до наступления половой зрелости. За это время происходит наработка максимальных возможностей Т-клеточного иммунитета, что будет во многом определять эффективность иммунного ответа человека на протяжении всей его жизни.
Рисунок 1. Сравнение размеров тимуса у новорождённого (а) и взрослого (б). К 50 годам тимус уменьшается в 5-7 раз по сравнению с первоначальным размером. Рисунок с сайта my.bpcc.edu.
Тимус — военная база иммунной системы
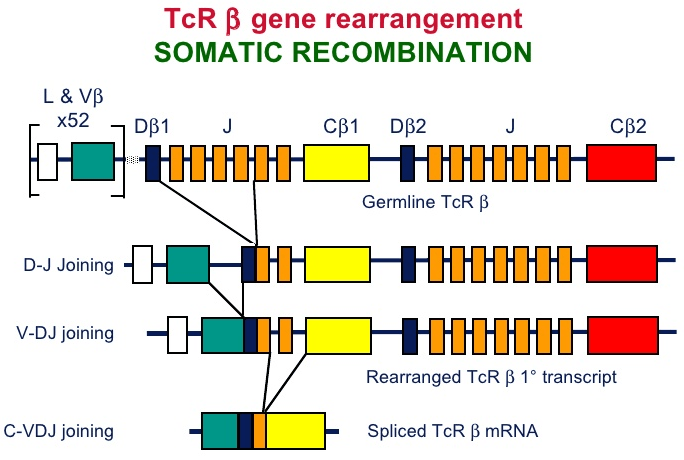
В тимусе иммунная система обучает своих «солдат». Предшественники Т-лимфоцитов размножаются в костном мозге и с кровью попадают в тимус. В нём происходит ключевое событие в жизни Т-клеток, определяющее их специфичность к антигену, с которым они никогда ещё не встречались — соматическая рекомбинация (также V(D)J-рекомбинация, рис. 2). Она заключается в перетасовке участков генов, кодирующих гипервариабельные участки α и β цепей Т-клеточного рецептора (TCR). С помощью TCR Т-клетки распознают «свой» антиген, к которому они специфичны, в составе главного комплекса гистосовместимости (MHC) антиген-презентирующих клеток (рис. 3). Благодаря этому процессу создаётся гигантское разнообразие TCR — около 6 × 10 5 возможных вариантов на каждые 10 6 Т-клеток [2]. В силу такой огромной вариабельности Т-клеточных рецепторов существует высокая вероятность того, что при проникновении в организм какого-либо чужеродного агента найдётся Т-клетка, TCR которой окажется специфичным именно ему. Соматическая рекомбинация происходит в кортикальной части тимуса, из неё клетки мигрируют в медуллярную часть и претерпевают негативный отбор: в экземплярах, реагирующих на собственные антигены, экспрессируемые организмом, запускается апоптоз.
Рисунок 2. Соматическая рекомбинация на примере β цепи TCR. Исходная последовательность в гене, кодирующем β цепь TCR содержит V (variable), D (diversity), J (Joining) и C (constant) сегменты. Сначала один из двух D-сегментов соединятеся с одним из 13 J-сегментов. Получившийся DJ-сегмент присоединяется к одному из 50 V-сегментов. Сегменты выбираются случайным образом, и механизм их сшивки также предполагает случайное варьирование количества пар оснований, это обеспечивает разнообразие TCR. Аналогичный процесс происходит c последовательностью, кодирующей α-цепь только без D-сегмента. Рисунок с сайта Slideshare.
Рисунок 3. Взаимодействие TCR и антиген-презентирующей клетки. а — Т-клетка (фиолетовая) взаимодействует с антиген-презентирующей клеткой (APC, синяя). б — APC презентирует антиген в составе MHC. Гетеродимер TCR состоит из α и β цепей, охватывающих MHC с антигеном. С антигеном главным образом взаимодействуют области CDR3 — это домены, отвечающие за специфичность TCR к данному антигену. Рисунок с сайта Genomemedicine.
После наступления пубертатного периода производство тимусом наивных Т-клеток резко снижается и на протяжении всей взрослой жизни человека активность этого органа остаётся на самом базальном уровне. Чем это грозит? Созданное за такой короткий период огромное разнообразие TCR действительно обеспечивает эффективный иммунный ответ на большинство потенциальных угроз. Но это разнообразие остаётся константным только некоторое время.
Мы теряем наших бойцов!
По результатам последних исследований [2], доля наивных Т-клеток как в CD4 + (Т-хелперы) так и в CD8 + (Т-киллеры) субпопуляциях периферической крови человека линейно уменьшается с возрастом. В детстве она составляет 50–80% от всего Т-клеточного пула и уменьшается на 0,75% каждый год, к 70 годам она составляет одну четверть первоначального изобилия. Авторы исследования [2] создали новый подход к использованию технологии секвенирования нового поколения компании Illumina для получения наиболее точных индивидуальных профилей репертуара TCR у людей различных возрастных групп. Было показано, что разнообразие TCR в периферической крови человека коррелирует с процентным содержанием в ней наивных Т-клеток и почти линейно уменьшается с возрастом — примерно на 5 × 10 3 вариантов TCR в год. Наивные Т-клетки сосуществуют в крови с Т-клетками памяти, клоны которых образуются в результате пролиферации наивных Т-клеток, повстречавших «свой» антиген. Размножившиеся клоны с каждым годом занимают всё большую долю доступного для пролиферации пространства в крови, это отражается на численности наивных Т-клеток, так как общее количество Т-клеток в крови человека относительно стабильно.
* — Но не стоит забывать, что кроме популяций в периферической крови, у человека есть гораздо более мощная локальная армия Т-лимфоцитов «на местах»: «Т-лимфоциты: путешественники и домоседы» [4]. — Ред.
Общее разнообразие TCR определяется количеством редких клонов в пуле Т-клеток, поэтому отсутствие возрастных изменений в разнообразии наиболее многочисленных Т-клеточных клонов указывает на то, что клоны наивных Т-клеток теряются с возрастом. Это связано с тем, что клоны наивных Т-клеток обычно малочисленны, поэтому вероятность того, что ни одна клетка данного клона не сможет поделиться или погибнет в результате каких-то случайных событий гораздо выше, чем для клонов с большим числом клеток.
Старики с высоким разнообразием TCR
Другое объяснение явления увеличения разнообразия TCR после 70 лет заключается в том, что люди этой возрастной группы уже перешагнули определённый возрастной порог, пройдя в некотором смысле проверку на прочность — уникальный набор физиологических параметров, включая особенности иммунной системы, сделал их наиболее приспособленными среди всех особей популяции в данных условиях. Из этого можно заключить, что повышенное содержание наивных Т-клеток в субпопуляции CD4 + периферической крови человека коррелирует с долгожительством. Увеличение доли наивных Т-клеток в пуле CD4+, а значит и увеличение разнообразия TCR обеспечивает лучшую иммунорегуляторную функцию, что снижает общее воспаление, усиливающееся по мере старения организма из-за активации аутоиммунных процессов, увеличивает эффективность распознавания раковых клеток и обеспечивает более сбалансированный иммунный ответ [2].
Долгая, но бездетная жизнь
Рисунок 4. Придворные евнухи в Китае. Некоторые евнухи жили более ста лет. Рисунок с сайта Lacasamundo.
Исследование о придворных евнухах династии Чозунь в Корее 2012 года [6] показало, что продолжительность жизни евнухов составляла на 15–20 лет больше, чем продолжительность жизни мужчин с нормальной репродуктивной функцией, живущих в тех же условиях (рис. 4). Возможно, их продолжительность жизни увеличивалась именно благодаря отсутствию инволюции тимуса под влиянием половых гомонов, а следовательно благодаря большему разнообразию TCR наивных Т-клеток. В пользу этой гипотезы можно привести данные о том, что у женщин производство тимусом наивных Т-клеток происходит более эффективно, чем у мужчин, и уменьшение их содержания в периферической крови у женщин выражено в меньшей степени, чем у мужской части населения [7]. Возможно, лучшая работа иммунной системы у женщин связана с тем, что во время беременности иммунитет женщины необходимо «обуздать», сделав его толерантным к фактически чужеродному телу — плоду, что требует участия сложных регуляторных путей. Высокая точность регуляции иммунного ответа очень важна, так как ошибка приведёт к потере потомства. К этим рассуждениям можно прибавить и тот факт, что у женщин с наступлением менопаузы яичники перестают вырабатывать эстрогены, а у мужчин выработка половых гормонов не прекращается. Это объясняет большую продолжительность жизни у женщин, чем у мужчин, характерную для любых национальностей. В Европе и США женщины живут дольше мужчин на 4,5–5 лет, в России — на 13 [6].
Мальчик, которому сделают орхеэктомию (удаление яичек), может быть, и получит дополнительные 10–15 лет жизни, вместе с тем лишившись возможности иметь детей и получив набор других не совсем приятных последствий. Существуют менее радикальные решения, основанные на приёме определённых препаратов, способствующих восстановлению функции тимуса. Одно из таких веществ — грелин, этот гормон вырабатывается слизистой оболочкой желудка и вызывает чувство голода, действуя на центры гипоталамуса. Оказалось, что грелин участвует в Т-клеточном сигналлинге, способен снижать связанное с возрастными изменениями воспаление, способствует восстановлению структуры тимуса и стимуляции его функций. Ряд цитокинов и факторов роста (интерлейкины 7 и 22, фактор роста кератиноцитов) являются потенциальными кандидатами для решения проблемы восстановления функции тимуса у взрослых людей. Интерлейкины обеспечивают дифференцировку и выживание тимоцитов. Фактор роста кератиноцитов необходим для пролиферации и дифференцировки функциональных тканей тимуса, его использование вызывает пролиферацию тимоцитов и увеличивает размеры органа. Возможно также использование веществ, блокирующих выработку стероидных гормонов, таких как аналоги гонадотропин-релизинг гормона, например, люпрона. Люпрон действует на гипофиз, блокируя рецепторы к гонадотропин-релизинг гормону, из-за чего уменьшается выработка лютеинизирующего и фолликуло-стимулирующего гормонов, что ведёт к снижению продукции эстрогена и тестостерона. И всё же, все вышеперечисленные вещества имеют неоднозначное воздействие на организм, и пока ещё нет данных о долгосрочных последствиях их приёма, поэтому их назначают только в случае восстановления после химиотерапии или при ВИЧ-инфекции, когда стимуляция работы тимуса необходима для реконституции иммунной системы [1].
Хранение наивных Т-клеток — полезная инвестиция в будущее
Есть ли иной способ продлить мужскую жизнь? Авторов статьи [2] посетила смелая идея решения этой проблемы. Кроме того, что редко встречающиеся клоны наивных Т-клеток в результате случайных событий теряются с возрастом, они, как и все клетки организма, могут поделиться лишь ограниченное количество раз (примерно 50 — лимит Хейфлика), что обусловлено укорочением теломерных участков хромосом после каждой репликации ядерной ДНК, а делятся наивные Т-клетки раз в 1–2 года. Значит примерно к 70 годам основная часть Т-клеток выйдет из строя. Решение есть — можно запасать наивные Т-клетки! У молодых людей в возрасте до 15–20 лет, когда процессы формирования основного пула наивных Т-клеток уже заканчиваются, нужно брать образцы крови в таком объёме, чтобы количества наивных Т-клеток в них хватило для полного восстановления их пула уже в пожилом возрасте, и заморозить. Очень важно, чтобы забор произошёл именно в этот промежуток времени. Если брать кровь у более взрослых людей, количества циркулирующих наивных Т-клеток просто не хватит для полной реставрации их пула в будущем. Конечно же, такой подход будет эффективен и для женского пола. Эти образцы крови будут не только средством продления жизни, но ещё и подстраховкой в случае аутоиммунных заболеваний или рака, они помогут восстановить иммунную систему после химиотерапии. Создание подобных банков с замороженными образцами крови стало бы ключевым событием в становлении абсолютно новых подходов к лечению заболеваний иммунной системы. Например, СПИД можно было бы вылечить введением в здоровые размороженные Т-клетки заразившегося СПИДом мутации по гену мембранного рецептора CCR5 (CD195), люди с такой мутацией обладают природной резистентностью к ВИЧ [8], и их пересадкой больному, предварительно прошедшему курс химиотерапии.
Итоги
Как бы молодо не выглядел человек, параметры его иммунной системы будут объективно отражать возраст. Такие параметры как количество наивных Т-клеток и разнообразие TCR практически линейно снижаются по мере старения. Если вы являетесь счастливым обладателем повышенного разнообразия TCR, можете надеяться на несколько бонусных лет жизни. В будущем человечество ожидают новые дерзкие подходы к увеличению продолжительности жизни с использованием собственных наивных Т-лимфоцитов, собранных и замороженных много лет назад.
Самый загадочный орган иммунной системы
Вплоть до средних веков одним из претендентов на роль телесного вместилища души считался тимус. В наши дни самой удивительной особенностью этого органа называют его склонность к раннему старению и полной деградации с возрастом. Почему так происходит? Если взрослые могут обходиться без этой железы, то зачем она нужна детям?
Вилочковая железа
Тимус относится к центральным элементам иммунной системы. Свое название железа получила в честь душистого растения чебрец (Thymus), из клеток которой было выделено азотистое основание тимин, входящее в состав ДНК. Это небольшой орган розовато-серого цвета, мягкой консистенции, расположенный в центральной части грудной клетки. Он покрыт капсулой из плотной соединительной ткани, от которой в глубину отходят перемычки, делящие его на дольки. Верхние, более узкие, концы долей выходят за пределы грудной полости, иногда достигая щитовидной железы. Доли тимуса напоминают двузубую вилочку, что и дало название этому органу — «вилочковая железа».
Если тимус недостаточно развит, как, например, при таком генетическом заболевании, как синдром ДиДжорджи, то у детей развивается врожденный иммунодефицит. Болезнь приводит к уменьшению количества Т-лимфоцитов в крови и проявляется повышенной чувствительностью к вирусным, грибковым и некоторым бактериальным инфекциям. Иногда в зрелом возрасте наблюдается особое нарушение иммунологических процессов, связанное с патологией тимуса и других лимфоидных органов, что может быть причиной внезапной смерти от наркоза во время операции.
Его задача — обнаружить клетки, которые в силу различных повреждений превратились в чужеродные, например, под воздействием вируса
Клетки-няньки и школа для лимфоцитов
В отличие от костного мозга, который дает начало практически всем клеткам иммунной системы (эритроцитам, тромбоцитам, гранулоцитам, моноцитам, лимфоцитам), тимус «специализируется» на продукции исключительно Т-лимфоцитов. Буква Т в названии указывает 
Часовые клеточного иммунитета
На внешней оболочке Т-лимфоцитов находятся белки, распознающие специфичные молекулы тканевой совместимости данного организма. Т-лимфоцит похож на часового, который охраняет организм от чужаков, спрашивая «пароль» у каждой клетки, встречающейся на его пути. Его задача — обнаружить клетки, которые в силу различных повреждений превратились в чужеродные, например, под воздействием вируса. Если клетка выглядит подозрительно, то она незамедлительно подлежит разрушению. Для выполнения этой функции Т-лимфоциты должны быть способны распознать собственные антигены тканевой совместимости, специфичные для каждого организма. При этом Т-лимфоциты не должны реагировать на аутоантигенные пептиды, связанные с собственными антигенами тканевой совместимости. Из широчайшего спектра вариантов антигенов тканевой совместимости лишь немногие экспрессированы на клетках данного индивида и нуждаются в распознавании Т-лимфоцитами. Именно поэтому селекция тимоцитов сопровождается большими энергетическими затратами и 95% гибелью. Зато зрелые периферические Т-лимфоциты живут долго и способны отвечать клональной экспансией в случае встречи со специфическим чужеродным антигеном.
Размеры тимуса являются максимальными в детском возрасте, но после начала полового созревания этот орган подвергается значительной атрофии и инволюции
Инволюция тимуса
Размеры тимуса являются максимальными в детском возрасте, но после начала полового созревания этот орган подвергается значительной атрофии и инволюции. У новорожденного тимус уже полностью развит и в течение первого года жизни достигает максимальных размеров — 25 см3: его длина составляет 5 см, ширина — 4 см, толщина — 6 мм. У 6-месячного ребенка масса тимуса достигает от 12 до 20 г, что составляет 0,5% массы тела. Сложная структура и напряженное функционирование железы сохраняются в течение первых 2–3 лет жизни. Самая высокая продукция Т-лимфоцитов происходит до 2 лет, а затем быстро уменьшается. Тимус продолжает расти до наступления половой зрелости, достигая максимального размера (длина до 7,5–16 м) и массы (35–40 г), а после 14–15 лет начинается процесс инволюции. К 20 годам половина функционирующей ткани тимуса замещается жировой тканью и у 25-летних масса железы уменьшается до 25 г с сохранением ее общих очертаний. В течение первых 50 лет жизни ежегодно теряется по 3% истинно тимической ткани. К 50–60 годам инволюция тимуса завершается, его масса составляет менее 15 г, а к 70–75 — около 6 г. Атрофии подвергаются главным образом латеральные участки железы и отчасти нижние, так что железа у взрослого человека принимает более удлиненную форму. По мере инволюции тимус утрачивает былой цвет и за счет увеличения в нем доли стромы и жировых клеток становится более желтым. Вместе с деградацией органа значительно уменьшается и почти полностью прекращается выработка Т-лимфоцитов, с чем отчасти связывают снижение иммунитета у лиц пожилого возраста.
Почему тимус деградирует?
Из всех органов иммунной системы только для тимуса характерна возрастная инволюция. Однако следует отметить, что количество Т-лимфоцитов долгое время сохраняется на достаточном уровне. Дело в том, что значительную часть популяции Т-лимфоцитов составляют долгоживущие клетки, которые не нуждаются в постоянном обновлении. Более того, зрелые Т-лимфоциты подвергаются так называемой колониальной экспансии, то есть избирательной пролиферации при встрече со своим антигеном, за счет чего их численность увеличивается, поэтому количество Т-клеток может поддерживаться во взрослом организме и при отсутствии тимуса. Кроме того, иммунная система располагает некоторыми компенсаторными возможностями для замещения отдельных функций недостающих Т-лимфоцитов. Да и в целом необходимость в генерации новых Т-лимфоцитов с возрастом снижается. Первичные контакты с инфекционными агентами происходят в основном в первые годы жизни, а в дальнейшем встреча с новыми патогенами случается не так часто, поэтому энергозатраты на содержание тимуса становятся нецелесообразными. К тому же постоянная активность тимуса с возрастом чревата развитием стрессовой гиперчувствительности иммунной системы, имеющей патологические последствия.
Тимусзависимая старость
Как видим, возрастная инволюция тимуса не вызывает катастрофического снижения иммунитета. Однако встреча с вирусами кори или ветрянки приводит к более тяжелым осложнениям у взрослых по сравнению с детьми, у которых тимус функционирует в полную силу. Не зря именно в течение первых трех лет жизни, то есть в период «расцвета» тимуса, врачи стараются вакцинировать ребенка против всех наиболее опасных и частых инфекционных заболеваний: туберкулеза, полиомиелита, дифтерии, столбняка, коклюша, кори. В этом возрасте иммунная система организма, как правило, отвечает на введение вакцины выработкой активного иммунитета, в частности путем формирования клонов долгоживущих Т-клеток. Благодаря этому впоследствии при встрече с болезнетворным микроорганизмом включается сигнал колониальной экспансии, активирующий Т-лимфоциты. Несмотря на это, предполагают, что возрастное ослабление иммунной системы, проявляющееся в виде слабой устойчивости к инфекциям, невосприимчивости к вакцинам и аутоиммунным заболеваниям, обусловлено прежде всего старением тимуса. Ведь разнообразные инфекции атакуют человека на протяжении всей его жизни, и «запастись» специфичными иммунными клетками на все случаи практически невозможно, да и запас Т-лимфоцитов постепенно исчерпывается.
Из всех органов иммунной системы только для тимуса характерна возрастная инволюция. Однако следует отметить, что количество Т-лимфоцитов долгое время сохраняется на достаточном уровне
Можно ли «омолодить» тимус?
Фактически тимус начинает деградировать с первых лет жизни, однако это становится заметно в период полового созревания. Закономерно, что инволюция тимуса напрямую связана с влиянием половых гормонов. Отмечено, что инволюцию тимуса способны замедлить пептиды шишковидной железы. Аналогичным образом действует ее гормон мелатонин, способный даже вызывать «омоложение» органа. Поскольку с возрастом ткань тимуса заменяется жировыми клетками, логично, что тимус довольно хорошо восстанавливается при соблюдении низкокалорийной диеты. Способствует этому, скорее всего, «гормон голода» — грелин, правда, у него есть побочный эффект в виде ослабления сексуальной мотивации. У людей старше 70 лет отмечен более разнообразны набор Т-клеточных рецепторов по сравнению с теми, которые еще не преодолели 70-летний рубеж. Удивительно, что продукция Т-лимфоцитов тимусом, пусть и в небольшом количестве, сохраняется даже у людей 100-летнего возраста. При этом у долгожителей менее выражены популяции клеток-клонов — то есть клеток, произошедших от одного активированного Т-лимфоцита. Возможно, именно эти особенности иммунитета позволяют долгожителям лучше противостоять инфекциям и быть более здоровыми. При этом возникает «тимусная селекция», в результате которой люди со сниженным иммунитетом реже становятся долгожителями.
Теперь понятно, почему тимус деградирует с возрастом. Во-первых, производство каждого Т-лимфоцита является слишком энергозатратным процессом. Во-вторых, клетки, прошедшие все этапы созревания, дифференцировки и отбора, могут жить долго и в случае необходимости размножаться клонированием. В-третьих, специфичные наборы клеточных рецепторов практически на все случаи чужеродных антигенов способны сформироваться в течение первого десятилетия жизни, а затем шанс столкнуться с новым инфекционным агентом значительно уменьшается. В-четвертых, подвергать организм иммунологическому стрессу без острой на то необходимости не только нецелесообразно, но и крайне опасно
Татьяна Кривомаз, канд. биол. наук
Список литературы находится в редакции