валлеровская дегенерация что это
Валлеровская дегенерация что это
а) Терминология:
• Валлеровская дегенерация (ВаД)
• Вторичная антероградная дегенерация аксонов и их миелиновых оболочек, вызываемая нарушением целостности аксонов или повреждением нейронов
б) Визуализация валлеровской дегенерации:
• Первичное поражение коры или подкорковых структур с ВаД в нисходящих трактах белого вещества (БВ), ипсилатеральных месту повреждения нейронов:
о ВаД может наблюдаться в волокнах, пересекающих мозолистое тело, волокнах лучистого венца, свода мозга и ножек мозжечка
• КТ нечувствительна к выявлению ВаД в острой-подострой стадиях:
о В хронической стадии позволяет выявить атрофию КСТ
• Зависимость изменений в КСТ от времени по данным МРТ
о Сильная корреляция между ВаД, обнаруженной на Т2-ВИ и ДВИ, и долгосрочной заболеваемостью
о Изменении на ДВИ предшествуют развитию по данным рутинной МРТ
• DTI может позволить дифференцировать первичное поражение от связанной с ним валлеровской дегенерации (ВаД):
о Уменьшение фракционной анизотропии (ФА) в сочетании с увеличением средней диффузивности (MD) при инфаркте
о В КСТ наблюдается уменьшение ФА при нормальной MD
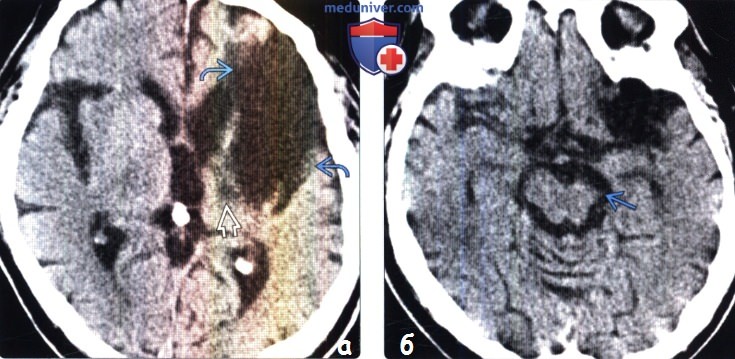
(б) Бесконтрастная КТ, аксиальный срез: у того же пациента визуализируется атрофия левой ножки мозга вследствие хронической валлеровской дегенерации кортикоспинальных трактов. Бесконтрастная КТ является нечувствительным для определения изменений в острую-подострую стадии методом, однако позволяет выявлять атрофические изменения пирамидных трактов в хроническую стадию валлеровской дегенерации. 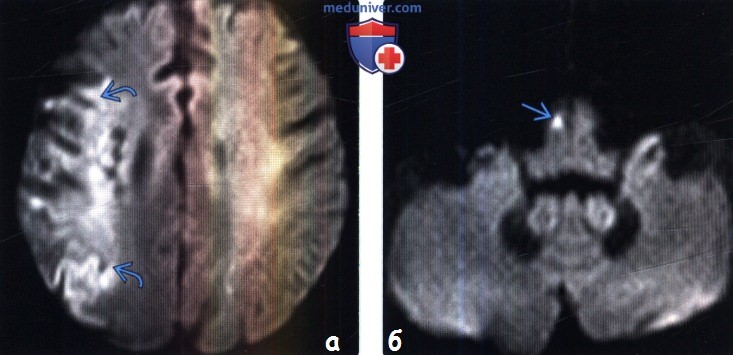
(б) МРТ, ДВИ, аксиальный срез: у того же пациента визуализируется ограничение диффузии в переднем отделе продолговатого мозга в области локализации кортикоспинальных трактов вследствие острой валлеровской дегенерации. ДВИ—наиболее чувствительный метод в определении валлеровской дегенерации на ранних стадиях по сравнению со стандартными МР-последовательностями.
в) Дифференциальная диагностика валлеровской дегенерации:
• Нейродегенеративные заболевания
• Глиома ствола мозга
• Демиелинизирующие и воспалительные заболевания
• Гипертрофическая дегенерация олив
• Метаболические заболевания
• Интоксикации (ингаляции героина)
• Повышение интенсивности сигнала при высокопольной МРТ в норме
Редактор: Искандер Милевски. Дата публикации: 5.5.2019
Валлеровская дегенерация что это
а) Терминология:
1. Сокращения:
• Валлеровская дегенерация (ВаД)
2. Определение:
• Вторичная антероградная дегенерация аксонов и их миелиновых оболочек, вызываемая нарушением целостности аксонов или повреждением нейронов
1. Общие характеристики валлеровской дегенерации:
• Лучший диагностический критерий:
о Непрерывная зона повышения интенсивности сигнала на T2-BИ на протяжении, топографически соответствующем локализации кортикоспинальных трактов (КСТ) во внутренней капсуле (ВК) и стволе мозга у пациентов с различными патологическими изменениями головного мозга
• Локализация:
о Первичное поражение: кора или подкорковые отделы
о ВаД: нисходящие тракты белого вещества (БВ), ипсилатеральные зоне поражения нейронов:
— КСТ, кортикобульбарные, кортикопонтинные тракты
о ВаД может наблюдаться в мозолистом теле, лучистом венце, своде мозга и ножках мозжечка
о Имеются данные о том, что мозолистое тело подвергается атрофическим изменениям при болезни Альцгеймера преимущественно за счет валлеровской дегенерации комиссуральных нервных волокон неокортекса
о Обусловленное судорогами поражение может вызвать вторичную дегенерацию БВ покрова и валика мозолистого тела
• Морфология:
о Изменения сигнала соответствуют конфигурации трактов БВ:
— Овальные зоны в заднем бедре ВК и ножке мозга; тонкие криволинейные участки в мосту

(б) Бесконтрастная КТ, аксиальный срез: у того же пациента визуализируется атрофия левой ножки мозга вследствие хронической валлеровской дегенерации кортикоспинальных трактов. Бесконтрастная КТ является нечувствительным для определения изменений в острую-подострую стадии методом, однако позволяет выявлять атрофические изменения пирамидных трактов в хроническую стадию валлеровской дегенерации.
2. КТ признаки валлеровской дегенерации:
• Бесконтрастная КТ:
о Нечувствительна к выявлению ВаД в острой-подострой стадиях
о Позволяет определять атрофию КСТ в хронической стадии:
— ↓ размеров соответствующих отделов ствола мозга
3. МРТ признаки валлеровской дегенерации:
• Т1-ВИ:
о Изменения в нисходящих трактах БВ в зависимости от времени:
— 1 стадия: без изменений
— 2 стадия: повышение интенсивности сигнала на Т1-ВИ
— 3 стадия: снижение интенсивности сигнала на Т1-ВИ
— 4 стадия: атрофия ствола головного мозга на стороне поражения ± снижение интенсивности сигнала
• Т2-ВИ:
о Изменения в нисходящих трактах БВ в зависимости от времени
— 1 стадия: у взрослых пациентов изменения отсутствуют
— 2 стадия: снижение интенсивности сигнала на Т2-ВИ
— 3 стадия: повышение интенсивности сигнала на Т2-ВИ
— 4 стадия: атрофия, лучшим образом визуализируемая в стволе головного мозга:
Иногда повышение интенсивности сигнала на Т2-ВИ может иметь постоянный характер
о Новорожденные и младенцы: определение ВаД на Т2-ВИ затруднительно вследствие высокого содержания воды и отсутствия миелинизации незрелого БВ
о Взрослые: сильная корреляция между выявленной на Т2-ВИ ВаД и долгосрочной заболеваемостью
• FLAIR:
о Та же картина, что и на Т2-ВИ
• ДВИ:
о Новорожденные и младенцы: позволяет определить острое повреждение БВ:
— На ДВИ признаки ВаД определяются раньше, чем на рутинных МР-последовательностях
— Может являться предвестником неблагоприятного прогноза
о Взрослые: корреляция изменений на ДВИ в области двигательных нисходящих трактов с развитием отдаленных неврологических нарушений
о Степень и тяжесть регионарной ишемии связана с повреждением нисходящих трактов БВ, выявляемом на ДВИ
о Повышение интенсивности сигнала на ДВИ и ↓ значений ИКД в пределах территориального инфаркта и ипсилатеральных КСТ:
— Временные изменения ИКД и на ДВИ в области территориального инфаркта и повреждения КСТ могут быть различными:
Относительно более позднее развитие изменений диффузии в нисходящих трактах БВ
о Аномальная интенсивность сигнала на ДВИ в нисходящих трактах БВ может иметь персистирующий характер, даже при снижении выраженности повышения интенсивности сигнала на ДВИ в ипсилатеральном большом полушарии
• Постконтрастные Т1-ВИ:
о Отсутствие контрастного усиления от дегенеративно измененных трактов
• МР-спектроскопия:
о Н-МР-спектроскопия позволяет оценить повреждение аксонов in vivo на основании интенсивности сигнала от N-ацетил аспартата (NAA)
о ↓ концентрации NAA во внешне нормальном БВ моста и ножек мозжечка на ранних стадиях рецидивирующе-ремитирующего рассеянного склероза (PC):
— Наиболее выражена корреляция с инвалидностью, продолжительностью PC и частотой рецидивов
• Диффузионно-тензорная MPT (DTI):
о Распад миелина приводит к I диффузионной анизотропии о В зоне инфаркта наблюдается снижение ФА в сочетании с повышением значения средней диффузивности (MD)
о В КСТ наблюдается уменьшение ФА при нормальном MD
о У пациентов с инфарктом в области локализации двигательных путей коэффициенты диффузии в дегенеративно измененном КСТ стабилизируются в течение 3-х месяцев; ранние изменения ФА в КСТ могут иметь прогностический характер в отношении долгосрочного клинического исхода
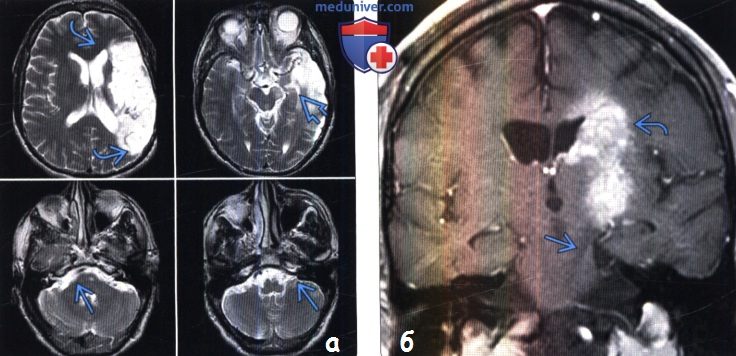
(б) МРТ, постконтрастное Т1-ВИ, корональный срез: по ходу левого лучистого венца определяется объемное образование, накапливающее контраст. Обратите внимание на гипоинтенсивный участок по ходу кортикоспинального тракта, обусловленный разрушением липидов и отеком вследствие валлеровской дегенерации.
4. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о МРТ
• Совет по протоколу исследования:
о ДВИ позволяет выявить изменения на ранних стадиях (1 стадия)
о Изменения на Т2-ВИ обнаруживаются после четырех недель
в) Дифференциальная диагностика валлеровской дегенерации:
2. Глиома ствола мозга:
• Гиперинтенсивное на Т2-ВИ объемное образование ± накопление контраста
3. Демиелинизирующие и воспалительные заболевания:
• Рассеянный склероз: перивентрикулярное повышение интенсивности сигнала на Т2-ВИ
• ОДЭМ: асимметричное повышение интенсивности сигнала от белого и серого вещества на Т2-ВИ после продромального периода вирусной инфекции
• Болезнь Бехчета: увеличение, повышение интенсивности сигнала на Т2-ВИ от ствола мозга ± таламусов
4. Гипертрофическая дегенерация олив:
• Вторичная дегенерация нижнего оливного ядра (НОЯ), обычно происходящая вследствие первичного поражения в зубчато-красноядерно-оливном пути
5. Метаболические заболевания:
• Х-сцепленная адренолейкодистрофия: перитригональная демиелинизации с накоплением контраста
• Болезнь Вильсона: поражение белого и серого вещества с вовлечением базальных ганглиев, зубчатого ядра, ствола мозга
• Гипогликемическая кома: обратимые изменения КСТ
6. Ингаляции героина:
• Симметричное повышение интенсивности сигнала от БВ задних отделов полушарий на Т2-ВИ, включая задние бедра внутренних капсул
7. Здоровые люди:
• Может наблюдаться повышение интенсивности сигнала от КСТ на T2-BИ/FLAIR при ЗТ МРТ (при нормальной полной миелинизации головного мозга)
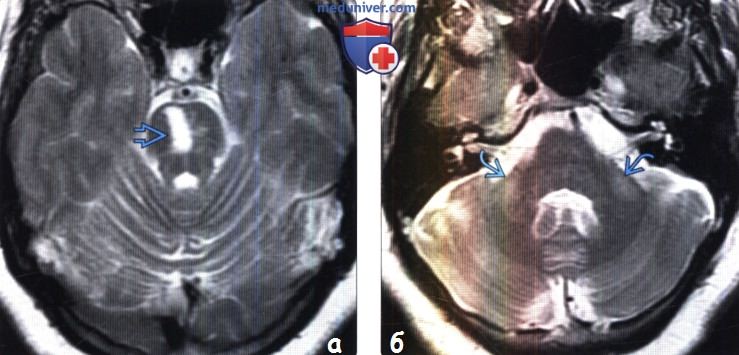
(б) МРТ, Т2-ВИ, аксиальный срез: у этого же пациента наблюдается легкая двусторонняя атрофия средних ножек мозжечка (СНМ) с гиперинтенсивными зонами в них вследствие валлеровской дегенерации. Данная картина является результатом перекреста волокон в мосту. При инфарктах моста на стороне инфаркта в процесс вовлекаются ядра и тракты моста, которые проходят через контрлатеральную среднюю ножку мозжечка, а также тракты, проходящие от контрлатеральных ядер.
1. Общие характеристики валлеровской дегенерации:
• Этиология:
о Инфаркт, кровоизлияние, новообразование, энцефалит
о Демиелинизирующее заболевание, травма, АВ-мальформация
о Также имеются сведения о развитии у пациентов с двигательными нарушениями
• Генетика:
о Процесс аксональной дегенерации имеет генетическую регуляцию
• Ассоциированные аномалии:
о Первичное поражение/заболевание, вызвавшее вторичную дегенерацию трактов БВ
2. Стадирование и классификация валлеровской дегенерации:
• 1 стадия (0-4 недели): дегенерация аксонов; легкие изменения в миелине
• 2 стадия (4-14 недель): распад белков миелина; липиды остаются интактными
• 3 стадия (> 14 недель): распад липидов миелина, глиоз, изменения содержания воды и структурные изменения
• 4 стадия (от нескольких месяцев до нескольких лет): атрофия ствола мозга на ипсилатеральной стороне
3. Макроскопические и хирургические особенности:
• Асимметрия ствола головного мозга вследствие атрофии на хронической стадии
4. Микроскопия:
• 1 стадия: начальные процессы распада миелина и аксонов
о Миелиновые оболочки распадаются на эллипсоиды и сферы, но сохраняют характерные свойства миелина при окрашивании
• 2 стадия: снижение отношения белки: липиды
• 3 стадия: нарастающий отек и дальнейший распад липидов
• 4 стадия: атрофия вследствие потери объема; удаление обломков аксонов микроглией, продолжающееся в течение двух лет (по сравнению с тремя неделями в периферическом отделе нервной системы)
• Экспрессия факторов транскрипции ATF3 и c-Jun ненейрональными клетками в процессе ВаД
• В ЦНС: нарушение процесса роста новых аксонов в матриксе с преобладанием астроцитов
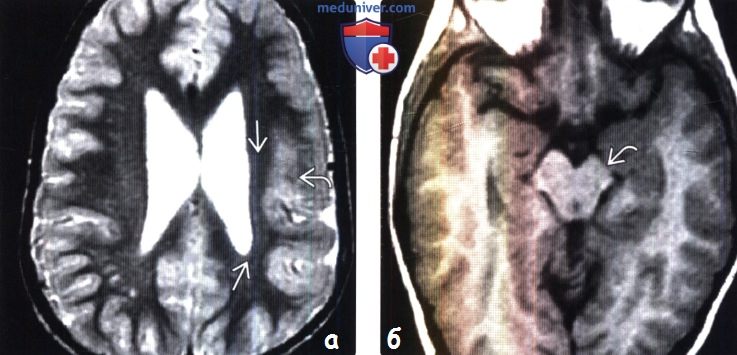
(б) МРТ, Т1-ВИ, аксиальный срез: у этого же пациента наблюдается уменьшение размеров левой ножки мозга. Данная аномалия миграции нейронов проявляется в четвертом слое коры на фоне сохранности нижележащего белого вещества. Кроме того, имеет место закономерная гипоплазия кортикоспинального тракта.
д) Клиническая картина валлеровской дегенерации:
1. Проявления валлеровской дегенерации:
• Наиболее частые признаки/симптомы:
о Валлеровская дегенерация (ВаД) в КСТ связана с персистирующим гемипарезом
2. Демография:
• Возраст:
о Сообщается о встречаемости во всех возрастных группах
• Пол:
о Отсутствие половой предрасположенности
• Эпидемиология:
о ВаД обычно является следствием поражения ЦНС:
— Сообщается, что ВаД в пирамидных трактах встречается в 78.6% случаев инфарктов в капсулярной области
3. Течение и прогноз:
• ВаД может начинаться в течение первой недели после поражения волокон трактов
• Демиелинизация может продолжаться в течение следующих 6-ти месяцев
• Необратимая потеря функции нейронов
• Степень валлеровской дегенерации (ВаД) связана с тяжестью двигательного дефицита
о Аномальная интенсивность сигнала на ДВИ в области КСТ может в остром периоде являться предиктором исхода в отношении двигательных функций при инфаркте у детей
4. Лечение валлеровской дегенерации:
• Специфическая терапия отсутствует
е) Диагностическая памятка. Советы по интерпретации изображений:
• При ишемическом инсульте: важно дифференцировать изменения на ДВИ, связанные с ВаД, от дополнительных очагов инфаркта
• Изменение интенсивности сигнала при ВаД в зависимости от времени → возможно определение давности первичного поражения
ж) Список литературы:
1. Kleinman JT: Early Wallerian degeneration on magnetic resonance imaging: underappreciated but highly relevant. Dev Med Child Neurol. 55(2): 104-5, 2013
2. Saksena S et al: The Corpus Callosum Wallerian Degeneration in the Unilateral Brain Tumors: Evaluation with Diffusion Tensor Imaging (DTI). J Clin Diagn Res. 7(2):320—5, 2013
3. Venkatasubramanian С et al: Natural history and prognostic value of corticospinal tract Wallerian degeneration in intracerebral hemorrhage. J Am Heart Assoc. 2(4): e000090, 2013
4. Domi T et al: Corticospinal tract pre-wallerian degeneration: a novel outcome predictor for pediatric stroke on acute MRI. Stroke. 40(3):780-7, 2009
5. Liang Z et al: Progression of pathological changes in the middle cerebellar peduncle by diffusion tensor imaging correlates with lesser motor gains after pontine infarction. Neurorehabil Neural Repair. 23(7):692—8, 2009
6. Oh MY et al: Ipsilateral wallerian degeneration of thedistal optic radiations after infarction at their root. J Neuroophthalmol. 29(2): 146—8, 2009
7. Yu C et al: A longitudinal diffusion tensor imaging study on Wallerian degeneration of corticospinal tract after motor pathway stroke. Neuroimage. 47(2):451-8, 2009
8. De Simone T et al: Wallerian degeneration of the pontocerebellar fibers. AJNR Am J Neuroradiol. 26(5): 1062-5, 2005
Редактор: Искандер Милевски. Дата публикации: 5.5.2019
Валлеровская дегенерация что это
а) Терминология:
• Дегенерация нижнего ядра оливы (НЯО):
о Уникальный тип транссинаптической нейрональной дегенерации
о Считается, что деафферентация оливы является источником последующей ее гипертрофической дегенерации (ГДО)
• Обычно является следствием первичного повреждения в зубчато-красноядерно-оливном пути (анатомический треугольник Гийена-Молларе)
• Треугольник Гийена-Молларе образован тремя анатомическими структурами:
о Зубчатым ядром (ЗЯ) мозжечка
о Ипсилатеральным красным ядром (КЯ)
о НЯО, ипсилатеральным по отношению к КЯ
б) Визуализация гипертрофической дегенерации олив мозга:
• Изначально НЯО гипертрофируется, а не подвергается атрофии
• Выделяюттри MPT-стадии ГДО:
о Повышение интенсивности сигнала без гипертрофии НЯО: в течение первых шести месяцев после приступа
о Повышение интенсивности сигнала + гипертрофия НЯО: между шестью месяцами и 3-4 годами после приступа
о Только повышение интенсивности сигнала от НЯО: появляется при разрешении гипертрофии (может сохраняться бесконечно долго)
• МРТ также позволяет выявить очаг первичного поражения, расположенный в ипсилатеральном центральном тракте покрышки или контрлатеральном ЗЯ

(б) На рисунке корональ-ного среза среднего мозга, моста и продолговатого мозга представлен треугольник Гийена-Молларе. Данный треугольник образован ипсилатеральным нижним ядром оливы (зеленый цвет), зубчатым ядром (синий цвет) контрлатерального полушария мозжечка и ипсилатеральным красным ядром (красный цвет). 
(б) МРТ, Т2-ВИ, аксиальный срез: у пациента с небным миоклонусом, возникшим ориентировочно через шесть месяцев после резекции кавернозной мальформации среднего мозга, отмечается увеличение размеров обоих олив и повышение интенсивности сигнала от них. Данная картина характерна для подострой стадии гипертрофической дегенерации олив, которая обычно возникает между шестью месяцами и 3-4 годами после повреждения зубчато-красноядерно-оливного тракта.
в) Дифференциальная диагностика:
• Инфаркт в бассейне кровоснабжения перфорирующих ветвей вертебробазилярных артерий
• Демиелинизация (PC, микрососудистые заболевания)
• Боковой амиотрофический склероз
• ВИЧ/СПИД
• Ромбэнцефалит
г) Клиническая картина гипертрофической дегенерации олив мозга:
• Небный миоклонус («тремор» мягкого неба)
• Обычно развивается через 10-11 месяцев после первичного поражения
• Клинические симптомы (тремор) разрешаются редко
Редактор: Искандер Милевски. Дата публикации: 5.5.2019
Кортикобазальная дегенерация
Кортикобазальная дегенерация — это отдельная клиническая форма избирательного дегенеративного процесса с преимущественным поражением лобно-теменной коры и подкорковых ганглиев. Клинические проявления патологии полиморфны, включают паркинсонизм, расстройство праксиса, тремор, миоклонии, фокальные дистонии, речевые нарушения. Диагностируется кортикобазальная дегенерация по результатам неврологического осмотра, нейропсихологического тестирования, ПЭТ и МРТ головного мозга. Этиопатогенетическая терапия заболевания не разработана, лечение симптоматическое.
МКБ-10
Общие сведения
Кортикобазальная дегенерация (КБД) впервые описана в 1968 году. Заболевание получило название в связи с сочетанием дегенеративных изменений в церебральной коре и базальных (подкорковых) структурах. Наряду с болезнью Альцгеймера, прогрессирующим надъядерным параличом (ПНП), болезнью Пика, мультисистемной атрофией КБД относится к таупатиям, сопровождающимся накоплением тау-протеина в церебральных клетках. Поскольку одним из ведущих клинических симптомокомплексов выступает олигобрадикинезия, в клинической неврологии кортикобазальная дегенерация считается вариантом паркинсонизма-плюс. Точная распространённость КБД неизвестна, отдельные исследования указывают, что патология составляет 0,9% всех случаев паркинсонизма. Пик заболеваемости приходится на возраст 50-60 лет.
Причины
Этиологические факторы возникновения КБД, причины избирательного поражения корково-подкорковых структур не определены. Заболевание имеет спорадический характер, по неподтверждённым данным встречаются единичные семейные случаи. Отдельные исследователи предполагают связь патологического метаболизма отдельных внутриклеточных белков с изменениями в генетическом аппарате нервных клеток. Вероятен полиэтиологический характер развития болезни, при котором совокупное воздействие нескольких этиофакторов приводит к реализации генетически детерминированного нарушения.
Патогенез
Основным патогенетическим механизмом признано нарушение белкового обмена в мозговых тканях. Результатом дисметаболизма является агрегация ряда протеинов внутри нейронов, глиальных клеток. Белковые включения изменяют нормальную жизнедеятельность клеток, возможно, запускают механизм их самоуничтожения (апоптоз). Патологический процесс имеет избирательную локализацию, поражаются преимущественно фронто-париетальные области коры, субстанция нигра, стриатум, вентролатеральное таламическое ядро, зубчатые ядра мозжечка. Макроскопическая картина представлена асимметричными атрофическими процессами указанной локализации. Микроскопически определяется уменьшение числа нервных клеток, демиелинизация волокон, внутринейрональные включения тау-белка. Патогномоничным признаком КБД является наличие в зонах поражения неокрашиваемых баллонообразных нейронов.
Симптомы кортикобазальной дегенерации
Клиническая картина отражает прогрессирующее поражение коры и базальных ганглиев. Последовательность развития и сочетание синдромов могут быть различными, что формирует полиморфизм и значительную вариабельность проявлений. Зачастую первым симптомом становится чувство онемения, неловкости в конечности (чаще в верхней), расстройство в ней сложных типов чувствительности: способности узнавать предметы на ощупь (стереогнозис), различать несколько одновременно воздействующих раздражителей (дискриминационное чувство). Указанные изменения распространяются на ипсилатеральную конечность, затем на противоположную сторону. В половине случаев возникает синдром «чужой» конечности (чаще руки) в сочетании с её непроизвольными движениями.
Симптоматика паркинсонизма присутствует у 100% больных, носит асимметричный характер с преобладанием акинетико-ригидных проявлений. Отмечаются иные экстрапирамидные расстройства: различные формы мышечной дистонии, миоклонии, постуральный тремор, реже — хорея, атетоз. У многих пациентов кортикобазальная дегенерация протекает с типичным тоническим состоянием верхней конечности со сгибанием и приведением плеча, предплечья, кисти и пальцев. В ряде случаев больные вынуждены носить мячик в руке, чтобы предупредить повреждение кисти ногтями резко согнутых пальцев. Глазодвигательные нарушения представлены некоторым ограничением амплитуды движений, явный парез взора наблюдается в 20% случаев. Возможны мозжечковая атаксия, лобные симптомы: паратония, сосательный, хватательный рефлексы.
При дебюте симптоматики в нижней конечности нарушения походки появляются на первом году заболевания, при локализации первых проявлений в руке — спустя 3 года. Определяется лобная дисбазия с частыми падениями. Пирамидная недостаточность ограничивается появлением стопных симптомов, гиперрефлексией. В большинстве случаев возникает дизартрия, имеющая смешанный корково-подкорковый характер, в 20-30% случаев — динамическая афазия. У 85% пациентов отмечается апраксия — нарушение программы последовательного выполнения действий. Интеллектуальное снижение обычно развивается после формирования выраженных двигательных нарушений. При этом известны случаи, когда кортикобазальная дегенерация манифестировала когнитивными расстройствами, и деменция являлась ведущим симптомом болезни.
Осложнения
Обусловленные дисбазией падения больного опасны серьёзным травмированием с ушибами и переломами. В последующем прогрессирующий паркинсонизм и апраксия лишают пациента возможности самообслуживания, являются причиной глубокой инвалидности. Локальные мышечно-тонические нарушения осложняются развитием контрактур. Постепенно утрачивается способность самостоятельно передвигаться. Постоянный постельный режим способствует развитию пролежней и целого ряда инфекционных осложнений: цистита, восходящего пиелонефрита, застойной пневмонии, сепсиса.
Диагностика
Кортикобазальная дегенерация диагностируется на основании следующих клинических критериев: L-ДОФА-резистентный паркинсонизм, апраксия, феномен «чужой» конечности, мышечные дистонии, миоклонии, грубый тремор. Постановка диагноза возможна при наличии трёх признаков из шести. Диагноз достоверно верифицируется по данным патоморфологического исследования церебральных тканей. В ходе диагностического поиска осуществляются следующие исследования:
В дебюте симптоматики кортикобазальная дегенерация требует дифференциации с болезнью Паркинсона, в дальнейшем – с клинически сходными опухолями головного мозга, дегенеративными заболеваниями: болезнью Галлервордена–Шпатца, Пика, Альцгеймера, ПНП, деменцией с тельцами Леви. От болезни Паркинсона КБД отличается наличием корковой симптоматики, нарушений речи, резистентностью к ДОФА-терапии. При ПНП выражена офтальмоплегия, отсутствуют миоклонии и очаговая корковая дисфункция. Болезнь Альцгеймера характеризуется преобладанием атрофических и гипометаболических изменений лобно-височной коры.
Лечение кортикобазальной дегенерации
Возможности лечения КБД ограничены, поскольку этиология заболевания остаётся неясной. Применяется преимущественно симптоматическая терапия. Терапевтическая схема, способная остановить прогрессирование дегенерации, пока отсутствует. Лечение направлено на облегчение состояния пациента, уменьшение выраженности симптоматики. Общепринятой считается комбинированная терапия с включением следующих составляющих:
Прогноз и профилактика
Кортикобазальная дегенерация характеризуется неуклонным прогрессированием неврологических проявлений. В среднем спустя 5 лет когнитивные и двигательные расстройства приковывают больного к постели. Продолжительность жизни большинства пациентов не превышает 10 лет от времени дебюта симптоматики. Причиной летального исхода обычно становится бронхопневмония. Разработка профилактических мероприятий не представляется возможной до момента установления этиологии КБД.