вакцинация живыми вакцинами что это
Штамм «Омикрон» – живая вакцина или новая угроза
Ситуация с коронавирусом в России находится на высоком плато: за сутки 30752 новых случая. Из них в Москве – чуть более 3 тысяч. По словам мэра Собянина, за месяц число пациентов в столичных больницах снизилось на 40%. В Челябинской области и в Кузбассе смягчают ограничения – там сняли запрет на работу кафе и ресторанов ночью. А в Оренбургской области в преддверии праздников, напротив, их ужесточают: запретили хороводы на новогодних мероприятиях. По данным ученых, новый штамм ковида «омикрон» в два-три раза быстрее приводит к пневмонии в сравнении с прежними мутациями ковида, а один из его симптомов у детей – необычная сыпь.
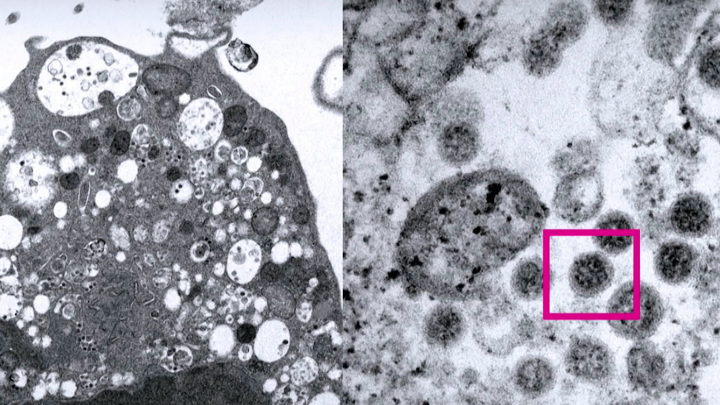
Первая фотосессия «омикрона» в Гонконге. Ученые поймали новый штамм с помощью электронного микроскопа. С виду все-то тот же шар с короной, но свойства иные. Это уже данные из института вирусологии во Франкфурте-на-Майне. Там в плазму вакцинированных добавили «омикрон» и проверили эффективность защиты.
«0% предотвращения заражения после двух мРНК-вакцин, 0% после сочетания векторной вакцины и мРНК-вакцины, 25% после трехкратной вакцинации. Для сравнения, для «дельты» нейтрализация была порядка 95%», – сделали вывод ученые.
Схожие данные получили в ЮАР. Эффективности вакцины от Pfizer в предотвращении заражений снизилась в 40 раз. По данным самой компании Pfizer, эффективность упала только на четверть, и бустер почти полностью восстанавливает защиту. Как на «омикрон» действует «Спутник» еще изучают. Но в любом случае: лабораторные результаты будут сильно отличаться от реальной жизни.
«Переносить впрямую цифры из тестов в пробирке на человека, во сколько раз ослабла защита, пока это пересчитать нельзя. Кроме того, у нас несколько ветвей защиты от коронавируса», – поясняет молекулярный биолог Максим Скулачев.
Первая линия защиты – антитела. Они связываются с шипом, не давая ему проникнуть в клетку. В случае с «омикроном» такой механизм действительно будет менее эффективен. Шип изменился так сильно, что антителам трудно его узнать. Но остается второй механизм – Т-лимфоциты. Они быстро убивают зараженные клетки, не давая вирусу размножаться в организме. Т-киллеры ориентированы не только на шипы и обмануть их у «омикрона» не получится.
«У абсолютного большинства и переболевших, и вакцинированных Т-клеточный ответ развивается. Даже при отсутствии антител Т-лимфоциты обеспечивают частично защиту от заражения», – рассказывает руководитель управления биомедицинских технологий Национального медицинского исследовательского центра гематологии Григорий Ефимов.
Т-клетки защитят вакцинированных и переболевших от тяжелого течения. Какие последствия «омикрон» может вызвать у людей без иммунитета к вирусу – вопрос пока открытый. Но африканские врачи настроены оптимистично.
«У меня хорошие новости: на данный момент мы наблюдаем гораздо более легкую симптоматику у зараженных «омикроном», чем у зараженных «дельтой», – говорит вирусолог Стелленбошского университета ЮАР Вольфган Прейзер.
Уже понятно: «омикрон» – самый заразный из существующих штаммов. Если инфицированный уханьским штаммом мог заразить двух человек, больной «дельтой» – пятерых, то носитель «омикрона» – уже шестерых. В Британии уже выявлено 440 зараженных. Прогнозируют, что это число будет ежедневно удваиваться, и к рождеству счет пойдет на десятки тысяч.
«Он распространяется очень быстро. И, думаю, в ближайшее время у нас будут циркулировать сразу оба штамма», – считает микробиолог Кембриджского университета Рави Гумпта.
Один из возможных сценариев: за счет заразности «омикрон» будет вытеснять «дельту». И если новый штамм действительно вызывает более мягкие симптомы – это может положить конец пандемии.
«В данном случае природа создала живую вакцину. То есть, что такое живая вакцина, – это вирус, который не вызывает каких-то патологий, но быстро распространяется и способен вызывать у людей иммунитет», – поясняет член-корреспондент РАН Петр Чумаков.
Возможны и другие варианты: «омикрон» будет вызывать не только легкое течение, а «дельта» не уйдет с арены. В таком случае в популяции будут циркулировать сразу два вируса. Выходом в этом случае станет двойная вакцинация. К адаптации существующих вакцин под «омикрон» уже приступили ведущие лаборатории мира.
ВАКЦИНОПРОФИЛАКТИКА
ВАКЦИНАЦИЯ – ЗАЛОГ ЗДОРОВОГО БУДУЩЕГО
Ежегодно в мире от инфекционных заболеваний погибают около 12 миллионов детей. Третья часть из них (4 миллиона) умирают от болезней, которые можно было предотвратить с помощью прививки. В XIX веке диагноз «корь», «дифтерия», «бешенство», «столбняк», считались смертным приговором. Начиная с XX века, благодаря достижениям в области микробиологии, вирусологии и фармакологии заболеваемость этими инфекциями сведена практически к нулю. Целью иммунизации является формирование специфического иммунитета к инфекционному заболеванию посредством искусственного создания инфекционного процесса, который в большинстве случаев протекает бессимптомно или в легкой форме (у непривитого человека течение этих болезней несет тяжелейший характер, иногда с летальным исходом).
МЕХАНИЗМ ДЕЙСТВИЯ ВАКЦИНЫ
В ответ на вакцинацию в организме возникает цепочка иммунологических реакций, подразделяющихся на три периода. Первый период (латентный, или «лаг-фаза») продолжается с момента введения вакцины до появления первых антител в крови. Длительность первого, латентного, периода варьирует от нескольких дней до 2 недель и зависит от вида вакцины, способа ее введения и особенностей иммунной системы организма. Второй период характеризуется повышением концентрации специфических антител в крови. После введения некоторых вакцин специфические антитела появляются очень быстро, содержание их в крови стремительно повышается, что позволяет использовать эти вакцинные препараты для экстренной профилактики при контакте с больными корью, полиомиелитом, эпидемическим паротитом и другими инфекциями. Второй период продолжается от 4 дней до 4 недель. Третий период наступает после достижения максимального уровня специфических антител, когда их количество начинает уменьшаться — вначале быстро, затем медленно. Такое уменьшение происходит в течение нескольких лет. При повторной встрече с антигеном (при ревакцинации или инфицировании привитого ребенка) «лаг-фаза» отсутствует, так как активируются В-клетки памяти и специфический иммунный ответ возникает быстрее и отличается большей интенсивностью.
ПОМНИТЕ, ПРИВИВКИ СПАСАЮТ ВАШЕ ЗДОРОВЬЕ И ЖИЗНЬ!
2. Все вакцины обладают определенной степенью реактогенности, которая лимитирована нормативной документацией на препараты.
3. В соответствии с Законом Российской Федерации “О лекарственных средствах”, утвержденным 22 июня 1998 г, производство лекарственных средств, к которым относятся и иммунобиологические препараты, осуществляется предприятиями-производителями лекарственных средств, имеющими лицензию на их производство”.
4. В России на 16 предприятиях производится 50 видов вакцин против 28 инфекционных заболеваний. Практически все вакцины соответствуют по основным показателям безопасности и эффективности требованиям.
Вакцинацию можно проводить следующими способами:
— накожно (скарификационная вакцинация) оптимальна при иммунизации живыми вакцинами против особо опасных инфекций (чумы, туляремии и др.). Вакцины наносят на наружную поверхность плеча, а затем сухим оспопрививочным пером делают насечки через каплю.;
ОДНОВРЕМЕННОЕ ВВЕДЕНИЕ НЕСКОЛЬКИХ ВАКЦИН
Живые и неживые вакцины
Сегодня перед каждым родителем встает важнейший вопрос вакцинирования ребенка. Да и самим взрослым периодически необходимо ставить прививки. Многие сторонники «естественной медицины» уверяют, что вакцинация — это опасное и вредное мероприятие, которое служит ослаблению иммунитета и направлено на финансирование медицинских экспериментов. Но давайте отложим все «теории заговора» и подойдем к вопросу о вакцинировании честно и беспристрастно.
Цель вакцинации
Прежде чем рассуждать о типах вакцин, следует разобраться в том, что такое вакцина вообще.
Вакцина — это вещество, которое позволяет организму приобрести временную или постоянную невосприимчивость к тому или иному виду вирусов. Механизм работы вакцины довольно прост и понятен — вещество, содержащее в себе мизерную долю микроорганизмов или продуктов их жизнедеятельности, вводится в организм человека. Организм «знакомится» с таким веществом и при встрече с настоящим вирусом проявляет стойкий иммунитет.
Вакцинация помогает защититься от тяжелых вирусных заболеваний: туберкулеза, оспы, полиомиелита, паротита. Организм вырабатывает иммунитет к этим заболеваниям и становится устойчив к вирусам.
Опасности вакцинации
Следует сказать пару слов об опасностях вакцинирования. Действительно, некоторые люди, особенно дети, могут проявить аллергические реакции после введения вакцины. Обычно они выражаются в раздражении кожи, зуде, покраснении. Однако следует отметить, что:
Состав вакцины
Для выработки иммунитета ученые используют следующие типы раздражителей:
Живые и неживые вакцины
Живыми называют вакцины, в составе которых есть настоящие естественные микроорганизмы. Неживыми — все остальные. Многие родители предполагают, что живые вакцины более эффективны и безопасны для ребенка, однако на самом деле это правда лишь отчасти. Давайте рассмотрим различия между живыми и неживыми вакцинами.
Виды вакцин
Открытие метода вакцинации дало старт новой эре борьбы с болезнями.
В состав прививочного материала входят убитые или сильно ослабленные микроорганизмы либо их компоненты (части). Они служат своеобразным муляжом, обучающим иммунную систему давать правильный ответ инфекционным атакам. Вещества, входящие в состав вакцины (прививки), не способны вызвать полноценное заболевание, но могут дать возможность иммунитету запомнить характерные признаки микробов и при встрече с настоящим возбудителем быстро его определить и уничтожить.
Производство вакцин получило массовые масштабы в начале ХХ века, после того как фармацевты научились обезвреживать токсины бактерий. Процесс ослабления потенциальных возбудителей инфекций получил название аттенуации.
Сегодня медицина располагает более, чем 100 видами вакцин от десятков инфекций.
Препараты для иммунизации по основным характеристикам делятся на три основных класса.
В последние годы появился еще один вид вакцин — молекулярные. Материалом для них становятся рекомбинантные белки или их фрагменты, синтезированные в лабораториях путем применения методов генной инженерии (рекомбининтная вакцина против вирусного гепатита В).
Схемы изготовления некоторых видов вакцин
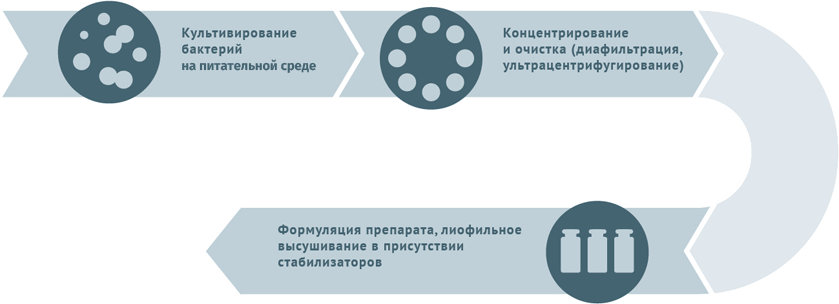
Живые бактериальные
Схема подходит для вакцины БЦЖ, БЦЖ-М.
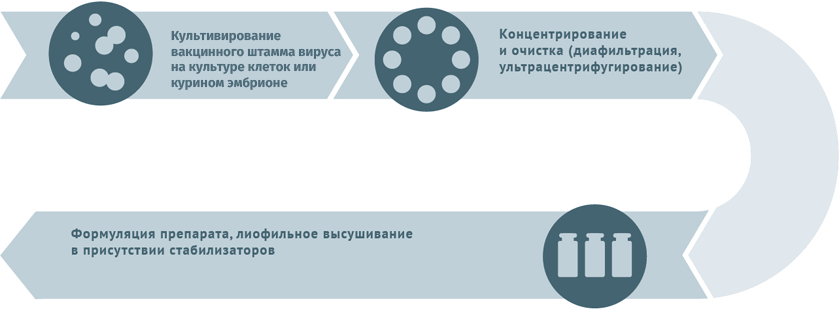
Живые противовирусные
Схема подходит для производства вакцин от гриппа, ротавируса, герпеса I и II степеней, краснухи, ветряной оспы.
Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться:
Первичный сырьевой материал очищают от клеточного дебриса в центрифугах и с помощью сложных фильтров.
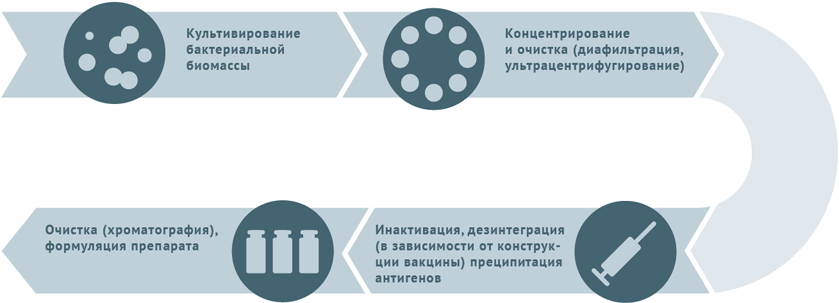
Инактивированные антибактериальные вакцины
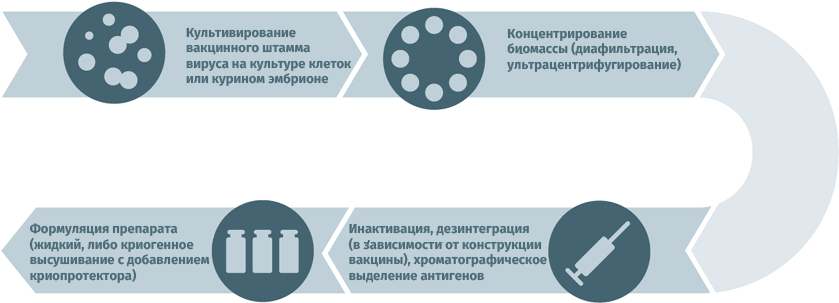
Инактивированные противовирусные вакцины
Схема подходит для производства прививочного материала против гепатита А, желтой лихорадки, бешенства, гриппа, полиомиелита, клещевого и японского энцефалитов.
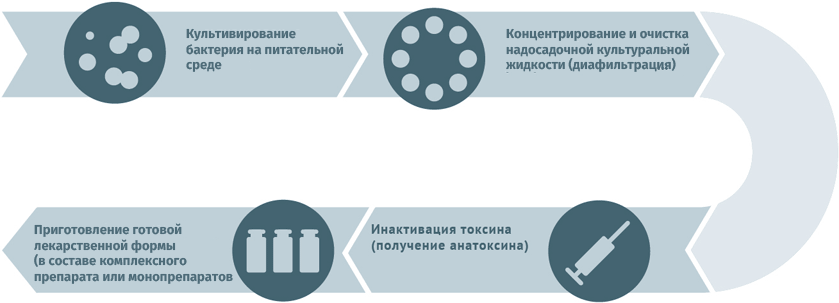
Анатоксины
Для дезактивации вредного воздействия токсинов используют методы:
Схема подходит для производства вакцин против столбняка и дифтерии.
По данным Всемирной Организации Здравоохранения (ВОЗ), на долю инфекционных заболеваний приходится 25 % от общего количества смертей на планете ежегодно. То есть инфекции до сих пор остаются в списке главных причин, обрывающих жизнь человека.
Одним из факторов, способствующих распространению инфекционных и вирусных заболеваний, являются миграция потоков населения и туризм. Перемещение человеческих масс по планете влияет на уровень здоровья нации даже в таких высокоразвитых странах, как США, ОАЭ и государства Евросоюза.
По материалам: «Наука и жизнь» № 3, 2006, «Вакцины: от Дженнера и Пастера до наших дней», академик РАМН В. В. Зверев, директор НИИ вакцин и сывороток им. И. И. Мечникова РАМН.
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Вопросы и ответы
Я много лет вакцинируюсь от гриппа вакциной французского производителя. В этом году терапевт предложила мне сделать прививку российской вакциной. Я ничего не знаю об отечественных вакцинах, какая из них качественная?
Отвечает Полибин Роман Владимирович
Российские препараты, которыми проводится вакцинацию в рамках ОМС, эффективны и безопасны. Для массовой иммунизации населения Минздравом используются вакцины Совигрипп (НПО «Микроген»), Ультрикс (ООО ФОРТ), УльтриксКвадри (ООО «ФОРТ» иФлю-М (СПбНИИВС ФМБА России). Препараты доказали высокий профиль безопасности и эффективности в ходе полного объема обязательных доклинических и клинических исследований, проведенных в соответствии с требованиями, предъявляемыми регуляторными органами РФ и Европы, а также длительного опыта успешного применения в России и динамики снижения заболеваемости. Подробнее о вакцинах можно узнать на официальных сайтах разработчиков.
Вакцина «Менюгейт» зарегистрирована в России? С какого возраста разрешена к применению?
Отвечает Харит Сусанна Михайловна
Да, зарегистрирована, вакцина – от менингококка С, сейчас также есть вакцина конъюгированная, но уже против 4 типов менингококков – А, С, Y, W135 – Менактра. Прививки проводят с 9 мес.жизни.
Муж транспортировал вакцину РотаТек в другой город.Покупая ее в аптеке мужу посоветовали купить охлаждающий контейнер,и перед поездкой его заморозить в морозильной камере,потом привязать вакцину и так ее транспортировать. Время в пути заняло 5 часов. Можно ли вводить такую вакцину ребенку? Мне кажется,что если привязать вакцину к замороженному контейнеру, то вакцина замерзнет!
Отвечает Харит Сусанна Михайловна
Моему сыну сейчас 7 месяцев.
В 3 месяца у него случился отек Квинке на молочную смесь Малютка.
Прививку от гепатита сделали в роддоме, вторую в два месяца и третью вчера в семь месяцев. Реакция нормальная, даже без температуры.
Но вот на прививку АКДС нам устно дали медотвод.
Я за прививки!! И хочу сделать прививку АКДС. Но хочу сделать ИНФАНРИКС ГЕКСА. Живем в Крыму. В крыму ее нигде нет. Посоветуйте как поступить в такой ситуации. Может есть зарубежный аналог? Бесплатную делать категорически не хочу. Хочу качественную очищеную, что бы как монжно меньше риска.
Отвечает Полибин Роман Владимирович
В Инфанрикс Гекса содержится компонент против гепатита В. Ребенок полностью привит против гепатита. Поэтому в качестве зарубежного аналога АКДС можно сделать вакцину Пентаксим. Кроме того, следует сказать, что отек Квинке на молочную смесь не является противопоказанием к вакцине АКДС.
Подскажите, пожалуйста, на ком и как тестируют вакцины?
Отвечает Полибин Роман Владимирович
Как и все лекарственные препараты вакцины проходят доклинические исследования (в лаборатории, на животных), а затем клинические на добровольцах (на взрослых, а далее на подростках, детях с разрешения и согласия их родителей). Прежде чем разрешить применение в национальном календаре прививок исследования проводят на большом числе добровольцев, например вакцина против ротавирусной инфекции испытывалась почти на 70 000 в разных странах мира.
Почему на сайте не представлен состав вакцин? Почему до сих пор проводится ежегодная реакция Манту (зачастую не информативна), а не делается анализ по крови, например, квантифероновый тест? Как можно утверждать реакции иммунитета на введенную вакцину, если еще ни кому не известно в принципе, что такое иммунитет и как он работает, особенно если рассматривать каждого отдельно взятого человека?
Отвечает Полибин Роман Владимирович
Состав вакцин изложен в инструкциях к препаратам.
Реакция Манту. По Приказу № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерациии» и Санитарным правилам СП 3.1.2.3114-13 «Профилактика туберкулеза», несмотря на наличие новых тестов, детям необходимо ежегодно делать реакцию Манту, но так как этот тест может давать ложноположительные результаты, то при подозрении на тубинфицирование и активную туберкулезную инфекцию проводят Диаскин-тест. Диаскин-тест является высоко чувствительным (эффективным) для выявления активной туберкулезной инфекции (когда идет размножение микобактерий). Однако полностью перейти на Диаскин-тест и не делать реакцию Манту фтизиатры не рекомендуют, так как, он не «улавливает» раннее инфицирование, а это важно, особенно для детей, поскольку профилактика развития локальных форм туберкулеза эффективна именно в раннем периоде инфицирования. Кроме того, инфицирование микобактерией туберкулеза необходимо определять для решения вопроса о ревакцинации БЦЖ. К сожалению, нет ни одного теста, который бы со 100% точностью ответил на вопрос, есть инфицирование микобактерией или заболевание. Квантифероновый тест также выявляет только активные формы туберкулеза. Поэтому при подозрении на инфицирование или заболевание (положительная реакция Манту, контакт с больным, наличие жалоб и пр.) используются комплексные методы (диаскин-тест, квантифероновый тест, рентгенография и др.).
Ребёнку 1 год и 8 месяцев, все прививки ставились в соответствии с календарем прививок. В том числе 3 пентаксима и ревакцинация в полтора года тоже пентаксим. В 20 месяцев надо ставить от полиомиелита. Очень всегда переживаю и отношусь тщательно к выбору нужных прививок, вот и сейчас перерыла весь интернет, но так и не могу решить. Мы ставили всегда инъекцию (в пентаксиме). А теперь говорят капли. Но капли-живая вакцина, я боюсь различных побочек и считаю, что лучше перестраховаться. Но вот читала, что капли от полиомиелита вырабатывают больше антител, в том числе и в желудке, то есть более эффективные, чем инъекция. Я запуталась. Поясните, инъекция менее эффективна (имовакс-полио, например)? Отчего ведутся такие разговоры? У каплей боюсь хоть и минимальный, но риск осложнения в виде болезни.
Отвечает Полибин Роман Владимирович
В настоящее время Национальный календарь прививок России предполагает комбинированную схему вакцинации против полиомиелита, т.е. только 2 первых введения инактивированной вакциной и остальные – оральной полиовакциной. Это связано с тем, чтобы полностью исключить риск развития вакциноассоциированного полиомиелита, который возможен только на первое и в минимальном проценте случаев на второе введение. Соответственно, при наличии 2-х и более прививок от полиомиелита инактивированной вакциной, осложнения на живую полиовакцину исключены. Действительно, считалось и признается некоторыми специалистами, что оральная вакцина имеет преимущества, так как формирует местный иммунитет на слизистых кишечника в отличие от ИПВ. Однако сейчас стало известно, что инактивированная вакцина в меньшей степени, но также формирует местный иммунитет. Кроме того, 5 введений вакцины против полиомиелита как оральной живой, так и инактивированной вне зависимости от уровня местного иммунитета на слизистых оболочках кишечника, полностью защищают ребенка от паралитических форм полиомиелита. В связи с вышесказанным вашему ребенку необходимо сделать пятую прививку ОПВ или ИПВ.
Следует также сказать, что на сегодняшний день идет реализация глобального плана Всемирной организации здравоохранения по ликвидации полиомиелита в мире, которая предполагает полный переход всех стран к 2019 году на инактивированную вакцину.
Национальный Фармацевтический журнал
Войти на сайт
ВАКЦИНЫ ПРОТИВ COVID-19 И АДЪЮВАНТЫ, УЛУЧШАЮЩИЕ ИХ СВОЙСТВА.

Новый адъювант для профилактических вакцин компании SEPPIC

• вакцины на основе цельного (полногеномного) ослабленного вируса;
• инактивированные вакцины на основе полностью нежизнеспособного вируса;
• векторные вакцины;
• генетические вакцины (ДНК и РНК вакцины);
• субъединичные вакцины на основе отдельных компонентов патогена, таких как белки, пептиды или генетический материал (например, белковые или рекомбинантные вакцины). Разработчики из различных стран на основании накопленных знаний и имеющихся у них результатов и методов исследований выбирают для разработки тот тип вакцины, который считают наиболее действенным для обеспечения эффективной защиты людей от вируса SARS-CoV-2 (Рис.1).
На настоящий момент среди вакцин-кандидатов против COVID-19, зарегистрированных в списке ВОЗ, можно найти практически все из вышеназванных типов вакцин. Коротко напомним, что представляет собой каждый из них и чем они отличаются друг от друга.

Векторные вакцины – это также вакцины на основе живых вирусов, однако здесь есть небольшой, но очень важный нюанс: это вакцины на основе хорошо изученных и достаточно безобидных для человека вирусов («векторов» или вспомогательных транспортных вирусов) с встроенными в них фрагментами генома «злого вируса» (Рис. 3). В случае векторных вакцин в геном хорошо изученного и, в целом, безобидного вируса, например, аденовируса («вектора»), путём генетических модификаций встраивается небольшой ген – участок генома SARS-CoV-2. При вводе в организм такой векторной вакцины генетически модифицированные вспомогательные вирусы провоцируют такой же сильный иммунный ответ на белки-антигены SARS-CoV-2, как в случае «живой» полногеномной вирусной вакцины.
Преимущество указанных вакцин, по замыслу разработчиков, в той же высокой эффективности, что и у вакцин на основе живых ослабленных вирусов, но в большей управляемости в связи с достаточной изученностью и предсказуемостью «вектора»-носителя. Векторные вакцины начали разрабатываться и изучаться относительно недавно, поэтому к массовому применению вакцин этого типа ученые также подходят с должной и необходимой осторожностью.

Еще два перспективных типа вакцин против COVID-19, разрабатываемые мировым сообществом, – вакцины на основе нуклеиновых кислот, а именно, ДНК- и РНК-вакцины. В случае ДНК-вакцины нуклеотидная последовательность, кодирующая антиген SARS-CoV-2, встраивается в вектор – бактериальную плазмиду – небольшую стабильную кольцевую молекулу ДНК, способную к автономной репликации. Сама по себе плазмида не вызывает нужного специфического иммунного ответа, для этого, собственно, в неё и вшивают гены иммуногенных белков. Указанный модифицированный геном направляется в клетку, встраивается в ее ядро и образует вирусный белок (антиген), индуцирующий иммунный ответ.
Согласно замыслу разработчиков, ДНК-вакцины не могут вызвать заражение SARS-Cov-2, однако иммунитет, который они обусловливают, должен оказаться таким же сильным, как в случае «живых» вакцин. Тем не менее, влияние ДНК-вакцин на живые организмы изучено еще в меньшей степени, чем влияние векторных вакцин, поэтому вряд ли в ближайшее время ДНК-вакцины будут допущены к массовому применению на людях. 
В случае применения РНК-вакцины получается двойной иммунный ответ: с одной стороны, выработку антител вызывают вирусные белки, с другой стороны, сами липидные частицы с мРНК могут стимулировать иммунный ответ, так как «похожи на вирус» и воспринимаются организмом соответственно. Разработчики предполагают, что при вакцинации РНК-вакцинами из-за их «двойного действия» в организме быстро возникнет сильный и стойкий иммунитет.
В случае генетических вакцин преимуществом является их относительно быстрое и экономически выгодное производство: небольшую молекулу мРНК можно довольно быстро воссоздать, наработка нужного антигена обойдется недорого. Это делает вакцину доступной широким массам. Тем не менее иммунологи очень осторожно относятся к РНК-вакцинам, так как из-за малого периода их изучения никто не знает наверняка, как именно мРНК будет вести себя в живом, особенно в репродуктивном, организме.

Одним из самых безопасных типов вакцин в настоящее время считаются субъединичные вакцины, то есть вакцины на основе белков или фрагментов вируса (Рис. 6), не имеющих в своем составе ни ДНК, ни РНК как, например, белковые вакцины.
Попадая в организм при вакцинации, смесь фрагментов вирусных белков-антигенов также способна вызывать иммунный ответ. При этом такая вакцина абсолютно безопасна, здесь невозможны мутации вируса, поэтому вызвать у человека заболевание COVID-19 такая вакцина не может. Недостатком субъединичных вакцин является довольно длительный и сложный процесс наработки и очистки – получить достаточное для вакцинации очищенное количество вирусного белка не так легко. Кроме того, в чистом виде белковые вакцины не вызывают сильный иммунный ответ, поэтому недостаточно эффективны. В связи с этим при разработке белковых вакцин очень важно:
а) усилить иммунный ответ, вводя в состав белковых вакцин соединения, усиливающие их эффективность (эти вещества называют адъюванты),
б) увеличить количество нарабатываемой вакцины также за счет добавления к наработанному вирусному белку существенного количества того же адъюванта.

Наконец, мы подошли к еще одному безопасному и перспективному типу вакцин – инактивированным вакцинам. Здесь так же, как и в случае «живых» вакцин на основе ослабленного вируса используется цельный геном SARS-Cov-2, но в случае инактивированных вакцин вирус полностью деактивирован либо высокой температурой, либо дезинфицирующими составами, либо определенным видом излучения, что делает его совершенно нежизнеспособным. Этот инактивированный вирус никогда не сможет инфицировать клетку. Тем не менее по структуре «неживой» инактивированный вирус остается полным аналогом «живого» вируса и поэтому вызывает в организме иммунный ответ. Проблема в том, что в чистом виде инактивированные вирусы индуцируют существенно более низкий иммунный ответ, нежели живые, пусть даже и ослабленные вирусы. В связи с этим в составах инактивированных вакцин так же, как и в случае субъединичных вакцин используют адъюванты – вещества, которые значительно усиливают иммунный ответ, делая эти вакцины схожими по эффективности с живыми.
Основываясь на вышесказанном, мы склоняемся к выводу, что наиболее безопасными для человека являются субъединичные и инактивированные вакцины. Для повышения эффективности указанных безопасных вакцин до уровня более иммуногенных «живых», векторных или генетических вакцин необходимо применение в их составах современных адъювантов. Что же такое адъюванты и какова их роль в вакцинах?

Адъювант (от лат. adjuvans – «помогающий, поддерживающий») – соединение или комплекс веществ, используемых для усиления иммунного ответа при введении одновременно с антигеном.
Адъюванты на протяжении десятилетий применяются для улучшения иммунного ответа на вакцинные антигены. Включение адъювантов в состав вакцин направлено на усиление, ускорение и продление специфического иммунного ответа до желаемого уровня. Таким образом, адъюванты играют ключевую роль в получении эффективного и длительного иммунитета.
Использование адъювантов в вакцинах позволяет:
• Усилить краткосрочный иммунный ответ;
• Увеличить продолжительность иммунитета, то есть сократить частоту требуемых бустерных иммунизаций;
• Направить иммунный ответ (гуморальный или клеточный иммунитет);
• Уменьшить антигенную нагрузку при сохранении эффективности вакцины;
• Улучшить иммунный ответ у ослабленных или иммунокомпроментированных вакцинируемых лиц;
• Снизить себестоимость вакцины;
• Повысить стабильность вакцины.
Интерес к адъювантам для вакцин резко возрос в 2000-е годы. Ведущие фармацевтические компании-производители путем применения адъювантов разработали более эффективные и безопасные вакцины против гриппа.
В последние годы появляется все больше и больше новых вакцин-кандидатов как для профилактики инфекционных заболеваний, так и для терапии самых тяжелых заболеваний человечества. В связи с низкой иммуногенностью таких вакцин во многих случаях требуется введение в их состав адъювантов. Новые достижения в области аналитической биохимии, очистке макромолекул, технологии рекомбинантной ДНК, улучшенное понимание иммунологических механизмов и патогенеза заболевания позволили улучшить техническую основу разработки и применения адъювантов.
В настоящее время известно довольно много эффективных адъювантов, которые классифицируются по природе происхождения, механизму действия и физическим или химическим свойствам.
Так, в современных вакцинах широко применяются гели гидроксида алюминия, фосфаты алюминия или кальция, препараты на основе масляных эмульсий и ПАВ, дисперсные адъюванты, например, виросомы, структурные комплексы сапонинов и липидов и многие другие типы адъювантов.
Как уже упоминалось выше, наиболее эффективно и поэтому чаще всего адъюванты используются в следующих категориях вакцин:
• вакцины на основе белков (рекомбинантные субъединичные);
• инактивированные;
• векторные вакцины (для уменьшения дозы).
Для каждой вакцины адъювант подбирается таким образом, чтобы получить оптимальное соотношение эффективности указанной вакцины (получение сильного и продолжительного иммунного ответа) и ее безопасности для человека (минимальная реактогенность и отсутствие побочных эффектов).
К сожалению, немаловажным аспектом уже зарегистрированных в настоящее время адъювантов является их недоступность широкому кругу разработчиков. Практически все имеющиеся на настоящий момент современные адъюванты, применяемые в профилактических вакцинах, за исключением соединений алюминия, являются собственностью крупнейших фармацевтических компаний (см. табл. 2). В первую очередь, к ним относятся адъюванты для приготовления эмульсионных вакцин. Эти адъюванты на настоящий момент считаются наиболее перспективными в профилактических вакцинах, но остаются при этом и наименее доступными, так как были специально разработаны крупными биофармацевтическими компаниями исключительно для вакцин собственного производства.
Эти недоступные широкому кругу разработчиков адъюванты ведущих фармацевтических компаний отлично зарекомендовали себя в составах готовых вакцин указанных производителей. К примеру, эмульсионные адъюванты масло-в-воде MF59, AS03 и AF03 продемонстрировали высокую эффективность в вакцинах против гриппа. Сегодня вакцинами на их основе провакцинировано >120 миллионов человек, их профиль безопасности и иммуногенности тщательно и глубоко изучен и подтвержден на значительном количестве клинических испытаний (см. табл. 3).

Франсуа Бертран, руководитель направления разработки и производства адъювантов компании Seppic, в своем выступлении по поводу выпуска адъюванта SEPIVAC TM SWE на мировой рынок сказал: «Указанная разработка иллюстрирует наше общее стремление привнести готовый эффективный и общедоступный адъювант в мировое сообщество разработчиков вакцин. Мы твердо верим, что SEPIVAC TM SWE ускорит разработку новых профилактических вакцин для людей и будет способствовать более здоровому будущему человечества во всем мире».