в чем выражается эффективность вакцины
Критерии оценки эффективности вакцинации
Приложение
Ваксигрип
(обзор)
КРИТЕРИИ ОЦЕНКИ ЭФФЕКТИВНОСТИ ВАКЦИНАЦИИ
Н.И. Брико
Московская медицинская академия им. И.М. Сеченова
Сегодня является бесспорным тот факт, что вакцинопрофилактика это наиболее мощный метод борьбы с инфекционной патологией. Вместе с тем, вакцинация относится к числу мероприятий, требующих значительных материальных затрат, поскольку предусматривает охват прививками широкие слои населения. В связи с этим важно иметь правильное представление об эффективности иммунизации. Вакцинопрофилактика как мероприятие оценивается по 3 группам критериев: показатели документированной привитости (охват прививками), уровень иммунологической или клинической эффективности (efficacy) и эпидемиологическая или полевая эффективность (effectiveness). Показатели охвата прививками позволяют косвенно оценить возможное состояние популяционного иммунитета. Объективными критериями качества вакцинного препарата, а также состояния защищенности коллектива против того или иного инфекционного заболевания являются показатели иммунологической (клинической) и эпидемиологической (полевой) эффективности. Иммунологическая эффективность отвечает на вопрос «работает ли вакцина?», в то время как эпидемиологическая – «защищает ли прививка людей?» [3,5]. Иными словами, иммунологическая эффективность вакцины и эффективность иммунизации как профилактического мероприятия – разные понятия. Если под иммунологической эффективностью вакцины принято понимать способность препарата вызывать иммунный ответ у привитого, то эффективность иммунизации – различия в заболеваемости в группе привитых и непривитых лиц [1,2].
Сбор сведений о привитости осуществляется на уровне педиатрического участка по данным журналов профилактических прививок (ф.064-У), карт профилактических прививок (ф.063-у), истории развития ребенка (ф.112-у), сертификата о профилактических прививках (ф.156-у). Эта информация передается в территориальные центры Госсанэпиднадзора, последние анализируют ее по территориям и передают в соответствующие ведомства. Оценка привитости проводится на основании изучения величины охвата прививками лиц декретированного возраста в соответствии с действующим календарем профилактических прививок, введенным Приказом МЗ РФ №375 от 18.12.97. Нормативными показателями охвата прививками в возрастных группах детей до 3-х лет следует считать 95,0%, в старших возрастных группах – 97-98%. Опыт борьбы с оспой показал, что 80-90% охват прививками недостаточен для ликвидации инфекции. Оспу удалось ликвидировать лишь при охвате 99% населения прививками. Это обстоятельство важно учитывать при решении задачи ликвидации других инфекций.
Оценка иммунологической эффективности осуществляется выборочно среди различных групп населения и прицельно в индикаторных группах населения (получающих в соответствии с возрастом прививки), а также в группах риска (детские интернаты, дома ребенка и др.). Основные требования к иммунологическим исследованиям сводятся к следующему: 1) короткий промежуток времени, в течение которого исследуются все испытуемые сыворотки; 2) стандартность используемых диагностических препаратов; 3) высокая чувствительность иммунологического теста [2]. Выбор теста для оценки иммунологической эффективности вакцины зависит от характера иммунитета при данной инфекции. Например, для таких инфекций как столбняк, дифтерия, корь, паротит критерием эффективности вакцины является определение уровня циркулирующих специфических антител, а для туберкулеза, туляремии и бруцеллеза и др. – клеточные реакции (например, кожные реакции замедленной гиперчувствительности). К сожалению, для большинства инфекций, при которых основой защиты является клеточное звено иммунитета, уровни иммунных клеточных реакций не установлены.
Изучение иммунологической эффективности вакцин проводится путем сопоставления титров специфических антител в сыворотке крови привитых до и в разные сроки после иммунизации, а также путем сравнения этих результатов с определяемыми уровнями антител, полученными в те же сроки при обследовании лиц, которым вводили плацебо или препарат сравнения. Плацебо помещают в точно такие же ампулы или флаконы, в которых содержится изучаемая вакцина. Первые сыворотки собираются непосредственно перед вакцинацией, последующие – обычно через месяц после введения препарата. При однократной вакцинации одновременному исследованию подлежат парные сыворотки крови. При двукратной – тройные сыворотки и т.д. Очень важно, чтобы сыворотки, собранные в разные сроки, титровались одновременно. В случае хранения сывороток, взятых в более ранние сроки, может произойти снижение их активности, в результате чего показатели иммуногенности будут искусственно завышены. Сыворотки следует хранить в замороженном состоянии, причем замораживанию должны быть подвергнуты все образцы как ранее собранных сывороток, так и свежих. В этом случае если и наблюдается снижение активности сывороток, то данный факт имеет равное значение для сывороток, полученных в разные сроки.
Необходимость проведения подобных исследований определена неоднозначностью понятий «привит» и «защищен». Имеющийся опыт свидетельствует, что эти понятия далеко не всегда совпадают (рядом авторов это отмечено при дифтерии, кори и эпидемическом паротите). Иммунологическая активность вакцин может отражать ее профилактическую эффективность в том случае, если известен защитный уровень иммунологических показателей при данной инфекции. Защитный уровень антител устанавливается заранее на основании результатов опытов с однонаправленным препаратом. Для каждой инфекции определяется защитный титр антител (для кори, паротита и гриппа он равен 1:10, столбняка 1:20, дифтерии 1:40 в РПГА; для коклюша 0,03 МЕ/мл, гепатита В 0,01 МЕ/мл в иммуноферментной реакции и т.д.). Для инфекций, при которых не установлен защитный уровень антител, приходится проводить испытания профилактической эффективности вакцин по показателям заболеваемости данной инфекцией.
Наиболее объективную оценку иммунологической эффективности вакцин можно получить при вакцинации серонегативных к специфическим антигенам людей. Из таких лиц формируют опытную и контрольную группы. Оценку иммуногенности вакцинного препарата осуществляют на основе определения разницы в числе лиц имеющих антитела в этих двух группах. Коэффициент иммунологической эффективности определяют по следующей формуле:
Сформировать группы лиц, у которых не определялись бы антитела к широко распространенным возбудителям (грипп, гепатит А и др.) подчас бывает довольно сложно. В таких случаях нередко эффективность препаратов оценивают по нарастанию титров специфических антител до и после вакцинации как в основной, так и в контрольной группе. Иммунологические сдвиги, возникающие при вакцинации, оцениваются также по проценту сероконверсии. Вакцина считается высоко эффективной, если процент сероконверсии составляет 90% и выше. Кроме того, важное значение имеет длительность поствакцинального протективного иммунитета, которая после введения, например, вакцины против желтой лихорадки составляет 10-15 лет, брюшного тифа (вакцины Вианвак и Тифим Ви) – 3 года, гепатита В не менее 7-10 лет. Опубликованы результаты исследований о сохранении антител к вирусу краснухи от 9 до 21 г. после прививки, причем серонегативность обнаруживалась только у 1% привитых вакциной Рудивакс [7].
Для оценки и слежения за уровнем популяционного иммунитета проводится плановый серологический (иммунологический) контроль. Он позволяет выявить группы людей, наиболее подверженных риску заболевания, оценить степень защищенности лиц, привитых с нарушением схемы иммунизации или не имеющих документов о вакцинации, дать оценку и составить прогноз изменения эпидемиологической ситуации на конкретной территории. Отбор лиц для обследования в целях изучения иммуноструктуры проводится на основе кластерной выборки, рекомендованной ВОЗ. Экстренный серологический контроль проводится в очагах инфекционных заболеваний с целью выявления неиммунных лиц, которые контактировали с источником инфекции и подлежат срочной активной или пассивной иммунизации. Он также показан для лиц с неясным прививочным анамнезом, при оценке вакцинального процесса у детей из групп риска, привитых щадящими методами, а также при развитии поствакцинальных осложнений. Результат оценки иммунологической (клинической) эффективности вакцин может дать представление, является ли вакцина иммуногенной и защищает ли она тех, кто привит. В то же время исследования относительной иммуногенности не могут дать ответ, какая из схем вакцинации обеспечивает лучшую защиту, и результаты испытаний клинической эффективности будут трудны для экстраполирования на условия рутинного применения вакцины в популяции. Таким образом, хотя исследования иммунологической эффективности вакцин необходимы, они часто не могут дать четкий ответ о выгоде, связанной с вакцинацией.
Для оценки эпидемиологической эффективности используются как «когортные» исследования, так и метод «случай-контроль». Сроки наблюдения в контролируемом эпидемиологическом опыте должны быть достаточными для определения длительности иммунитета, формирующегося у привитых изучаемой вакциной. При наличии соответствующей документации защитный эффект вакцинации может быть оценен и ретроспективно, т.е. на основе уже имеющейся информации о заболеваемости привитых и непривитых лиц. Метод «случай-контроль» используется при оценке эффективности вакцинации в группах лиц (на определенных территориях), где зарегистрированы случаи соответствующих заболеваний. Каждый случай (или выборка) заболеваний сравнивается индивидуально по признаку вакцинации с соответствующими случаями незаболевания у лиц идентичных по возрасту, полу, условиям проживания и т.д.
Среди исследований эпидемиологической (полевой) эффективности ретроспективный вид анализа наиболее распространен. Один из простых подходов, разработанных в середине 1980-х является скрининговый метод, широко применяющийся в оценочных программах вакцинации не только в развивающихся, но и в развитых странах. Скрининг-исследование требует только два типа данных контроля относительно каждой популяции: соотношение прошедших вакцинацию (PPV) и соотношение пациентов, которые были привиты, но заболели (PCV). Эффективность вакцинации рассчитывается с использованием алгебраического производного классического уравнения VE = 1 – относительный риск (5). Была разработана простая номограмма, позволяющая скрининг-исследованию быть легко применимым. Скрининг имеет два важных ограничения: для того, чтобы исследование было точным, частично привитые пациенты должны быть исключены из опыта, помимо этого большие погрешности могут иметь место всякий раз, когда PPV или PCV очень низки или очень высоки. Тем не менее, метод очень полезен, потому что, подобно всем скрининг-исследованиям, он показывает, являются ли клиническая (иммунологическая) и эпидемиологическая (полевая) эффективность вакцинации приемлемыми или требуют дальнейшего изучения.
В условиях плановой вакцинации применяют обычные эпидемиологические исследования, детально описанные Оренштейном и соавт. [6]. Исследования эпидемиологической (полевой) эффективности прививки прямо отвечают на вопрос, «защищает ли прививка людей?». Оценка эпидемиологической эффективности предусматривает сбор информации об уровне заболеваемости, проявлениях эпидемического процесса во времени, в пространстве и среди различных групп населения. Основными критериями оценки эффекта массовой иммунизации служат не только показатели заболеваемости, но и смертности, изменения в характере очаговости, сезонности и цикличности, возрастной структуре болеющих, а также клинического течения соответствующего инфекционного заболевания. Эти критерии учитываются за достаточно длительный период времени до и после проведения прививок. Предусматривается определение индекса эффективности, коэффициента (показателя) защищенности, коэффициента тяжести клинического течения болезни.
Коэффициент защищенности (Е) определяется по формуле
a – заболеваемость среди лиц, получивших препарат;
б – заболеваемость среди лиц, не получивших препарат.
По показателю защищенности можно определить, каков удельный вес людей из числа получающих вакцинный препарат защищенных от заболевания. Показатель защищенности может с известной долей достоверности выводиться из показателя непосредственного риска, определяемого в когортном эпидемиологическом исследовании.
Индекс эффективности вакцинации равен показателю относительного риска.
После вычисления коэффициентов эпидемиологической эффективности того или иного вакцинного препарата следует убедиться, что разница в заболеваемости является закономерной. Для этого следует провести соответствующую статистическую обработку полученного материала. Принято считать, что разница в показателях не является случайной, если уровень значимости p
Что такое эффективность вакцины и можно ли ею манипулировать?
Производители вакцин от коронавируса постоянно выпускают пресс-релизы, рассказывая об эффективности своих продуктов. Народу приятнее слышать цифры, близкие к 100%. Мол, именно такой и должна быть вакцина, иначе грош ей цена (даже той, которая будет распространяться бесплатно). Попробуем разобраться, что такое «эффективность вакцины» и какой она должна быть. Может, будет достаточно и 50%?
Само понятие эффективности вакцины складывается из множества «маленьких эффективностей»: предотвращать заражение — предотвращать развитие болезни — снижать интенсивность течения болезни — снижать риск смерти.
Например, препарат может помогать бороться с вероятными осложнениями и снижать вероятность фатальных случаев в случае развития заболевания, но быть не таким эффективным с точки зрения его предотвращения. Причем цифры варьируются в зависимости от дополнительных параметров, к которым относят те же возраст, сопутствующие заболевания (например, органов дыхания), состояния (к таким относится беременность) и другое.
К положительным эффектам необходимо добавить и отрицательные — побочные. В некоторых случаях применение вакцины с «неприятной» «побочкой» оправданно, в других — вряд ли.
Существуют разные методики расчета эффективности, хотя, конечно, есть и определенные общие стандарты. Тем не менее у производителей вакцин есть лазейки, которые позволяют продемонстрировать лучшие стороны разработки, скрыв худшие или не рассказав о них.
На определение эффективности уходит уйма времени: нужны исследования, испытания, наблюдения на протяжении многих лет (ведь неизвестно, какие могут быть последствия приема препаратов через 5—10 лет).
И наконец, эффективность бывает разной: та, которую вакцина показывает во время клинических испытаний (efficacy — «эффективность»), и демонстрируемая в реальных условиях (effectiveness — «результативность»). Это, кстати, одна из тех самых лазеек, упоминавшихся выше.
Вот весьма условный пример. Во время испытаний вакцины на 100 добровольцах у 50 появился иммунитет. «Лабораторная» эффективность — 50%? Сценарии сложнее, вот один из них: 10 000 добровольцев ничего не делают до появления симптомов у части из них — тех самых 100 человек. 10% от этих 100 получают препарат, а остальные из той же группы — плацебо.
Специалисты наблюдают за ними и высчитывают относительную разницу между количеством заболевших среди получивших плацебо и настоящую прививку. Так они получают данные об efficacy: если разницы нет, эффективность нулевая; если все заболевшие не были вакцинированы, эффективность — 100%.
В реальных условиях эффективность (которая effectiveness) совсем другая. Выходит вакцина с «лабораторной» эффективностью 80% в мир, где прививки получает миллион человек. А «результативность» оказывается на уровне 60%, в следующем году — 40% — так, например, происходит с вакциной от гриппа. Почему так случается? В клинические испытания, какой бы разнообразной ни была выборка, вряд ли возьмут женщин на позднем сроке беременности, совсем пожилых с букетом хронических болезней, раковых больных или несовершеннолетних. Будут и иные переменные, которые отсутствовали в лабораторных условиях. В жизни все получат вакцину — вот и пляска процентов.
Во Всемирной организации здравоохранения считают достаточной эффективность вакцины от COVID-19 от 50% и более. Почему так мало? Уже при таком уровне количество заболевших будет значительно сокращаться, снижая нагрузку на медицинскую инфраструктуру стран, а также их экономику. В мировых масштабах 50% — это уже огромное подспорье в свете сложившейся ситуации. Хотя, конечно, «желаемый показатель», по версии той же ВОЗ, составляет 70% и выше.
Важно понимать, что высокая эффективность вакцины не означает, что все сразу выздоровеют, не заболеют или перенесут болезнь в легкой форме. Людей необходимо как минимум привить (чем больше привитых, тем меньше шансов подхватить болезнь и у непривитых). По состоянию на конец января объемов препаратов разных производителей недостаточно для обеспечения не то что полной вакцинации, а даже той, которая обеспечит «коллективный иммунитет» (да и он в условиях постоянной мутации вирусов и вероятности повторных заражений отчасти под вопросом).
В The Financial Times собирают данные из открытых источников — можно примерно оценить масштабы проблемы. Лучшие показатели из расчета количества доз вакцины от «короны» на 100 человек населения имеет Израиль (52,3), на втором месте — ОАЭ (34,1), на третьем — Великобритания (14,2). Нужно принимать во внимание объем популяции тех или иных регионов. В США, например, распределено 30,8 млн доз вакцин, но на 100 человек приходится лишь 9,4 дозы. Для сравнения: в Израиле распределено 4,7 млн доз (но первое место по охвату). Всего же в мире распределено около 100 млн доз вакцин против новой заразы.
Цель (социальная) разработчиков вакцин — выпустить такую, которая обеспечит защиту от заражения. Однако и в этом случае остается возможность развития COVID-19 после того, как эффект вакцины сойдет на нет — через полгода-год. Чтобы этого не произошло, может потребоваться регулярная вакцинация, как в случае с гриппом (если не будет разработана «одноразовая» вакцина). Ученые не исключают, что COVID-19 станет системным заболеванием, искоренить которое при нынешнем уровне развития медицинских технологий невозможно.
«В истории человечества мы смогли победить только оспу. Но мы пока так и не смогли ликвидировать, например, полиомиелит и корь», — говорил ранее директор программы ВОЗ по чрезвычайным ситуациям Майкл Райан.
Но вернемся к заявленной эффективности вакцин, уже доступных для применения в том или ином виде. Данные могут меняться по описанным выше причинам: чем больше проведено вакцинаций, тем точнее данные. Многие вакцины вводятся в два захода, эффективность показана на разных стадиях испытаний (ряд ученых высказывает мнение, что она не может составлять 100%). Обычно препарат начинает действовать спустя какое-то время, поэтому прием первой дозы не означает развития «неуязвимости» — беречь себя все так же необходимо.
Список на самом деле длиннее (только в Китае испытания проходит полтора десятка вакцин от коронавируса, в мире насчитываются сотни вакцин-кандидатов), здесь же упомянуты наиболее «популярные».
Что означает «против тяжелых случаев»?
Как говорилось выше, эффективность вакцины складывается из набора факторов. В данном случае это означает, что ее прием обеспечит защиту от тяжелой формы заболевания (или развития осложнений) в указанной доле случаев — при этом течение болезни в легкой или средней степени тяжести возможно. Данные обычно базируются на результатах клинических испытаний и потому могут отличаться от реальных.
В отношении российской вакцины «Спутник V» то и дело звучит критика из-за сложности проверки предоставленной информации об эффективности. Аналогично обстоят дела с «Эпиваккороной», о 100%-ной эффективности которой заявили в пресс-службе Роспотребнадзора по итогам первых фаз испытаний. Сейчас на сайте ведомства в разделе «Топ-20 вопросов о вакцине ФБУН ГНЦ ВБ „Вектор“» вакцину много раз называют «безопасной и эффективной», но без конкретики.
Не дают покоя и остальные вакцины. Достается Pfizer & BioNTech (после приема фиксировались смерти возрастных пациентов от 79 до 93 лет), китайские препараты то критикуют за «раздутую статистику», то хвалят за высокую эффективность. А затем останавливают их введение из-за серьезных побочных эффектов. Почему так?
Традиционно все упирается в сроки. Ранее между созданием концепции и производством вакцин, не требующих срочного выпуска, проходило 20—30 лет (!): учитывались все нюансы, велись доработки и проверки. Это еще одна причина, по которой говорить об эффективности новых вакцин рано, равно как и рассуждать о периоде их действия — пока лишь прогнозы.
По словам Дэвида Палтиэла из Йельской школы общественного здоровья, вопрос не столько в самой вакцине, сколько в программах вакцинации: «Привив пару человек, вы не спасете остальных». Ссылаясь на исследование коллег, он отметил, что темпы распространения вакцин не менее важны, чем их эффективность. «Время уходит», — добавил он.
Эффективность вакцинации
Глобальный охват вакцинацией держится на стабильном уровне. При большинстве инфекций он не превышает 85%.
Несмотря на применяемые меры в России ежегодно регистрируется 30 млн случаев инфекционных заболеваний. Между тем, в 95% случаев заболеваний можно было бы избежать, вовремя сделав прививки.
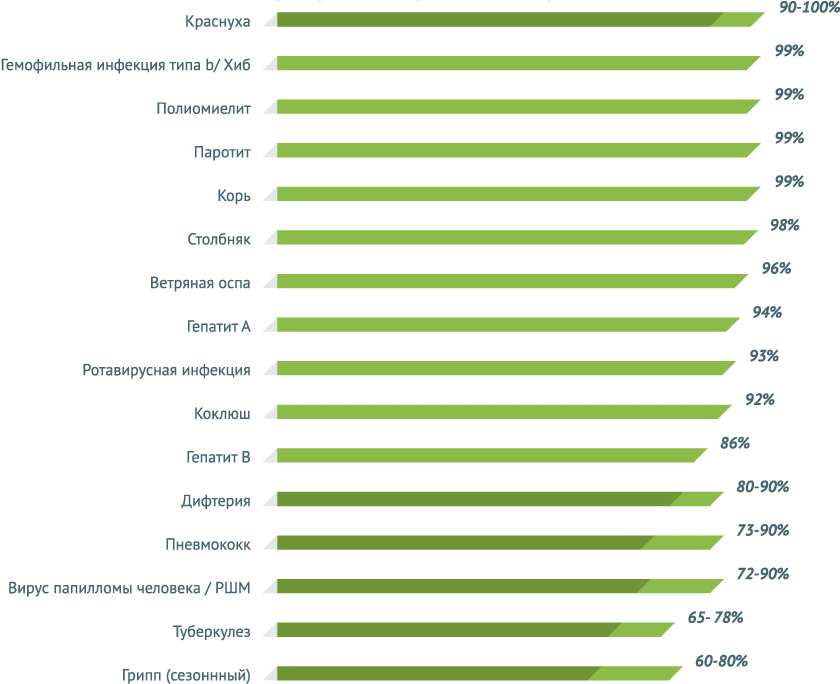
Эффективность вакцин при правильной схеме проведения прививок
Уровни предотвращения заболеваний или серьезных осложнений с помощью вакцин достаточно велики – куда больше, чем защита от получения серьезных травм при вождении мотоцикла и автомобиля по всем правилам безопасности.
Сравнение уровней защиты привычных средств с вакцинами
Шлем может защитить мотоциклиста от травм головного мозга только в половине случаев, а ремень безопасности в автомобиле лишь на 67% предохранит пассажиров и водителя от серьезных травм. Защитные функции вакцин существенно выше. Любая из представленных на диаграмме прививок обеспечивает защиту от соответствующего заболевания и осложнений в ходе болезни не менее чем на 80%.
К сожалению, ни одна из вакцин не является абсолютно безопасной. Все они обладают определенной степенью реактогенности, которая ограничена нормативной документацией на препараты. Однако степень безопасности иммунобиологических препаратов намного превышает таковую огромного количества лекарственных средств, которые люди принимают бесконтрольно и не по назначению врача, совершенно не заботясь в процессе самолечения ни о побочных эффектах этих лекарств, ни о показаниях, ни о противопоказаниях к их применению!
Факторы, способствующие возникновению побочных реакций, можно разделить на 4 группы:
Но даже несмотря на возможные осложнения при введении вакцин современная медицина признает значительное преимущество их полезных свойств для снижения возможных последствий болезни по сравнению с возможным естественным заражением.
Также, чтобы обезопасить ребенка от негативных последствий после вакцинации, следует ознакомиться со списком медицинских противопоказаний к проведению вакцинации.
Риск же осложнений после вакцинации несопоставим с риском осложнений от болезней.
Относительный риск осложнений после вакцинаций и соответствующих инфекций
Если сделать прививку
Вакцина
Возможные поствакцинальные осложнения
Если не делать прививку
Осложнения в ходе заболевания
Осложнения ветряной оспы регистрируются с частотой 5–6%. 30% осложнений – неврологические, 20% – пневмонии и бронхиты, 45% – местные осложнения, сопровождающиеся образованием рубцов на коже. У 10-20% переболевших вирус ветряной оспы пожизненно остается в нервных ганглиях и в дальнейшем вызывает другое заболевание, которое может проявиться в более старшем возрасте – опоясывающий лишай или герпес.
Летальность при заболевании
Если сделать прививку
Вакцина
Возможные поствакцинальные осложнения
Если не делать прививку
Осложнения в ходе заболевания
Летальность при заболевании
Болезнь ответственна за 20% всех детских смертей.
Если сделать прививку
Вакцина
Возможные поствакцинальные осложнения
Если не делать прививку
Осложнения в ходе заболевания
Энцефалопатия – до 1/1200.
Асфиксия, пневмония, разрывы мышц, переломы костей, компрессионные деформации позвоночника, инфаркт миокарда, остановка сердца, мышечные контрактуры и параличи III, VI и VII пар черепных нервов.
Летальность при заболевании
Если сделать прививку
Вакцина
Вирусы папилломавирусной инфекции
Возможные поствакцинальные осложнения
Тяжёлая аллергическая реакция – 1/600 000.
Если не делать прививку
Осложнения в ходе заболевания
Летальность при заболевании
Если сделать прививку
Вакцина
Возможные поствакцинальные осложнения
Тяжёлая аллергическая реакция – 1/500 000.
Если не делать прививку
Осложнения в ходе заболевания
Летальность при заболевании
Если сделать прививку
Вакцина
Возможные поствакцинальные осложнения
Если не делать прививку
Осложнения в ходе заболевания
Летальность при заболевании
(Вторая по значимости причина смертности от инфекционного агента (после ВИЧ- инфекции). Возбудителем туберкулеза инфицированы 2 млрд человек — треть населения нашей планеты.
Если сделать прививку
Вакцина
Возможные поствакцинальные осложнения
Если не делать прививку
Осложнения в ходе заболевания
Летальность при заболевании
Установленная частота осложнений после вакцинации
Вакцина
Установленная частота тяжелых реакций
Нужны ли людям вакцины? (под ред.Медуницына)
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Вопросы и ответы
Ребенку 1 г 10 мес. В 6 мес. была сделана прививка Инфанрикс-Гекса, две недели назад прививка корь-краснуха-паротит. Ребенок начал ходить в детский сад, сейчас узнала, что в группе есть дети, которым некоторое время назад сделали живую вакцину от полиомиелита.
Представляет ли пребывание с такими детьми опасность для моего ребенка?
Когда и какую можно сделать прививку от полиомиелита нам сейчас? У меня выбор: поставить комплексную АКДС Инфанрикс или только полиомиелит, можно ли сделать прививку от полиомиелита через две недели после Приорикса?
Отвечает Харит Сусанна Михайловна
Для защиты от любых форм полиомиелита ребенок должен иметь как минимум 3 прививки. При вакцинации других детей живой оральной вакциной против полиомиелита непривитые или не полностью привитые дети высаживаются из детского сада на 60 дней для предупреждения развития вакциноассоциированного полиомиелита.
Нет, через 2 недели вы не можете начать прививки, интервал между прививками не меньше 1 месяца. Вам нужно сделать как минимум 2 прививки против полиомиелита прежде, чем ребенок будет защищен от этой инфекции. Т.е если ребенок привит дважды, то только через 1 месяц после последней прививки выработается достаточный иммунитет. Лучше привиться 2-х кратно с интервалом в 1,5 месяца АКДС+ ИПВ(Пентаксим, ИнфанриксГекса), через 6-9 месяцев делается ревакцинация. АКДС+ИПВ/ОПВ(Пентаксим). Прививка против гепатита В у вас пропала, но если вы будете прививаться ИнфанриксГекса дважды с интервалом в 1,5 месяца, 3ю прививку против гепатита В можно сделать через 6 месяцев от первой. Рекомендую сделать полный курс вакцинации, поскольку ребенок посещает детский сад (организованный коллектив) и практически не имеет никакой защиты от опасных и тяжелых инфекций.
У меня вопрос несколько общего характера, но обращаюсь к вам, так как до сих пор не смог получить на него внятного ответа. Кому, на ваш взгляд, может быть выгодна кампания по дискредитации вакцинации и, в особенности, детской? Я не прошу, конечно же, назвать конкретных виновников, мне интереснее понять, какие стороны могут быть в этом заинтересованы? Или же это процесс спонтанный, сродни невежеству, не нуждающемуся в подпитке?
Отвечает Полибин Роман Владимирович
Моей дочери 13 лет и она не болела ветряной оспой. Хотим сделать прививку, правильно ли мы поступаем?
Отвечает Харит Сусанна Михайловна
Да, чем старше ребенок, тем, к сожалению, больше вероятность тяжелого течения ветряной оспы, А так как это девочка, то нужно подумать и о том, что если заболевают ветряной оспой во время беременности, то это приводит к тяжелой патологии плода.
Можно ли взрослому привиться от ротавируса, если каждый год болею этим, нет желчного пузыря, спасибо!
Отвечает Харит Сусанна Михайловна
Нет, смысла в вакцинации для взрослых нет. Взрослые не болеют очень тяжело, а задача вакцины против ротавируса – предотвратить тяжелые формы заболевания с обезвоживанием у младенцев. Потом на протяжении всей жизни все равно заболевания возможны, но в легкой форме. Возможно стоит поговорить с гастроэнтерологом о профилактических мерах, например, лечении биопрепаратами.
Отвечает Полибин Роман Владимирович
Для ребенка, особенно при наличии указанных состояний опасны не прививки, а инфекции. Для проведения вакцинации обязателен осмотр врача перед прививкой, клинический анализ крови, при необходимости – общий анализ мочи и осмотр врача специалиста, у которого наблюдается ребенок с имеющимися заболеваниями.
Что делает эта прививка? Как решается проблема с заражением столбняком.
Отвечает Харит Сусанна Михайловна
Прививка против столбняка защищает от развития заболевания. Заражение столбняком происходит путем попадания спор бактерий, находящихся в загрязненных землей предметах, в поврежденные ткани. Споры столбнячной палочки истребить невозможно, поэтому проблема с заболеванием решается путем плановой вакцинации.
Подскажите пожалйста, как лучше и более аргументировано ответить на мнение студента-медика и вообще любого медработника: «я не делаю прививку от гриппа, потому что не известно какой вирус будет в этом эпидсезон, а прививку от гриппа разрабатывают летом, когда еще на знают актуальные штаммы будущей эпидемии». Другими словами какая вероятность в % того, что тривакцина от гриппа, которой ппививают осенью «перекроет» актуальные штаммы вируса в наступающем эпидсезоне зимой с учетом того, что возможно появление одного или нескольких новых штаммов. Буду также благодарен, если Вы сбросите ссылки на первоисточники таких данных, чтобы мои слова были более убедительны.
Отвечает Полибин Роман Владимирович
Главными аргументами в необходимости профилактики гриппа являются сведения о высокой контагиозности, тяжести, многообразии осложнений этой инфекции. Грипп чрезвычайно не только для групп риска, но и для здоровых людей среднего возраста. Такое частое осложнение как пневмония протекает с развитием РДС и летальностью, достигающей 40%. В результате гриппа могут развиваться синдром Гудпасчера, Гийена-Барре, рабдомиолиз, синдром Рейе, миозит, неврологические осложнения и т.д. Причем среди умерших и лиц с тяжелыми осложнениями привитых людей не наблюдается!
Вакцинация согласно ВОЗ является самой эффективной мерой профилактики гриппа. Практически все современные противогриппозные вакцины содержат три типа вируса – H1N1, H3N2 и В. В последние годы зарубежом зарегистрировано несколько четырехвалентных вакцин, создан такой препарат и в России. Разновидности вируса меняются каждый год. И существует сеть специальных Национальных центров ВОЗ по гриппу, которые проводят наблюдение за циркулирующими вирусами, отбирают пробы, осуществляют выделение вирусов и антигенную характеристику. Информацию о циркуляции вирусов и впервые выделенные штаммы отправляют в сотрудничающие центры и головные контрольные лаборатории ВОЗ для проведения антигенного и генетического анализа, в результате которого разрабатываются рекомендации о составе вакцины для профилактики гриппа в южном и северном полушариях. Эта система Глобального надзора за гриппом. Таким образом, состав вакцины на грядущий сезон не «угадывается», а прогнозируется на основании уже выделенных антигенов при начавшейся циркуляции вируса и заболеваемости в одной из частей света. Прогноз является высокоточным. Ошибки бывают редко и связаны с распространением от животных нового типа вируса. Наличие защиты против штаммов вирусов гриппа не входящих в состав вакцины категорически не опровергается. Так лица привитые сезонной вакциной в эпидемическом сезоне 2009/2010 г.г. имели легкое течение гриппа, вызванного пандемическим штаммом, не вошедшим в состав вакцины и среди умерших не было людей, привитых от гриппа.
Информацию о системе Глобального Надзора за гриппом можно найти на официальном сайте ВОЗ или сайте Европейского Региона ВОЗ.