в чем разница вакцин вектора и гамалеи
«ЭпиВакКорона». Чем вакцина от COVID-19 Центра «Вектор» лучше остальных
МОСКВА, 3 июл — РИА Новости. Вакцина «ЭпиВакКорона» против коронавирусной инфекции разработана в новосибирском наукограде Кольцово, в гражданском обороте — с декабря прошлого года. Препарат не содержит вируса, его частей и генетического аппарата, практически не дает побочных эффектов. Это очень безопасная вакцина. По состоянию на июнь произведено более трех миллионов доз.
Состав вакцины «ЭпиВакКорона»
«ЭпиВакКорона» содержит пептидные антигены — короткие куски белков коронавируса SARS-CoV-2, которые способствуют выработке антител в организме. Три пептида имитируют эпитопы шиповидного белка коронавируса (S-белка), то есть участки, сильнее всего активирующие иммунный ответ.
Эти пептиды синтезированы искусственно и объединены в единую молекулу с белком-носителем, который наработан биотехнологическим способом. Белок-носитель представляет собой оболочечный белок SARS-CoV-2 (N-белок).
Для усиления иммунного ответа в композицию добавлен адъювант — гидроксид алюминия. Есть также несколько вспомогательных веществ.
Принцип действия и отличия от других вакцин
Разработка Государственного научного центра вирусологии и биотехнологии «Вектор» Роспотребнадзора относится к классу пептидных вакцин. По сути, это коктейль из коротких белковых последовательностей — пептидов.
В отличие от «Спутника V» и «КовиВак», в препарате нет вируса, ДНК, РНК. Все пептиды синтетические. Они имитируют маленькие участки белков реального коронавируса, вызывающие выработку защитных антител.
Из-за того, что организму предъявляют не весь вирус, иммунный ответ на «ЭпиВакКорону» слабее. В крови вырабатываются только специфические вируснейтрализующие антитела.
В «Векторе» поясняют, что их разработка эффективна против различных штаммов коронавируса, поскольку содержит консервативные, то есть редко изменяющиеся, эпитопы.
Пептидная вакцина «ЭпиВакКорона» продуцирует антитела против коронавируса. Для этого в ее молекуле содержатся В- и Т-эпитопы S-белка SARS-CoV-2, направленные на активацию разных иммунных клеток. Пептиды вместе с белком-носителем попадают в В-лимфоцит в виде эндосомы, там они расщепляются на части и вместе с белками главного комплекса гистосовместимости II класса выставляются на поверхности для распознания.
Инструкция по применению
Подготовка к вакцинации
В инструкции по применению к «ЭпиВакКороне» не оговаривается необходимость как-то специально готовиться к вакцинации. Ранее один из разработчиков, заведующий отделом зоонозных инфекций и гриппа «Вектора» Александр Рыжиков рекомендовал делать прививку в относительно здоровом состоянии, чтобы «дать организму возможность сосредоточиться на антигенах вакцины».
В Минздраве заявили, что тест на наличие антител к SARS-CoV-2 перед вакцинацией не обязателен, также как и ПЦР-теста на наличие РНК коронавируса.
Как делается прививка «ЭпиВакКороной»
Перед прививкой пациента осматривает врач, чтобы исключить заболевания в острой стадии, измеряет температуру.
Ампулу с препаратом выдерживают несколько минут при комнатной температуре, поскольку она хранится замороженной. Встряхивают, набирают в одноразовый шприц дозу 0,5 миллилитра. Укол делают в дельтовидную мышцу плеча либо латеральную широкую мышцу бедра. После введения необходимо в течение получаса находится под наблюдением медицинских работников.
С недавних пор «ЭпиВакКорона» доступна в шприц-дозах, что значительно облегчает процесс иммунизации.
Уже после первой дозы пациент получает бумажный сертификат, где указаны тип введенной вакцины и дата второй прививки. Информация о процедуре появляется в личном кабинете на сайте «Госуслуги».
Упаковка шприц-доз вакцины «ЭпиВакКорона» для профилактики COVID-19, произведенной на предприятии «Вектор-БиАльгам» в Новосибирске.
Что нельзя делать после прививки
В последующие дни после вакцинации необходимо избегать переохлаждения, перегрева.
Минздрав при проведении вакцинации против COVID-19 не рекомендует мочить место укола в течение трех дней, посещать баню, сауну, принимать алкоголь, испытывать тяжелые физические нагрузки.
Интервал между прививками
Вакцинация проходит в два этапа, интервал между первой и второй прививками составляет не менее 14-21 дня. «ЭпиВакКорона» — однокомпонентная вакцина, то есть состав и объем обеих доз одинаков.
Когда появятся антитела к коронавирусу
Согласно результатам I-II фазы клинических исследований, опубликованным в журнале «Инфекция и иммунитет», наибольшая концентрация антител к пептидным антигенам вакцины «ЭпиВакКорона» наблюдалась на 42 день после введения первой дозы.
Иммунологическая эффективность вакцины близка к ста процентам. По сообщению Александра Рыжикова, антительный ответ формируется у 90 процентов людей. В силу особенностей организма антитела могут образоваться не у всех.
Из-за особенностей действия вакцины антительный ответ не выявляется большинством коммерческих тест-систем, они не достаточно чувствительны. «Вектор» разработал собственную ИФА тест-систему «SARS-CoV-2-IgG-Вектор»для определения иммунного ответа у привитых «ЭпиВакКороной».
Побочные эффекты от вакцины «ЭпиВакКорона»
Во время I-II фазы клинических испытаний «ЭпиВакКороны» волонтеры отмечали небольшую боль в месте укола, которая держалась максимум день-два. Никаких аллергических реакций на вакцину не зафиксировано.
Также не было связанных с вакциной гриппоподобных симптомов, включающих головную боль, миалгию, лихорадку, астению. Разработчики оценивают препарат как «низко реактогенный, безопасный и хорошо переносимый». В то же время в описании к «ЭпиВакКороне» говорится, что возможно кратковременное повышение температуры тела не более 38,5 градуса.
Продолжительность действия
Ученые смогли предварительно оценить продолжительность иммунитета у приматов, которым ввели «ЭпиВакКорону» весной прошлого года. У животных до сих пор обнаруживаются антитела. В тоже время для усиления защитного эффекта им потребовалось ввести третью дозу вакцины.
Ученые продолжают наблюдать за привитыми добровольцами. Согласно текущим данным, антитела присутствуют в крови и спустя девять месяцев. Ожидается, что они сохраняют защитные функции год. Точная длительность иммунитета, которую дает «ЭпиВакКорона», будет известна после завершения III фазы клинических исследований на трех тысячах добровольцах.
Противопоказания для вакцинации
В целом для всех вакцин существуют общие противопоказания — острые инфекции, обострение хронических болезней, жизнеугрожающие и неотложные состояния. Прививку проводят через месяц после выздоровления, а в случае нетяжелых ОРВИ, острых инфекционных заболеваний ЖКТ — после снижения температуры.
Согласно рекомендациям оперштаба Москвы, вакцинацию не проводят перенесшим COVID-19 менее полугода назад.
Наличие антител к SARS-CoV-2 не входит в число противопоказаний.
В инструкции к «ЭпиВакКороне» перечислены особые противопоказания, такие как гиперчувствительность к гидроксиду алюминия и другим компонентам препарата, тяжелые аллергии, реакции на предыдущие введения вакцины, первичный иммунодефицит, злокачественные заболевания крови и новообразования.
Есть также ряд состояний, при которых прививку делают с осторожностью, включая хронические заболевания печени и почек, сахарный диабет II типа, тяжелые заболеваниях системы кроветворения, эпилепсии, инсульты.
В настоящее время «ЭпиВакКорону» не делают беременным, кормящим материям и детям до 18 лет, поскольку клинические испытания вакцины на этой категории граждан еще не проведены.
Ревакцинация
По словам генерального директора «Вектора» Рината Максютова, вакцина «ЭпиВакКорона» подходит для ревакцинации. Сейчас ученые работают над трехкратной системой вакцинации. Еще одну дозу можно будет вводить через шесть, девять или двенадцать месяцев после второй.
Отзывы врачей и привитых «ЭпиВакКороной»
Разработчики испытали «ЭпиВакКорону» на себе в числе первых. Так, по словам Александра Рыжикова, после нескольких вакцинаций у него сохраняется хороший титр антител.
Среди привитых «ЭпиВакКороной» еще осенью прошлого года — глава Роспотребнадзора, главный санитарный врач России Анна Попова и вице-премьер Татьяна Голикова. Они отмечали хорошее самочувствие после вакцинации.
«В условиях эпидпроцесса, который сейчас идет, эта вакцина показана для предупреждения коронавируса для категории лиц, которые имеют хронические заболевания, для старшего поколения, потому что на нее реакция минимальна», — такое мнение высказал врач-инфекционист Евгений Тимаков.
Где можно привиться «ЭпиВакКороной»
Вакцинация «ЭпиВакКороной», как и двумя другими российскими вакцинами от коронавируса, бесплатна. Препарат поставляют в медицинские учреждения всех регионов России и прививочные пункты. Уточнить его наличие можно по телефону горячей линии регионального органа здравоохранения.
«Спутник V», «ЭпиВакКорона» и «КовиВак»: чем отличаются препараты, в чем их плюсы и минусы
На сегодняшний день жителям Петербурга доступны три вакцины от коронавируса: «Спутник V», «ЭпиВакКорона» и «КовиВак». Рассказываем, что известно о препаратах, сравниваем их плюсы и минусы.
В Санкт-Петербурге набирает обороты массовая вакцинация от коронавируса, которую подстегивает рост заболеваемости, опасные штаммы и новые рекорды по смертям от COVID за сутки. Задают темп и власти Северной столицы, которые периодически намекают о введении COVID-free зон и других неприятных ограничений для непривитых.
Сейчас петербуржцам доступны три вакцины на выбор: «Спутник V», «ЭпиВакКорона» и «КовиВак». Рассказываем, что известно о препаратах, сравниваем их плюсы и минусы.
Плюсы и минусы вакцины «Спутник V» от НИИ Гамалеи
«Спутник V» от НИИ Гамалеи — это первая зарегистрированная в России вакцина от коронавируса. На данный момент, это самый распространенный в стране препарат. «Спутник V» — это векторная вакцина. Это означает, что препарат состоит из неспособных к размножению аденовирусов-векторов. Попадая в организм человека, они добавляют в него встроенный ген коронавирусного S-белка.
Основной плюс препарата — это практически отсутствие строгих противопоказаний к его применению, так как он не содержит живого вируса. Они есть, но все же их немного. А также, как рассказал «Царьграду» профессор Анатолий Давидович Альтштейн, вирусолог, сотрудник НИЦ эпидемиологии и микробиологии имени Гамалеи, то, что препарат уже успел доказать свою эффективность.
Эта вакцина на аденовирусном векторе, она прошла все три стадии клинических испытаний. Во время третьей фазы клинических испытаний она показала защитный эффект на 90%. Вакцину применили уже на порядка 15 млн человек, насколько я помню, было изготовлено больше 20 млн доз. Точно судить как она действует в процессе эпидемии пока что сложно, таких данных не было, но скорее всего она вполне эффективна. Сейчас в мире существуют четыре вакцины на аденовирусном векторе: в России, в Китае, США — вакцина Johnson & Johnson, а также в Великобритании. В общем, наша вакцина наиболее эффективная в отношении профилактики коронавирусной инфекции, — заявил Альтштейн.
Касательно минусов, профессор отметил, что вакцин без минусов не бывает. А главный минус каждого препарата — его побочные эффекты.
Вакцин без минусов не бывает. Обычно минус — это побочные эффекты вакцинации, и здесь они довольно выражены. Может подняться температура до 38 градусов, один-два дня человек может чувствовать себя плохо. Но это происходит далеко не с каждым. Большинство людей переносят вакцинацию легко, — рассказал вирусолог.
Противопоказания к «Спутнику V»
Как упоминалось выше, строгих противопоказаний к вакцине немного. А точнее, всего шесть: гиперчувствительность к компонентам препарата или тяжелая форма аллергии. Кроме того, необходимо повременить с прививкой в случае острых заболеваний или обострения хронических, а также при грудном вскармливании и беременности. Еще один момент: вакцину от COVID не прививают детям, но это актуально для всех препаратов.
Что касается противопоказаний, то в общем, человек, который подвергается вакцинации, должен быть здоров. У него не должно быть температуры, наличие различных хронических инфекций, как правило, при вакцинации допускается, но если это какие-то аутоиммунные болезни, то ему, конечно, нужно консультироваться со своим специалистом-аллергологом, — добавил вирусолог.
Плюсы и минусы вакцины «ЭпиВакКорона» от центра «Вектор»
«ЭпиВакКорона» от центра «Вектор» — это вторая зарегистрированная в России вакцина от коронавируса. «Спутник» — векторная вакцина, а «ЭпиВакКорона» — пептидная. На практике это означает, что первая содержит безопасный для человека вирус, а вторая — целиком синтетическая. «ЭпиВакКорону» вводят вакцинируемому внутримышечно в два этапа с интервалом в две-три недели.
Как сообщается на сайте Роспотребнадзора, ожидаемыми преимуществами «ЭпиВакКороны» являются ее эффективность против разных штаммов, поскольку препарат содержит консервативные эпитопы SARS-CoV-2, а также то, что в отличии от большинства субъединичных препаратов, она содержит только короткие участки вирусного белка. На практике это означает то, что ее могут использовать люди с ослабленным иммунитетом, а также во время иммунодепрессивных и иммуносупрессивных состояниях. Кроме того, плюс вакцины в ее температуре хранения от 2 до 8 градусов, что упрощает логистику препарата.
Касательно минусов, эксперты заявили о не долгосрочности работы антител после прививки «ЭпиВакКороной»:
По состоянию на три и шесть месяцев мы фиксируем наличие антител у всех вакцинированных добровольцев. По состоянию на девять месяцев больше чем у половины добровольцев также наблюдаем детектируемый уровень антител к вирусу, — заявил Ринат Максютов в интервью каналу «Россия 24».
Противопоказания к «ЭпиВакКороне»
Противопоказания к применению «ЭпиВакКороны» примерно такие же, как и для других препаратов. Перед вакцинацией этой вакциной стоит пройти обследование врача или повременить с прививкой людям, которые имеют гиперчувствительность к компонентам препарата, тяжелые формы аллергии, поствакцинальное осложнение после других препаратов, острые заболевания или обострение хронических, первичный иммунодефицит, злокачественные заболевания крови, а также беременные и кормящие женщины. Как и в случае с другими препаратами, прививку не делают несовершеннолетним.
Плюсы и минусы вакцины «КовиВак» центра им. Чумакова
«КовиВак» от центра им. Чумакова зарегистрировали в конце февраля. Это третья отечественная вакцина от коронавируса, а от предыдущих ее отличает то, что она создана по схеме, которую можно назвать классической. В основе препарата находится инактивированный, другими словами — «убитый», цельный вирус SARS-CoV-2. Для сравнения: в «Спутнике» используются два типа аденовируса человека со встроенными фрагмента гена SARS-CoV-2, а в «ЭпиВакКороне» — пептидная платформа, состоящая из искусственно синтезированных фрагментов гена вируса.
Как и в случае с другими вакцинами, «КовиВак» — двухфазный препарат. Интервал между введением доз составляет две недели.
Стоит отметить, что в Санкт-Петербурге эта вакцина оказалась весьма популярна, настолько, что достаточно быстро закончилась и сейчас запись на вакцинацию этим препаратом приостановлена.
К плюсам «КовиВака» можно отнести его проверенную классическую схему создания. Кроме того, как и «ЭпиВакКорона», этот препарат хранится при температуре от 2 до 8 градусов, что значительно упрощает его логистику. Для сравнения, «Спутник» требует при транспортировке очень низких отрицательных температур около 27-28 градусов.
С вопросом об эффективности «КовиВака» «Царьград» обратился к профессору Анатолию Альтштейну, вирусологу, сотруднику НИЦ эпидемиологии и микробиологии имени Гамалеи. Как отметил эксперт, этот препарат был сделан по классической проверенной временем схеме.
Так была сделана вакцина от клещевого энцефалита, хороший препарат, против гриппа делают такие же вакцины. Принцип, по которому делается «КовиВак», он правильный. Что конкретно получится с этой вакциной, пока не ясно. Потому что принципы — это хорошо. Если вакцина делается против принципов, то там могут быть серьезные трудности. Но как она реально будет работать, мы пока не знаем, потому что третьей фазы клинических испытаний не проводилось. А в принципе, это может быть и неплохая вакцина, она может быть даже менее реактогенна (реактогенность – свойство вакцины вызывать при введении в организм побочные эффекты, например, повышение температуры тела – Ред.), чем «Спутник», но будет ли она так же эффективна, сказать трудно, потому что мы сейчас имеем пример китайских и индийских вакцин такого же рода и боюсь, что они не блещут, — рассказал Альтштейн.
Еще один минус «КовиВака» — его малая масштабируемость. В России, по словам экспертов, очень мало производственных площадок, которые в состоянии работать с необходимыми для создания этого препарата технологическими процессами. А они требуют особой биологической безопасности, так как вакцина содержит настоящий цельный вирус.
Противопоказания к «КовиВак
Как отметил Альтштейн, «Спутник» скорее всего более реактогенный, чем «КовиВак», потому противопоказаний у второй вакцины должно быть меньше. Но в целом, они примерно одинаковые.
Препарат противопоказан при тяжелых аллергических реакциях, при беременности и грудном вскармливании. Повременить с прививкой стоит в случае острых заболеваний и обострениях хронических. В этих случаях необходима консультация лечащего врача. В инструкции к «КовиВаку» указано, что препарат не противопоказан людям с иммуносупрессивным или иммунодефицитным состоянием.
Выводы
Заболеваемость и число летальных случаев в Северной столице растет, а власти и эксперты все чаще говорят о необходимости ускорения темпов вакцинации для скорейшего достижения коллективного иммунитета. Сейчас у петербуржцев есть выбор из трех вакцин, а тем временем вакцинация из добровольной становится добровольно-принудительной. Впрочем, как отмечают эксперты, это вынужденная мера.
Проблема выбора пептидов для «ЭпиВакКороны» и разбор статьи разработчиков вакцины о клинических испытаниях первой и второй фаз
Вакцина «ЭпиВакКорона» уже поступила в гражданский оборот и предлагается населению в поликлиниках. Она позиционируется как более «мягкая», чем «Спутник V» и при этом эффективная. Разберемся, есть ли предпосылки для эффективности у этой вакцины, и что не так с публикацией о ней.
рисунок автора статьи
Автор
Редакторы
В журнале «Инфекция и иммунитет» появилась публикация разработчиков вакцины «ЭпиВакКорона» — ГНЦ «Вектор», — о чем было краткое сообщение в конце моей статьи «ЭпиВакКорона в иллюстрациях», опубликованной в «Троицком варианте». Статью о первых фазах клинических испытаний вакцины «Вектора» в научном мире очень ждали. При полной непрозрачности разработки любая информация, проливающая на неё свет, крайне желательна. Разберем, как устроена вакцина «ЭпиВакКорона», и что стало известно из публикации о ней.
Стоит заметить, что редакция журнала «Инфекция и иммунитет», в которой опубликована работа [1], входит в структуру Роспотребнадзора — ведомства, частью которого является и сам разработчик «ЭпиВакКороны» — ГНЦ «Вектор». Увы, но при таком раскладе независимость оценок данной публикации рецензентами в этом журнале не гарантирована.
В начале февраля ТАСС опубликовал следующее заявление:
Государственный научный центр вирусологии и биотехнологии “Вектор” Роспотребнадзора направил результаты клинических исследований вакцины фазы I–II в зарубежные научные рецензируемые журналы. Их публикация ожидается в ближайшее время. В Роспотребнадзоре подчеркнули, что до выхода международных публикаций обнародование результатов в русскоязычных научных изданиях не представляется “целесообразным” из-за “эксклюзивности и значимости для широкого круга потенциально заинтересованных лиц”.
Наблюдается противоречие между намерением разработчиков вакцины печататься в зарубежных изданиях в начале февраля и реальностью, в которой статья выходит в российском издании, аффилированном с Роспотребнадзором, во второй половине марта. Можно предположить, что рецензенты зарубежных изданий не пропустили статью в печать.
Увы, публикация о вакцине «Вектора» начинает разочаровывать с самого начала. В статье много недоработок и странностей. В предисловии состав оригинальной и необычной вакцины «ЭпиВакКорона», у которой в мире нет аналогов, описан всего одним предложением. Более того, в тексте статьи не приведены аминокислотные последовательности пептидов (фрагментов шиповидного белка), которые входят в состав вакцины и, по замыслу разработчиков, должны стимулировать выработку нейтрализующих вирус антител. Читателям приходится последовательности пептидов искать в других публикациях [2] и в патентах (№№ 2738081, 2743594 и 2743595).
Как устроена вакцина
Прежде чем дальше разбирать публикацию «Вектора» в журнале «Инфекция и иммунитет», хочется рассказать, как устроена вакцина «ЭпиВакКорона». Эта вакцина (согласно публикации [2]) состоит из трёх искусственно синтезированных коротких фрагментов вирусного шиповидного белка — пептидов, которые, по мнению разработчиков «ЭпиВакКороны», должна распознавать иммунная система человека.
Чтобы продолжить рассказ, мне нужно объяснить, что такое антигенный эпитоп. Он представляет собой часть макромолекулы антигена (в нашем случае вируса), которая распознается иммунной системой. Бывает два типа антигенных эпитопов: конформационные и линейные. Первые составлены из участков молекулы, которые не обязательно соседствуют в первичной структуре белка, но соседствуют в пространстве в его третичной или четвертичной структурах. Линейные же эпитопы представлены цепочками аминокислот, которые соседствуют в первичной структуре белка и соответствуют пептидам, то есть фрагментам аминокислотной последовательности белка. Антитела в организме при борьбе с инфекцией могут образовываться и на конформационные, и на линейные эпитопы. Эпитопы, которые узнаются антителами [3], а не Т-лимфоцитами, называются B-клеточными эпитопами. Принципы устройства иммунной системы можно восстановить в памяти, прочтя статью «Иммунитет: борьба с чужими и. своими» [4].
По замыслу разработчиков «ЭпиВакКороны», пептиды, входящие в состав этой вакцины, должны содержать участки шиповидного белка, в которых есть В-клеточные эпитопы, доступные в природном вирусе антителам вакцинированных.
Все пептиды вакцины конъюгированы (соединены) с белком-носителем. В качестве белка-носителя использован продукт так называемого химерного гена. Его аминокислотная последовательность приведена в патентах №№ 2738081, 2743594 и 2743595 и ниже в секции «Химерный белок». Этот ген методами генетической инженерии был составлен из двух генов, происходящих из разных организмов: гена, кодирующего нуклеокапсидный вирусный белок, и гена, кодирующего бактериальный белок, способный связывать сахар мальтозу (maltose binding protein, MBP). Соединенные гены этих двух организмов были экспрессированы в кишечной палочке. Продуктом экспрессии стал химерный белок, который для производства вакцинного препарата сначала проходит несколько стадий очистки, а затем конъюгируется с пептидами.
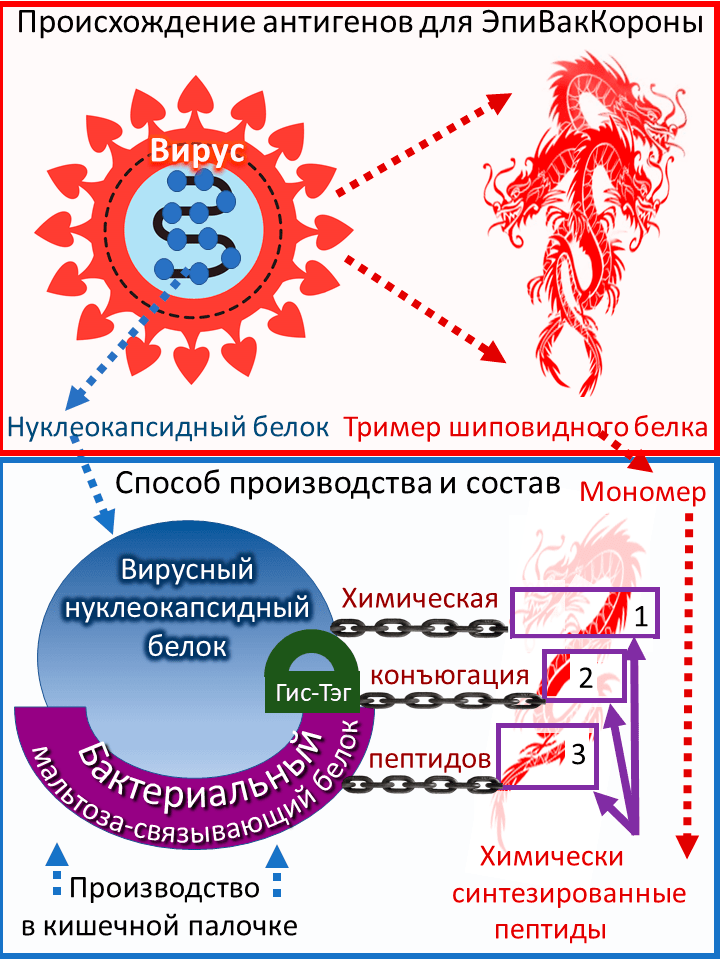
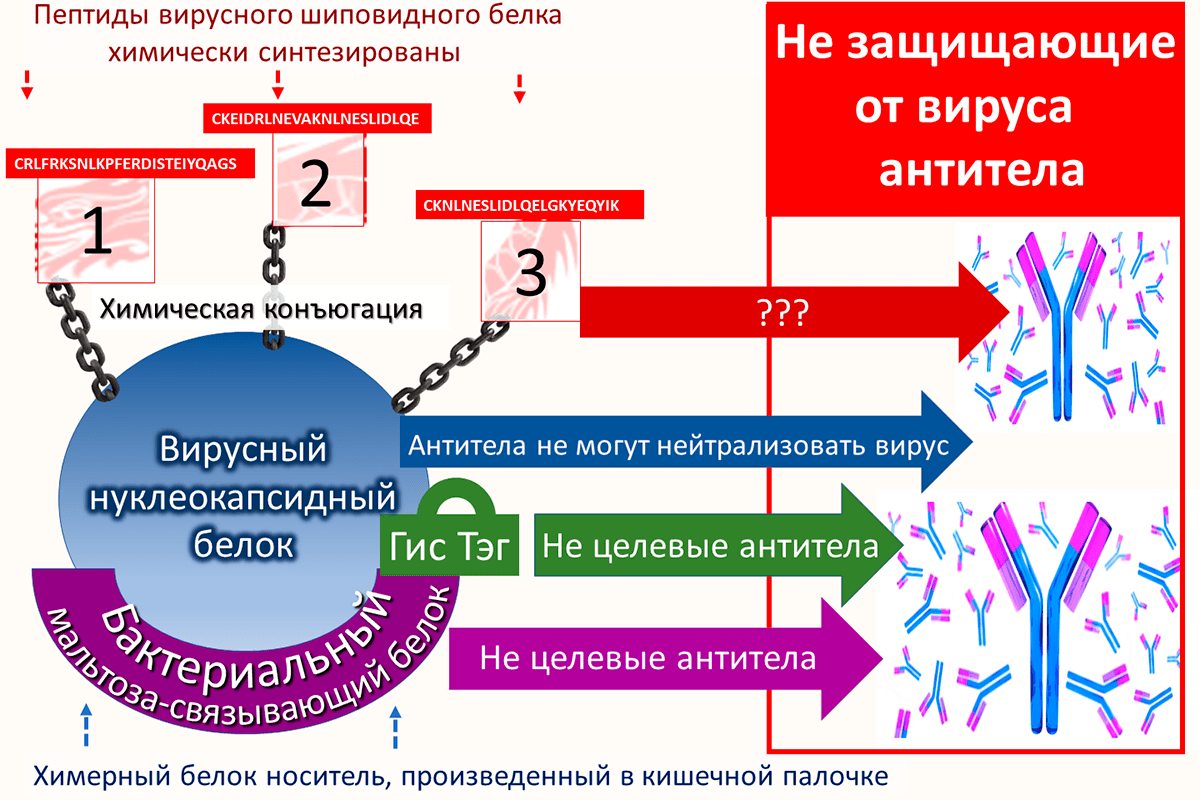
Генетический конструкт для производства белка-носителя вакцины «ЭпиВакКорона» кроме химерного гена включает и короткий генетический фрагмент, кодирующий полигистидиновый пептид (шесть остатков гистидина) и сокращенно называемый гис-тэг; он используется для очистки химерного белка из лизата кишечной палочки. Для этой же цели используется и участок бактериального белка MBP. После очистки к каждой молекуле химерного белка присоединяется в процессе конъюгации только один вариант пептида. В результате получается три типа конъюгированных молекул: химерный белок с присоединенным пептидом номер 1, тот же белок с пептидом номер 2 и, наконец, тот же белок с пептидом номер 3. Все три типа конъюгированных молекул входят в состав вакцины. Рисунок 1 показывает происхождение антигенов вакцины и способ ее производства. Напомню, что антигенами называются чужеродные молекулы в организме.
Рисунок 1. Состав «ЭпиВакКороны», происхождение антигенов и способ ее производства. В образе трехглавого дракона (сверху) представлен тример шиповидного белка коронавируса. Снизу показано химическое соединение пептидов, которые изображены фрагментами дракона, с химерным белком. Последний изображен синим кругом (это вирусный нуклеокапсидный белок) с лиловой дугой снизу (бактериальный белок MBP).
рисунок автора статьи
Химерный белок
В последовательности химерного белка, приведенной ниже, можно выделить часть, соответствующую бактериальному белку MBP (лиловым фоном), гис-тэг (темно-зеленым фоном) и часть, соответствующую вирусному нуклеокапсидному белку (синим фоном) (по патенту №2738081):
MKIEEGKLVIWINGDKGYNGLAEVGKKFEKDTGIKVTVEHPDKLEEKFPQVAATGDGPDIIFWAHDRFGGYAQSGLLAEITPDKAFQDKLYPFTWDAVRYNGKLIAYPIAVEALSLIYNKDLLPNPPKTWEEIPALDKELKAKGKSALMFNLQEPYFTWPLIAADGGYAFKYENGKYDIKDVGVDNAGAKAGLTFLVDLIKNKHMNADTDYSIAEAAFNKGETAMTINGPWAWSNIDTSKVNYGVTVLPTFKGQPSKPFVGVLSAGINAASPNKELAKEFLENYLLTDEGLEAVNKDKPLGAVALKSYEEELAKDPRIAATMENAQKGEIMPNIPQMSAFWYAVRTAVINAASGRQTVDEALKDAQTNSSSNNNNNNNNNNLGIEGRGGSG HHHHHH SGSDNGPQNQRNAPRITFGGPSDSTGSNQNGERSGARSKQRRPQGLPNNTASWFTALTQHGKEDLKFPRGQGVPINTNSSPDDQIGYYRRATRRIRGGDGKMKDLSPRWYFYYLGTGPEAGLPYGANKDGIIWVATEGALNTPKDHIGTRNPANNAAIVLQLPQGTTLPKGFYAEGSRGGSQASSRSSSRSRNSSRNSTPGSSRGTSPARMAGNGGDAALALLLLDRLNQLESKMSGKGQQQQGQTVTKKSAA
Такая сложная конструкция химерного белка объясняется необходимостью его тщательной очистки из лизата кишечной палочки, в которой он производится для вакцинации. Одним из наиболее известных и эффективных способов добиться хорошего синтеза и очистки вирусного или другого нужного исследователям белка в микробах заключается в соединении вирусного белка с мальтозосвязывающим белком (MBP). Это соединение позволяет проводить одностадийную очистку химерного продукта с использованием амилозной смолы.
Пептиды вакцины «ЭпиВакКорона»
Пептиды вакцины «ЭпиВакКорона-H»
Проблема выбора пептидов для вакцины
Я уже кратко писала о проблеме выбора пептидов для такой вакцины в более ранней публикации в газете «ТрВ». Здесь я напишу подробнее, почему пептиды, выбранные «Вектором» для вакцины, не оптимальны.
Как я писала выше, пептиды вакцины «ЭпиВакКорона», по замыслу разработчиков, должны имитировать линейные B-клеточные эпитопы шиповидного белка коронавируса, а соответствующие фрагменты вирусного белка должны быть доступны для взаимодействия с антителами в организме человека. Если фрагменты белка плохо доступны, то антитела, выработанные на эти участки белка, не смогут связаться с вирусом и не смогут способствовать его элиминации. Шиповидный белок коронавируса имеет сложные третичную и четвертичную молекулярные структуры [7]. И в этих структурах много мест, абсолютно не доступных антителам.
Экспериментальным поиском линейных B-клеточных эпитопов шиповидного белка, хорошо доступных для взаимодействия с антителами, занимались сразу несколько лабораторий [8–13]. Идея такого поиска в том, чтобы изучить антитела переболевших COVID-19 людей и найти те, которые способны связываться с пептидами, соответствующими последовательности шиповидного белка. Если такие пептиды найдутся, то, иммунизируя человека этими пептидами в составе вакцины, можно надеяться на получение антител, которые будут связываться с B-клеточными эпитопами шиповидного белка и выполнять протективную функцию.
Исследователи из разных стран независимо друг от друга провели скрининговое картирование почти всех пептидных фрагментов шиповидного белка и выявили пептиды, с которыми связываются антитела хотя бы 20% переболевших COVID-19 людей. Таким образом идентифицировали пептиды, которые соответствуют фрагментам белка, где располагаются B-клеточные эпитопы.
Эксперименты были построены так: на подложку последовательно, по принципу черепичной укладки, иммобилизовали пептиды шиповидного белка. Каждый последующий пептид перекрывался с предыдущим на половину своей длины или больше. Поэтому на подложке были представлены почти все линейные В-клеточные эпитопы шиповидного белка. Таких подложек готовилось много. Потом на каждую подложку наливалась плазма крови выздоровевших после COVID-19 людей. Далее методом иммуноферментного анализа (ИФА) [14] происходила идентификация пептидов, с которыми связались антитела.
После первичного картирования и выявления линейных фрагментов шиповидного белка, которые узнаются антителами, последовала вторая фаза исследования. В этой фазе экспериментально установили, какие пептиды способны помешать реакции нейтрализации вируса сывороткой переболевших. Фазу идентификации этих пептидов можно провести разными способами, например реакцией конкурентного вытеснения. Исследователи обогащают плазму переболевшего COVID-19 человека определенным антителом, которое способно связываться с изучаемым пептидом, а потом исследуют, может ли этот пептид помешать реакции нейтрализации живого вируса [9], [10], [13]. Если да, то это означает, что у данного пептида в составе пептидной вакцины больше шансов спровоцировать образование нейтрализующих антител. Хотя гарантий иммуногенности именно такого пептида в составе вакцины всё равно нет.
При систематическом скрининге пептидов шиповидного белка коронавируса (результаты приведены на рис. 2) обнаружили пептиды, с которыми связываются антитела переболевших COVID-19. Выявленные участки отличались у разных людей, но были найдены универсальные закономерности. Некоторые пептиды соответствовали «слепым» или «полуслепым» зонам иммунитета (на соответствующие участки шиповидного белка крайне редко образуются антитела). Некоторые пептиды, наоборот, соответствовали «острому зрению» иммунитета (к этим участкам образовывались антитела у многих людей, перенесших COVID-19). Хорошо видимые иммунной системой фрагменты белка соответствуют так называемым иммунодоминантным эпитопам. Именно эти участки вирусного белка хорошо доступны для связывания антител в организме инфицированного человека.
рисунок автора статьи
Экспериментально также определили фрагменты шиповидного белка, связывание которых с антителами приводит к нейтрализации вируса [9], [10], [13]. Однако ни один из выявленных в этих работах фрагментов вирусного шиповидного белка не совпал с пептидами, вошедшими в состав «ЭпиВакКороны».
Увы, выбранные «Вектором» для синтеза вакцинных пептидов участки молекулы шиповидного белка, которые должны имитировать линейные B-клеточные эпитопы, на самом деле находятся почти в «слепой зоне» иммунной системы человека. Следует заметить, что на рисунке 2 выделены только участки белка, на которые образуются антитела хотя бы у 20% переболевших COVID-19 людей. Можно назвать эти участки иммунодоминантными.
При этом разработчики сами говорят, что старались избегать таких районов: «Всем известно, что иммунодоминантные районы вызывают на себя иммунный ответ, подвергаются прессингу при развитии, в том числе, и живого вируса, не только вакцины. Под иммунным прессингом происходит мутация, образуются эскейп-мутанты, и мы сейчас имеем мутации по всем иммунодоминатным районам. Таким образом, наш консервативный пептид, который входит в состав вакцины сейчас, — он именно от таких мутаций ускользнул».
Тем не менее в вышеприведенных высказываниях разработчиков есть правильная логика; конечно, участки белка, соответствующие пептидам вакцины, должны быть консервативны в эволюции. Иначе пептидная вакцина станет хуже работать для мутантных вариантов вируса. Однако эти участки белка должны быть все же видны иммунной системе большинства людей и должны располагаться в доступном для антител месте. Существующие экспериментальные данные говорят нам о том, что этого не наблюдается; дополнительные доказательства приведены в таблице 1.
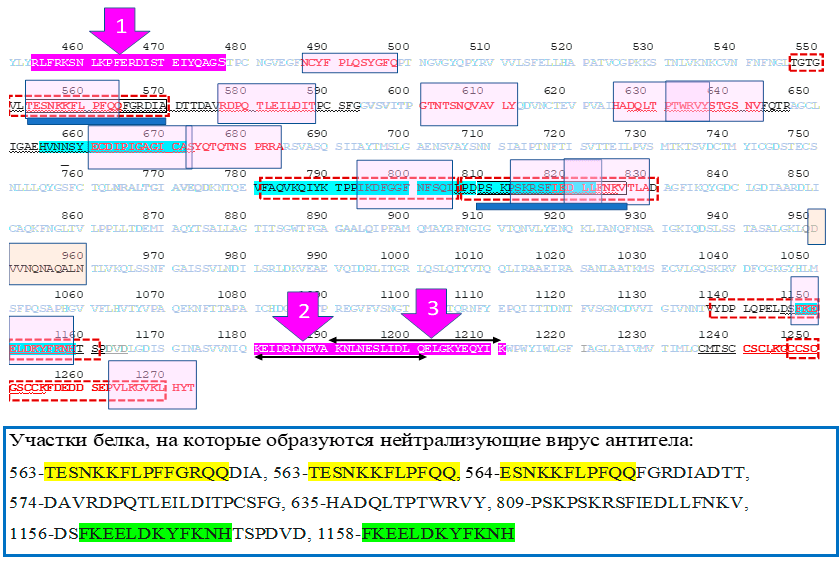
На основании опубликованной работы [8] и сообщения автора публикации [10] профессора Чжиган И (Zhigang Yi) из Университета Фудань (Китай) была создана таблица 1. Она показывает, что антитела на фрагменты шиповидного белка почти c такой же локализацией, как и пептиды «ЭпиВакКороны», формируются не более чем у 9% людей. Видимо, последовательные цепочки аминокислот в соответствующих местах белка недоступны для взаимодействия с антителами, поскольку частично или полностью спрятаны в третичной или четвертичной структуре белковой молекулы.
| Ссылка | Начало | Пептид | Конец | Процент переболевших с антителами к пептиду | Средний сигнал в контрольной группе | Средний сигнал в группе переболевших |
|---|---|---|---|---|---|---|
| Участок рецептор-связывающего мотива в шиповидном белке 454 RLFRKSNLKPFERDISTEIYQAGS 477 | ||||||
| [8] | 451 | YLY RLFRKSNLK | 462 | 5,7% | 42 | 157 |
| 457 | RKSNLKPFERDI | 468 | 1,2% | 56 | 49 | |
| 463 | PFERDISTEIYQ | 474 | 2,2% | 20 | 174 | |
| 469 | STEIYQAGS TPC | 480 | 0,0% | 14 | 22 | |
| [10], личное сообщение | 454 | RLFRKSNLKPFERDISTEIY | 473 | 9% | Значения не определялись | |
| 464 | FERDISTEIYQAGST PCNGV | 483 | 5% | |||
| Участок гепта-повтора 2 1181 KEIDRLNEVAKNLNESLIDLQE 1201 ; 1191 KNLNESLIDLQELGKYEQYIK 1211 | ||||||
| [8] | 1178 | NIQ KEIDRLNEV | 1189 | 7,2% | 8 | 148 |
| 1184 | DRLNEVAKNLNE | 1195 | 1,2% | 6 | 37 | |
| 1190 | AKNLNESLIDLQ | 1201 | 10,5% | 62 | 148 | |
| 1196 | SLIDLQELGKYE | 1207 | 0,0% | 90 | 110 | |
| 1202 | ELGKYEQYIK WP | 1213 | 9,2% | 33 | 144 | |
| [10], личное сообщение | 1176 | VVNIQ KEIDRLNEVAKNLNE | 1195 | 9% | Значения не определялись | |
| 1186 | LNEVAKNLNESLIDLQELGK | 2005 | 1% | |||
| 1196 | SLIDLQELGKYEQYIK WPWY | 1215 | 2% | |||
Пептиды в таблице или в работах, результаты которых суммированы на рисунке 2, в каждом конкретном эксперименте отличаются по длине от пептидов «ЭпиВакКороны». Однако эксперименты с иммобилизованными на подложке пептидами самой разнообразной длины — 12, 18, 20 или даже 50 аминокислот [8–13] — выявляют сходные участки в молекуле белка, которые хорошо видны иммунной системе. Хотя, следует отметить, что 50-меры хуже взаимодействуют с антителами и не выявляют некоторых антител, которые выявляют более короткие пептиды длиной от 12 до 20 аминокислот.
В то же время ни один из экспериментов разработчиков «ЭпиВакКороны» (из описанных в патентах или в публикациях) не демонстрирует того, что у переболевших COVID-19 могут образовываться антитела именно на участки белка, соответствующие пептидам, выбранным для этой вакцины. Казалось бы, такой эксперимент сравнительно легко провести. Но в открытой печати результаты таких экспериментов не описаны. Зато экспериментаторы из лабораторий в других странах в интересующих нас участках белка (соответствующих пептидам «ЭпиВакКороны») хорошо доступных для антител фрагментов не видят [8–13].
Если у людей очень редко образуются антитела, способные взаимодействовать с определенными фрагментами вирусного белка, то это означает, что при иммунизации соответствующими пептидами антитела на эти пептиды не смогут узнать и связать вирус у большинства людей. Нужны ли такие пептиды в вакцине для иммунизации?
Как разработчики «ЭпиВакКороны» искали пептиды и почему этот поиск мог привести к артефактам?
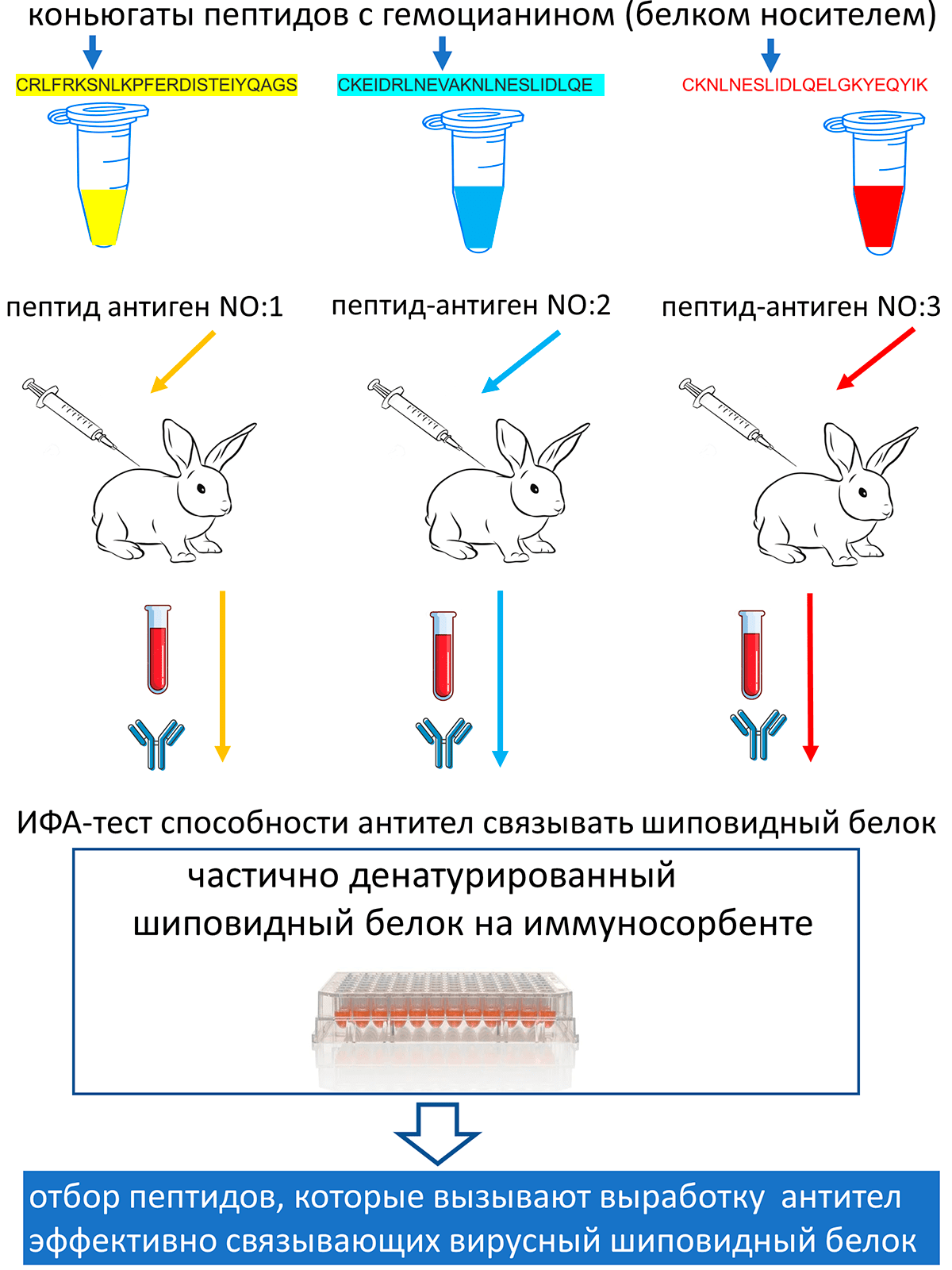
Разработчики «ЭпиВакКороны» иммуногенность пептидов оценивали, вводя разные пептиды в качестве антигенов кроликам (патент РФ на изобретение №2738081). Точнее, кроликов иммунизировали последовательно набором пептидов, соединенных с белком-носителем. Далее у животных собирали кровь и методом иммуноферментного анализа (ИФА) определяли, насколько хорошо антитела, выработанные на каждый отдельный пептид-антиген, связывали вирусный шиповидный белок, который был иммобилизован на иммуносорбенте. Этот подход схематично изображен на рисунке 3.
Самые иммуногенные пептиды, антитела на которые лучше всего связывались с шиповидным белком и давали самый сильный ИФА-сигнал, отбирали для дальнейшей вакцинной разработки. Идея такого отбора в том, что если антитела, выработанные на пептид-антиген, хорошо связывают вирусный шиповидный белок, то этот же пептид в составе вакцины будет вызывать образование антител у человека, которые будут связывать вирусный белок у вириона и, возможно, выполнять протективную противовирусную функцию.
Однако в этом подходе важно, чтобы шиповидный белок в тесте ИФА имел такую же или очень похожую структуру и конформацию, как и нативный белок в вирусе, когда тот находится в человеческом организме. Похоже, что это условие не было соблюдено в экспериментах разработчиков «ЭпиВакКороны». Согласно их протоколу, при посадке шиповидного белка на иммуносорбент для ИФА-теста белок инкубировали, используя рН буфера (9,5–9,7). При таком рН белок может частично денатурировать. Последующая промывка иммобилизованного на иммуносорбенте белка нейтральным буфером может не восстановить его нативную структуру и конформацию. В результате антитела после иммунизации кроликов пептидными антигенами могут связываться с участками денатурированного белка, которые в природе у вируса спрятаны в третичную или четвертичную структуру. Таким образом, этот скрининговый метод может приводить к артефактам и выбору таких пептидов для вакцины, антитела на которые не будут иметь протективной противовирусной функции.
Рисунок 3. Схема отбора пептидов-антигенов для «ЭпиВакКороны»
рисунок автора статьи
Еще одной проблемой такого скрининга является разница между рецепотрами В-клеток человека (B-cell receptor, BCR) и животных. Для того чтобы B-клетка смогла начать вырабатывать антитела на какой-то эпитоп антигена, ей нужно сначала этот эпитоп «узнать» своим BCR-рецептором. В процессе узнавания этот рецептор должен вступить во взаимодействие с эпитопом антигена и образовать комплекс. Так вот, даже у людей BCR различаются между собой. То есть у разных людей эти рецепторы, например, узнают несколько разные участки шиповидного белка коронавируса или пептиды, моделирующие и воспроизводящие эти участки: см. рис. 4. Тем более эти рецепторы различаются у людей и животных. Поэтому метод поиска пептидов для вакцины путем иммунизации кроликов чрезвычайно ненадежен.
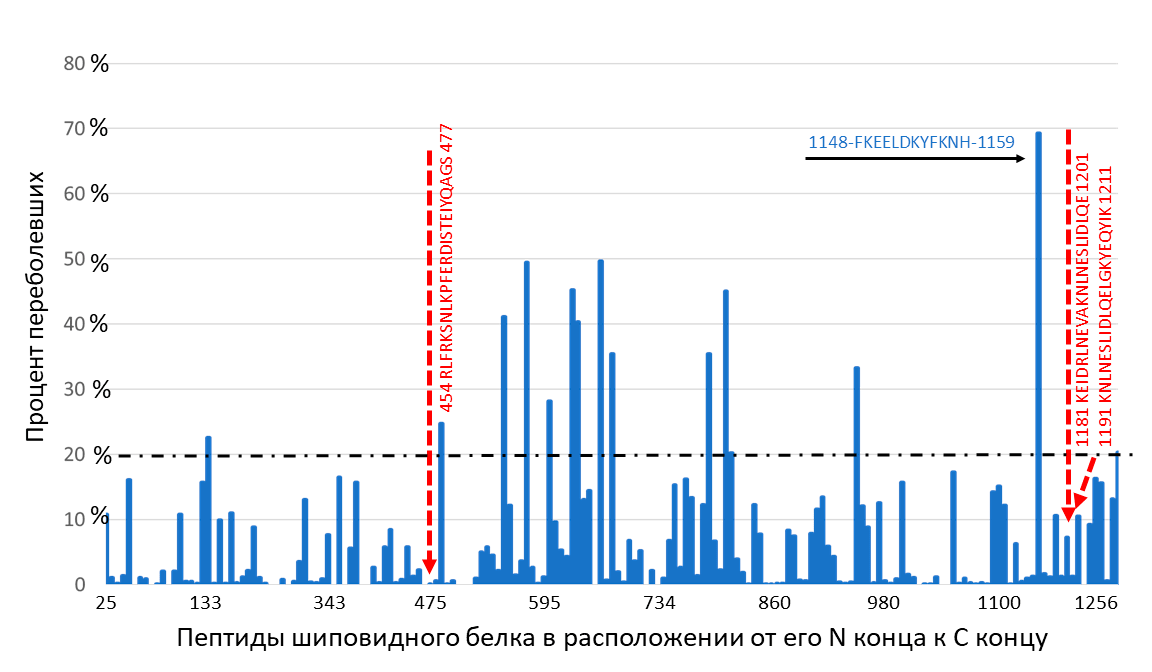
Рисунок 4. Частота образования антител, узнающих короткие пептиды шиповидного белка, у переболевших COVID-19. Показан процент реконвалесцентов (переболевших COVID-19 людей), у которых образовались антитела на каждый отдельный пептид, иммобилизованный на подложке иммуносорбента. Каждый пептид длиной 12 аминокислот на половину длины перекрывает предыдущий. В эксперименте на подложку последовательно, по принципу черепичной укладки, иммобилизованы пептиды шиповидного белка. На графике по оси абсцисс расположены пептиды в направлении от N- к C-концевому участку, по оси ординат — процент людей, у которых есть антитела на этот пептид. 20-процентный порог отмечен горизонтальным пунктиром. Черной стрелкой указан пептид, с которым, согласно публикации [8], реагируют антитела 70% людей, перенесших заболевание. Красными прерывистыми стрелками указаны пептиды, перекрывающиеся с пептидами «ЭпиВакКороны».
рисунок автора статьи
Неудивительно, что пептиды, найденные при скрининге и иммунизации кроликов, не совпадают с пептидами, которые узнаются антителами хотя бы у 20% переболевших COVID-19, согласно исследованиям независимых экспериментаторов [8–13].
Тут еще стоит добавить, что разработчики «ЭпиВакКороны» провели и другие эксперименты, которые тоже, увы, скорее всего, показывает артефактное взаимодействие антител с вирусным шиповидным белком. Антитела животных [2] и людей [1], выработанные при иммунизации пептидами на белковом носителе, проверяли на способность взаимодействовать с вирусом, иммобилизованным на иммуносорбенте [2]. Однако вирус для этого опыта был инактивирован бета-пропиолактоном с последующим нагреванием [2]. Такая инактивация также может приводить к разрушению водородных связей и, соответственно, структуры белка. Поэтому для взаимодействия с антителами могут открыться участки белка, закрытые в природном, нативном, варианте белка в составе вирусной частицы.
Таким образом, из всего вышеперечисленного можно заключить, что способ выбора пептидов на основании вышеописанных экспериментов не свободен от возможности появления серьезных артефактов. На основании факта наличия взаимодействия антител с вирусным шиповидным белком на иммуносорбенте нельзя сделать вывод о том, что антитела на пептиды в вакцине могут провзаимодействовать с коронавирусом и защитить организм от вирусной инфекции.
Формирование антител после вакцинации
Роспотребнадзор сообщает: «Многие тест-системы недостаточно чувствительны, чтобы выявить малый спектр формируемых вакциной антител. Чтобы их обнаружить, нужно использовать специальные ИФА-тесты от центра “Вектор”». Таким образом, разработчики вакцины утверждают, что антитела к шиповидному белку не выявляются у вакцинированных «ЭпиВакКороной» при использовании обычных ИФА-тестов, где на подложку наносится полноразмерный тримерный шиповидный белок, полученный в эукариотических клетках. Это утверждение говорит, что вакцина не вызывает образования антител против главного иммуногена коронавируса.
Итак, для определения уровня антител после вакцинации нужен спецтест. Этот спецтест не описан в открытых документах. Как он устроен — остается загадкой.
В то же время, согласно разработчикам «ЭпиВакКороны»: «вакцинация двумя дозами препарата вызвала у 100% добровольцев выработку антител, специфичных к антигенам, входящим в состав вакцины». Так какие это антитела и антигены?
Согласно описанию состава вакцины, антигенами «ЭпиВакКороны» могут стать не только три пептида шиповидного белка, но и химерный белок, состоящий из двух частей (вирусного нуклеокапсидного и бактериального MBP), и гис-тэг. Последний, как говорилось выше, представляет собой короткий пептид, который введен в состав вакцины для очистки химерного белка из бактериального лизата. На все эти антигены формируются нецелевые антитела, которые, скорее всего, не обладают защитной функцией. Только антитела к шиповидному, но не нуклеокапсидному вирусному белку могут связаться с вирусом, поскольку нуклеокапсидный белок находится внутри вирусной частицы и не экспонирован наружу.
Способность антител против пептидов, вошедших в состав «ЭпиВакКороны», связываться с вирусом и выполнять нейтрализующую или другую защитную противовирусную функцию, вызывает сомнения не только у автора этой статьи. Похожие сомнения высказывают и другие специалисты: «Первая научная статья об ЭпиВакКороне. Часть 1» и «Учёные говорят про “ЭпиВакКорону”». Рисунок 5 иллюстрирует проблему присутствия в вакцине антигенов, антитела к которым по своей природе не могут защищать от инфекции.
Рисунок 5. Антигены вакцины и антитела, которые провоцируют эти антигены у вакцинированных. Показаны все антигены вакцины «ЭпиВакКорона», а именно пептиды шиповидного белка, нуклеокапсидный вирусный белок, бактериальный белок и гис-тэг. Все эти антигены могут провоцировать образование нецелевых антител без протективной противовирусной функции.
рисунок автора статьи
Эксперимент А.А. Чепурнова
Основная интрига, связанная с вакциной «ЭпиВакКорона», заключается в противоречивости утверждений тех, кто тем или иным образом связан с разработкой и испытаниями вакцины. Особенно важен вопрос о нейтрализующих антителах. Если вакцина не вызывает образования нейтрализующих вирус антител, то она вряд ли сможет предупредить COVID-19 у вакцинированных. Отсутствие протективного действия вакцины может привести к заражению и смерти людей, считающих себя защищенными.
Согласно научной работе в журнале «Инфекция и иммунитет» [1], у всех добровольцев-участников клинических исследований 1 и 2 фаз испытаний выработались нейтрализующие вирус антитела. В то же время добровольцы 3 фазы клинических исследований говорят, что даже у тех, у кого выявлялись антитела специальной тест-системой «Вектора», не было обнаружено нейтрализующих антител. Эти данные получил опытный вирусолог, специалист по особо опасным вирусным инфекциям профессор А.А. Чепурнов. Он исследовал в реакции нейтрализации несколько десятков зашифрованных сывороток вакцинированных или переболевших людей. После расшифровки выяснилось, что нейтрализующие антитела выявлены во всех сыворотках переболевших или вакцинированных вакциной «Спутник V» (по 5 сывороток в группе), но полностью отсутствуют, начиная с разведения 1:2, у 19 из 20 человек, привитых вакциной «ЭпиВакКорона». У одного привитого, но заболевшего COVID-19 на 43 день после начала вакцинации (!), нейтрализующие антитела были обнаружены.
Подробно об анализе антител у добровольцев-участников клинических испытаний 3 фазы вакцины «ЭпиВакКорона» можно почитать в ранее опубликованной статье в «ТрВ».
Имеющиеся данные позволяют считать, что необходима официальная комиссионная проверка наличия нейтрализующих антител у людей, привитых этой вакциной. Это недорогое и быстро выполнимое исследование. По его результатам можно принять обоснованное решение о целесообразности использования вакцины в гражданском обороте и о продолжении разработки на данной платформе. Хочу отметить, что ряд крупнейших биотехнологических компаний мира (Sanofi, Merck), свернули свою работу над вакциной, убедившись в неэффективности выбранных ими платформ (ничего зазорного в этом нет).
Т-клеточный иммунитет
В статье [1] полностью отсутствуют данные по Т-клеточному иммунитету, хотя авторы заявляют в СМИ, что «кроме гуморального иммунного ответа, вакцина индуцирует Т-клеточный ответ, в результате чего гибель заражённых клеток не даёт вирусу распространиться дальше и заражать здоровые клетки». Мы часто встречаем заявления разработчиков, что вакцина стимулирует образование так называемых Т-хелперов, способствующих образованию антител у провакцинированных. Так, разработчики вакцины сообщают: «Для оценки Т-клеточного ответа, который может формироваться под влиянием “ЭпиВакКороны”, необходимо учесть ряд особенностей: во-первых, в данном случае должна происходить стимуляция преимущественно Т-хелперных клеток, несущих маркер CD4+, а не CD8+ Т-цитотоксических лимфоцитов. Кроме того, стимуляция в данном случае должна идти по Тh-2-зависимому пути (ведущему к появлению защитных антител), и таким образом, маркером активации Т-лимфоцитов будет являться не гамма-интерферон (определение его уровня ничего не покажет), а интерлейкин-4».
Итак, разработчики вакцины подробно информируют граждан, что они — граждане — не могут сами изучать свой Т-клеточный противовирусный иммунитет доступными коммерческими тестами после вакцинации «ЭпиВакКороной». То есть тест компании «Генериум» не может быть использован для этой цели. Более того, на вопрос добровольцев-участников клинических испытаний «ЭпиВакКороны»: «У какого процента вакцинированных наблюдается CD4+ Т-клеточный ответ по Th2-типу после “ЭпиВакКороны”?» был получен следующий письменный ответ «Вектора»: «Данный вопрос не исследовался».
Проблема ИФА-тестов
Тестирование наличия, титра и характеристик антител у вакцинированных — это очень важная задача научной работы. Увы, эта задача выполнена создателями вакцины, судя по публикации [1], не на высоком уровне.
Первый тест на антитела из статьи в журнале «Инфекция и иммунитет»
Есть крайне неубедительное объяснение разработчиков, почему обычные ИФА-тесты не выявляют антитела к нативному шиповидному белку после иммунизации пептидной вакциной: они считают, что антитела возникают «всего» против трех антигенных детерминант этого белка (в соответствии с тремя используемыми в вакцине пептидами), а этого слишком мало для положительного сигнала. Однако в сыворотках вакцинированных должны появиться три типа антител, которым ничто не должно мешать присоединиться к своим эпитопам, то есть на каждую молекулу антигена-тримера от 1 до 3 молекул антител молекулярного веса 150 кДа (сравнимо с молекулярным весом антигена). Отрицательный тест на антитела к шиповидному белку означает, что такие антитела после вакцинации не образуются. При этом антитела на пептиды, возможно, образуются (не доказано), но они не способны связаться с шиповидным белком коронавируса (доказано).
В статье отсутствует информация, необходимая для воспроизведения экспериментов и понимания результатов. Например, отсутствует описание тест-системы для анализа антител к антигенам вакцины. В статье используется тест-система «Вектор ИФА Корона-АТ», ТУ 21.10.60-092-05664012-2020 (см. в статье в разделе «Материалы и методы» тесты ИФА). Это так называемый спецтест с неизвестными антигенами. Скорее всего, антитела, выявляемые спецтестом, обнаруживают смесь антигенов, имеющихся в вакцине (пептиды, мальтозасвязывающий белок E. coli, гис-тэг, нуклеокапсидный белок коронавируса). Результаты теста показывают, что вакцина вызывает образование антител. Тест, однако, не позволяет понять, могут ли какие-либо из этих антител взаимодействовать с главным иммуногенным антигеном коронавируса — нативным вирусным шиповидным белком.
Тест «Вектора» на антитела к вакцинным антигенам «ЭпиВакКороны», помимо прочего, умудрился показать неплохие результаты у плацебо-группы, вакцинированной физраствором на 0, 14 и 21 дни эксперимента. На 35 и 42 дни антитела к антигенам «ЭпиВакКороны» у группы плацебо детектироваться перестали, и объяснения этого странного феномена в работе нет.
Второй тест на антитела из статьи в журнале «Инфекция и иммунитет»
Второй ИФА-тест основан на использовании инактивированных вирионов SARS-CoV-2. Поскольку оболочка у части вирионов при инактивации и адсорбции на подложку может быть повреждена, этот тест, вероятно, способен выявлять как антитела к шиповидному, так и к нуклеокапсидному белкам коронавируса. Таким образом, в статье не доказано, что вакцина способна вызывать образование антител именно к шиповидному белку.
Более того, ранее разработчики утверждали, что антитела к шиповидному белку не выявляются у вакцинированных «ЭпиВакКороной» при использовании обычных ИФА-тестов, где на подложку наносится полноразмерный тримерный шиповидный белок, полученный в эукариотических клетках. Это говорит о том, что вакцина не вызывает образования антител против главного иммуногена коронавируса.
Но если нет антител к этому белку, нельзя объяснить наличие нейтрализующих антител в ответ на вакцину.
Тест на антитела, способные к нейтрализации вируса
В статье [1] показали нейтрализующие свойства сывороток у вакцинированных. Только этот эксперимент был проведен по достаточно «оригинальной» методике. Классическим методом оценки вирус-нейтрализующих антител в вирусологии принято считать методику реакции нейтрализации с детекцией по цитопатическому действию (метод ЦПД). Метод заключается в прямом подсчете погибших клеток, и именно этот метод используют другие российские разработчики вакцин (Институт им. Гамалеи и Центр им. Чумакова) для оценки вирус-нейтрализующих свойств сывороток вакцинированных. Именно эту методику использовал и проф. А. Чепурнов. Используемая «Вектором» методика нейтрализации отличается от метода ЦПД и основана на детекции нуклеокапсидного белка SARS-CoV-2 в зараженных клетках, то есть является вариантом ИФА. У данной методики потенциально есть важный недостаток — низкая специфичность. Антитела часто дают «неспецифику» (ложноположительный сигнал). Этот недостаток хорошо известен разработчикам тест-систем ИФА, и каждый разработчик тест-системы определяет и указывает не только чувствительность, но и специфичность методики. К сожалению, специфичность методики «Вектора» неизвестна. Кроме того, методика определения нейтрализующих антител по 50%-ному (а не 100%-ному, как в обычном тесте) подавлению вируса может завышать титр нейтрализующих антител в 2–4 раза и принципиально искажать важные результаты.
Использование «альтернативной» методики — это не очень большая проблема, если в эксперименте есть необходимые контроли. В эксперименте от «Вектора» отрицательный контроль — это группа плацебо, но полученные значения в этой группе вызывают недоумение. Методикой «Вектора» в отрицательном контроле плацебо определяются (!) вирус-нейтрализующие антитела. Но их быть не должно, и возникает вопрос — что измеряет данная методика? Подтверждает ли наличие вируснейтрализующих антител в группе плацебо гипотезу о низкой специфичности методики? Кроме того, в эксперименте полностью отсутствует положительный контроль — сыворотки переболевших COVID-19. С чем мы можем сравнить эффективность измеряемой в эксперименте нейтрализации? Какие выводы мы можем сделать по эксперименту без адекватных отрицательных и положительных контролей?
Таким образом, создается впечатление, что утверждение о наличии нейтрализующих антител в сыворотках людей, вакцинированных «ЭпиВакКороной», крайне сомнительно.
Интересная дополнительная критика способов тестирования уровня антител у провакцинированных «ЭпиВакКороной» приведена в статьях «Первая научная статья об ЭпиВакКороне. Часть 2» и «Первая научная статья об ЭпиВакКороне. Часть 3».
«ЭпиВакЭбола» — предшественник «ЭпиВакКороны»
Так как успех создания вакцины «Спутник V» в СМИ освещается довольно широко, то, возможно, многие читатели знают предысторию создания этой вакцины. Аденовирусная платформа первоначально была использована для создания российской вакцины от лихорадки Эбола. Группа разработчиков под руководством Дениса Логунова создала вакцину и опубликовала результаты 1–2 фаз клинических испытаний [16].
Группа создателей вакцины «ЭпиВакКорона» тоже испытывала свою платформу при создании собственной пептидной вакцины от вируса Эбола. Вакцина «ЭпиВакЭбола» была не только зарегистрирована Минздравом, но и получила похвальные отзывы от руководства Минздрава и Роспотребнадзора, была названа уникальной по безопасности. В 2019 году Роспатент назвал патент этой разработки одним из интереснейших патентов 2018 года. Учитывая уникальность разработки пептидной вакцины, имеет смысл познакомиться с патентом и публикациями о вакцине-предшественнике.
Член-корреспондент РАН Сергей Викторович Нетёсов, в прошлом заместитель генерального директора центра «Вектор», в своем интервью о вакцинах против вируса Эбола говорит об «ЭпиВакЭболе», как о завершенной разработке. Он указывает на появление двух работ об испытаниях этой вакцины.
К сожалению, обе работы вместе занимают меньше страницы А4, так как это по сути тезисы конференции, опубликованные в журнале «Инфекция и иммунитет» [17], [18]. В этих коротких тезисах декларируются безопасность и иммуногенность вакцины. Именно декларируются, так как никаких доказательств в тексте не приведено. По мнению профессора Нетёсова, вакцина «ЭпиВакЭбола» готова к полевым испытаниям, то есть к третьему этапу клинических испытаний. Хотя в интервью говорится о том, что с 2016 года можно отследить серию публикаций о создании и испытании пептидной вакцины «ЭпиВакЭбола», но ссылается Сергей Викторович только на эти тезисы «Материалов XI съезда ВНПОЭМП» в Москве 16–17 ноября 2017 года. Никаких серьезных доказательных журнальных публикаций с тех пор не появилось. Хотя в интернете встречаются утверждения о проведении третьего этапа клинических испытаний на 350 добровольцах (первоисточник нам найти не удалось), но никаких результатов испытаний не продемонстрировано.
Единственным источником информации о вакцине становится патент, интересный по двум причинам. Во-первых, он высоко оценен Роспатентом, назван одной из лучших работ 2018 года. А во-вторых, значительная часть текста патента и в русском, и в английском вариантах опубликована в «битой кодировке» и совершенно не поддается прочтению. Вероятно, безразличие к этому тексту было в равной степени и у тех, кто его писал, и у тех, кто его хвалил. В результате и мы тоже не будем тратить время на анализ патента.
Утверждение разработчиков «ЭпиВакКороны» о том, что за их плечами находится успешный опыт создания вакцины «ЭпиВакЭбола» совершенно не подкреплено доказательствами. Нет результатов ни одной из фаз испытаний, нет публикаций, фактически нет патента. Научная полемика по этому вопросу невозможна.
Проблемы и нестыковки в представлении результатов
Вопросов к работе [1] возникает немало: тут и очень странные таблицы данных, и расхождения между значениями в этих таблицах и в описательной части, и главное — непонятные контроли и их отсутствие там, где они критически важны (например, в реакции нейтрализации). Перечислим самое интересное (и самое печальное), а за более подробным анализом этой публикации отсылаем читателя к посту Coronamed.channel в «Фейсбуке».
Отсутствуют положительные контроли
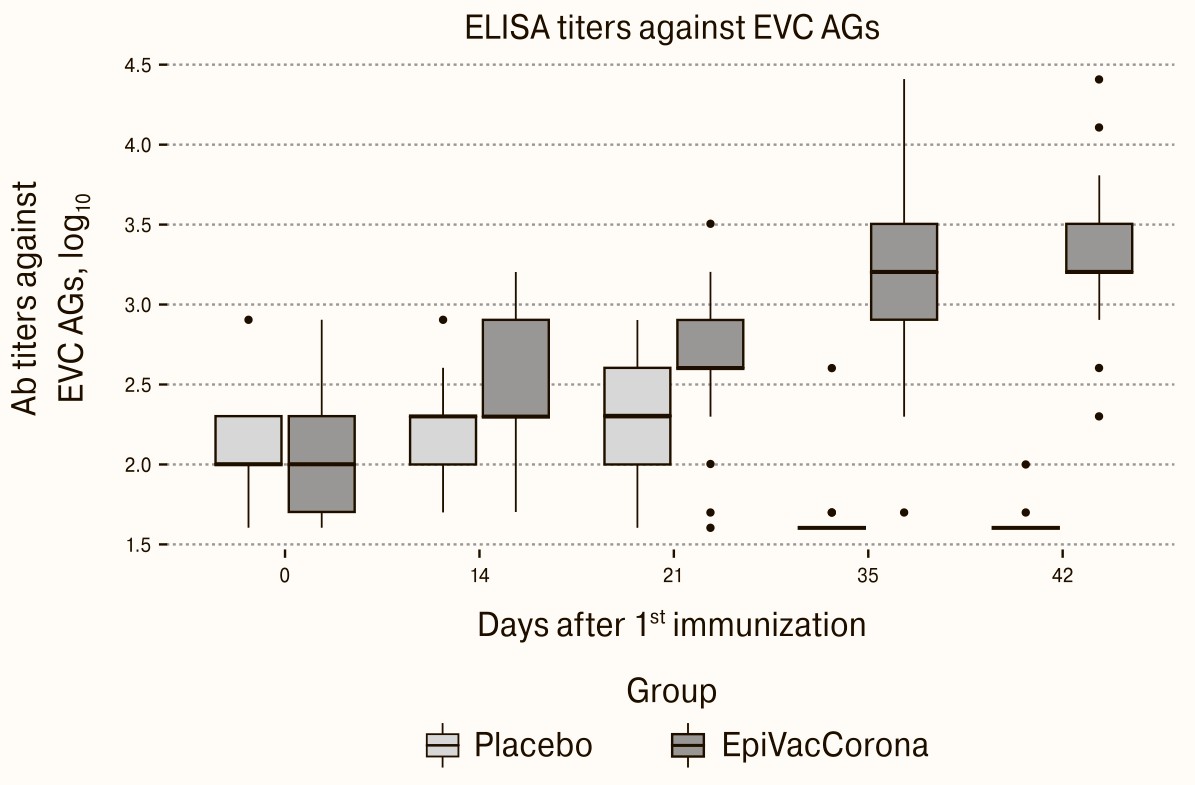
Отсутствует положительный контроль с плазмой реконвалесцентов в эксперименте с титрами антител к антигенам вакцины (рис. 6). На рисунке приведен результат анализа ИФА-тестом антител испытуемых, которых провакцинировали «ЭпиВакКороной» на антигены вакцины.
Рисунок 6. Специфические антитела к антигенам «ЭпиВакКороны» на 0, 14, 21, 35 и 42 дни после вакцинации. По оси ординат результаты ИФА теста в логарифмической шкале.
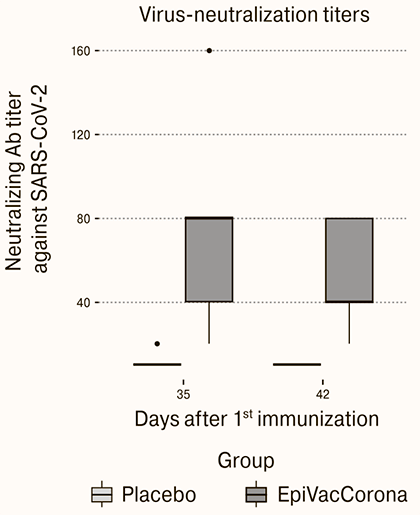
Рисунок 7. Вирус-нейтрализующие антитела (обратные титры) в сыворотках добровольцев-испытуемых на 35 и 42 дни после первой иммунизации
В эксперименте с вирус-нейтрализующими антителами (рис. 7) этот контроль также отсутствует. Показаны результаты анализа обратных титров вирус-нейтрализующих антител в сыворотке испытуемых на 35 и 42 дни после вакцинации.
Обнаружены антитела к антигенам вакцины в контрольной группе испытуемых
Данные, представленные на Fig. 2 из [1] (рис. 6), вызывают много вопросов. На этом рисунке отсутствует положительный контроль, а отрицательный контроль в виде данных для группы плацебо выглядит странно. В этой группе на 0–21 дни после вакцинации обнаруживаются высокие титры антител по тесту «Вектора», а на 35 и 42 сутки они пропадают.
Более того, в таблице «Иммуногенность и исследования вирус-нейтрализующей способности» данные по группе вакцины и группе плацебо представлены полностью не для всех временных отметок. Максимальный титр у кого-то из группы плацебо достиг 1:800, а средний геометрический титр в этой группе к 21 дню вплотную подобрался к 1:200. Такой же минимальный титр специальных антител к вакцинным антигенам «ЭпиВакКороны» указан для группы вакцинированных на последней временной отметке. Если разработчики сообщают о 100%-ной иммунологической эффективности в группе вакцины, означает ли это, что титр 1:200 по тесту «Вектора» в группе плацебо входит в границы эффективности?
Вызывает сомнения статистическая достоверность полученных результатов
На рисунке 6 ошибки титров антител в группе вакцинированных и в группе плацебо перекрываются. В таблице 3 представлены очень большие стандартные отклонения титров антител на 35 и 42 сутки.
Вакцина продемонстрировала слабую иммуногенность
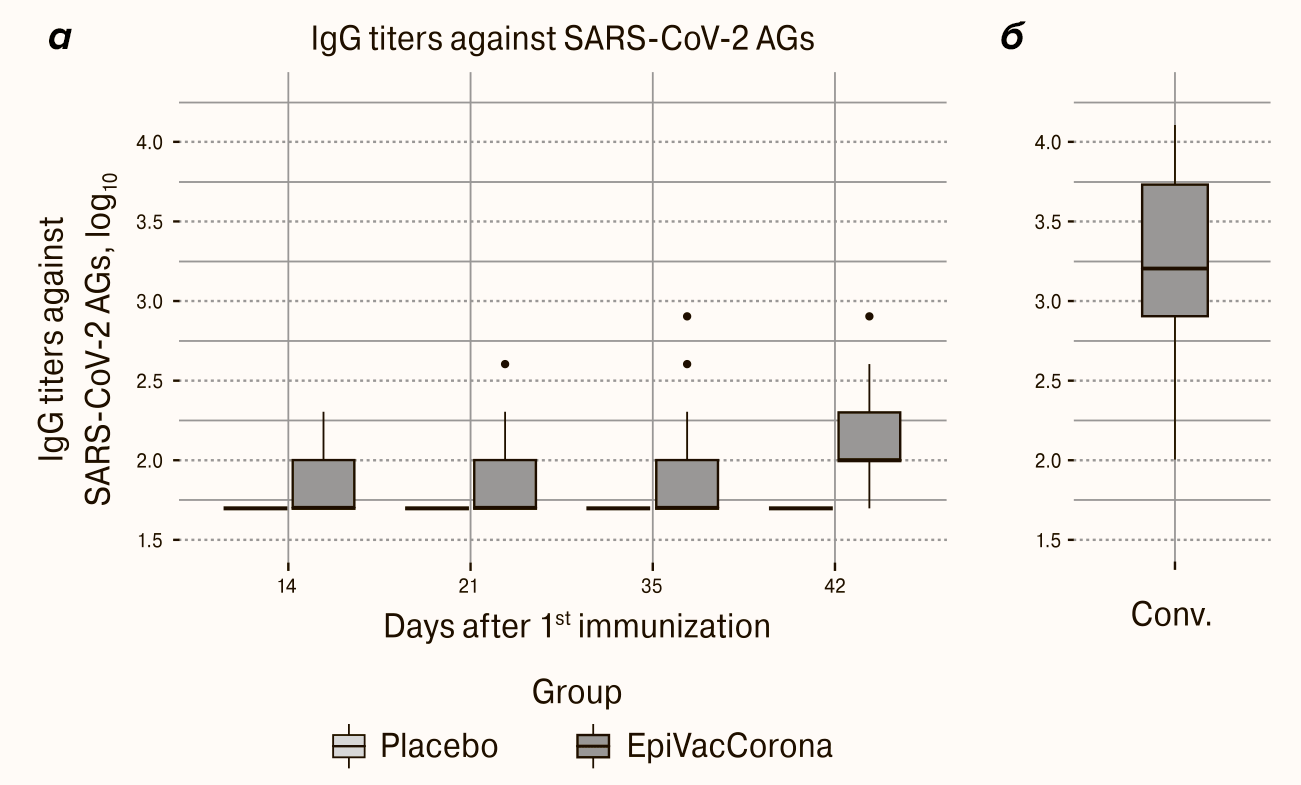
В эксперименте с титрами антител к антигенам SARS-CoV-2 (рис. 8) средние геометрические титры после вакцины на последней временной отметке более чем в 10 раз ниже титров антител переболевших. На панели а показаны титры антител к антигенам вируса в сыворотках испытуемых, которые определялись в разные сроки после вакцинации. Определение производилось для сывороток, полученных на 14, 21, 35 и 42 дни после вакцинации. На панели б показан титр антител у переболевших COVID-19. Значения титров показано в логарифмической шкале.
Рисунок 8. Специфические антитела к антигенам вируса SARS-CoV-2: а — в сыворотках испытуемых на 14, 21, 35 и 42 дни после иммунизации (логарифмическая шкала); б — в сыворотках реконвалесцентов (переболевших COVID-19) (логарифмическая шкала).
Проблема использования вакцины для пожилых
Заявления «Вектора» о безопасности и иммуногенности вакцины «ЭпиВакКорона» для пожилых, а также людей с хроническими заболеваниями, по-прежнему не подтверждены открытыми научными данными. Участники испытаний — это сравнительно молодые и здоровые люди. В списке участников испытаний людей старшего возраста и людей с хроническими заболеваниями нет.
Тут еще стоит немного отвлечься от анализа статьи и рассказать, на основании каких испытаний вакцина была-таки рекомендована пожилым. Специалисты в разработке вакцин выделяют четыре фазы клинических испытаний вакцин, как и других лекарственных препаратов [19]. Первые две фазы нужны для получения первичных данных о побочных эффектах вакцины и ее иммунологических характеристиках. Кроме того, они помогают подобрать дозировки иммуногенного вакцинного материала при введении в организм, а также режим введения вакцины. В качестве иммунологических характеристик чаще всего оценивают выработку антител, хотя есть и другие параметры, такие как клеточный иммунитет. В первых двух фазах, как правило, участвует от нескольких десятков до нескольких сотен человек.
Исследования фазы III делаются уже на большой группе людей — как правило, много тысяч. Эти исследования обычно спланированы таким образом, чтобы получить надежные статистические результаты о способности вакцины предотвращать инфекцию. То есть сравнивают заболеваемость в группе вакцинированных с группой плацебо. На маленькой выборке людей такие исследования проводить невозможно. Ведь только небольшая часть из них заболеет, а надо получить надежную разницу в числе заболевших в группе вакцинированных и плацебо. При этом разница должна быть статистически значимой. Испытания третьей фазы изучают эпидемиологическую эффективность вакцины.
Испытания четвертой фазы проводятся для изучения того, как долго длится иммунитет и нет ли у вакцины долгосрочных побочных эффектов. В принципе, в России действуют примерно такие же правила изучения новых вакцин. Однако в связи с пандемией Минздрав РФ счел возможным регистрировать и даже разрешать выпускать в гражданский оборот вакцины после первых двух фаз, что, по сути, проблематично. В большинстве других стран вакцину выпускают в оборот и дают временное право использования на основании результатов третьей фазы, а именно клинических испытаний, показавших, что в группе вакцинированных заболеваний статистически значимо меньше, чем в контрольной группе. В пандемию эти общие правила не изменились, хотя процедура получения временного разрешения после третьей фазы клинических испытаний упростилась и ускорилась.
Что же было сделано с испытанием вакцины «ЭпиВакКорона» на пожилых людях? Испытания были проведены на сравнительно маленькой группе людей (меньше 150 человек) без контрольной группы и названы «третьей/четвертой фазой». То есть вакцина, про которую абсолютно неизвестно, способна ли она предотвращать инфекцию у пожилых (впрочем, у молодых тоже), разрешена к применению на пожилых людях. Формально с вакциной всё в порядке, и считается, что испытания третьей фазы состоялись. Роспотребнадзор сообщает: «Завершено пострегистрационное клиническое исследование вакцины с участие 150 добровольцев старше 60 лет. Отчет представлен в Минздрав России. Дальнейшее наблюдение за добровольцами через 3 и 6 месяцев будет осуществляться вне рамок настоящего исследования».
Случаи заражения COVID-19 во время клинических испытаний
В работе описываются два случая лабораторно подтвержденного COVID-19 у участников исследования: один из них в группе вакцины. При этом эти случаи и их влияние на результаты исследования не обсуждаются. Например, после полного курса вакцинации произошло заражение COVID-19 18-летнего участника 1 фазы, протекавшее с высокой температурой и вирусной нагрузкой (положительный ПЦР с Ct 21).
Увы, но далеко не единичные случаи заболевания коронавирусом, в том числе среди тех, у кого выработались антитела на антигены «ЭпиВакКороны», были зафиксированы добровольцами-испытателями, самоорганизовавшимися в сообщество в мессенджере Telegram. По моим сведениям, полученным от личного общения с членами этого сообщества, значительная часть участников исследования потеряла веру в вакцину и привилась «Спутником V». Это грустно, потому как означает, что ответ на вопрос о том, какая у вакцины «ЭпиВакКорона» протективность против COVID-19, мы можем так и не получить.
Вывод в отношении опубликованной работы
Обсуждаемую работу [1] вряд ли можно назвать научной статьей, выполненной на хороших научном и методическом уровнях. С учетом перечисленных замечаний, касающихся контролей, расхождения данных, доверительных интервалов и статистической значимости, статья представляется сырой. Поэтому ее выводы пока не могут быть приняты в качестве подтверждения заявлений разработчиков.
Таким образом, опубликованная статья [1] не помогает ответить на вопросы научного сообщества, касающиеся иммунологической эффективности данной вакцинной разработки. Наоборот, она только порождает новые вопросы. Остается непонятным, есть ли у «ЭпиВакКороны» потенциал защиты от тяжелого заболевания.
Основной вывод: данные разработчиков об образовании нейтрализующих антител в ответ на вакцину «ЭпиВакКорона», а, следовательно, о ее иммуногенности, глубоко сомнительны. Требуется независимая проверка результатов разработчиков.