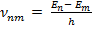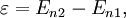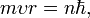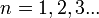в чем недостатки теории бора
Достоинства и недостатки теории Бора.



О достоинствах модели атома водорода, предложенной Бором, мы так или иначе уже сказали. Резюмируем их.
-Теория Бора впервые и совершенно точно указала на факт наличия стационарных энергетических состояний атома, образующих дискретный набор. Этот факт оказался общим свойством объектов микромира.
-В рамках модели Бора удалось получить формулы для вычисления частот спектра атома водорода и объяснить размер атома. Классическая физика была не в состоянии решить эти проблемы.
Однако теория Бора, разумеется, не могла претендовать на роль общей теории, описывающей микромир. Модель Бора обладала рядом существенных недостатков.
-Теория Бора не смогла дать адекватное описание самого простого после водорода атома гелия. Подавно не могло быть и речи о распространении теории Бора на более сложные атомы.
-Даже в самом атоме водорода теория Бора смогла описать не всё. Например, дав выражения для частот спектральных линий, модель Бора не объясняла различие в их интенсивностях. Кроме того, неясен оставался механизм образования молекулы водорода из двух атомов.
Постулаты Бора. Теория Бора строения атома водорода. Недостатки этой теории

Следующий шаг в развитии представлений об устройстве атома в 1913 году сделал выдающийся датский физик Н. Бор. Проанализировав всю совокупность опытных фактов, Бор пришел к выводу, что при описании поведения атомных систем следует отказаться от многих представлений классической физики. Он сформулировал постулаты, которым должна удовлетворять новая теория о строении атомов.
Первый постулат Бора (постулат стационарных состояний) гласит: атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не излучает.

где h – постоянная Планка. Отсюда можно выразить частоту излучения:
Второй постулат Бора также противоречит электродинамике Максвелла, так как частота излучения определяется только изменением энергии атома и никак не зависит от характера движения электрона.
Достоинства теории Бора строения атома: объяснила дискретность энергетических состояний водородоподобных атомов; теория Бора подошла к объяснению внутриатомных процессов с принципиально новых позиций, стала первой полуквантовой теорией атома; эвристическое значение теории Бора состоит в смелом предположении о существовании стационарных состояний и скачкообразных переходов между ними. Эти положения позднее были распространены и на другие микросистемы; объясняет границу таблицы Менделеева. Последний атом, способный существовать физически, имеет порядковый номер 137, так как, начиная со 138-го элемента 1s-электрон должен двигаться со сверхсветовой скоростью, что противоречит специальной теории относительности.
Недостатки теории Бора: не смогла объяснить интенсивность спектральных линий; справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева без экспериментальных данных (энергии ионизации или других); теория Бора логически противоречива: не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно — уравнение движенияэлектрона — классическое, другое — уравнение квантования орбит — квантовое; теория Бора являлась недостаточно последовательной и общей. Поэтому она в дальнейшем была заменена современной квантовой механикой, основанной на более общих и непротиворечивых исходных положениях. Сейчас известно, что постулаты Бора являются следствиями более общих квантовых законов. Но правила квантования широко используются и в наши дни как приближённые соотношения: их точность часто бывает очень высокой.
Теория Бора
Теория Бора
Теория Бора разработана Нильсом Бором в 1913 г. и представляет собой первую квантовую теорию атома водорода, позволившую объяснить дискретность уровней энергии и вывести формулу для частот спектральных линий.
Содержание
Полуклассическая теория Бора
1.
где 
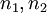
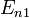
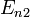
2. Правило квантования момента импульса:
Далее исходя из соображений классической физики о круговом движении электрона вокруг неподвижного ядра по стационарной орбите под действием кулоновской силы притяжения, Бором были получены выражения для радиусов стационарных орбит и энергии электрона на этих орбитах:
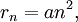
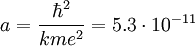
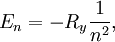
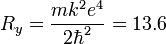
Достоинства теории Бора
Недостатки теории Бора
Теория Бора являлась недостаточно последовательной и общей. Поэтому она в дальнейшем была заменена современной квантовой механикой, основанной на более общих и непротиворечивых исходных положениях. Сейчас известно, что постулаты Бора являются следствиями более общих квантовых законов. Но правила квантования типа широко используются и в наши дни как приближенные соотношения: их точность часто бывает очень высокой.
См. также
Полезное
Смотреть что такое «Теория Бора» в других словарях:
теория Бора — Boro atomo teorija statusas T sritis fizika atitikmenys: angl. Bohr’s atom theory vok. Bohrsche Atomtheorie, f rus. теория Бора, f pranc. théorie de Bohr de l’atome, f … Fizikos terminų žodynas
теория Бора-Зоммерфельда — Boro ir Zomerfeldo atomo teorija statusas T sritis fizika atitikmenys: angl. Bohr Sommerfeld’s atom theory vok. Bohr Sommerfeldsche Atomtheorie, f rus. теория Бора Зоммерфельда, f pranc. théorie de Bohr Sommerfeld, f … Fizikos terminų žodynas
Бора постулаты — основные, интуитивно введенные допущения, на которых основывалась теория атома великого датского физика Нильса Бора, явившаяся предшественницей современной квантовой (волновой) механики, в которой эти постулаты получили частичное объяснение. Эти… … Начала современного естествознания
КВАНТОВ ТЕОРИЯ — КВАНТОВ ТЕОРИЯ. Квант (от лат. quantum определенное количество) понятие, характеризующее прерывность взаимодействий элементарных частиц вещества электронов, протонов, атомов и молекул между собой и со светом. Представление о К. введено М. Планком … Большая медицинская энциклопедия
КАЧЕСТВЕННАЯ ТЕОРИЯ ДИФФЕРЕНЦИАЛЬНЫХ УРАВНЕНИЙ — в банаховом пространстве раздел функционального анализа, в к ром исследуется поведение на действительной оси J или на положительной (отрицательной) полуоси J+ (J ) решений эволюционных уравнений в банаховом пространстве. Рассматриваются уравнения … Математическая энциклопедия
Кубический нитрид бора — – абразивный материал, в основном, состава BN с плотной кубической упаковкой атомов бора и азота в тетраэдрической координации, изготовленный искусственным путем. [ГОСТ 21445 84] Рубрика термина: Абразивы Рубрики энциклопедии: Абразивное… … Энциклопедия терминов, определений и пояснений строительных материалов
Зонная теория — твёрдого тела квантовомеханическая теория движения электронов в твёрдом теле. В соответствии с квантовой механикой свободные электроны могут иметь любую энергию их энергетический спектр непрерывен. Электроны, принадлежащие… … Википедия
когерентная теория истины — КОГЕРЕНТНАЯ ТЕОРИЯ ИСТИНЫ (от лат. cohaerentia сцепление, связь) концепция, сводящая проблему истинности к критерию самосогласованности, непротиворечивости: напр., предложение истинно, если оно является элементом логически взаимосвязанной … Энциклопедия эпистемологии и философии науки
квантовая теория — Другой путь исследований изучение взаимодействия материи и радиации. Термин «квант» связывают с именем М. Планка (1858 1947). Это проблема «черного тела» (абстрактное математическое понятие для обозначения объекта, аккумулирующего всю энергию … Западная философия от истоков до наших дней
Модель Бора: описание теории, противоречия модели
Долгое время строение атома было дискуссионной темой среди физиков, пока не появилась созданная датским ученым Нильсом Бором модель. Он не был первым, кто попытался описать движение субатомных частиц, но именно его наработки позволили создать непротиворечивую теорию с возможностью прогнозирования местонахождения элементарный частицы в тот или иной момент времени.
Жизненный путь
Нильс Бор родился 7 октября 1885 года в Копенгагене и умер там же 18 ноября 1962 года. Он считается одним из величайших физиков и неудивительно: именно ему удалось построить непротиворечивую модель водородоподобных атомов. По легенде он увидел во сне, как вокруг некоего светящегося разреженного центра вращалось что-то вроде планет. Затем эта система резко уменьшилась до микроскопических размеров.

С тех пор Бор упорно искал способ воплотить сон в формулах и таблицах. Тщательно изучая современную литературу по физике, экспериментируя в лаборатории и размышляя, он смог достичь своей цели. Обнародовать результаты ему не помешала даже врожденная застенчивость: он стеснялся выступать перед большой аудиторией, начинал путаться, и слушатели ничего не понимали из объяснений ученого.
Предшественники
До Бора ученые пытались создать модель атома, основанную на постулатах классической физики. Наиболее успешная попытка принадлежала Эрнесту Резерфорду. В результате многочисленных опытов он пришел к выводу о существовании массивного атомного ядра, вокруг которого двигаются по орбитам электроны. Поскольку графически такая модель была похожа на строение Солнечной системы, за ней укрепилось название планетарной.
Но в ней имелся существенный недостаток: атом, отвечающий резерфордовским уравнениям, оказывался нестабильным. Рано или поздно электроны, двигавшиеся с ускорением по орбитам вокруг ядра, должны были упасть на ядро, а их энергия тратилась бы на электромагнитное излучение. Для Бора модель Резерфорда стала отправным пунктом в построении собственной теории.
Первый постулат Бора
Главным новшеством Бора стал отказ от использования классической ньютоновской физики в построении теории атома. Изучив полученные в лаборатории данные, он пришел к выводу, что в мире элементарных частиц не работает такой важный закон электродинамики, как равноускоренное движение без волнового излучения.
Итогом его размышлений стал закон, который звучит так: атомная система стабильна, только если она находится в одном из возможных стационарных (квантовых) состояниях, каждому из которых соответствует определенная энергия. Смысл этого закона, иначе называемого постулатом квантовых состояний, состоит в признании отсутствия электромагнитного излучения, когда атом находится в таком состоянии. Также следствием первого постулата является признание наличия в атоме энергетических уровней.
Правило частот
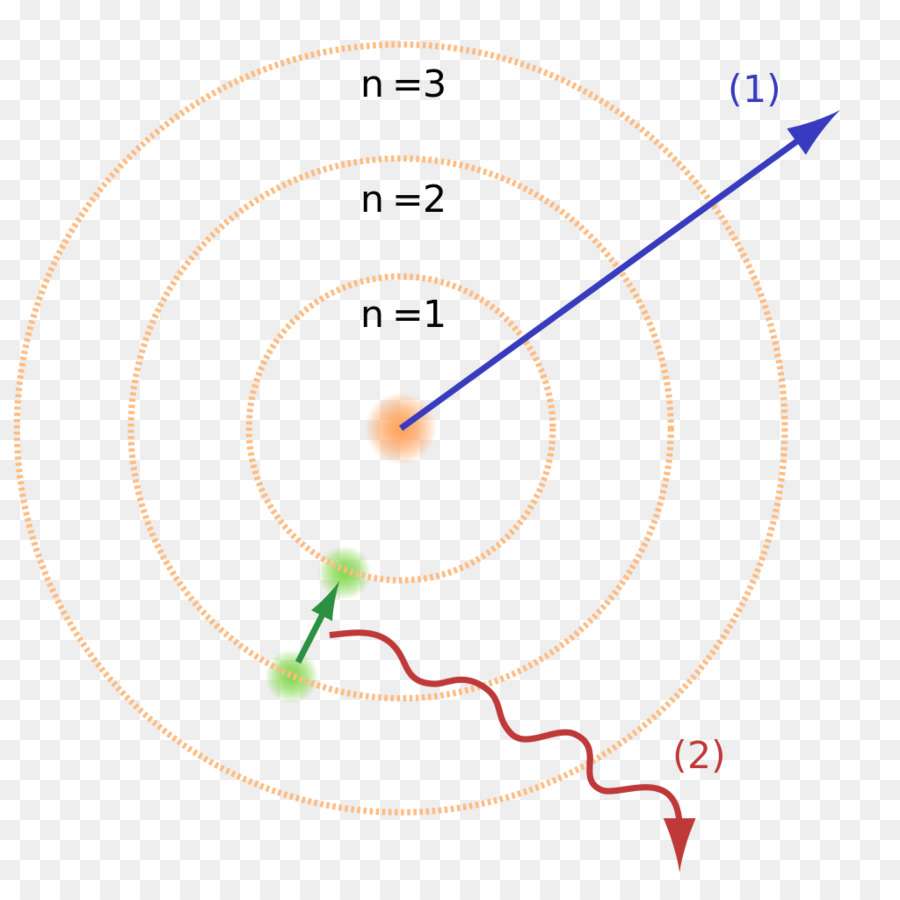
Однако было очевидно, что атом не может все время находиться в одном и том же квантовом состоянии, поскольку стабильность отрицает любое взаимодействие, а значит, не было бы ни Вселенной, ни движения в ней. Кажущееся противоречие разрешил второй постулат модели строения атома Бора, известный как правило частот. Атом способен перейти из одного квантового состояния в другое с соответствующим изменением энергии, излучая или поглощая при этом квант, энергия которого равна разности энергий стационарных состояний.
Второй постулат тоже противоречит классической электродинамике. Согласно теории Максвелла, характер движения электрона не может воздействовать на частоту его излучения.
Спектр атома
Квантовая модель Бора стала возможной благодаря тщательному изучению спектра атома. Долгое время ученых смущало, что вместо ожидаемой непрерывной цветовой области, получаемой при изучении спектров небесных светил, спектрограмма атома была прерывистой. Линии яркого цвета не переходили друг в друга, а разделялись внушительными темными участками.
Теория перехода электрона из одного квантового состояния в другое объясняла эту странность. Когда электрон переходил с одного энергетического уровня на другой, где от него требовалась меньшая энергия, он испускал квант, что отражалось на спектрограмме. Теория Бора сразу же продемонстрировала способность к прогнозированию дальнейших изменений в спектрах простых атомов вроде водорода.
Недостатки
Теория Бора не до конца порывала с классической физикой. Она по-прежнему сохраняла идею орбитального движения электронов в электромагнитном поле ядра. Идея о квантовании при переходе из одного стационарного состояния в другое удачно дополняла планетарную модель, но все же не разрешала всех противоречий.
Хотя в свете модели Бора электрон не мог перейти в движение по спирали и упасть на ядро, непрерывно излучая энергию, оставалось непонятным, почему он не мог последовательно подниматься на более высокие энергетические уровни. В этом случае все электроны рано или поздно оказались бы в наинизшем энергетическом состоянии, что привело бы разрушению атома. Другой проблемой стали аномалии в атомных спектрах, которые теория не объясняла. Еще в 1896 году Питер Зееман провел любопытный эксперимент. Он поместил атомный газ в магнитное поле и снял спектрограмму. Оказалось, что некоторые спектральные линии расщепились на несколько. Такой эффект в теории Бора объяснения не получал.
Построение модели атома водорода по Бору
Несмотря на все недостатки своей теории, Нильс Бор смог построить соответствующую действительности модель атома водорода. При этом он использовал правило частот и законы классической механики. Расчеты Бора по определению возможных радиусов орбит электрона и вычислению энергии квантовых состояний оказались достаточно точными и подтвердились экспериментально. Частоты излучений и поглощений электромагнитных волн соответствовали расположению темных промежутков на спектрограммах.
Таким образом, на примере атома водорода было доказано, что каждый атом представляет собой квантовую систему с дискретными энергетическими уровнями. Кроме того, ученый смог найти способ совместить классическую физику и свои постулаты с помощью принципа соответствия. Он гласит, что квантовая механика включает в себя законы ньютоновской физики. При определенных условиях (например, если квантовое число было достаточно большим), квантовая и классическая механика сближаются. Это доказывалось тем, что при увеличении квантового числа протяженность темных промежутков на спектре уменьшалась вплоть до полного исчезновения, как это и ожидалось в свете ньютоновских представлений.
Значение
Введение принципа соответствия стало важным промежуточным этапом на пути к признанию существования особой квантовой механики. Модель атома Бора стала для многих отправной точкой в конструировании более точных теорий движения субатомных частиц. Нильс Бор не смог подобрать точной физической интерпретации правилу квантования, но он и не мог этого сделать, поскольку лишь с течением времени были обнаружены волновые свойства элементарных частиц. Луи де Бройль, дополнив теорию Бора новыми открытиями, доказал, что каждая орбита, по которой движется электрон, представляет собой волну, распространяющуюся от ядра. С этой точки зрения стационарным состоянием атома стали считать такое, что образуется в случае, когда волна, сделав полный оборот вокруг ядра, повторялась.
Недостатки теории Бора



Теория Бора являлась недостаточно последовательной и общей. Поэтому она в дальнейшем былазаменена современной квантовой механикой, основанной на более общих и непротиворечивых исходныхположениях. Сейчас известно, что постулаты Бора являются следствиями более общих квантовых законов.Но правила квантования типа широко используются и в наши дни как приближенные соотношения: ихточность часто бывает очень высокой.
Ква́нтовое число́ в квантовой механике — численное значение какой-либо квантованной переменной микроскопического объекта (элементарной частицы, ядра, атома и т. д.), характеризующее состояние частицы. Задание квантовых чисел полностью характеризует состояние частицы. Некоторые квантовые числа связаны с движением в пространстве и характеризуют вид волновой функции частицы. Некоторые другие квантовые числа никак не связаны с перемещением в обычном пространстве, а отражают «внутреннее» состояние частицы.
Если электрону приписывается собственный механический момент импульса (спин) Ls, то ему соответствует собственный магнитный момент pms. Согласно общим выводам квантовой механики,спин квантуется по закону