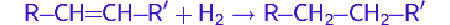в чем находится водород
Водород и его свойства
Что такое водород
Водород — самый легкий химический элемент, занимающий в периодической таблице Менделеева начальное место.
Его атомный номер — единица. На одноатомную форму водорода приходится около 75% барионной массы, она считается самым распространенным веществом во всей Вселенной. Водородная плазма — основное вещество звезд, за исключением компактных.
У водорода три изотопа:
К общим характеристикам относятся следующие свойства: не имеет цвета запаха, вкуса. Двухатомная форма ( Н 2 ) нетоксична, однако в соединении с воздухом (или О 2 ) пожароопасна и склонна к взрывам. Взрывоопасность также проявляется в присутствии прочих газов-окислителей, например, фтора, хлора.
На Земле водород присутствует в составе молекулярных соединений, например, вода. Его роль в кислотно-основных реакциях трудно переоценить.
Нахождение в природе, изучение его свойств
Звездная температура позволяет существовать водороду в виде плазмы. Это примерно 6000оС. Однако пространство между звездами заполнено отдельными молекулами, атомами и ионами, которые зачастую образовывают молекулярные скопления различных размеров и форм — облака. Плотность вещества при этом не является постоянной величиной, как и его температура.
В коре Земли водород считается десятым по распространенности элементом. Его массовая доля равна 1%. В то же время по числу атомов он достигает 17%. Это второе место после кислорода, доля которого равна 52%. Отсюда и значительная роль водорода в природе, особенно в химических превращениях.
Водород, в отличие от кислорода, не может существовать в свободном состоянии, только в связанном. Исключение составляет атмосфера, в сухом остатке которой 0,00005% простого вещества — водорода.
Все органические вещества включают в свой состав водород. Велика его доля в живых клетках (по количеству атомов его удельный вес достигает 63%).
В составе воды водород имеет большое значение в протекании геохимических процессов. Так, вулканические газы вызывают истечение определенных количестве водорода вдоль разломов (причина — рифтогенез). По этой же причине часто обнаруживают водород в районе угольных месторождений.
Натуральные минералы могут содержать Н2 в виде ионов аммония, гидроксил-ионов и воды.
Причина появления молекул Н2 в атмосфере — разложение формальдегида — участника окисления метана и прочих органических соединений. Кроме того, причина его образования — неполное сгорание топлива и биомассы, фиксация азота некоторыми микроорганизмами, содержащимися в воздухе.
Молекулы водорода легкие, поэтому имеют высокую тепловую скорость. При попадании в верхние слои атмосферы такие молекулы часто улетают в космос, при этом их потери могут достигать 3 кг каждую секунду.
Химические и физические свойства
Начиная говорить о химических свойствах водорода, нужно отметить чрезвычайную прочность его двухатомной молекулы. Для того, чтобы она распалась и атомы могли провзаимодействовать с другими участниками химической реакции, необходима энергия:
Обычные температурные условия обеспечивают протекание реакций только с металлами высокой активности, к примеру, с кальцием:
1 2 C a + H 2 → C a H 2
Исключение составляет реакция с фтором, продуктом которой является фтороводород:
1 2 F 2 + H 2 → 2 H F
Если имеется возможность повышения температуры (либо при другом воздействии, к примеру, освещении), водород может вступать в реакцию с большинством металлов и неметаллов:
1 2 O 2 + 2 H 2 → 2 H 2 O
В реакциях с галогенами образуются галогеноводороды:
1 2 H 2 + F 2 → 2 H F (в темноте происходит взрыв)
1 2 H 2 + C l 2 → 2 H C l (на свету происходит взрыв)
В реакции с оксидами водород проявляет восстановительные свойства:
1 2 C u O + H 2 → H 2 O + C u
Высокая температура делает возможной реакцию с сажей:
1 2 C + 2 H 2 → C H 4
Когда активные металлы соединяются с водородом, образуются гидриды, например гидрид натрия (NaH), гидрид кальция (CaH2), гидрид магния (MgH2). Эти солеобразные твердые, легко гидролизирующиеся вещества:
1 2 C a H 2 + 2 H 2 → C a ( O H ) 2 + 2 H 2
Оксиды металлов, реагируя с водородом, восстанавливаются с выделением воды:
1 2 F e 2 O 3 + 3 H 2 → 2 F e + 3 H 2 O
Благодаря свойствам водорода, он нашел применение для восстановления органических веществ. Протекают реакции с участием катализатора, а также при высоких параметрах давления и температуры. К примеру, насыщенные алканы образуются в результате гидрирования ненасыщенных алкенов и алкинов.
Физические свойства водорода:
Хорошо растворяется в металлах, поэтому способен диффундировать в них. В серебре не растворим.
Получение водорода, как добыть вытеснением из воды
Потребление в мире водорода составляет порядка 75 млн т. Основная масса приходится на нефтепереработку и производство аммиака. Получение водорода для таких промышленных нужд происходит в основном из природного газа (его расход составляет 205 млрд м3). Оставшуюся часть берут из угля. Примерно 100 тыс т вырабатывают с помощью реакции электролиза.
Получение водорода сопровождается поступлением в атмосферу 830 млн т углекислого газа. Стоимость получения водорода из газа составляет от полутора до трех долларов за каждый кг.
Получение водорода методом электролиза в химии выглядит так:
1 2 2 N a C l + 2 H 2 O → 2 N a O H + C l 2 + H 2
Метод конверсии метана при температуре 1000оС с водяными парами:
1 2 C H 4 + H 2 O ↔ C O + 3 H 2
Следующий способ получения — пропускание водяных паров над горящим коксом (температура не менее 1000оС):
1 2 H 2 O + С ↔ С O + H 2
Свободный водород выделяется в результате реакции катализа окислением кислородом:
1 2 2 C H 4 + O 2 ↔ 2 C O + 4 H 2
В промышленности H2 часто получают путем электролиза водных растворов активных металлов:
а также путем крекинга и риформинга углеводородов при переработке нефти.
Существуют способы получения Н2 лабораторными способами:
В промышленности используется очистка водорода из сырья, которое содержит углерод (в частности — водородсодержащий газ ВСГ). Методы следующие:
Получение и собирание водорода в домашних условиях, техника безопасности
Реальным способом получения водорода в домашних условиях является реакция щелочи с алюминием. Газ получается гораздо чище, чем в реакции с кислотой. Схема следующая. В качестве алюминия используют фольгу, щелочного раствора — средство «Крот».
Берем стеклянную емкость, засыпаем в нее немного средства против засора «Крот» и наливаем 100 г воды обычной температуры. Перемешиваем до полного растворения и помещаем сюда же фольгу, скатанную в небольшие шарики. Выделение тепла свидетельствует о начале реакции, после чего ее скорость активируется. Через 20-60 секунд можно добавить новую порцию фольги.
Чтобы образовавшийся водород собрать, можно закрыть банку крышкой, сделав в ней отверстие, в которое вставить трубку. Второй конец трубки закрепить в воздушном шарике.
Поскольку водород является взрывоопасным веществом, делать это нужно крайне осторожно, начиная от момента возможного вытеснения крышки до конца процесса. Попадание водорода в воду приведет к образованию вещества, способного вызвать обморожение.
Особенности применения водорода
Водород используется во многих производственных сферах, что отражено в таблице:
| Применение | Доля |
| Производство аммиака | 54 % |
| Нефтепереработка и химическая промышленность | 35 % |
| Производство электроники | 6 % |
| Металлургия и стекольная промышленность | 3 % |
| Пищевая промышленность | 2 % |
В химической промышленности активный водород идет на производство аммиака (50%), метанола (8%). В нефтеперерабатывающей — для гидрокрекинга и гидроочистки. На эти цели расходуется около 37% всего водорода, что производится.
Пищевая и косметическая промышленность «пользуется» водородом для производства пищевых добавок, а также саломаса, маргарина, мыла, косметических продуктов.
Для химических лабораторий водород — газ-носитель для газовой хроматографии, а для метеорологии — наполнитель оболочек метеозондов.
Водород — ценное ракетное топливо, однако, ввиду незначительного диапазона температур, используется смесь жидкой и твердой фаз.
В электроэнергетике водород применяют для охлаждения электрогенераторов. Его высокая теплопроводность позволяет использовать газ для заполнения сфер гирокомпасов и колб LED-лампочек.
Водород
Водород является первым элементом периодической системы элементов. Широко распространён в природе. Катион (и ядро) самого распространённого изотопа водорода 1 H— протон. Свойства ядра 1 H позволяют широко использовать ЯМР-спектроскопию в анализе органических веществ.
Трое из пяти изотопов водорода имеют собственные названия: 1 H— протий (Н), 2 H— дейтерий (D) и 3 H— тритий (радиоактивен) (T).
Простое вещество водород— H2— лёгкий бесцветный газ. В смеси с воздухом или кислородом горюч и взрывоопасен. Нетоксичен. Растворим в этаноле и ряде металлов: железе, никеле, палладии, платине.
История водорода
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в XVI и XVII веках на заре становления химии как науки. Прямо указывал на выделение его и М. В. Ломоносов, но уже определённо сознавая, что это не флогистон. Английский физик и химик Г. Кавендиш в 1766 году исследовал этот газ и назвал его «горючим воздухом». При сжигании «горючий воздух» давал воду, но приверженность Кавендиша теории флогистона помешала ему сделать правильные выводы. Французский химик А. Лавуазье совместно с инженером Ж. Менье, используя специальные газометры, в 1783г. осуществил синтез воды, а затем и её анализ, разложив водяной пар раскалённым железом. Таким образом он установил, что «горючий воздух» входит в состав воды и может быть из неё получен.
Происхождение названия водород
Лавуазье дал водороду название hydrogène (от ὕδωρ — «вода» и γενναω — «рождаю»)— «рождающий воду». Русское наименование «водород» предложил химик М.Ф.Соловьев в 1824 году— по аналогии с ломоносовским «кислородом».
Распространённость водорода
Во Вселенной
Водород — самый распространённый элемент во Вселенной. На его долю приходится около 92% всех атомов (8% составляют атомы гелия, доля всех остальных вместе взятых элементов — менее 0,1%). Таким образом, водород — основная составная часть звёзд и межзвёздного газа. В условиях звёздных температур (например, температура поверхности Солнца
6000 °C) водород существует в виде плазмы, в межзвёздном пространстве этот элемент существует в виде отдельных молекул, атомов и ионов и может образовывать молекулярные облака, значительно различающиеся по размерам, плотности и температуре.
Земная кора и живые организмы
Массовая доля водорода в земной коре составляет 1%— это десятый по распространённости элемент. Однако его роль в природе определяется не массой, а числом атомов, доля которых среди остальных элементов составляет 17% (второе место после кислорода, доля атомов которого равна
52%). Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и кислорода. В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях, практически весь водород на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества содержится в атмосфере (0,00005% по объёму).
Водород входит в состав практически всех органических веществ и присутствует во всех живых клетках. В живых клетках по числу атомов на водород приходится почти 50%.
Получение Водорода
Промышленные способы получения простых веществ зависят от того, в каком виде соответствующий элемент находится в природе, то есть что может быть сырьём для его получения. Так, кислород, имеющийся в свободном состоянии, получают физическим способом— выделением из жидкого воздуха. Водород же практически весь находится в виде соединений, поэтому для его получения применяют химические методы. В частности, могут быть использованы реакции разложения. Одним из способов получения водорода служит реакция разложения воды электрическим током.
Основной промышленный способ получения водорода— реакция с водой метана, который входит в состав природного газа. Она проводится при высокой температуре (легко убедиться, что при пропускании метана даже через кипящую воду никакой реакции не происходит):
В лаборатории для получения простых веществ используют не обязательно природное сырьё, а выбирают те исходные вещества, из которых легче выделить необходимое вещество. Например, в лаборатории кислород не получают из воздуха. Это же относится и к получению водорода. Один из лабораторных способов получения водорода, который иногда применяется и в промышленности,— разложение воды электротоком.
Обычно в лаборатории водород получают взаимодействием цинка с соляной кислотой.
Получение водорода в промышленности
1.Электролиз водных растворов солей:
2NaCl +2H2O → H2↑ +2NaOH +Cl2
2.Пропускание паров воды над раскаленным коксом при температуре около 1000°C:
H2O +C ⇄ H2↑ +CO↑
3.Из природного газа.
Конверсия с водяным паром:
CH4 +H2O ⇄ CO↑ +3H2↑ (1000°C)
Каталитическое окисление кислородом:
2CH4 +O2 ⇄ 2CO↑ +4H2↑
4. Крекинг и риформинг углеводородов в процессе переработки нефти.
Получение водорода в лаборатории
1.Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную соляную кислоту:
Zn +2HCl → ZnCl2 +H2↑
3.Гидролиз гидридов:
NaH +H2O → NaOH +H2↑
Дополнительная информация про Водород
Биореактор для производства водорода
Физические свойства Водорода
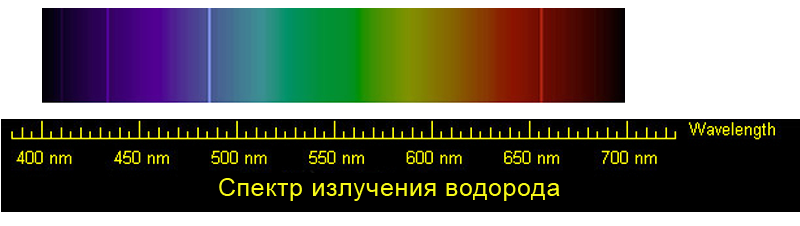
Спектр излучения водорода

Эмиссионный спектр водорода
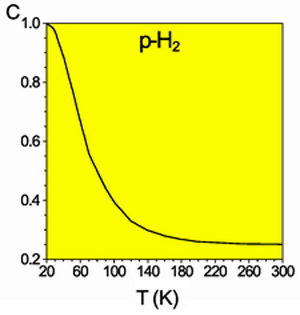
Равновесная мольная концентрация пара-водорода
Разделить модификации водорода можно адсорбцией на активном угле при температуре жидкого азота. При очень низких температурах равновесие между ортоводородом и параводородом почти нацело сдвинуто в сторону последнего. При 80 К соотношение форм приблизительно 1:1. Десорбированный параводород при нагревании превращается в ортоводород вплоть до образования равновесной при комнатной температуре смеси (орто-пара: 75:25). Без катализатора превращение происходит медленно (в условиях межзвездной среды— с характерными временами вплоть до космологических), что даёт возможность изучить свойства отдельных модификаций.
Водород — самый лёгкий газ, он легче воздуха в 14,5 раз. Очевидно, что чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха.
Молекула водорода двухатомна — Н2. При нормальных условиях — это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н.у.), температура кипения −252,76 °C, удельная теплота сгорания 120.9·10 6 Дж/кг, малорастворим в воде — 18,8 мл/л. Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов на 1объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
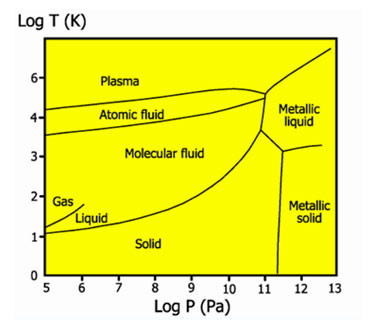
Фазовая диаграмма водорода
Жидкий водород существует в очень узком интервале температур от −252,76 до −259,2 °C. Это бесцветная жидкость, очень лёгкая (плотность при −253 °C 0,0708 г/см3) и текучая (вязкость при −253 °C 13,8 спуаз). Критические параметры водорода очень низкие: температура −240,2 °C и давление 12,8 атм. Этим объясняются трудности при ожижении водорода. В жидком состоянии равновесный водород состоит из 99,79% пара-Н2, 0,21% орто-Н2.
Твердый водород, температура плавления −259,2 °C, плотность 0,0807 г/см3 (при −262 °C) — снегоподобная масса, кристаллы гексогональной сингонии, пространственная группа P6/mmc, параметры ячейки a=3,75 c=6,12. При высоком давлении водород переходит в металлическое состояние.
Изотопы
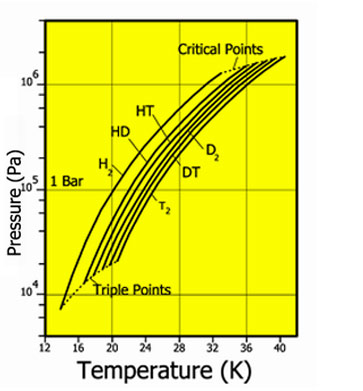
Давление пара для различных изотопов водорода
Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: 1 H— протий (Н), 2 Н— дейтерий (D), 3 Н— тритий (радиоактивный) (T).
Протий и дейтерий являются стабильными изотопами с массовыми числами 1и 2. Содержание их в природе соответственно составляет 99,9885±0,0070% и 0,0115 ± 0,0070%. Это соотношение может незначительно меняться в зависимости от источника и способа получения водорода.
Изотоп водорода 3 Н (тритий) нестабилен. Его период полураспада составляет 12,32 лет. Тритий содержится в природе в очень малых количествах.
В литературе также приводятся данные об изотопах водорода с массовыми числами 4— 7и периодами полураспада 10 −22 — 10 −23 с.
Природный водород состоит из молекул H2 и HD (дейтероводород) в соотношении 3200:1. Содержание чистого дейтерийного водорода D2 ещё меньше. Отношение концентраций HD и D2, примерно, 6400:1.
Из всех изотопов химических элементов физические и химические свойства изотопов водорода отличаются друг от друга наиболее сильно. Это связано с наибольшим относительным изменением масс атомов.
| Температура плавления, K | Температура кипения, K | Тройная точка, K /kPa | Критическая точка, K /kPa | Плотность жидкий /газ, кг/м³ | |
|---|---|---|---|---|---|
| H2 | 13.95 | 20,39 | 13,96 /7,3 | 32,98 /1,31 | 70,811 /1,316 |
| HD | 16,60 | 22,13 | 16,60 /12,8 | 35,91 /1,48 | 114,80 /1,802 |
| HT | 22,92 | 17,63 /17,7 | 37,13 /1,57 | 158,62 /2,310 | |
| D2 | 18,62 | 23,67 | 18,73 /17,1 | 38,35 /1,67 | 162,50 /2,230 |
| DT | 24.38 | 19,71 /19,4 | 39,42 /1,77 | 211,54 /2,694 | |
| T2 | 25,04 | 20,62 /21,6 | 40,44 /1,85 | 260,17 /3,136 |
Дейтерий и тритий также имеют орто- и пара- модификации: p-D2, o-D2, p-T2, o-T2. Гетероизотопный водород (HD, HT, DT) не имеют орто- и пара- модификаций.
Химические свойства
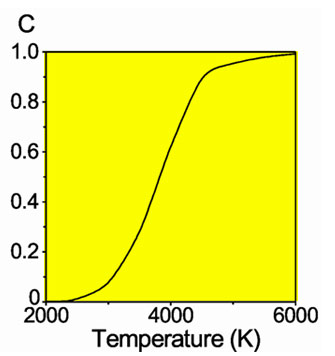
Доля диссоциировавших молекул водорода
Молекулы водорода Н2 довольно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция:
и с единственным неметаллом— фтором, образуя фтороводород:
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например при освещении:
Он может «отнимать» кислород от некоторых оксидов, например:
Записанное уравнение отражает восстановительные свойства водорода.
С галогенами образует галогеноводороды:
F2 +H2 → 2HF, реакция протекает со взрывом в темноте и при любой температуре, Cl2 +H2 → 2HCl, реакция протекает со взрывом, только на свету.
С сажей взаимодействует при сильном нагревании:
Взаимодействие со щелочными и щёлочноземельными металлами
При взаимодействии с активными металлами водород образует гидриды:
Гидриды— солеобразные, твёрдые вещества, легко гидролизуются:
Взаимодействие с оксидами металлов (как правило, d-элементов)
Оксиды восстанавливаются до металлов:
Гидрирование органических соединений
Молекулярный водород широко применяется в органическом синтезе для восстановления органических соединений. Эти процессы навзывают реакциями гидрирования. Эти реакции проводят в присутствии катализатора при повышенных давлении и температуре. Катализатор может быть как гомогенным (напр. Катализатор Уилкинсона), так и гетерогенным (напр. никель Ренея, палладий на угле).
Так, в частности, при каталитическом гидрировании ненасыщенных соединений, таких как алкены и алкины, образуются насыщенные соединения — алканы.
Геохимия водорода
На Земле содержание водорода понижено по сравнению с Солнцем, гигантскими планетами и первичными метеоритами, из чего следует, что во время образования Земля была значительно дегазирована и водород вместе с другими летучими элементами покинул планету во время аккреции или вскоре после неё.
Свободный водород H2 относительно редко встречается в земных газах, но в виде воды он принимает исключительно важное участие в геохимических процессах.
В состав минералов водород может входить в виде иона аммония, гидроксил-иона и кристаллической воды.
В атмосфере водород непрерывно образуется в результате разложения воды солнечным излучением. Имея малую массу, молекулы водорода обладают высокой скоростью диффузионного движения (она близка ко второй космической скорости) и, попадая в верхние слои атмосферы, могут улететь в космическое пространство.