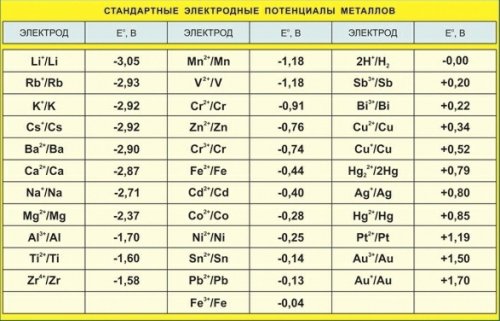
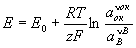в чем измеряется электродный потенциал
Электродный потенциал
Электро́дный потенциа́л — разность электрических потенциалов между электродом и находящимся с ним в контакте электролитом (чаще всего между металлом и раствором электролита).
Возникновение электродного потенциала обусловлено переносом заряженных частиц через границу раздела фаз, специфической адсорбцией ионов, а при наличии полярных молекул (в том числе молекул растворителя) — ориентационной адсорбцией их. Величина электродного потенциала в неравновесном состоянии зависит как от природы и состава контактирующих фаз, так и от кинетических закономерностей электродных реакций на границе раздела фаз.
Равновесное значение скачка потенциалов на границе раздела электрод/раствор определяется исключительно особенностями электродной реакции и не зависит от природы электрода и адсорбции на нём поверхностно-активных веществ. Эту абсолютную разность потенциалов между точками, находящимися в двух разных фазах, нельзя измерить экспериментально или рассчитать теоретически.
Измерение потенциалов
Практическое значение имеют относительные электродные потенциалы, обычно называемые просто электродные потенциалы, представляющие собой разность электродных потенциалов рассматриваемого электрода и электрода сравнения — чаще всего нормального водородного электрода, электродный потенциал которого условно принимается равным нулю (для водных систем).
Способы устранения омической составляющей при измерении
См. также
Полезное
Смотреть что такое «Электродный потенциал» в других словарях:
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ — разность электрических потенциалов (напряжений) между электродом и находящимся с ним в контакте электролитом. Появление Э. п. вызвано образованием у поверхности электрода двойного электрического слоя. На практике используют значения так… … Большая политехническая энциклопедия
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ — в электрохимии разность электрических потенциалов на границе фаз электрод электролит. На практике пользуются значениями т. н. относительного электродного потенциала, равного разности электродного потенциала, данного электрода и электрода… … Большой Энциклопедический словарь
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ — ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ, мера способности электрода вступать в реакцию. Электрод из элемента М, помещенный в раствор его ионов (М+), представляет собой ПОЛУЭЛЕМЕНТ. Теоретически в ходе реакций типа ММ++е между электродом и раствором всегда… … Научно-технический энциклопедический словарь
Электродный потенциал — мера способности электрода вступать в реакцию. Между электродом и раствором всегда образуется разность потенциалов. Стандартные потенциалы электродов определяют относительно водородного электрода при определенных величинах температуры,… … Официальная терминология
электродный потенциал — — [Я.Н.Лугинский, М.С.Фези Жилинская, Ю.С.Кабиров. Англо русский словарь по электротехнике и электроэнергетике, Москва, 1999 г.] Тематики электротехника, основные понятия EN electrode potentialelectrolytic potentialelectropolarization… … Справочник технического переводчика
электродный потенциал — [electrode potential] разность электрических потенциалов между электродами и находящимся с ним в контакте электролитом (чаще всего между металлом и раствором электролита). Практическое значение имеют относительные электродные потенциалы,… … Энциклопедический словарь по металлургии
электродный потенциал — 3.8 электродный потенциал: Мера способности электрода вступать в реакцию. Между электродом и раствором всегда образуется разность потенциалов. Стандартные потенциалы электродов определяют относительно водородного электрода при определенных… … Словарь-справочник терминов нормативно-технической документации
Электродный потенциал — Electrode potential Электродный потенциал. Потенциал электрода в электролизе измеренный относительно электрода сравнения. В электродный потенциал не входят потери противодействия потенциалу, как в растворе, так и внешней цепи. Он представляет… … Словарь металлургических терминов
электродный потенциал — elektrodo potencialas statusas T sritis Standartizacija ir metrologija apibrėžtis Dydis, išreiškiamas potencialų skirtumu, susidarančiu tarp joninės terpės (elektrolito tirpalo ar lydalo) ir į ją įdėto elektrodo. atitikmenys: angl. electrode… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
электродный потенциал — elektrodo potencialas statusas T sritis Standartizacija ir metrologija apibrėžtis Elektrodo potencialas kito kūno arba terpės, kurioje jis yra, atžvilgiu. atitikmenys: angl. electrode potential vok. Elektrodenpotential, n rus. потенциал электрода … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Электродный потенциал. Измерение электродных потенциалов



Электрохимические системы
Общая характеристика
Гальванические элементы используются как автономные и малогабаритные источники энергии для машин, радиотехнических устройств и приборов управления. При помощи электролиза получают различные вещества, обрабатывают поверхности, создают изделия нужной формы.
Электрохимические процессы не всегда служат на пользу человеку, а иногда приносят большой вред, вызывая усиленную коррозию и разрушение металлических конструкций. Чтобы умело использовать электрохимические процессы и бороться с нежелательными явлениями, их надо изучить и уметь регулировать.
Причиной возникновения электрохимических явлений служит переход электронов или изменение степени окисления атомов веществ, участвующих в электрохимических процессах, то есть окислительно-восстановительные реакции, протекающие в гетерогенных системах. В окислительно-восстановительных реакциях электроны непосредственно переходят от восстановителя к окислителю. Если процессы окисления и восстановления пространственно разделить, а электроны направить по металлическому проводнику, то такая система будет представлять собой гальванический элемент. Причиной возникновения и протекания электрического тока в гальваническом элементе является разность потенциалов.
Электродный потенциал. Измерение электродных потенциалов
Если взять пластину какого либо металла и опустить ее в воду, то ионы поверхностного слоя под действием полярных молекул воды отрываются и гидратированными переходят в жидкость. В результате такого перехода жидкость заряжается положительно, а металл отрицательно, поскольку на нем появляется избыток электронов. Накопление ионов металла в жидкости начинает тормозить растворение металла. Устанавливается подвижное равновесие
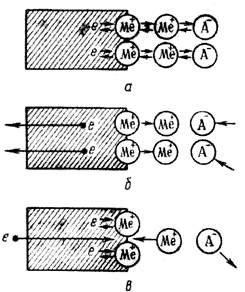
Рис. Процесс перехода иона из металла в раствор:
а – равновесие; б – растворение; в – осаждение
Потенциал каждого электрода зависит от природы металла, концентрации его ионов в растворе и температуры. Если металл опустить в раствор его соли, содержащей один моль-ион металла на 1 дм 3 (активность которого равна 1), то электродный потенциал будет постоянной величиной при температуре 25 о С и давлении 1 атм. Такой потенциал называется стандартным электродным потенциалом (Е о ).
Ионы металла, имеющие положительный заряд, проникая в раствор и перемещаясь в поле потенциала границы раздела металл-раствор, затрачивают энергию. Эта энергия компенсируется работой изотермического расширения от большей концентрации ионов на поверхности к меньшей в растворе. Положительные ионы накапливаются в приповерхностном слое до концентрации со, а затем уходят в раствор, где концентрация свободных ионов с. Работа электрического поля ЕnF равна изотермической работе расширения RTln(сo/с). Приравняв оба выражения работы можно вывести величину потенциала
где Е – потенциал металла, В; R – универсальная газовая постоянная, Дж/моль К; Т – температура, K; n – заряд иона; F – число Фарадея; с – концентрация свободных ионов;
со– концентрация ионов в поверхностном слое.
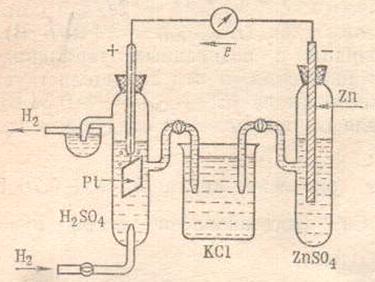
Непосредственно измерить величину потенциала не представляется возможным, так как невозможно экспериментально определить со. Опытным путем определяют величины электродных потенциалов относительно величины другого электрода, потенциал которого условно принимают равным нулю. Таким стандартным электродом или электродом сравнения является нормальный водородный электрод (н.в.э.). Устройство водородного электрода показано на рисунке. Он состоит из платиновой пластинки, покрытой электролитически осаждённой платиной. Электрод погружен в 1М раствор серной кислоты (активность ионов водорода равна 1 моль/дм 3 ) и омывается струей газообразного водорода под давлением 101 кПа и Т = 298 К. При насыщении платины водородом на поверхности металла устанавливается равновесие, суммарный процесс выражается уравнением
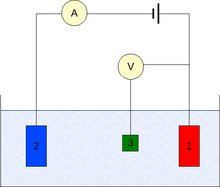
Если пластинку металла, погруженного в 1М раствор соли этого металла, соединить внешним проводником со стандартным водородным электродом, а растворы электролитическим ключом, то получим гальванический элемент (рис. 32). Электродвижущая сила этого гальванического элемента будет являться величиной стандартного электродного потенциала данного металла (Е о ).
Схема измерения стандартного электродного потенциала
относительно водородного электрода
Взяв в качестве электрода цинк находящийся в 1 М растворе сульфата цинка и соединив его с водородным электродом, получим гальванический элемент, схему которого запишем следующим образом
В схеме одна черта означает границу раздела между электродом и раствором, две черты – границу между растворами. Анод записывается слева, катод справа. В таком элементе осуществляется реакция Zn о + 2H + = Zn 2+ + Н2, а электроны по внешней цепи переходят от цинкового к водородному электроду. Стандартный электродный потенциал цинкового электрода (-0,76 В).
Взяв в качестве электрода медную пластинку, при указанных условиях в сочетании со стандартным водородным электродом, получим гальванический элемент
Что такое электродный потенциал
Явления растворения металлов в электролитах используются в химических источниках электроэнергии. Металлическая пластина, опушенная в раствор своей же соли, в той или иной мере стремится в ней раствориться. Это стремление иногда называется упругостью растворения металла.
Эти заряды будут противодействовать дальнейшему переходу металла в раствор — отрицательные пластины удерживают положительный ион металла, а положительный заряд электролита отталкивает ион металла назад на пластину. Иными словами, электрическое поле двойного слоя на границе металл — жидкость противодействует дальнейшему переходу ионов металла в раствор. Устанавливается равновесие между химическими по своей природе силами стремления металла перейти в раствор и электрическими силами, им противодействующими.
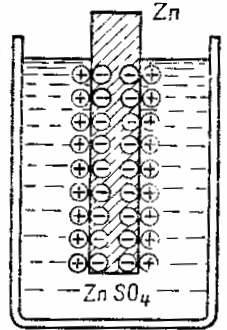
Схема образования двойного электрического слоя на границе металла и электролита
Таким образом, вследствие растворения в электролите металлический электрод приобретает по отношению к электролиту определенный электродный (иначе электрохимический) потенциал, зависящий от материала электрода и состава электролита.
Однако электродные потенциалы могут иметь положительное значение. Это имеет место в тех случаях, когда положительные ионы раствора переходят на электрод, заряжая его положительно, а слой электролита — отрицательно, например, когда медная пластина погружена в достаточно концентрированный раствор сернокислой меди (CuSO4).
Двойной электрический слой можно уподобить конденсатору, одна из обкладок которого представляет собой поверхность металла, а другая — слой ионов в растворе у поверхности металла. Между разноименно заряженными обкладками и возникает разность, или скачок, потенциала.
Скачок потенциала на границе электрод-раствор может служить мерой окислительно-восстановительной способности системы. Однако невозможно произвести измерение такого скачка потенциала или, что то же, разности потенциалов между двумя фазами. Но можно произвести измерение э. д. с. элементов, составленных из интересующих нас электродов и какого-нибудь одного (одинакового во всех случаях) электрода, потенциал которого условно принят за нуль.
Измеренная э. д. с. будет характеризовать окислительно-восстановительную способность интересующего нас электрода относительно некоторого условного нуля. Полученная таким способом величина называется собственным потенциалом металла.
Чтобы измерить электродный потенциал любого металла, необходимо поместить в электролит второй электрод, который и свою очередь будет обладать определенным электродным потенциалом, зависящим от его материала. Следовательно, непосредственно измерить можно только алгебраическую сумму двух электродных потенциалов.
По этой причине электродные потенциалы различных материалов определяются по отношению к стандартному (водородному электроду, потенциал которого условно принимают за нуль.
Для измерения могут применяться и другие электроды сравнения, потенциал которых относительно водородного стандартного электрода известен. Этот потенциал также находят на основании измерения э. д. с. цепи, составленной из выбранного электрода сравнения и стандартного водородного электрода.
Если в соответствующий электролит помещены две пластины из металлов, имеющих различный электродный потенциал, например, в раствор серной кислоты (H2SO4) помещены цинковая (Zn) и медная (С u ) пластины, то вольтметр, присоединенный к этим пластинам, покажет между ними напряжение немного более 1 В.
Это напряжение, называемое в данном случае э. д. с. гальванической пары, будет обусловлено разностью электродных потенциалов меди, обладающей небольшим положительным потенциалам, и цинка, обладающего значительным отрицательным потенциалом. Такое устройство является простейшим гальваническим элементом — элементом Вольта.
В гальваническом элементе происходит превращение химической энергии в электрическую и с его помощью можно совершить электрическую работу за счет энергии химической реакции.
Измерение э. д. с. гальванических элементов необходимо производить при отсутствии тока в цепи элемента. В противном случае измеренная э. д. с. будет меньше, чем величина, определяемая как разность равновесных потенциалов обоих электродов. Действительно, равновесному потенциалу отвечает определенная концентрация электронов на электродах: на более положительном она ниже, на более отрицательном выше. Сообразно с этим различно и строение той части двойного слоя, которая расположена в растворе.
Измерение э. д. с. элемента без протекания тока обычно производится компенсационным методом. Для осуществления его необходимо иметь некоторый эталон э. д. с. Таким эталоном служит так называемый нормальный элемент. Чаще всего пользуются ртутно-кадмиевым нормальным элементом Вестона, э. д. с. которого равна 1,01830 В при 20 °С.
Если Вам понравилась эта статья, поделитесь ссылкой на неё в социальных сетях. Это сильно поможет развитию нашего сайта!
Подписывайтесь на наш канал в Telegram!
Просто пройдите по ссылке и подключитесь к каналу.
Не пропустите обновления, подпишитесь на наши соцсети:
Электродный потенциал
Полезное
Смотреть что такое «Электродный потенциал» в других словарях:
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ — разность электрических потенциалов (напряжений) между электродом и находящимся с ним в контакте электролитом. Появление Э. п. вызвано образованием у поверхности электрода двойного электрического слоя. На практике используют значения так… … Большая политехническая энциклопедия
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ — в электрохимии разность электрических потенциалов на границе фаз электрод электролит. На практике пользуются значениями т. н. относительного электродного потенциала, равного разности электродного потенциала, данного электрода и электрода… … Большой Энциклопедический словарь
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ — ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ, мера способности электрода вступать в реакцию. Электрод из элемента М, помещенный в раствор его ионов (М+), представляет собой ПОЛУЭЛЕМЕНТ. Теоретически в ходе реакций типа ММ++е между электродом и раствором всегда… … Научно-технический энциклопедический словарь
Электродный потенциал — мера способности электрода вступать в реакцию. Между электродом и раствором всегда образуется разность потенциалов. Стандартные потенциалы электродов определяют относительно водородного электрода при определенных величинах температуры,… … Официальная терминология
электродный потенциал — — [Я.Н.Лугинский, М.С.Фези Жилинская, Ю.С.Кабиров. Англо русский словарь по электротехнике и электроэнергетике, Москва, 1999 г.] Тематики электротехника, основные понятия EN electrode potentialelectrolytic potentialelectropolarization… … Справочник технического переводчика
электродный потенциал — [electrode potential] разность электрических потенциалов между электродами и находящимся с ним в контакте электролитом (чаще всего между металлом и раствором электролита). Практическое значение имеют относительные электродные потенциалы,… … Энциклопедический словарь по металлургии
электродный потенциал — 3.8 электродный потенциал: Мера способности электрода вступать в реакцию. Между электродом и раствором всегда образуется разность потенциалов. Стандартные потенциалы электродов определяют относительно водородного электрода при определенных… … Словарь-справочник терминов нормативно-технической документации
Электродный потенциал — У этого термина существуют и другие значения, см. Потенциал. Электродный потенциал разность электрических потенциалов между электродом и находящимся с ним в контакте электролитом (чаще всего между металлом и раствором электролита). Возникновение… … Википедия
Электродный потенциал — Electrode potential Электродный потенциал. Потенциал электрода в электролизе измеренный относительно электрода сравнения. В электродный потенциал не входят потери противодействия потенциалу, как в растворе, так и внешней цепи. Он представляет… … Словарь металлургических терминов
электродный потенциал — elektrodo potencialas statusas T sritis Standartizacija ir metrologija apibrėžtis Dydis, išreiškiamas potencialų skirtumu, susidarančiu tarp joninės terpės (elektrolito tirpalo ar lydalo) ir į ją įdėto elektrodo. atitikmenys: angl. electrode… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
электродный потенциал — elektrodo potencialas statusas T sritis Standartizacija ir metrologija apibrėžtis Elektrodo potencialas kito kūno arba terpės, kurioje jis yra, atžvilgiu. atitikmenys: angl. electrode potential vok. Elektrodenpotential, n rus. потенциал электрода … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Стандартный электродный потенциал
Содержание
Вычисление стандартных электродных потенциалов
Электродный потенциал не может быть получен эмпирически. Потенциал гальванической ячейки вытекает из «пары» электродов. Таким образом, невозможно определить величину для каждого электрода в паре, используя эмпирически полученный потенциал гальванической ячейки. Для этого установлен водородный электрод, для которого этот потенциал точно определён и равен 0,00 В, и любой электрод, для которого электронный потенциал ещё неизвестен, может быть соотнесён со стандартным водородным электродом с образованием гальванической ячейки — и в этом случае потенциал гальванической ячейки даёт потенциал неизвестного электрода.
Так как электродные потенциалы традиционно определяют как восстановительные потенциалы, знак окисляющегося металлического электрода должен быть изменён на противоположный при подсчёте общего потенциала ячейки. Также нужно иметь в виду, что потенциалы не зависят от количества передаваемых электронов в полуреакциях (даже если оно различно), так как они рассчитаны на 1 моль переданных электронов. Отсюда при расчёте какого-либо электродного потенциала на основании двух других следует проявлять внимательность.
Fe 3+ + 3e − → Fe(тв) −0.036 В
Fe 2+ + 2e − → Fe(тв) −0.44 В
Для получения третьего уравнения:
Fe 3+ + e − → Fe 2+ (+0.77 В)
следует умножить потенциал первого уравнения на 3, перевернуть второе уравнение(поменять знак) и умножить его потенциал на 2. Сложение этих двух потенциалов даст стандартный потенциал третьего уравнения.
Таблица стандартных электродных потенциалов
В гальванической ячейке, где самопроизвольная окислительно-восстановительная реакция заставляет ячейку производить электрический потенциал, Энергия Гиббса ΔG o должна быть отрицательной, в соответствии со следующим уравнением:
где n это количество молей электронов на моль продуктов, а F является постоянной Фарадея,
96485 Кл/моль. Таким образом применимы следующие правила:
если E o яч> 0, тогда процесс самопроизвольный (гальваническая ячейка) если E o яч
Нестандартные условия
Стандартные электродные потенциалы даны при стандартных условиях. Однако, реальные ячейки могут действовать и при нестандартных условиях. При данном стандартном потенциале, потенциал при нестандартных эффективных концентрациях может быть вычислен с использованием уравнения Нернста:
Величины E 0 зависят от температуры (кроме стандартного водородного электрода) и обычно относятся к стандартному водородному электроду при этой температуре. Для конденсированных фаз величины потенциалов также зависят от давления.
См. также
Литература
Ссылки
Полезное
Смотреть что такое «Стандартный электродный потенциал» в других словарях:
СТАНДАРТНЫЙ ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ — (нормальный электродный потенциал) потенциал электрода в растворе, в котором ионы, определяющие электродный процесс, имеют активность, равную единице. Стандартный потенциал данного электрода измеряется относительно стандартного (нормального)… … Большая политехническая энциклопедия
стандартный электродный потенциал — standartinis elektrodo potencialas statusas T sritis chemija apibrėžtis Potencialų skirtumas, susidarantis metalui arba nemetalui liečiantis su tirpalu, kurio elektrochemiškai veiklių jonų koncentracija 1 mol/l. atitikmenys: angl. standard… … Chemijos terminų aiškinamasis žodynas
Стандартный электродный потенциал — Standard electrode potential Стандартный электродный потенциал. Обратимый потенциал для электродного процесса, где все продукты и реакции находятся на шкале активности, на которой потенциал полуэлемента водорода равен нулю. (Источник: «Металлы и… … Словарь металлургических терминов
Электродный потенциал — У этого термина существуют и другие значения, см. Потенциал. Электродный потенциал разность электрических потенциалов между электродом и находящимся с ним в контакте электролитом (чаще всего между металлом и раствором электролита). Возникновение… … Википедия
Нормальный электродный потенциал — В электрохимии стандартный электродный потенциал, обозначаемый Eo, E0, или EO, является мерой индивидуального потенциала обратимого электрода (в равновесии) в стандартном состоянии, которое осуществляется в растворах при эффективной концентрации… … Википедия
нормальный электродный потенциал — standartinis elektrodo potencialas statusas T sritis chemija apibrėžtis Potencialų skirtumas, susidarantis metalui arba nemetalui liečiantis su tirpalu, kurio elektrochemiškai veiklių jonų koncentracija 1 mol/l. atitikmenys: angl. standard… … Chemijos terminų aiškinamasis žodynas
Потенциал электростатический — Классическая электродинамика Магнитное поле соленоида Электричество · Магнетизм Электростатика Закон Кулона … Википедия
СТАНДАРТНЫЙ ЭЛЕКТРОД — (эталонный ЭЛЕКТРОД), в ЭЛЕКТРОХИМИИ ПОЛУЭЛЕМЕНТ, состоящий из других полуэлементов и служащий эталоном. Главным стандартным электродом является водородный электрод платиновый электрод, погруженный в молярный раствор ионов водорода и покрытый… … Научно-технический энциклопедический словарь
Электростатический потенциал — У этого термина существуют и другие значения, см. Потенциал. Классическая электродинамика … Википедия
Окислительно-восстановительный потенциал — (редокс потенциал от англ. redox reduction oxidation reaction, Eh или Eh) мера способности химического вещества присоединять электроны (восстанавливаться[1]). Окислительно восстановительный потенциал выражают в милливольтах (мВ).… … Википедия