в чем хранить жидкий кислород
Физические свойства кислорода
Где бы мы ни находились, нас всюду окружает кислород воздуха.
Почему же мы не замечаем и не чувствуем его? Кислород, азот, аргон и другие газы, входящие в состав воздуха, бесцветны и не имеют ни запаха, ни вкуса. Газообразный воздух нельзя ни видеть, ни ощущать.
Воздух из газообразного состояния можно перевести в жидкое. Одновременно с основной массой воздуха — азотом — в жидкое состояние перейдут кислород и большинство других газов, входящих в его состав.
Чтобы газообразный кислород превратить в жидкость, его нужно сжать до 50 атмосфер и охладить до —119°.
Жидкий кислород можно получить и при атмосферном давлении, но для этого нужно газообразный кислород охладить до температуры —183°. При более сильном охлаждении, до температуры —220°, жидкий кислород затвердевает и превращается в снегообразную массу.
Если на некоторое время в жидкий кислород поместить кусочек резины, она потеряет свою эластичность и под ударом разлетится на мелкие части.
Такую же хрупкость приобретает и цинковая пластинка, охлажденная в жидком кислороде до температуры —183°. Жидкая ртуть при такой температуре превращается в твердую массу, которую можно ковать, как свинец, а свинец приобретает способность звенеть, как бронзовый колокольчик.
Жидкий кислород имеет голубоватый цвет. Его можно легко переливать из сосуда в сосуд. При переливании жидкий кислород «парит». Но это не пары кислорода, а пары воды. Жидкий кислород, испаряясь, поглощает много тепла из окружающего воздуха. Воздух сильно охлаждается, и влага, находящаяся в воздухе, конденсируется, образуя туман. Этот туман и создает впечатление пара, исходящего из самой жидкости.
Температура кипения жидкого кислорода равна —183°.
Если фарфоровый стакан с жидким кислородом вынести зимой на мороз 30—40°, он будет кипеть более бурно, чем вода на самом сильном огне газовой плиты.
При комнатной температуре испарение жидкого кислорода идет еще энергичнее, и он быстро переходит в газообразное состояние.
Чтобы использовать жидкий кислород, его необходимо сохранить. Как же заставить эту бурно кипящую жидкость не так быстро испаряться?
Для этого служат специальные сосуды, в которых легко удается «укротить» эту быстро испаряющуюся жидкость.
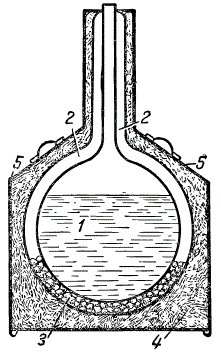
Стеклянный сосуд для хранения небольшого количества жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — поверхности, посеребренные внутри.
Сосуд для хранения жидкого кислорода представляет собой цилиндр с двойными стенками. Внутренние стороны стенок обычно покрывают тонким слоем серебра. Воздух между стенками сосуда выкачивается.
Разреженные газы плохо проводят тепло, а зеркальная поверхность серебра хорошо отражает его. Таким образом, жидкий кислород, который находится в сосуде, изолирован от внешнего тепла, что обеспечивает сохранение жидкого кислорода в течение одних-двух суток.
При испарении жидкого кислорода объем его увеличивается почти в 800 раз. Из кубического сантиметра жидкого кислорода образуется около 800 кубических сантиметров газообразного.
Хранить жидкий кислород в закрытых сосудах опасно: внутри сосуда может образоваться большое давление, приводящее к взрыву. Поэтому сосуды для хранения жидкого кислорода сверху открыты. Воздух, находящийся над жидкостью, сильно охлаждается и предохраняет кислород от наружного тепла, замедляя дальнейшее испарение.
Для перевозки небольших количеств жидкого кислорода используют металлические емкостью 15—25 литров.
Металлические сосуды состоят из двух шаров или цилиндров, вставленных друг в друга. Внутренний шар или цилиндр имеет высокое и узкое горло, через которое сосуд заполняется жидким кислородом. Горло всегда остается открытым. Из пространства между стенками сосуда воздух выкачан, и создан высокий вакуум, то есть сильное разрежение.
Металлический сосуд для перевозки жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — силикагель; 4 — теплоизоляционный материал; 5 — железный цилиндр.
Чтобы поддержать высокий вакуум, часть пространства между стенками заполняется силикагелем, способным при низкой температуре поглощать количество газа в сотни раз больше своего собственного объема. Если через стенки или через места спайки со временем просочится небольшая часть воздуха, он поглотится силикагелем и разрежение не уменьшится. Высокий вакуум обеспечивает постоянную изоляцию сосуда от внешнего тепла и дает возможность в течение двух и более суток сохранять в нем жидкий кислород. Такие сосуды обычно помещают в железные цилиндры.
Пространство между сосудом и наружным цилиндром заполняют теплоизоляционным материалом. Для переноски на наружном цилиндре имеются ручки.
Большие количества жидкого кислорода перевозятся по железной дороге и автотранспортом в специальных цистернах или танках. Они хорошо изолированы от внешнего тепла. Емкость транспортных танков различна: от 1 тысячи до 10 тысяч литров. Цистерны, в которых жидкий кислород перевозят по железной дороге, вмещают до нескольких десятков тонн.
Жидкий кислород можно получить из жидкого воздуха, который образуется при низких температурах и высоком давлении.
Высокое давление создают в машинах, которые называются компрессорами. Их приводят в движение электродвигатели.
Источник: В. Медведовский. Кислород. Государственное Издательство Детской литературы Министерства Просвещения РСФСР. Ленинград. Москва. 1953
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Как перевозят жидкий кислород: правила транспортировки газа и типы автоцистерн
Жидкий кислород относится к веществам второго класса опасности, и для его транспортировки необходимо соблюдение правил как в части организации перевозки, так и в части требований к техническому оснащению транспортного средства. О тонкостях доставки этого газа читайте в нашей статье.
Правила перевозки
жидкого кислорода
В малых объемах жидкий кислород можно перевозить в баллонах, сосудах Дьюара или криоцилиндрах. Для транспортировки больших объемов газа используют специальные емкости – криогенные транспортные цистерны, которые (в зависимости от своей конструкции) могут быть установлены в кузове бортового автомобиля, на шасси полуприцепа или на контейнеровозе.
Обязательно нужно учесть, что если объем газа превышает 1000 литров на один автомобиль, то груз попадает под требования ДОПОГ и транспортировать сжиженный кислород можно только по правилам перевозки опасных грузов.
Требования ДОПОГ включают в себя следующие пункты:
Ограничения по весу транспортного средства
При эксплуатации любого транспортного средства, предназначенного для транспортировки жидкого кислорода (будь то самостоятельный грузовой автомобиль или тягач с полуприцепом) обязательно следует учитывать следующие характеристики:
Поэтому при заказе автоцистерны стоит заранее выяснить, сколько жидкого кислорода она сможет перевозить с учетом вместимости и допустимой нагрузки. Так, максимально возможный вес кислорода, который может за один маршрут перевезти полуприцеп-цистерна от «Техгаз-ТК» заводской марки ASTRA-M, составляет 22 тонны.
Виды транспортных средств
для перевозки жидкого кислорода

— металлообрабатывающим предприятиям;
— больницам или другим медицинским учреждениям.
Такие криогенные цистерны можно самостоятельно возить на заправку в специальные пункты, что снижает зависимость предприятия от внешних поставщиков кислорода.
Посмотреть решения
Такое оборудование чаще всего приобретают производители медицинского и/или технического кислорода, транспортные компании, которые оказывают услуги по перевозке сжиженного газа, а также представители региональной власти.
Посмотреть решения

— Высокая скорость погрузки и выгрузки цистерны;
— Дополнительная защита криогенной емкости, что особенно актуально при переброске с одного вида транспорта на другой;
— Цистерну в контейнере можно использовать отдельно от контейнеровоза, например, в качестве временного хранилища.
Посмотреть решения
Если вы ищите надежную криогенную транспортную цистерну или полуприцеп-цистерну для транспортировки жидкого кислорода, обращайтесь напрямую к заводу-изготовителю «Техгаз-ТК»!
Контакты и обратная связь
Екатеринбург
ул. Машинная 42а, офис 1101
Работаем с 9:00 до 17:00, суббота и воскресенье — выходные дни.
Кислород медицинский
Срок годности Кислорода медицинского
Запрещается применять кислород жидкий медицинский по истечении срока годности.
Сроки годности указаны на упаковке. Медицинский кислород взрывоопасен, поэтому хранить его при высокой температуре запрещено. Низкие температуры сильно не влияют на качество.
Кислород медицинский можно использовать за 5-10 дней до окончания срока годности. В этот период он не нанесет вред здоровью.
Просроченный медицинский кислород улетучивается, упаковка может быть не герметичной.
Кислород медицинский нельзя использовать если:
Кислород медицинский нельзя использовать после окончания срока годности, т.к. он утрачивает свои лекарственные свойства.
Длительный период хранения обусловлен медленным распадом кислорода.
Как хранить в домашних условиях
Условия хранения:
Важно хранить кислород медицинский на максимально открытой местности, вдали огня, обогревателей и детей.
Кислород хранится исключительно в заводской упаковке.
Нельзя хранить кислород:
Аналогов Кислорода медицинского не имеется.
Как хранить кислородную подушку
После процедуры изделие необходимо наполнить кислородом и хранить при температуре в пределах +1…+25 градусов и влажности – не менее 65%.
Когда лечебная смесь в подушке закончится, ее нельзя оставлять пустой, так как стенки подушки могут склеиться, после чего подушка станет непригодной.
Кислородная подушка не должна находиться рядом с бытовыми приборами, выделяющими тепло. Подальше ее нужно держать и от горюче-смазочных веществ.
Правила хранения в аптеках и клиниках
Кислород медицинский утилизируется на фабриках по производству лекарств, у которых есть на это разрешение. Это регламентировано СанПинН 2.1.7.2790-1. В случае выявления некачественных баллонов или подушек составляется акт на возврат товара.
Согласно ФЗ N61 «Об обращении лекарственных средств» от 12.04.2010, газовые баллоны перевозятся отдельно от остальных лекарственных средств. Перевозятся только в сухую погоду крытым транспортом. Баллоны должны плотно прилегать друг к другу, чтобы избежать падения и возможного взрыва.
Жидкий кислород. Общие сведения
Газ кислород
Кислород – один из важнейших элементов на планете. Он участвует в процессе дыхания, в метаболизме живых организмов, а также в круговороте веществ в биосфере. Кроме того, он способствует гниению и разложению органических остатков.
В нормальных условиях он является бесцветным газом, который не имеет вкуса и запаха. Он тяжелее воздуха и с трудом растворяется в воде. В химическом плане он очень активен и способен образовывать соединения практически со всеми элементами.
В свободном состоянии в виде молекул О2, состоящих из двух атомов оксигена, он находится в атмосфере. Благодаря такому строению элемент также называется «дикислородом», но он может существовать и в других вариациях. При определенных условиях его атомы могут образовывать «трикислород» с молекулой О3, которая представляет собой голубой газ озон со специфическим запахом.
В атмосфере содержание кислорода составляет примерно 21 % по массе, в земной коре его доля значительно выше и составляет около 47 % по массе. Элемент входит в состав более полутора тысяч разнообразных пород и минералов, большая часть из которых являются силикатами. Там он присутствует в виде соединений. В воде его содержание доходит до 85 %, и это не удивительно, ведь атомы оксигена и образуют воду вместе с элементом гидрогеном.
Справка
Кислород — химический элемент с атомным номером 8, обозначающийся символом О, а также вещество (газ при нормальных условиях), молекула которого состоит из двух атомов кислорода (O2). Кислород является самым лёгким элементом из группы халькогенидов (6 группа периодической системы).
История открытия
Официально считается, что кислород был открыт английским химиком Джозефом Пристли 1 августа 1774 путём разложения оксида ртути в герметично закрытом сосуде (Пристли направлял на это соединение солнечные лучи с помощью мощной линзы).
Однако Пристли первоначально не понял, что открыл новое простое вещество, он считал, что выделил одну из составных частей воздуха (и назвал этот газ «дефлогистированным воздухом»). О своём открытии Пристли сообщил выдающемуся французскому химику Антуану Лавуазье.
Несколькими годами ранее (возможно, в 1770-м) кислород получил шведский химик Карл Шееле. Он прокаливал селитру с серной кислотой и затем разлагал получившийся оксид азота. Шееле назвал этот газ «огненным воздухом» и описал своё открытие в изданной в 1777 году книге (именно потому, что книга опубликована позже, чем сообщил о своём открытии Пристли, последний и считается первооткрывателем кислорода). Шееле также сообщил о своём опыте Лавуазье.
Важным этапом, который способствовал открытию кислорода, были работы французского химика Петра Байена, который опубликовал работы по окислению ртути и последующему разложению её оксида.
Наконец, окончательно разобрался в природе полученного газа А. Лавуазье, воспользовавшийся информацией от Пристли и Шееле. Его работа имела громадное значение, потому что благодаря ей была ниспровергнута господствовавшая в то время и тормозившая развитие химии флогистонная теория. [Лавуазье провел опыт по сжиганию различных веществ и опроверг теорию флогистона, опубликовав результаты по весу сожженных элементов. Вес золы превышал первоначальный вес элемента, что дало Лавуазье право утверждать, что при горении происходит химическая реакция (окисление) вещества, в связи с этим масса исходного вещества увеличивается, что опровергает теории флогистона.]
Таким образом, заслугу открытия кислорода фактически делят между собой Пристли, Шееле и Лавуазье.
Происхождение названия
Название oxygenium («кислород») происходит от греческих слов, обозначающих «рождающий кислоту»; это связано с первоначальным значением термина «кислота». Ранее этим термином называли оксиды.
Нахождение в природе
Получение
В настоящее время в промышленности жидкий кислород получают из воздуха. В лабораториях пользуются кислородом промышленного производства, поставляемым в стальных баллонах под давлением около 15 МПа. Важнейшим лабораторным способом его получения служит электролиз водных растворов щелочей. Небольшие количества кислорода можно также получать взаимодействием раствора перманганата калия с подкисленным раствором пероксида водорода.
Физические свойства
Газ без цвета, вкуса и запаха. Растворим в воде, причем растворяется тем лучше, чем ниже ее температура. Поэтому плотность живых организмов в холодных приполярных водах может быть значительно выше, чем в теплых экваториальных.
Химические свойства
Биологическая роль кислорода
Кислород участвует в окислительно-восстановительных реакциях. Живые существа дышат кислородом воздуха. Широко используется кислород в медицине. При сердечнососудистых заболеваниях, для улучшения обменных процессов, в желудок вводят кислородную пену («кислородный коктейль»). Подкожное введение кислорода используют при трофических язвах, слоновости, гангрене. Для обеззараживания и дезодорации воздуха и очистки питьевой воды применяют искусственное обогащение озоном. Радиоактивный изотоп кислорода 15O применяется для исследований скорости кровотока, лёгочной вентиляции.
Токсические производные кислорода
Некоторые производные кислорода (т. н. реактивные формы кислорода), такие как синглетный кислород, перекись водорода, супероксид, озон и гидроксильный радикал, являются высокотоксичными продуктами. Они образуются в процессе активирования или частичного восстановления кислорода. Супероксид (супероксидный радикал), перекись водорода и гидроксильный радикал могут образовываться в клетках и тканях организма человека и животных и вызывают оксидативный стресс.
предлагает оборудование для производства азота и технического кислорода
Жидкий кислород
В жидком состоянии кислород окрашивается в голубой оттенок и усиливает некоторые свойства газообразного вещества. Так, он ведет себя более агрессивно в химических реакциях, а также становится сильным парамагнетиком и может притягиваться магнитом.
Перевод жидкого кислорода в газообразный формула
Для превращения жидкого кислорода в газообразный служат газификационные установки. Их производительность достигает 15—20 м 3 /ч. Применяют два типа газификационных установок: насосные и безнасосные. Насосная газификационная установка СГУ-1, показанная на рис. 4, предназначена для газификации непереохлажденного кислорода и наполнения баллонов (реципиентов газообразным кислородом под давлением до 24 МПа (240 кгс/см 2 ). Кислород от реципиентов подается по трубопроводу к местам потребления через центральный рамповый редуктор под требуемым давлением порядка 1,2-2 МПа (15-20 кгс/см 2 ) для процессов газопламенной обработки. Имеются газификационные станции, насосы которых рассчитаны на давление 20 МПа (200 кгс/см 2 ) и служат для подачи кислорода в сеть через буферную емкость. В промышленности применяют также автомобильные передвижные газификационные установки.
Безнасосные газификаторы имеют рабочее давление до 1,6 МПа (16 кгс/см 2 ) при относительно постоянном и равномерном расходе кислорода, подаваемого по трубопроводу к местам потребления (рис. 5). Сосуд газификатора снабжен вакуумно-порошковой изоляцией и рассчитан на максимальное рабочее давление. Первоначально давление в сосуде создается испарением кислорода в испарителе 9 и автоматически поддерживается постоянным регулятором 2. В зависимости от расхода газа жидкий кислород через регулятор 8 поступает в испаритель 7 и затем в виде газа идет в трубопровод к потребителю. Избыток газа в газификаторе сбрасывается при заданном давлении также в трубопровод потребителя через регулятор 3. Сосуд 1 наполняется жидким кислородом через штуцер 4 и вентили 5 и 6.
Химические свойства
Газообразный кислород является окислителем. Сам по себе он негорюч, но хорошо поддерживает процесс горения, а при значительной концентрации и высоких температурах является взрывоопасным.
С активными веществами (например, щелочными металлами) он может вступать в реакции даже при комнатной температуре и при обыкновенной концентрации в воздухе, образуя с ними соединения оксиды. Результат хорошо виден на многих металлах, на которых он проявляется в виде коррозии.
Жидкий кислород также обладает сильными окислительными свойствами. Многие пропитанные им вещества легко воспламеняются и горят с выделением энергии и тепла. Хлопок, бумага, дерево, уголь и некоторые другие материалы могут взрываться.
Получение
Самым распространенным и легким в получении источником кислорода является воздух. К тому же он неиссякаем и присутствует в нашей жизни повсеместно. Чтобы получить из него необходимые вещества, его сжижают, а затем разделяют на жидкий азот и кислород.
Еще один способ получения жидкости – конденсация ее из газа. Для этого достаточно опустить медный змеевик в контейнер с жидким азотом, а затем пропустить через змеевик газообразный кислород. Температура азота ниже, чем у кислорода, поэтому, проходя по медной трубке, газ будет конденсироваться и превратится в жидкость. При этом на поверхности змеевика образуется небольшой слой снега.
Применение
Сегодня его чаще применяют в медицине, фармацевтике, в металлургии, стекольной, химической, бумажной и других видах промышленности. С его помощью получают различные полезные соединения, например окись титана, которая участвует в производстве лакокрасочных изделий, бумаги и пластмасс. При изготовлении стекла он нужен для поддержания жара в печах, а также для уменьшения количества окиси азота, попадающей в атмосферу. В космической авиации жидкий кислород является одним из компонентов ракетного топлива, где он используется в качестве окислителя, а в роли самого топлива выступает водород или керосин.
В медицине и фармацевтике без него тоже не обходится. Жидкий кислород входит в состав биореакторов, а также используется в качестве добавки к ферментам. В медицине он необходим для анестезии, приготовления кислородных ванн и коктейлей, лечения или облегчения состояния при интоксикации, астме и других недугах. Здесь он чаще всего не используется напрямую в виде жидкости, а является источником газообразного кислорода.
Использование жидкого кислорода
Из многочисленных технических применений кислорода выделить самые необычные — довольно трудно. Почти повсеместно его функции — те же, что и в организме, окислительные.
Кислород может быть не только дополнительным источником тепла, но и источником холода. В реактивных двигателях, например, он работает не только в качестве окислителя, но и как хладоагент. Разумеется, в этих случаях используют жидкий кислород—подвижную летучую жидкость голубого цвета. Кстати, в жидкое состояние кислород переходит при минус 183 градусах, а затвердевает — при минус 219. Как видим, температурный интервал жидкого состояния у этого простого вещества довольно значителен.
Кислородно-конвертерное производство стали, пожалуй, может считаться исключением. Конечно, и здесь главная задача кислорода— окислить избыточный углерод, содержащийся в чугуне. (Первым использовать в этом процессе вместо воздуха кислород предложил еще сто лет назад, в 1876 г., известный русский металлург Д. К. Чернов.) Но у кислородно-конвертерного способа есть одна важная особенность: главный металлургический передел, превращение чугуна в сталь, происходит без затрат топлива. Под действием кислорода примеси, содержащиеся в чугуне (углерод, марганец, кремний и другие), окисляются с выделением значительных количеств тепла. Это тепло и поддерживает металл в жидком состоянии — дополнительный подогрев оказывается ненужным. На данный момент в России подобные методы в металлургическом производстве интенсивно внедряются. Например, на предприятии https://rdmetall.ru/armatura-dlya-fundamenta/armatura-a1-gost-5781/ где производят арматуру. Для производства более качественного металла для арматуры активно применяется сжиженный кислород.
Жидкий кислород стал одним из компонентов довольно мощных взрывчатых веществ — оксиликвитов, довольно долго применявшихся в горном деле. В годы Великой Отечественной войны предпринимались попытки использовать эти вещества и в военных целях, в бомбах из бетона, наполненных каким-либо твердым горючим веществом, пропитанным жидким кислородом.
Как не трудно догадаться слово «оксиликвит» происходит от латинских обозначений кислорода — oxigenium и жидкостей — U-quidus, значит жидкий.
Оксиликвиты — это органические поглотители, например древесный уголь, торф или мелкие опилки, пропитанные кислородом. Из поглотителя формовали специальные патроны, которые замачивали затем в жидком кислороде. Делали это непосредственно перед использованием. Подрывали их с помощью капсюлей-детонаторов.
Оксиликвиты были самым дешевым из всех промышленных взрывчатых веществ. Ими пользовались, и достаточно широко, в строительстве в годы первых пятилеток, в частности при сооружении Днепрогэса. Почему же тогда рассказ о них ведется в прошедшем времени? Дело в том, что оксиликвиты в наше время полностью вытеснены из горного дела и строительства другими взрывчатыми веществами, прежде всего аммонитами. Оксиликвиты нельзя хранить хоть сколько-нибудь долго: жидкий кислород в процессе транспортировки и хранения активно испаряется. Затраты на теплоизоляцию плюс потери перекрывают экономический выигрыш от дешевизны жидкого кислорода и других компонентов оксиликвита…
Взрывчатые вещества (ВВ) с жидким кислородом по существу уже отошли в прошлое, и видимо, навсегда. Зато продолжает расширяться диапазон соединений кислорода, пригодных в качестве ВВ. В прошлом десятилетии были синтезированы первые десятки истинных химических соединений благородных газов — ксенона и криптона. Среди них оказались два вещества большой взрывчатой силы. Эти окислы ксенона. При взрыве этих веществ образуются только газообразные продукты — ксенон и кислород, причем последний способен окислить, превратить в газ другие возможные компоненты взрывчатого вещества. Поэтому, несмотря на сложности синтеза (в прямой реакции окислы ксенона не образуются), окислы ксенона перспективны — и как ВВ, и как очень своеобразные сильные окислители.
Хранение и меры предосторожности
Жидкий кислород не возгорается и не взрывается сам по себе, он не токсичен для человека и не вреден для окружающей среды. Однако активная реакция в химических процессах, а также криогенный эффект делают его не совсем безопасным веществом.
При работе с ним нужно держать подальше смазочные, горючие и легковоспламеняющиеся материалы, а также всегда использовать перчатки и спецодежду. Кислород очень низкой температуры легко повреждает кожу и может привести к обморожению, травмам и отмиранию живых клеток. Если жидкость покрывает значительную часть тела, все может закончиться даже летальным исходом.
Технический и медицинский жидкий кислород хранят сосудах Дьюара, которые делают преимущественно из стали или алюминия. Это цилиндрические контейнеры с двойными стенками, между стенками которых располагается вакуумная полость, а также теплоизоляционные материалы. Они работают по принципу термосов, хорошо сохраняя жидкости внутри.