гемагглютинин вируса что это
Иммуногенность новой гриппозной вакцины
Грипп и гриппоподобные заболевания занимают первое место по частоте и количеству случаев в мире. Эпидемия гриппа ежегодно приходит с наступлением осенне-зимнего сезона, и каждый раз иммунная система не готова к встрече с
Грипп и гриппоподобные заболевания занимают первое место по частоте и количеству случаев в мире. Эпидемия гриппа ежегодно приходит с наступлением осенне-зимнего сезона, и каждый раз иммунная система не готова к встрече с ним. Почему? Грипп является чемпионом среди вирусов по способности к генетической изменчивости, которая позволяет ему уходить от иммунного надзора. Вирус с изменившимися поверхностными белками уже не распознается специфическими противогриппозными антителами к штаммам-предшественникам.
Наиболее эффективным, безопасным и экономически оправданным средством профилактики гриппа является вакцинация. Чтобы вакцина защищала от гриппа, должно быть четкое соответствие вакцинных штаммов эпидемическим. В отличие от большинства других вакцинных препаратов, существует необходимость ежегодного обновления штаммового состава противогриппозных вакцин и, следовательно, необходимость ежегодной иммунизации. Проблема гриппа давно вышла за пределы одной страны. Центрами по гриппу ВОЗ, организованными по всему миру, проводится регулярный мониторинг и сбор информации по сезонным циркулирующим штаммам вируса гриппа и вспышкам заболеваемости. На основании анализа присланного материала эксперты делают прогнозы относительно разновидностей гриппа, которые будут циркулировать в следующем эпидсезоне, а также предлагают вирусы-кандидаты в вакцинные штаммы для производителей.
С учетом того, что дифференциальная диагностика гриппа от других ОРВИ затруднена, показатели иммуногенности вакцин принято оценивать по уровню специфических антител к гемагглютинину (ГА). Защитный эффект ГА-специфических антител неоднократно был продемонстрирован как у животных, так и у людей. Антитела нейтрализуют вирус гриппа, предотвращая его связывание с рецепторами, при этом уровень антител к гемагглютинину напрямую коррелирует с уровнем защищенности. При оценке потенциальной эффективности вакцины титр антител не менее чем 1:40 считают защитным. Антитела к другому изменчивому поверхностному белку вируса гриппа — нейраминидазе — не могут предотвратить инфекцию, однако играют важную роль в защите от тяжелых форм гриппа, препятствуя выходу вирусных частиц из инфицированных клеток и дальнейшему распространению вируса в организме. Гемагглютинин и нейраминидаза названы протективными белками, а вакцины, содержащие только эти очищенные белки, — субъединичными.
Современные достижения вирусологии, развитие технологий фармацевтической индустрии, интеграция исследователей разных стран в сфере контроля и борьбы с гриппом позволили вывести на новый уровень разработку и производство гриппозных вакцин. Вакцина Гриппол® Нео — результат международного сотрудничества двух компаний («Солвей Биолоджикалз Б. В.» и ФК «ПЕТРОВАКС»). Эта субъединичная вакцина содержит иммуноадъювант Полиоксидоний® и антигены (гемагглютинин и нейраминидазу) европейского качества, полученные из вируса, выращенного на культуре клеток. Рост вируса для вакцины осуществляется по современной технологии с использованием клеточной линии MDCK (Madine-Darbin Canine Kidney) в бессывороточной среде и является стандартизированным закрытым процессом, исключающим возможность контаминации любыми, в том числе неизвестными агентами. Применение культур клеток для наработки вирусного материала стало уже традиционным для целого ряда вакцинных препаратов. Но только благодаря разработкам специалистов компании «Солвей Биолоджикалз» технология стала доступной и для гриппозных вакцин. В 2001 году была зарегистрирована вакцина Инфлювак ТС (Нидерланды), в 2009 году в России — Гриппол ® Нео.
Снижение антигенной нагрузки в вакцинирующей дозе обеспечивает максимальный профиль безопасности препарата. Антигены с адъювантом образуют комплекс, который стимулирует гуморальное и клеточное звенья иммунитета. Это приводит к образованию специфических к протективным белкам антител, отвечающих за защиту от гриппа, и повышает общую резистентность организма к инфекции.
Клинические исследования безопасности и иммуногенности Гриппол ® Нео проводились с участием добровольцев в высокоспециализированных исследовательских центрах по изучению вакцинных препаратов и поствакцинальных реакций.
Материалы и методы
Вакцины
В клиническом испытании были использованы три инактивированные субъединичные вакцины, содержащие иммуноадъювант Полиоксидоний® и антигены (гемагглютинин и нейраминидазу) актуальных для эпидемического сезона 2008/2009 штаммов вируса гриппа: H1N1 A/Brisbane/59/2007; H3 N2 A/Uruguay/716/2007; B/Florida/4/2006. Два тестируемых препарата представляли собой две серии вакцины Гриппол® Нео производства ООО «ФК «ПЕТРОВАКС», содержащие по 5 либо по 10 мкг гемагглютинина каждого из трех штаммов и 500 мкг Полиоксидония®. В качестве препарата сравнения использовали коммерческую вакцину Гриппол® производства ФГУП «НПО «Микроген», содержащую по 5 мкг ГА штаммов вирусов гриппа типа А (H1N1 и H3N2), 11 мкг гемагглютинина вируса гриппа типа В, 500 мкг Полиоксидония®. Препараты, используемые в исследовании, были контролированы в ГИСК им. Л. А. Тарасевича на соответствие нормативной документации; испытуемые серии Гриппол® Нео и препарат сравнения зашифрованы специалистами ГИСКа, не принимающими участия в данном исследовании. Дешифровка была проведена после завершения клинического исследования и представления всех результатов в ГИСК.
Дизайн исследования
Исследования проведены в соответствии с утвержденными протоколами и согласно разрешению МЗ РФ на клинических базах ФГУ НИИ ДИ Росздрава и ГОУ ВПО СПбГМУ им. ак. И. П. Павлова в соответствии с требованиями Надлежащей клинической практики (GCP).
Дизайн исследования: рандомизированное, двойное слепое, контролируемое сравнительное в параллельных группах. Вакцинация добровольцев проведена после подписания информированного согласия.
Участники были отобраны в соответствии с критериями включения/исключения, определенными протоколом клинического испытания. Всего было вакцинировано 300 здоровых добровольцев в возрасте 18–55 лет (средний возраст — 24,5 ± 0,5 года). Перед прививкой все добровольцы были осмотрены врачом, было проведено измерение температуры тела, артериального давления, женщинам — тест на беременность.
Методом случайного выборочного распределения было сформировано три группы по 100 человек. Вакцинацию проводили однократно в дельтовидную мышцу в объеме 0,5 мл.
Постановка реакции и учет результатов
Парные сыворотки добровольцев, взятые до и через 21 день после вакцинации, исследовали с помощью стандартной методики в реакции торможения гемагглютинации (РТГА), как описано в МУ 3.3.2 1758–03. Постановка РТГА включала следующие этапы: подготовка сывороток, определение гемагглютинирующего титра в РГА и рабочей дозы вируса, постановка самой реакции. Для удаления неспецифических ингибиторов сыворотку обрабатывали RDE по методу, описанному в инструкции к препарату. В качестве рабочей дозы антигена использовалась доза 4АЕ, приготовленная из диагностикумов «Диагностикумы гриппозные для реакции торможения гемагглютинации сухие» (ФСП 42–0321–4042–03) трех штаммов, соответствующих вакцинным. Сыворотки титровали начиная с разведения 1:10. При учете результатов титр 1:1280 — равным 1:1280.
Иммуногенность оценивали в соответствии с требованиями Европейского комитета к противогриппозным вакцинам (СPMP/BWP/214/96), согласно которым должен выполняться по крайней мере один из трех критериев:
Статистика
Результаты исследований статистически обработаны с использованием t-критерия Стьюдента. Вариационный анализ полученных результатов проводили с применением пакета прикладных программ Statistica 6.0.
Результаты и обсуждение
Серологическое обследование с целью оценки иммунологической эффективности вакцинации проводили, сравнивая уровень антител в парных сыворотках, взятых до прививки и на 21-й день после вакцинации. Во всех экспериментальных группах в сыворотках привитых регистрировали статистически достоверное нарастание титров антител. По всем анализируемым критериям не наблюдалось статистически достоверной разницы в иммунном ответе на серии вакцины Гриппол® Нео с различными дозировками антигенов. В таблицах приведены данные, относящиеся к серии, содержащей по 5 мкг гемагглютинина каждого штамма.
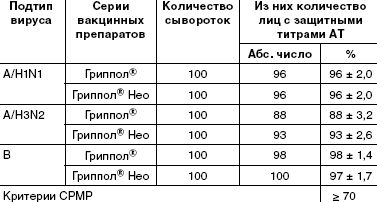
Подсчеты числа лиц с серопротекциями (защитными титрами антител (≥ 1:40)) показали, что в каждой группе уровень этих антител соответствует критерию CPMP (табл. 1).
Известно, что человеческая популяция неоднородна по наличию антител к различным штаммам и подтипам вируса гриппа вследствие гриппозных эпидемий и предыдущих вакцинаций. Среди вакцинированных добровольцев выявлены как серонегативные, так и серопозитивные участники (исходно имевшие защитный титр). Представлялось интересным оценить эффективность иммунизации в общей популяции людей (табл. 3).
Выводы и заключение
В настоящее время вакцина Гриппол ® Нео зарегистрирована (РУ № ЛСР-006029/09 от 23.07.2009 г.). Таким образом, семейство вакцин Гриппол ® пополнилось новым полноправным членом, а профилактическая медицина обрела новый инструмент для контроля такого заболевания, как грипп. Гриппол ® Нео стал первой в мире субъединичной адъювантной вакциной с клеточной технологией получения антигенов. При этом впервые вакцинация против гриппа разрешена людям с аллергией на белок куриного яйца. Исследования по расширению показаний к применению вакцины продолжаются.
Е. М. Войцеховская *
В. С. Вакин *, кандидат медицинских наук
А. А. Васильева *
Е. В. Кузнецова *, кандидат биологических наук
Н. И. Лонская **, кандидат медицинских наук
Г. А. Ельшина **, кандидат медицинских наук
М. А. Горбунов **, доктор медицинских наук
А. А. Соминина *, доктор медицинских наук
Ю. А. Зайцева ***
* ГУ НИИ гриппа РАМН, Санкт-Петербург
** ФГУН ГИСК им. Л. А. Тарасевича Роспотребнадзора, Москва
*** ООО ФК «ПЕТРОВАКС», Москва
Ключевые слова: вакцина, грипп, Гриппол ® Нео, клеточная культура
Иммуногенность новой гриппозной вакцины
Грипп и гриппоподобные заболевания занимают первое место по частоте и количеству случаев в мире. Эпидемия гриппа ежегодно приходит с наступлением осенне-зимнего сезона, и каждый раз иммунная система не готова к встрече с
Грипп и гриппоподобные заболевания занимают первое место по частоте и количеству случаев в мире. Эпидемия гриппа ежегодно приходит с наступлением осенне-зимнего сезона, и каждый раз иммунная система не готова к встрече с ним. Почему? Грипп является чемпионом среди вирусов по способности к генетической изменчивости, которая позволяет ему уходить от иммунного надзора. Вирус с изменившимися поверхностными белками уже не распознается специфическими противогриппозными антителами к штаммам-предшественникам.
Наиболее эффективным, безопасным и экономически оправданным средством профилактики гриппа является вакцинация. Чтобы вакцина защищала от гриппа, должно быть четкое соответствие вакцинных штаммов эпидемическим. В отличие от большинства других вакцинных препаратов, существует необходимость ежегодного обновления штаммового состава противогриппозных вакцин и, следовательно, необходимость ежегодной иммунизации. Проблема гриппа давно вышла за пределы одной страны. Центрами по гриппу ВОЗ, организованными по всему миру, проводится регулярный мониторинг и сбор информации по сезонным циркулирующим штаммам вируса гриппа и вспышкам заболеваемости. На основании анализа присланного материала эксперты делают прогнозы относительно разновидностей гриппа, которые будут циркулировать в следующем эпидсезоне, а также предлагают вирусы-кандидаты в вакцинные штаммы для производителей.
С учетом того, что дифференциальная диагностика гриппа от других ОРВИ затруднена, показатели иммуногенности вакцин принято оценивать по уровню специфических антител к гемагглютинину (ГА). Защитный эффект ГА-специфических антител неоднократно был продемонстрирован как у животных, так и у людей. Антитела нейтрализуют вирус гриппа, предотвращая его связывание с рецепторами, при этом уровень антител к гемагглютинину напрямую коррелирует с уровнем защищенности. При оценке потенциальной эффективности вакцины титр антител не менее чем 1:40 считают защитным. Антитела к другому изменчивому поверхностному белку вируса гриппа — нейраминидазе — не могут предотвратить инфекцию, однако играют важную роль в защите от тяжелых форм гриппа, препятствуя выходу вирусных частиц из инфицированных клеток и дальнейшему распространению вируса в организме. Гемагглютинин и нейраминидаза названы протективными белками, а вакцины, содержащие только эти очищенные белки, — субъединичными.
Современные достижения вирусологии, развитие технологий фармацевтической индустрии, интеграция исследователей разных стран в сфере контроля и борьбы с гриппом позволили вывести на новый уровень разработку и производство гриппозных вакцин. Вакцина Гриппол® Нео — результат международного сотрудничества двух компаний («Солвей Биолоджикалз Б. В.» и ФК «ПЕТРОВАКС»). Эта субъединичная вакцина содержит иммуноадъювант Полиоксидоний® и антигены (гемагглютинин и нейраминидазу) европейского качества, полученные из вируса, выращенного на культуре клеток. Рост вируса для вакцины осуществляется по современной технологии с использованием клеточной линии MDCK (Madine-Darbin Canine Kidney) в бессывороточной среде и является стандартизированным закрытым процессом, исключающим возможность контаминации любыми, в том числе неизвестными агентами. Применение культур клеток для наработки вирусного материала стало уже традиционным для целого ряда вакцинных препаратов. Но только благодаря разработкам специалистов компании «Солвей Биолоджикалз» технология стала доступной и для гриппозных вакцин. В 2001 году была зарегистрирована вакцина Инфлювак ТС (Нидерланды), в 2009 году в России — Гриппол ® Нео.
Снижение антигенной нагрузки в вакцинирующей дозе обеспечивает максимальный профиль безопасности препарата. Антигены с адъювантом образуют комплекс, который стимулирует гуморальное и клеточное звенья иммунитета. Это приводит к образованию специфических к протективным белкам антител, отвечающих за защиту от гриппа, и повышает общую резистентность организма к инфекции.
Клинические исследования безопасности и иммуногенности Гриппол ® Нео проводились с участием добровольцев в высокоспециализированных исследовательских центрах по изучению вакцинных препаратов и поствакцинальных реакций.
Материалы и методы
Вакцины
В клиническом испытании были использованы три инактивированные субъединичные вакцины, содержащие иммуноадъювант Полиоксидоний® и антигены (гемагглютинин и нейраминидазу) актуальных для эпидемического сезона 2008/2009 штаммов вируса гриппа: H1N1 A/Brisbane/59/2007; H3 N2 A/Uruguay/716/2007; B/Florida/4/2006. Два тестируемых препарата представляли собой две серии вакцины Гриппол® Нео производства ООО «ФК «ПЕТРОВАКС», содержащие по 5 либо по 10 мкг гемагглютинина каждого из трех штаммов и 500 мкг Полиоксидония®. В качестве препарата сравнения использовали коммерческую вакцину Гриппол® производства ФГУП «НПО «Микроген», содержащую по 5 мкг ГА штаммов вирусов гриппа типа А (H1N1 и H3N2), 11 мкг гемагглютинина вируса гриппа типа В, 500 мкг Полиоксидония®. Препараты, используемые в исследовании, были контролированы в ГИСК им. Л. А. Тарасевича на соответствие нормативной документации; испытуемые серии Гриппол® Нео и препарат сравнения зашифрованы специалистами ГИСКа, не принимающими участия в данном исследовании. Дешифровка была проведена после завершения клинического исследования и представления всех результатов в ГИСК.
Дизайн исследования
Исследования проведены в соответствии с утвержденными протоколами и согласно разрешению МЗ РФ на клинических базах ФГУ НИИ ДИ Росздрава и ГОУ ВПО СПбГМУ им. ак. И. П. Павлова в соответствии с требованиями Надлежащей клинической практики (GCP).
Дизайн исследования: рандомизированное, двойное слепое, контролируемое сравнительное в параллельных группах. Вакцинация добровольцев проведена после подписания информированного согласия.
Участники были отобраны в соответствии с критериями включения/исключения, определенными протоколом клинического испытания. Всего было вакцинировано 300 здоровых добровольцев в возрасте 18–55 лет (средний возраст — 24,5 ± 0,5 года). Перед прививкой все добровольцы были осмотрены врачом, было проведено измерение температуры тела, артериального давления, женщинам — тест на беременность.
Методом случайного выборочного распределения было сформировано три группы по 100 человек. Вакцинацию проводили однократно в дельтовидную мышцу в объеме 0,5 мл.
Постановка реакции и учет результатов
Парные сыворотки добровольцев, взятые до и через 21 день после вакцинации, исследовали с помощью стандартной методики в реакции торможения гемагглютинации (РТГА), как описано в МУ 3.3.2 1758–03. Постановка РТГА включала следующие этапы: подготовка сывороток, определение гемагглютинирующего титра в РГА и рабочей дозы вируса, постановка самой реакции. Для удаления неспецифических ингибиторов сыворотку обрабатывали RDE по методу, описанному в инструкции к препарату. В качестве рабочей дозы антигена использовалась доза 4АЕ, приготовленная из диагностикумов «Диагностикумы гриппозные для реакции торможения гемагглютинации сухие» (ФСП 42–0321–4042–03) трех штаммов, соответствующих вакцинным. Сыворотки титровали начиная с разведения 1:10. При учете результатов титр 1:1280 — равным 1:1280.
Иммуногенность оценивали в соответствии с требованиями Европейского комитета к противогриппозным вакцинам (СPMP/BWP/214/96), согласно которым должен выполняться по крайней мере один из трех критериев:
Статистика
Результаты исследований статистически обработаны с использованием t-критерия Стьюдента. Вариационный анализ полученных результатов проводили с применением пакета прикладных программ Statistica 6.0.
Результаты и обсуждение
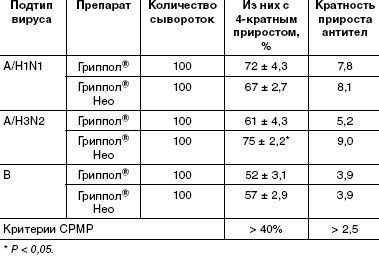
Серологическое обследование с целью оценки иммунологической эффективности вакцинации проводили, сравнивая уровень антител в парных сыворотках, взятых до прививки и на 21-й день после вакцинации. Во всех экспериментальных группах в сыворотках привитых регистрировали статистически достоверное нарастание титров антител. По всем анализируемым критериям не наблюдалось статистически достоверной разницы в иммунном ответе на серии вакцины Гриппол® Нео с различными дозировками антигенов. В таблицах приведены данные, относящиеся к серии, содержащей по 5 мкг гемагглютинина каждого штамма.
Подсчеты числа лиц с серопротекциями (защитными титрами антител (≥ 1:40)) показали, что в каждой группе уровень этих антител соответствует критерию CPMP (табл. 1).
Известно, что человеческая популяция неоднородна по наличию антител к различным штаммам и подтипам вируса гриппа вследствие гриппозных эпидемий и предыдущих вакцинаций. Среди вакцинированных добровольцев выявлены как серонегативные, так и серопозитивные участники (исходно имевшие защитный титр). Представлялось интересным оценить эффективность иммунизации в общей популяции людей (табл. 3).
Выводы и заключение
В настоящее время вакцина Гриппол ® Нео зарегистрирована (РУ № ЛСР-006029/09 от 23.07.2009 г.). Таким образом, семейство вакцин Гриппол ® пополнилось новым полноправным членом, а профилактическая медицина обрела новый инструмент для контроля такого заболевания, как грипп. Гриппол ® Нео стал первой в мире субъединичной адъювантной вакциной с клеточной технологией получения антигенов. При этом впервые вакцинация против гриппа разрешена людям с аллергией на белок куриного яйца. Исследования по расширению показаний к применению вакцины продолжаются.
Е. М. Войцеховская *
В. С. Вакин *, кандидат медицинских наук
А. А. Васильева *
Е. В. Кузнецова *, кандидат биологических наук
Н. И. Лонская **, кандидат медицинских наук
Г. А. Ельшина **, кандидат медицинских наук
М. А. Горбунов **, доктор медицинских наук
А. А. Соминина *, доктор медицинских наук
Ю. А. Зайцева ***
* ГУ НИИ гриппа РАМН, Санкт-Петербург
** ФГУН ГИСК им. Л. А. Тарасевича Роспотребнадзора, Москва
*** ООО ФК «ПЕТРОВАКС», Москва
Ключевые слова: вакцина, грипп, Гриппол ® Нео, клеточная культура
Гемагглютинин вируса что это
Каждый год осенью и зимой человечество захлестывает новая волна гриппа. Но грипп гриппу рознь! Об этом поговорим в нашей статье.
Всего в природе циркулирует 4 типа вирусов гриппа – A, B, C и D. Для людей наибольший интерес представляют вирусы гриппа A и B. Именно они вызывают сезонные эпидемии болезни.
Вирус гриппа C тоже заражает человека, но не вызывает тяжелых случаев болезни. А вирусы группы D и вовсе инфицируют только свиней и крупный рогатый скот, случаев заболевания среди людей не зарегистрировано.
Вирус гриппа отличается чрезвычайной изменчивостью генома. Больше всего мутациям подвержен вирус гриппа А.
Каждый сезон появляются новые генетические варианты вируса, отличающиеся по своим антигенным характеристикам от предшественников, и имеющийся у нас иммунитет оказывается бесполезен против них.
Чтобы понять, почему борьба с гриппом продолжается десятилетиями и никак не заканчивается, нужно разобраться в структуре вируса гриппа. В особенности нам интересна внешняя мембрана.
На поверхности вирусной частицы находятся главные мишени иммунной системы — белки гемагглютинин (HA) и нейраминидаза (NA). Первый необходим для проникновения в клетку хозяина, а второй — для успешного высвобождения вирусной частицы. И именно эти белки задействованы в мутациях вируса гриппа.
Вариантов изменчивости вируса гриппа может быть два: антигенный дрейф и антигенный шифт.
Антигенный дрейф — это постепенное накопление мутаций за счет ошибок, которые делает вирусная полимераза во время копирования генома. Из-за постепенных небольших изменений в гемагглютинине и нейраминидазе возникают штаммы вируса, настолько отличающиеся от предыдущих вариантов, что наша иммунная система распознает их как новые. Соответственно каждый сезон циркулирует новый штамм гриппа, именно поэтому состав вакцины ежегодно обновляется.
Учитывая то, что в природе для вируса гриппа А найдено 18 подтипов гемагглютинина и 11 подтипов нейраминидазы, комбинаций может быть довольно много.
Среди людей обнаружены штаммы с комбинациями H1N1 (гемагглютинин подтипа 1 и нейраминидаза подтипа 1), H2N2 и H3N2.
Как может произойти такая мутация? Если одну и ту же клетку заразят два вируса с разными комбинациями, может произойти реассортация — перетасовка вариантов, в результате которой образуется вирус с новой комбинацией подтипов гемагглютинина и нейраминидазы.
Именно в результате таких мутаций возникают самые смертоносные пандемии гриппа, в том числе и пандемия «свиного» гриппа в 2009 году.
Обнаружено место связывания «Арбидола» с вирусом гриппа
Комплекс умифеновира (желтый цвет) с гемагглютинином
Rameshwar U. Kadam and Ian A. Wilson, PNAS, 2016
Американские ученые определили место связывания умифеновира (известного под торговыми названиями «Арбидол», «Афлюдол», «Арпефлю», «ОРВИтол НП» и другими) с одним из основных антигенов вируса гриппа — гемагглютинином. Результаты работы опубликованы в журнале Proceedings of the National Academy of Sciences.
Умифеновир (до регистрации под этим международным непатентованным названием — метилфенилтиометилдиметиламинометилгидроксиброминдолкарбоновой кислоты этиловый эфир) разработан в СССР в 1970-х годах, с 1988 года разрешен к применению как иммуномодулятор. Позже был переклассифицирован как противовирусное средство, применяется в России, Китае и большинстве постсоветских республик. Несмотря на его широкую популярность среди врачей и пациентов, Всемирная организация здравоохранения считает клинические испытания препарата, проведенные с 1993 по 2004 год, не отвечающими требованиям доказательной медицины. В одном исследовании была показана способность высоких концентраций умифеновира in vitro ингибировать гемагглютинин, необходимый для проникновения вируса гриппа в клетку. В настоящее время ведутся мультицентровые клинические испытания препарата ARBITR, финансируемые его основным производителем — компанией «Фармстандарт».
Сотрудники Исследовательского института Скриппса провели рентгеноструктурный анализ гемагглютининов H3/HK68 пандемического штамма 1968 года H3N2 (A/Hong Kong/1/1968) и H7/SH2 выделенного в 2013 году птичьего штамма H7N9 (A/Shanghai/2/2013), соединенных с умифеновиром. Эти антигены относятся ко 2 группе (в нее входят гемагглютинины Н3, Н4, Н7, Н10, Н14 и Н15), к которой препарат проявляет большее сродство, чем к 1 группе (гемагглютинины Н1, Н2, Н5, Н6, Н8, Н9, Н11-13 и Н16-18).
Выяснилось, что умифеновир связывается с гидрофобной полостью в стволе мономеров гемагглютинина — по одной молекуле препарата на каждый из стволов тримера. Связи преимущественно гидрофобные, однако умифеновир вызывает также изменения конформации молекулы, способствующие образованию в ней солевых мостиков. Все это стабилизирует гемагглютинин в конформации, препятствующей его присоединению к клетке и последующему слиянию клеточной мембраны и оболочки вируса, а следовательно, проникновению вируса в клетку.
Место связывания умифеновира с гемагглютинином вируса гриппа
Rameshwar U. Kadam and Ian A. Wilson, PNAS, 2016