галавит или циклоферон что лучше
Эффективность таблетированной (кишечнорастворимой) формы циклоферона в терапии герпетической инфекции
Среди лекарственных препаратов, применяемых для лечения герпетической инфекции, наибольшее распространение в клинической практике приобрели синтетические аналоги пуриновых и пиримидиновых нуклеозидов, ингибирующих ключевые ферменты репликации вируса: — ац
Среди лекарственных препаратов, применяемых для лечения герпетической инфекции, наибольшее распространение в клинической практике приобрели синтетические аналоги пуриновых и пиримидиновых нуклеозидов, ингибирующих ключевые ферменты репликации вируса: — ацикловир (вролекс, зовиракс, ациклогуанозин), а также валцикловир (валтрекс), фамцикловир (пенцикловир), фоскарнет, видарабин и их всевозможные комбинации, а также препараты ненуклеозидной природы — интерфероны, ДС-РНК, ингибиторы протеолиза и др.
Однако опыт длительного применения этих средств, особенно ацикловира, показал существенное снижение клинического эффекта во времени, что обусловлено образованием резистентных штаммов вируса герпеса.
Вследствие этого в настоящее время наибольшее внимание уделяется разработке комбинированных методов лечения с применением аналогов нуклеозидов, ингибиторов ферментов, цитокинов и индукторов интерферона.
В настоящее время наиболее изученным из разрешенных к клиническому применению индукторов интерферона является препарат циклоферон, выпускаемый в виде раствора для инъекций и хорошо себя зарекомендовавший для лечения широкого спектра вирусных и бактериальных инфекций, в том числе герпетической.
Исследования показали, что препарат in vitro полностью подавляет репликацию вируса герпеса первого типа и цитомегаловируса в культуре клеток, и проявляет высокую эффективность in vivo на моделях герпетического поражения (герпетический конъюнктивит и герпетический энцефалит) у экспериментальных животных (кроликов).
Учитывая эпидемиологию герпетической инфекции и необходимость амбулаторного применения препарата, представляется целесообразным внедрение в клиническую практику более удобной оральной формы циклоферона.
Целью настоящей работы явилось проведение рандомизированного клинико-лабораторного исследования эффективности оральной лекарственной формы циклоферона у 90 пациентов для лечения герпетической инфекции двойным слепым методом.
Исследуемый препарат: циклоферон (Cycloferonum) N-метил-N-(1-дезокси-d-глуцитол-1-ил) аммоний-10-карбоксиметиленакридон в виде таблеток коричневого цвета с кишечнорастворимой оболочкой по 0,15 г. Вводился орально один раз в сутки в дозе 0,3-0,6 г (две-четыре таблетки).
Препарат сравнения: ацикловир (Acyclovirum, производства AZT, Россия) в виде таблеток по 0,2 г. Принимается орально пять раз в сутки в суточной дозе 80-100 мг/кг.
В клиническое исследование были включены больные герпетической инфекцией, удовлетворяющие следующим условиям: возраст 14-60 лет; отсутствие тяжелых сопутствующих заболеваний.
Диагноз герпетической инфекции ставился на основе клинико-эпидемиологических данных и подтверждался лабораторными методами (ПЦР, ИФА).
Всего было обследовано 125 пациентов, из них 42 мужчины и 83 женщины. Возраст — от 18 до 60 лет, в среднем 33,9±10,3 лет. Диагноз H.labialis был поставлен 23 пациентам, H.henitalis — у 94, сочетанная форма — у 8.
Длительность заболевания колебалась от 0,5 лет до 16 лет, составляя в среднем 4,1±0,8 лет.
35 пациентов ранее использовали ацикловир или его аналоги в лечении герпетической инфекции.
Было сформировано три группы больных.
Первая группа (группа I) из 38 пациентов получала циклоферон по одной таблетке орально два раза в сутки на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23, 26, 29-й день лечения. Курс лечения один месяц. Всего на курс лечения 24 таблеток циклоферона.
Вторая группа (группа II) из 36 человек получала ацикловир ежедневно по две таблетки по 0,2 г пять раз в день в течение 8—10 дней. Всего на курс лечения 40—50 таблеток ацикловира.
Третья группа (группа III) из 51 пациентов принимала циклоферон по одной таблетке на прием два раза в сутки на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23, 26, 29-й день лечения и дополнительно ацикловир ежедневно по одной таблетке пять раз в день в течение 8—10 дней.
Рандомизация больных осуществлялась по очередности поступления (первый в группу I, второй в группу II и т. д.).
Эффективность проводимой терапии оценивалась по клиническим и лабораторным критериям оценки протекания герпетической инфекции.
Для этого использовали следующие клинические показатели:
— частота обострений;
— длительность обострений;
— интенсивность обострений.
Частота обострений у пациентов с положительной динамикой показана в табл. 1.
Таблица 1. Количество обострений в год
При сравнении действия препаратов на пациентов каждой группы было выявлено, что частота обострений в группе I снизилась на достоверно большую величину (Р
Таблица 2. Длительность обострений, дни
Среднее значение снижения длительности рецидивов в группе I было достоверно выше (Р
Таблица 3. Интенсивность обострений, в баллах по 5-балльной шкале
Степень проявления инфекции у пациентов I группы снижалась на достоверно большую величину, чем у пациентов II группы (Р
Таблица 4. Содержание общего сывороточного IFN, ME/мл (норма: 0-8)
Как видно из таблицы, содержание IFN под действием ацикловира увеличивалось в среднем на 7%, тогда как циклоферон повышал уровень IFN в крови в среднем на 18%. Наиболее эффективным оказалось сочетание этих двух препаратов, их совместное применение приводило к повышению содержания IFN в среднем на 22%. Различие по этому показателю между группами II и III было статистически достоверным (Р
Таблица 5. Уровень продукции IFN-a/b, ME/мл (норма: 250—520)
Из таблицы видно, что монотерапия циклофероном и сочетание циклоферона с ацикловиром приводили к увеличению уровня продукции IFN-a/b практически до нормы, тогда как у пациентов, принимавших ацикловир, уровень продукции интерферона после лечения оставался ниже нормальных значений.
Наибольший стимулирующий эффект в отношении продукции интерферонов a и b наблюдался у пациентов III группы, принимавших одновременно циклоферон и ацикловир.
Сравнение средних величин относительного приращения уровня продукции IFN-g показало отсутствие значимых различий между группами. Таким образом, на основании полученных результатов можно сделать вывод о том, что изучаемые препараты и их сочетание равноценны по своему воздействию на продукцию IFN-g клетками.
Естественные цитотоксические клетки (natural killer — NK), обладающие спонтанной цитотоксической активностью в отношении широкого спектра клеток-мишеней, в том числе клеток, инфицированных вирусами, являются важным клеточным звеном неспецифического иммунного ответа. Эти клетки представляют первую линию защиты от вирусинфицированных клеток, а также продуцируют ряд цитокинов.
Средние значения активности NK-клеток у больных с положительными изменениями представлены в табл. 6.
Таблица 6. Цитотоксическая активность NK-клеток, % (норма: 46—50)
Как видно из таблицы, активность NK-клеток в группах II и III повышается на большую величину, чем в группе II, причем в группах I и III показатель активности после лечения практически достигал нормы, тогда как в группе II эти значения до и после лечения оставались ниже нормальных показателей.
Терапия циклофероном как в отдельности, так и в сочетании с ацикловиром более эффективно повышала активность мононуклеарных фагоцитов, чем терапия ацикловиром, средние показатели фагоцитоза после лечения в группах I и III практически соответствовали норме, тогда как в группе II и после лечения эти величины оставались пониженными.
Спонтанная миграция клеток увеличивалась приблизительно на треть. Статистический анализ показал, что достоверных различий между группами по этому показателю нет.
Наибольшее среднее приращение результатов НСТ-теста наблюдалось в группе II, однако статистический анализ свидетельствует о том, что различия между группами недостоверны.
Определение сывороточных иммуноглобулинов является одним из основных количественных тестов, позволяющих оценить состояние гуморального звена иммунитета. В данном исследовании измеряли концентрацию иммуноглобулинов трех основных классов — М, А и G. Для определения использовали метод радиальной иммунодиффузии по Манчини.
Различия в величине приращения концентрации Ig М после лечения были статистически недостоверны для всех трех групп.
Циклоферон и ацикловир по отдельности вызывают сходные эффекты. Продукции Ig А и их средние значения статистически не отличаются друг от друга. Сочетанное применение этих препаратов, напротив, повышало уровень Ig А в крови.
Эффект воздействия циклоферона и ацикловира на уровень IgG был одинаков.
Для оценки специфического гуморального ответа, направленного против вируса герпеса, определяли IgG к вирусу простого герпеса I и II типа методом иммуноферментного анализа.
Различия в эффектах препаратов между группами были статистически недостоверны.
В рамках данного исследования определялось наличие или отсутствие делеции гена GSTM1. Этот анализ проводился с целью проверки предположения о том, что продукт этого гена участвует в метаболизме циклоферона в организме и тем самым способствует интерферон-индуцирующей активности этого препарата. Группы пациентов, получавших циклоферон (группы I и III), были разделены на две подгруппы: пациенты, имеющие ген (GSTM+), и пациенты с делецией гена (GSTM 0/0). В этих подгруппах анализировали результаты клинических наблюдений (частота и длительность рецидивов, интенсивность проявления обострений заболевания) и данные лабораторных исследований (интерфероновый статус и активность NK-клеток). Сравнивались изменения как в подгруппе в целом, так и отдельно у пациентов с положительными и отрицательными изменениями.
Проведенный статистический анализ данных не выявил достоверных различий между подгруппами GSTM 0/0 и GSTM1+ по эффекту препаратов на частоту и длительность рецидивов, интенсивность обострений, уровень общего интерферона в сыворотке, продукцию интерферонов a, b и g in vitro, а также цитотоксическую активность NK-клеток.
На основе полученных данных можно предположить, что действие циклоферона не связано с его метаболизмом, и это позволяет одинаково эффективно использовать этот препарат в генетически гетерогенных группах пациентов.
Заключение
При проведении исследования было использовано несколько схем терапии таблетированным препаратом циклоферон. Помимо стандартной схемы, описанной выше, наиболее эффективными, особенно с профилактической точки зрения, оказались короткие схемы приема препарата (по одной таблетке два раза в день в течение недели) с месячным перерывом.
В целом результаты исследования позволяют сделать следующие выводы.
1. Таблетированная форма циклоферона хорошо переносится и не вызывает побочных эффектов при использовании вышеупомянутых схем терапии. В настоящем исследовании не было отмечено случаев индивидуальной непереносимости препарата.
2. Наиболее эффективной в терапии рецидивирующей герпетической инфекции оказалась схема лечения, сочетающая использование противовирусного препарата (в нашем исследовании ацикловир) и индуктора интерферона циклоферон.
3. Препарат циклоферон не обладает иммунотоксическими эффектами, об этом можно судить по отсутствию подавления функциональных и количественных параметров иммунной системы.
5. Самостоятельный курс приема таблеток циклоферона в виде монотерапии может эффективно использоваться при лечении герпетической инфекции.
6. Отсутствие различий в эффективности терапии у генетически гетерогенных по экспрессии гена, кодирующего глутатион-S-трансферазу, пациентов может быть важным доказательством того, что именно неизменная молекула циклоферона является действующим индуктором.
Полученные данные позволяют рекомендовать таблетки циклоферона в стандартных дозах различным пациентам независимо от их способности к метаболизму ксенобиотиков.
Литература
1. Кондратьева Г. А., Екимова В. И., Иовлев В. И. Определение противовирусной активности интерферонов человека микрометодом / Реаферон (сборник научных трудов). Л., 1988, с. 105-109.
2. Manaseki S., Searle R. F. Natural killer (NK) cells activity of first trimester human decidua // Cellular Immunology. 1989. Vol. 121. № 1. P. 166-173.
3. Park B. H. Infection and nitroblutetrasolium reduction by neutrophis // Lancet. 1968. Vol. 2. P. 532-534.
Иммуномодуляторы в комплексной терапии ОРВИ: возможности применения препарата Галавит
Опубликовано в журнале:
«Российский медицинский журнал» №3, 2013г.
Т.В. Сологуб, О.Ю. Осиновец
Северо–Западный государственный медицинский университет им. И.И. Мечникова, Санкт–Петербург
Острые респираторные вирусные инфекции (ОРВИ) являются наиболее массовыми заболеваниями, поражающими ежегодно до 25% населения стран мира. По данным ВОЗ, ежегодно каждый взрослый 2–4 раза болеет острыми респираторными заболеваниями, школьник – 4–5 раз, дети первого года жизни – от 2 до 12 раз [1]. В России отмечается подъем заболеваемости ОРВИ, доля которых в структуре всей регистрируемой инфекционной патологии достигает 85–90% (до 30 млн человек, 10–15% трудоспособного населения, 45– 60% – дети). С ОРВИ связано 30–50% потерь рабочего времени у взрослых и 60–80% пропусков школьных занятий у детей, а ежегодный суммарный экономический ущерб от ОРВИ оценивается в 40 млрд руб.
К возбудителям ОРВИ относят более 200 видов респираторных вирусов, среди них вирусы гриппа (типы А, В, С), парагриппа (4 типа), аденовирусы (около 60 сероти-пов), риновирусы (более 100 серотипов), коронавирусы (4 серотипа), респираторно–синцитиальные вирусы (2 серо-типа) и др. В настоящее время отмечается тенденция к снижению частоты инфицирования вирусом гриппа (тип А – 12%, тип В – 3%) и росту активности других респираторных вирусов, в том числе парагриппа – до 50%, аденовирусов – до 5%, респираторно–синцитиальных вирусов – 4%, а также энтеровирусов – 1,2%, смешанных инфекций – около 23% случаев [5,6]. Кроме того, отмечается снижение общего иммунитета среди населения, что способствует росту заболеваемости ОРВИ, а иммунодепрессив-ное действие респираторных вирусов является причиной повторных ОРВИ и бактериальных осложнений [6].
Очевидной становится необходимость качественно новых подходов к профилактике и лечению ОРВИ и гриппа, т.к., несмотря на высокую эффективность современных вакцин против гриппа (80–90%), вакцинация не может защитить от других возбудителей ОРВИ. Поэтому заболеваемость ОРВИ среди вакцинированных лиц в осенне–зимний период остается высокой [6].
Если для профилактики и лечения гриппа в настоящее время используются специфические вакцины и противогриппозные химиопрепараты, то для борьбы с другими многочисленными видами респираторных вирусов средств специфической защиты и этиотропной терапии не существует. Поэтому современный подход к профилактике и лечению ОРВИ заключается в применении препаратов, повышающих защитные силы организма, способствующих созданию барьера на пути проникновения вируса. К таким препаратам относятся интерфероны, индукторы интерферонов и иммуномодуляторы – средства патогенетического действия [2,3,6].
Важно отметить, что противовирусные химиопрепараты для лечения гриппа обладают строгой этиотропной направленностью действия: блокаторы М2–белка (ремантадин) эффективны только против вируса гриппа типа А, ингибиторы нейраминидазы (занамивир, оселтамивир) – против разных штаммов вирусов гриппа А и нескольких штаммов вируса гриппа В, что ограничивает их широкое применение при ОРВИ, вызванных другими этиологическими возбудителями. В отличие от специфических химио-препаратов интерфероны, индукторы интерферонов и иммуномодуляторы проявляют неспецифическое действие при ОРВИ, что позволяет применять их против различных типов респираторных вирусов без точной лабораторной диагностики и расширяет клинические возможности.
Обоснованием к их применению при ОРВИ и гриппе служат полученные данные о патогенетической роли цитокиновых реакций, которые запускают каскад иммунологических реакций клеточного и гуморального типа. Исследования иммунопатогенеза гриппа и ОРВИ последних лет убедительно показали, что респираторные вирусы грубо вмешиваются в сбалансированную систему цитокинов. От адекватности иммунологических реакций зависят характер клинического течения и исход заболевания. В организме первый эшелон антиинфекционной защиты обеспечивается клетками врожденного иммунитета (моноциты/макрофаги, дендритные клетки и естественные киллеры), которые организуют реакции адаптивного иммунитета в ответ на внедрение патогена. При этом запускаются пролиферация и дифференцировка лимфоцитов, активируются макрофаги, в дальнейшем подключаются вспомогательные или антигенпрезентирующие клетки. В результате наблюдается выброс цитокинов, запускающих как местные, так и системные воспалительные реакции [4]. Таким образом, в ответ на внедрение возбудителя включаются факторы адаптивного и специфического к данному вирусу иммунитета, представленного цитотоксическими Т–лимфоцитами и антителами изотипов IgM, A, G, E, обладающих специфичностью к различным патогенам.
Иммуномодуляторы применяются не только в комплексной терапии ОРВИ, но и в составе комплексной профилактики наряду со специфической иммунизацией (вакцинацией). Действие иммуномодуляторов направлено на активацию естественного и коррекцию адаптивного иммунитета и относится к методам неспецифической защиты населения.
Иммуномодуляторы представляют собой наиболее многочисленную группу лекарственных препаратов различного происхождения и химической природы [7]. К таким лекарственным средствам относится препарат Галавит (ЗАО «Медикор») – синтетический иммуномодулятор с дополнительным противовоспалительным действием, который применяется в клинической практике с 1997 г. Механизм действия препарата связан с его способностью воздействовать на функционально–метаболическую активность фагоцитарных клеток (моноцитов/макрофагов, нейтрофилов, естественных киллеров). Кроме этого, Галавит нормализует антителообразование, опосредованно стимулирует выработку эндогенных интерферонов (ИФН–α и ИФН–γ). При воспалительных заболеваниях препарат обратимо на 6–8 ч ингибирует избыточный синтез гиперактивированными макрофагами фактора некроза опухоли–α, интерлейкина–1, интерлейкина–6 и других провоспалительных цитокинов, активных форм кислорода, уровень которых определяет степень воспалительных реакций, их цикличность, а также выраженность интоксикации и уровень оксидантного стресса. Нормализация функционального состояния макрофагов приводит к восстановлению антигенпредставляющей и регулирующей функций макрофагов, снижению уровня аутоагрессии. Галавит стимулирует активность нейтрофильных гранулоцитов, усиливая фагоцитоз и повышая неспецифическую резистентность организма к инфекционным заболеваниям. Препарат доказал свою эффективность в лечении и профилактике различных инфекций бактериальной и вирусной этиологии. При применении Галавита побочные эффекты практически отсутствуют – за исключением редких случаев индивидуальной непереносимости.
Изучение лечебного эффекта препарата Галавит при гриппе.
Эффективность препарата Галавит изучалась у больных гриппом на кафедре инфекционных болезней СЗГМУ им. И.И. Мечникова в эпидсезон 2009 г. Под наблюдением находились 45 больных в возрасте от 21 до 28 лет (средний возраст – 25,1±1,3 года); диагноз гриппа подтверждался с помощью ПЦР. Все пациенты имели легкую и среднетяжелую форму заболевания и получали дезинтоксикационную и симптоматическую терапию. 20 больных получали дополнительно иммуномодулятор Галавит в дозировке 4 табл./сут. курсом 10 дней. Оценка эффективности проводимой терапии проводилась по результатам данных клинических и лабораторных исследований после курса лечения. Основными критериями эффективности служили положительная динамика клинических симптомов и результаты клинического исследования крови.
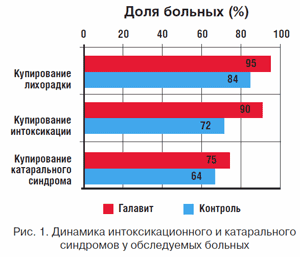
Препарат Галавит положительно влиял на клинические показатели, уменьшая продолжительность лихорадки, интоксикационного и катарального синдромов, и ускорял наступление выздоровления. Купирование температурной реакции отмечалось быстрее у больных, получавших Галавит: уже на 2–й день заболевания температура нормализовалась у 15% больных, принимавших Галавит, и ни у одного из пациентов контрольной группы. К 5–му дню лечения лихорадка купировалась у 95% пациентов из группы принимавших Галавит и только у 84% больных контрольной группы. Первые три дня заболевания интоксикация сохранялась у половины больных, но к 4–му дню явления интоксикации приобрели умеренный характер и сохранялись у 25% больных, получавших Галавит, и почти у половины пациентов из контрольной группы; быстрее исчезал катаральный синдром, проявлявшийся заложенностью носа, першением в горле и кашлем (рис. 1).
Изучение периферической крови пациентов позволило также отметить положительное влияние препарата на нормализацию некоторых показателей. Так, у пациентов, получавших Галавит, к моменту выписки наблюдалась нормализация уровня лейкоцитов, СОЭ, не было палочкоядерного сдвига. У пациентов контрольной группы сохранялся лейкоцитоз и была повышена СОЭ. Кроме того, дополнительно изучались показатели тиолдисульфидного равновесия (SH/SS). Было выявлено, что у пациентов, принимавших Галавит, коэффициент SH/SS увеличился на 15% (против 3% в группе контроля), что свидетельствовало об антиоксидантном действии препарата. Это действие объясняет быструю положительную динамику интоксикационного синдрома.
Важными аспектами, касавшимися повышения качества жизни больных, являлись субъективное улучшение самочувствия, повышение настроения в течение всего периода лечения у пациентов, принимавших Галавит.
Таким образом, можно заключить, что применение удобного в практике препарата Галавит оказалось весьма эффективным при лечении больных гриппом.
Изучение профилактического эффекта препарата Галавит при ОРВИ и гриппе.
В эпидсезон с октября по декабрь 2011 г. было проведено эпидемиологическое наблюдение, касавшееся эффективности применения препарата Галавит с целью профилактики ОРВИ, в организованных коллективах детей в 4 школах–интернатах Москвы. Наблюдались 279 детей в возрасте от 12 до 18 лет; большая часть из них относилась к группе часто болеющих детей или имела хронические заболевания в анамнезе. Случайным образом были выделены две группы.
В контрольной группе (81 человек) применялась только вакцинация против гриппа; в основной (197 человек) вакцинация дополнялась применением Галавита в дозе 50 мг/сут.: у 99 человек ежедневно в течение 5 дней через 2 нед. после вакцинации и у 98 человек – через день курсом 10 дней до вакцинации. Наблюдаемые группы детей не различались по половозрастным характеристикам. Период наблюдения для лиц всех групп составил 30 дней. Оценка эффективности проводилась на основании выявления случаев заболевания ОРВИ и гриппом с расчетом показателей эпидемиологической эффективности: индекса эффективности и показателя защищенности.
Показатели заболеваемости детей в группах эпидемиологического исследования представлены в таблице 1. В основной группе, получавшей курс Галавита в дополнение к вакцинации, заболело 9 детей, причем в подгруппе применения Галавита до вакцинации. Были поставлены диагнозы ОРВИ, острый ринофарингит (7 человек) и ОРВИ, острый ринофаринготрахеит (2 человека). Случаи заболевания ОРВИ регистрировались спустя 16– 18 дней после окончания приема Галавита. В контрольной группе было 4 заболевших; заболевания регистрировались с 8–го по 29–й день наблюдения. Важно отметить, что продолжительность заболеваний в основной группе была на 2 дня меньше, чем в контрольной.
Таблица 1.
Показатели заболеваемости
| Группы | Особенности вакцинации | Число заболевших ОРВИ |
|---|---|---|
| Основная | До начала курса Галавита (n=99) | 9 (9,2%) |
| После курса Галавита (n=98) | 0 | |
| Контрольная | В начале наблюдения (n=81) | 4 (4,9%) |
Для оценки профилактической эффективности применения препарата Галавит рассчитывались эпидемиологические показатели. В основной подгруппе с выявленными случаями заболевания ОРВИ индекс эффективности составил 2,0 при показателе защищенности 50% (уровень достоверности р≤0,05). Полученные данные показали хорошую эффективность комплексной профилактики гриппа и ОРВИ при сочетании вакцинации с приемом короткого курса иммуномодулятора Галавит.
Таким образом, проведенные исследования свидетельствуют об эффективности комплексного лечения и профилактики ОРВИ и гриппа с помощью иммуномодулятора Галавит. Препарат способствует сокращению сроков заболевания и ускорению выздоровления больных благодаря наличию дополнительного противовоспалительного действия.
Галавит может дополнять специфическую противогриппозную вакцинацию для повышения профилактического эффекта против широкого спектра возбудителей ОРВИ, а также использоваться с лечебной целью в комплексе с другими симптоматическими средствами лечения ОРВИ врачами амбулаторно–поликлинического звена, особенно в эпидемический период. Препарат Галавит имеет удобную для амбулаторного применения лекарственную форму в виде таблеток для сублингвального рассасывания по 25 м г. Обычно применяется схема ежедневного приема 100 мг (50 мг для детей) 5 дней, затем по 100 мг (50 мг для детей) через день в течение 10 дней.
Литература
1. Материалы ВОЗ 2006–2009 гг.
2. Ершов Ф.И., Романцов М.Г. Антивирусные средства в педиатрии. М., 2005. 243 с.
3. Романцов М.Г., Киселев О.И., Сологуб Т.В. Этиопатогенетическая фармакотерапия ОРВИ и гриппа // Лечащий врач. 2011. № 2. С. 92–96.
4. Ершов Ф.И., Наровлянский А.Н., Мезенцева М.В. Ранние цитокиновые реакции при вирусных инфекциях // Цитокины и воспаление. 2004. № 1. С. 3–6.
5. Деева Э.Г. Грипп. На пороге пандемии. М., 2008. 208 с.
6. Лыткина И.Н., Малышев Н.А. Профилактика и лечение гриппа и острых респираторных вирусных инфекций среди эпидемиологически значимых групп населения // Лечащий врач. 2010. № 10. С. 66–69.
7. Иммуномодуляторы с противовирусной активностью: учебное пособие / Под ред. М.Г. Романцова. М., 2005. 74 с.