что нового в лечении рмж
Что нового в лечении рмж
HR+ HER2- рак молочной железы
1) Представлены обновленные результаты по общей выживаемости исследования PALOMA-3 (abstr. 1000).
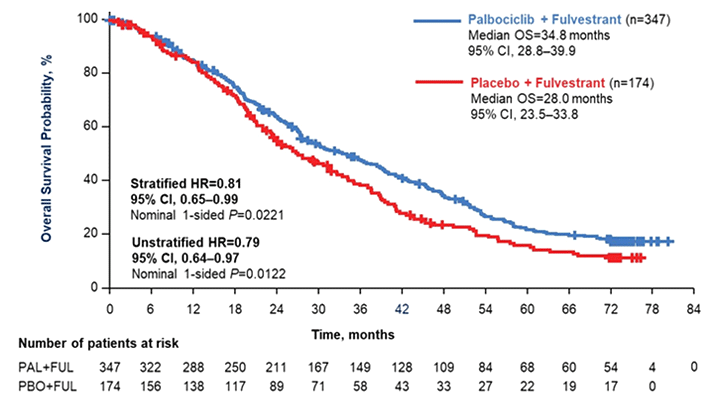
Комбинация ингибиторов CDK4/6 и гормонотерапии (ГТ) в настоящее время является золотым стандартом 1-2 линий лечения метастатического рака молочной железы (мРМЖ), так как она продемонстрировала увеличение частоты объективного ответа (ЧОО), выживаемости без прогрессирования (ВБП) и, в некоторых исследованиях, общей выживаемости (ОВ). В исследовании III фазы PALOMA-3 было показано, что добавление палбоциклиба к фулвестранту во второй линии гормонотерапии метастатического HR+HER2- рака молочной железы достоверно увеличивает медиану ВБП. Однако анализ ОВ при медиане наблюдения в 44,8 месяца не показал достоверных различий между изучаемыми группами, хотя отмечалось существенное численное преимущество медианы ОВ в группе палбоциклиба. Медиана ОВ составила 34,9 месяца в группе палбоциклиба против 28,0 месяцев в группе плацебо (отношение рисков [ОР] 0,814; 95% доверительный интервал [ДИ] 0,644-1,029; р=0,0429).
На ASCO2021 были доложены обновленные данные по ОВ при медиане наблюдения 73,3 месяца. Добавление палбоциклиба к фулвестранту достоверно улучшило 5-летнюю ОВ по сравнению с фулвестрантом – 23,3% против 16,8% (ОР 0,81; 95% ДИ 0,65-0,99; p=0,0221).
Подгрупповой анализ исследования показал, что достоверные различия наблюдались во всех подгруппах, кроме пациенток с гормонорезистентным раком (прогрессирование на предыдущей линии гормонотерапии в сроки менее 6 мес.) и получивших ранее химиотерапию.
2) Представлены обновленные результаты по общей выживаемости исследования MONALEESA-3 (abstr. 1001).
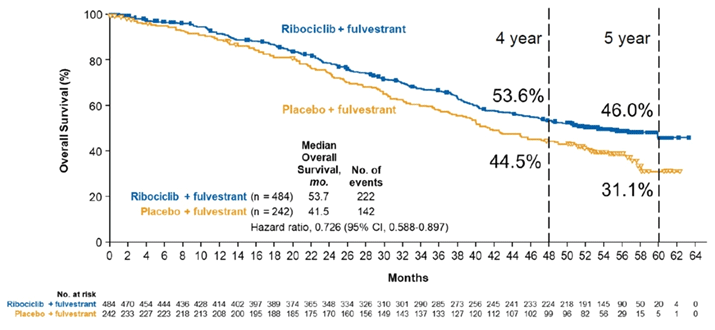
В исследовании III фазы MONALEESA-3 ранее было продемонстрировано статистически значимое улучшение ОВ при добавлении рибоциклиба к фулвестранту в 1-й или 2-й линии терапии пациенток в постменопаузе с метастатическим HR+HER2- раком молочной железы. Медиана ОВ не была достигнута в группе рибоциклиба и составила 40 месяцев в группе плацебо (ОР 0,72; 95% ДИ 0,57-0,92; р=0,00455).
На ASCO2021 были представлены данные по ОВ при медиане наблюдения 56,3 месяца. Медиана ОВ составила 53,7 месяца в группе рибоциклиба против 41,5 месяца в группе плацебо (ОР 0,73; 95% ДИ 0,59-0,90). Преимущество в ОВ от добавления рибоциклиба к фулвестранту наблюдалось как при назначении в 1-й (медиана ОВ не достигнута против 51,8 мес. [ОР 0,64; 95% ДИ 0,46-0,88]), так и во 2-й линии терапии (медиана ОВ 39,7 против 33,7 мес. [ОР 0,78; 95% ДИ 0,59-1,04]). Таким образом, продемонстрированное ранее преимущество в ОВ при добавлении рибоциклиба к фулвестранту сохраняется при медиане наблюдения 4,5 года.
3) Представлены результаты исследования DAWNA-1 (abstr. 1002).
В клиническом исследовании III фазы DAWNA-1 сравнивалась эффективность комбинации нового ингибитора CDK4/6 далпициклиба в комбинации с фулвестрантом по сравнению с фулвестрантом и плацебо во второй и последующих линиях терапии метастатического HR+HER2- рака молочной железы у пациенток в постменопаузе. Первичной конечной точкой была медиана ВБП. В исследование включена 361 пациентка, которые рандомизировались 2:1 в группы далпициклиба и плацебо. При медиане наблюдения 10,5 месяца было показано, что добавление далпициклиба к фулвестранту достоверно улучшает медиану ВБП – 15,7 месяца против 7,2 месяца (ОР 0,42; 95% ДИ 0,31-0,58; р 2 внутривенно в 1, 8, 15 дни 28-дневного цикла) и фамитиниб (20 мг внутрь 1 раз в сутки, непрерывно). Частота объективного ответа (ЧОО) составила 81,3% (39 из 48), что является самым высоким показателем ЧОО при метастатическом тройном негативном раке молочной железы; для сравнения ЧОО на фоне терапии антрациклинами составляет 30-50%, комбинацией антрациклинов и циклофосфаида – 45-55%, таксанами – 37-54%, комбинацией наб-паклитаксела и атезолизумаба при положительной экспрессии PD-L1 – 58,9%. Медиана времени до достижения ответа в данном исследовании составила 1,8 месяца. При медиане наблюдения 9 месяцев медиана ВБП и продолжительности ответа не достигнуты, 62,5% пациентов продолжают лечение без признаков прогрессирования заболевания. Наиболее частыми нежелательными явлениями 3-4 степени стали нейтропения (33,3%), в том числе фебрильная нейтропения (10,4%), анемия (10,4%), тромбоцитопения (8,3%), гипертензия (4,2%), гипотиреоз (4,2%), сепсис (2,1%) и иммунный миокардит (2,1%). Частота отмены терапии в связи с возникновением нежелательных явлений составила 6,3%. У двух пациентов наблюдались серьезные нежелательные эффекты, связанные с лечением. Не сообщалось о случаях смерти, связанной с нежелательными явлениями терапии. Комбинация камрелизумаба (анти-PD-1), наб-паклитаксела и фамитиниба показала многообещающие результаты в первой линии терапии метастатического тройного негативного рака молочной железы, ожидаются результаты проспективного рандомизированного исследования FUTURE-SUPER (NCT 04395989), изучающего эффективность данной комбинации.
Новый терапевтический подход в лечении ранних стадий рака молочной железы
FDA одобрила применение ингибитора CDK4/6 абемацклиба для лечения подтипов РМЖ HR+ и HER2 на ранних стадиях
FDA одобрила применение ингибитора CDK4/6 абемацклиба (препарат Verzenio) для лечения рака молочной железы (РМЖ) определенных подтипов. Это стало первым крупным достижением за последние 20 лет для данной группы пациентов.
Абемациклиб прежде уже был одобрен для лечения подтипов РМЖ HR+ и HER2- местно-распространенной или метастатической стадии. Теперь же препарат можно использовать для более ранних стадий у пациентов, находящихся в группе высокого риска, с узловой формой РМ и при опухолях с показателем Ki-67 более 20%. Это первый ингибитор CDK4/6, который был одобрен для данной группы пациентов (при этом около 70% случаев РМЖ приходится на подтипы HR+ и HER2-).
Одобрение основано на результатах исследования monarchE, которые были представлены на ежегодном собрании Европейского общества онкологии и опубликованы в Journal of Clinical Oncology. Исследование включало 5637 пациентов, разделенных на 2 равные группы.
В работе было показано, что абемациклиб в комбинации с эндокринной терапией (тамоксифен или ингибиторы ароматазы) значительно улучшает выживаемость без прогрессии. Двухлетний показатель составил 92.2% в комбинированной группе и 88.7% в группе контроля для общей популяции пациентов (относительный риск HR = 0.643; 95% ДИ, 0.475 – 0.872; P = 0.0042). Риск рецидива или смерти был ниже на 37% в группе с комбинированным лечением (HR, 0.626; 95% ДИ, 0.49 – 0.80). Это может стать новым стандартным подходов в терапии РМЖ.
Профиль безопасности соответствовал ожиданиям. Наблюдались следующие основные побочные эффекты: диарея, инфекции, нейтропения, слабость, лейкопения, тошнота, рвота, анемия, головные боли, стоматит, лимфопения, тромбоцитопения, снижение аппетита, увеличение АЛТ и АСТ, головокружение, сыпь и алопеция.
Современные методы лечения рака молочной железы
За последние десятилетия прогнозы для женщин, у которых был диагностирован рак молочной железы, существенно улучшились. По данным американских экспертов, с 1989 года выживаемость при раке груди увеличилась почти на 40%.
Во многом это достигнуто за счет скрининга и ранней диагностики. Врачи стали выявлять опухоли на ранних стадиях, когда шансы на ремиссию высоки. Второй важный фактор – прогресс в онкологии. За последние годы появились новые эффективные методы лечения рака молочной железы. Практически все они практикуются на территории России. Для того чтобы получить современное лечение, не обязательно ехать за границу.
Органосохраняющие операции
Все операции при раке молочной железы можно разделить на две большие группы:
С эстетической точки зрения явные преимущества за первой группой вмешательств, ведь они позволяют сохранить молочную железу. Но не повышается ли при этом риск рецидива?
Долгое время врачи считали, что органосохраняющие операции можно выполнять только на ранних стадиях. Если опухоль успела сильно вырасти, лучше не рисковать и выполнить мастэктомию.
В настоящее время доказано, что зачастую мастэктомия не имеет преимуществ. Если удалить только часть груди и провести курс лучевой терапии, прогноз не ухудшится.
Но многое зависит от уровня мастерства врача. Там, где один специалист засомневается и предпочтет провести мастэктомию, более опытный хирург сможет сохранить грудь. Наши специалисты знают, где искать таких врачей.
Сентинель-биопсия
Хотя сентинель-биопсия является диагностической процедурой, о ней обязательно стоит упомянуть, говоря о современных методах лечения рака груди.
Во время операции хирургу нужно ответить на важный вопрос: стоит ли удалять регионарные (близлежащие по отношению к молочной железе) лимфатические узлы? С одной стороны, если есть риск, что в них распространились раковые клетки, их обязательно нужно убрать. С другой стороны, такое вмешательство чревато серьезным осложнением – лимфедемой, состоянием, при котором нарушается отток лимфы от руки. Возникает отек, любая небольшая ранка грозит инфекцией.
У современных хирургов есть надежный ориентир. Во время операции можно провести сентинель-биопсию, или биопсию сторожевого лимфоузла. В опухоль вводят специальный краситель и смотрят, в какой лимфатический узел он распространяется в первую очередь. Этот лимфоузел называется сторожевым, он – первый на пути распространения раковых клеток. Его удаляют и проводят биопсию. Если сторожевой узел «чистый», то удалять другие не имеет смысла, в них тоже нет опухолевых клеток.
Новые классы препаратов
Классически при раке молочной железы применяют химиотерапию. Это эффективный метод лечения рака груди, но он имеет некоторые недостатки. Химиопрепараты атакуют не только раковые, но и нормальные быстро размножающиеся клетки, поэтому они вызывают серьезные побочные эффекты. Иногда опухоли вырабатывают резистентность – перестают реагировать на химиотерапию.
Решить эти проблемы помогает относительно новый класс лекарственных средств – таргетные препараты. Каждый такой препарат имеет строго определенную мишень – молекулу, которая нужна для бесконтрольного размножения и выживания раковых клеток.
В каждой пятой злокачественной опухоли груди на поверхности клеток находится большое количество белков-рецепторов HER2, которые заставляют их размножаться. В таких случаях применяют таргетные препараты-блокаторы рецепторов HER2: трастузумаб (герцептин), пертузумаб, лапатиниб, нератиниб.
Существуют и другие типы таргетных препаратов. Некоторые из них уже применяют при раке молочной железы, другие проходят клинические исследования.
К новым методам лечения рака груди можно отнести и иммунотерапию – набор методик, которые задействуют ресурсы иммунной системы для борьбы с опухолью. В настоящее время проходят испытания некоторых видов иммунотерапии при раке молочной железы.
Персонализированное лечение
Достижения молекулярной биологии и генетики позволяют проводить молекулярно-генетический анализ опухолевых клеток и выбирать сочетания химиопрепаратов, оптимальные для конкретной женщины. Такой подход называется персонализированным лечением. Такую услугу уже предлагают некоторые онкологические клиники в России.
Молекулярно-генетический анализ помогает повысить эффективность химиотерапии, помочь пациенткам, которым перестали помогать стандартные комбинации химиопрепаратов.
Поддерживающая терапия
Лечение рака зачастую сопровождается побочными эффектами. Иногда они снижают качество жизни и создают угрозу для здоровья. Подход современных онкологов состоит в том, что каждый пациент должен переносить курс лечения комфортно. В этом помогают современные методы поддерживающей терапии.
Важно и психологическое благополучие женщины, ее близких людей. На Западе этими вопросами занимаются психоонкологи. В России найти такого специалиста очень сложно, но в некоторых клиниках они есть.
Где можно воспользоваться новыми методами лечения рака молочной железы в Москве?
В столице есть клиники, где можно получить лечение на уровне ведущих западных онкологических центров. Хирургические вмешательства любой сложности, оригинальные препараты последних поколений – все это есть. Центр Комплексной Медицины сотрудничает с лучшими онкологическими клиниками Москвы.
Лечение рака молочной железы
Способы лечения рака молочной железы зависят от стадии онкопроцесса и наличия вторичных образований.
Лечение рака молочной железы опирается на результаты генетического, иммунологического исследования, изменений в общеклинических и биохимических анализах, а также от наличия сопутствующих заболеваний.
Новые технологии приходят в Россию.
Приглашаем пациентов принять участие в новых методах лечения онкологических заболеваний, а также в клинических испытаниях препаратов на основе Т-клеток (LAK-терапия). Терапия проводится в различных научно-исследовательских онкологических центрах, в зависимости от вида опухоли.
Отзыв о методе профессора Скворцовой В.И.
Комментарий о клеточных технологиях главного онколога России, академика Давыдова М.И.
Виды терапии РМЖ на ранних стадиях

2. Вторая стадия – радикальное удаление, зачастую проводится расширенная мастэктомия. Лечение рака молочной железы дополняется лучевой и химиотерапией, возможны к назначению иммунологические и гормональные средства.
В настоящее время основная тенденция на начальных этапах – максимально сохранить нетронутые опухолью ткани. Зачастую лечение рака молочной железы сочетается с проведением радиотерапии, чтобы минимизировать размеры злокачественности во время хирургического лечения.
Существующие методики
Их можно разделить на 2 большие группы:
• местного воздействия – облучение, операция,
• системного влияния – химио-, гормоно- и иммунотерапия.
При этом врачи руководствуются преимущественно следующими критериями:
• Маленькие онкоочаги и отсутствие отдаленных метастаз – секторальная резекция железы или мастэктомия с иссечением лимфоузлов, проведение инраоперационной биопсии, по результатам которой обычное удаление заменяют расширенной мастэктомией.
• В случае крупного онкообразования и наличия отдаленных патологий – химиотерапия и другое консервативное лечение рака молочной железы.
Гормонотерапия
РМЖ часто является гормонозависимой опухолью, на рост которой влияют различные железы внутренней секреции. В ходе клинических наблюдений выявилось, что некоторые гормоны, в первую очередь эстрогены, прямо или опосредованно влияют на появление и дальнейшую скорость роста. Поэтому еще недавно самым популярным лечением рака молочной железы была овариоэктомия (удаление яичников), хотя полное излечение при этом наступало лишь у трети женщин.
Впоследствии были более досконально изучены механизмы воздействия гормонов на опухолевую ткань, включая действие по принципу положительной и обратной отрицательной связи. И с начала семидесятых годов прошлого столетия наступил прорыв в лечении рака молочной железы: были созданы и протестированы различные новые лекарственные препараты, обеспечивающие блокирование рецепторов гормонозависимых опухолей (тамоксифен, торемифен) или подавляющие производство эстрогенов (аримидекс, фемара).
Достаточно успешной альтернативой удалению яичников стал препарат госерилин (золадекс), который успешно подавляет образование эстрогенов на строго определенное время. Создавая таким образом состояние медикаментозного климакса и применяя комплексную терапию можно добиться успеха в лечении рака молочной железы. А после завершения терапевтического курса и при прекращении приема золадекса, яичники начинают функционировать снова.
Препараты
Лечение рака молочной железы препаратом Тамоксифен является наиболее часто используемым лекарством при гормонозависимых раках. Однако у него имеются серьезные побочные эффекты, включая малигнизацию эндометрия и повышение риска возникновения тромбоэмболии.Поэтому в последние годы был предложен целый ряд лекарств, ингибирующих ароматазу, например:
Другие средства – аромазин, фемара. Они особенно показаны после приема тамоксифена в течение 5 последних лет.
Разработки ученых увенчались успехом, найден способ воздействовать на опухоль – это таргетные препараты. Сегодня таргетная терапия является серьезным продвижением в современной онкологии.
Хирургическое оперативное вмешательство
Органосохраняющую операцию выполняют в случае размера онкоочага до 2,5 см. Однако в качестве профилактики рецидива возможно иссечение регионарных лимфоузлов. При классической мастэктомии происходит полное удаление всех тканей железы. Установка протеза и пластика груди выполняются или непосредственно во время хирургического вмешательства, или спустя шесть месяцев. Это зависит от общего состояния пациентки и характера операции.
Объемы операции
Онкохирурги рекомендуют следующие виды удаления молочной железы:
• иссечение лишь ее сектора – лампэктомия,
• полностью, но без резекции лимфоузлов подмышечной группы,
• с удалением лимфоузлов регионарных – модифицированная радикальная мастэктомия,
• единым блоком с прилежащими к ней мышцами – радикальная мастэктомия (расширенная),
• удаляются все ткани железы за исключением кожи и соска (важно для последующей реконструкции груди).
Радиотерапия
В лечебных дозах ионизирующее излучение угнетает развитие онкоклеток и вызывает их разрушение. Таким способом можно воздействовать на первичную патологию, и метастазы. Радиооблучение может стать единственным вариантом в качестве самостоятельного метода при неоперабельности новообразования или использоваться с целью минимизации размеров злокачественного процесса перед проведением хирургии.
После мастэктомии облучение ложа опухоли существенно уменьшает вероятность рецидива. В качестве основного метода радиотерапии обычно используется дистанционное облучение. Современные аппараты позволяют минимизировать поражение здоровых тканей, концентрируя свое пагубное воздействие именно в пределах опухолевого очага. Поэтому сегодня крайне редко наблюдаются типичные осложнения, возникающие после завершения курса радиотерапии, включая радиационные ожоги.
Как бороться с метастазами
Обычно молочный рак имеет свойство метастазировать практически во все органы, включая легкие, кости, печень, брюшную полость и кожные покровы. Лечение отдаленных от материнского новообразования опухолей зависит от следующих факторов:
• размеры метастаз, их количество, локализация,
• степень чувствительности онкоклеток к эстрогенам, прогестерону,
• особенности функционирования яичников (состояние фертильности или климакс).
Наиболее успешно в лечении метастаз РМЖ считаются следующие средства:
Они часто сочетаются с медикаментами, уменьшающими токсичность первых и снижающими вероятность возникновения или выраженность уже существующих побочных эффектов. Например, при добавлении преднизона снижается токсическое воздействие на кроветворную систему и органы пищеварения, однако повышается вероятность появления тромбозов и вторичной инфекции. С целью повышения терапии цитостатиками также могут назначаться предварительные курсы иммуномодуляторами, включая интерфероны, интерлейкины и различные моноклональные антитела.
В случае рецидива показаны гормональные препараты и цитостатики. Если же положительного эффекта не наблюдается, то рекомендуют клеточную биоиммунотерапию или использование препаратов, проходящих клинические испытания.
Диспансеризация
После хирургического иссечения необходимо встать на учет у онколога и регулярно являться на контрольные осмотры. Они нужны для того, чтобы своевременно заметить возобновление злокачественного роста и предпринять соответствующие меры. Сначала визиты к доктору необходимы каждые 5 месяцев, а по прошествии 5 лет – ежегодно. На фоне лечения тамоксифеном важно ежегодно проходить ПЭТ или МРТ органов малого таза, чтобы своевременно обнаружить раковое перерождение клеток эндометрия. А при употреблении ингибиторов ароматазы – остеоденситометрию (проверку минеральной плотности костей). В случае рецидива или обнаружения МТС назначается курс химио- и лучевой терапии.
Прогноз и продолжительность жизни
Когда дело касается онкобольных, то основным критерием эффективности проводимого лечения является показатель пятилетней выживаемости. Молочный рак имеет показатель чуть более 50%. Однако, перешагнув эту черту, рецидивов в ближайшие годы уже практически дальше не наблюдается.
Продолжительность жизни зависит от таких факторов, как:
• характер и скорость ее роста,
Наиболее неблагоприятным считается прогноз при диффузном типе роста клеток и запущенной форме болезни при наличии отдаленных МТС. В этом случае показатель пятилетней выживаемости практически равен нулю.
Однако при ранней диагностике заболевания и начале своевременного лечения шансы увеличить порог выживаемости значительно возрастают. Так при второй стадии 80% женщин живут более 5, а чаще и 10 лет, а свыше половины из них перешагнут и двадцатилетний рубеж. Вероятность успешного излечения значительно повышается при использовании сразу нескольких видов терапии.
В случае третьей стадии рака 5 и более лет живут 40-60% женщин (зависит от того, подстадия 3А или 3В). Однако и здесь адекватная медицинская помощь способна повысить продолжительность жизни и сделать ее более комфортной.
Для подбора эффективного метода лечения вы можете обратиться за
— методы инновационной терапии;
— возможности участия в экспериментальной терапии;
— как получить квоту на бесплатное лечение в онкоцентр;
— организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Что нового в лечении рмж
C 8 по 11 декабря 2020 года состоялся 43-й Ежегодный симпозиум по раку молочной железы в Сан-Антонио (43 rd Annual San Antonio Breast Cancer Symposium – SABCS). В этом году исследователями из более чем 80 стран было представлено рекордное количество абстрактов (1194 абстракта), что еще раз доказывает актуальность проведения клинических исследований, несмотря на пандемию COVID-19. Прошлый 2020 год ознаменовался прогрессом в лечении больных раком молочной железы, в США зарегистрировано 4 новых противоопухолевых препарата для лечения больных с агрессивными подтипами метастатического рака молочной железы (РМЖ).
ER+ HER2- ранний РМЖ (рРМЖ)
Kalinsky и соавт. представили результаты одного из наиболее ожидаемых и обсуждаемых исследований SWOG S1007 RxPONDER по изучению стандартной адъювантной эндокринотерапии ± химиотерапии среди больных ER+ HER2- рРМЖ со шкалой рецидива 25 и менее с 1-3 пораженными лимфатическими узлами (ЛУ) [1]. Значение оценки риска рецидива Oncotype DX для определения больных с (ЛУ-) HR+HER2- рРМЖ, которым может не проводится химиотерапия (ХТ), было установлено в ходе исследования TAILORx в 2018 году. Однако оставалось неясным, могут ли результаты TAILORx быть экстраполированы на больных с (ЛУ+) РМЖ. В обоих клинических исследованиях для оценки риска рецидива применялся мультигенный тест Oncotype Dx.
В исследовании SWOG S1007 RxPONDER были проанализированы сведения о 5083 больных (медиана наблюдения составила 5,1 лет). В результате были зарегистрированы 447 случаев рецидива инвазивного заболевания. При первичном анализе преимущество ХТ в зависимости от шкалы рецидива не было статистически значимым (p=0,30). Однако в группе высокого риска наблюдалось снижение выживаемости без рецидива инвазивного заболевания (ОР 1,06; 95% ДИ 1,04-1,07; p 15% – среди 27,7%. Риск рецидива по CPS-EG ≥3 отмечен у 54,7% больных. Дополнительно к таргетной терапии палбоциклибом половина пациентов (50,1%) получала ингибиторы ароматазы, 49,8% – тамоксифен, 6,6% – ингибиторы ароматазы + агонисты гонадотропин-рилизинг гормона и 9,7% – тамоксифен + агонисты гонадотропин-рилизинг гормона.
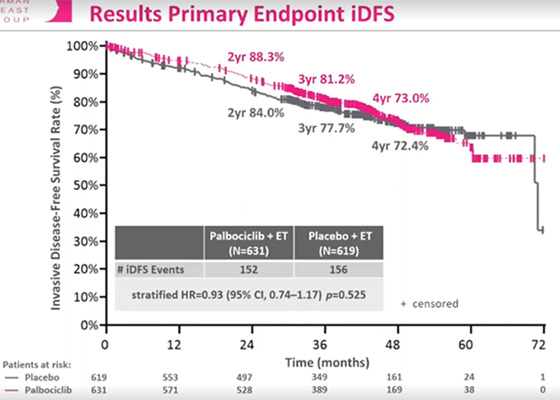
Согласно результатам, при медиане наблюдения 43 месяца дополнительное назначение палбоциклиба не привело увеличению БРВ (ОР 0,93; 95% ДИ 0,74-1,17; р=0,525). Показатель безрецидивной выживаемости равнялся 88,3% в группе палбоциклиб + ГТ против 84% в группе плацебо + ГТ в течение 2 лет; 73% против 72,4% в течение 4 лет. Также не установлено различий в показателях ОВ. Докладчиком отмечена необходимость получения в будущем информации о результатах долгосрочного наблюдения при применении других CDK4/6 ингибиторов с целью оценки их эффективности. Одной из причин неудачи исследования, возможно, является отличие в определении больных группы высокого риска рецидива. В исследование включались только пациенты с резидуальным РМЖ, у которых не наблюдалось полного патоморфологического ответа (pCR). Число испытуемых в исследовании PENELOPE-B было в 4 раза меньше, чем в исследовании PALLAS и МonarchE, а также использовался как предикторный фактор рецидива CPS-EG индекс, а не стадия заболевания. Возможно, абемациклиб является более эффективным CDK4/6 ингибитором, однако это не подтверждается в исследованиях 1-й линии метастатического РМЖ, при которых отмечались схожие результаты при лечении палбоциклибом.
Рисунок 3. Исследование III фазы PENELOPE-B: палбоциклиб в комбинации с ГТ для лечения
пациентов с HR+ HER2- ранним (операбельным) РМЖ высокого риска рецидива после НАХТ.
РЕАБИЛИТАЦИЯ БОЛЬНЫХ РАННИМ РМЖ
В исследование биопсихосоциального подхода в реабилитации больных рРМЖ [4] были включены сведения о 228 больных, получивших комплексное лечение заболевания. Из них 114 больных были включены в проспективное исследование и на протяжении лечения подвергались реабилитационным мероприятиям в рамках биопсихосоциального подхода и 114 больных были подобраны в контрольную группу ретроспективно по методике попарного отбора. Реабилитационные мероприятия в рамках биопсихосоциальной модели улучшили показатели бессобытийной БСВ в группе больных рРМЖ: БСВ составила 18,3 мес. против 14,5 мес. в контрольной группе (ОР 0,91; 95% ДИ 0,83-0,99; p=0,0034). При многофакторном анализе ключевыми факторами, влияющими на БСВ, были НАХТ (ОР 0,79; 95% ДИ 0,69-0,94; р=0,0025), возраст (ОР 0,87; 95% ДИ 0,71-1,09; р=0,0027) и менопаузальный статус (ОР 0,85; 95% ДИ 0,84-0,95; р=0,0022). Кроме того, важно отметить, что биопсихосоциальная модель реабилитация больных рРМЖ позволяет учитывать не только биологические (генетические, анатомические, физиологические, биохимические и др.), но и психологические факторы, включающие в себя психические процессы, индивидуальные психологические особенности личности и поведения, а также социальные факторы.
МЕТАСТАТИЧЕСКИЙ РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
Трижды негативный метастатический РМЖ
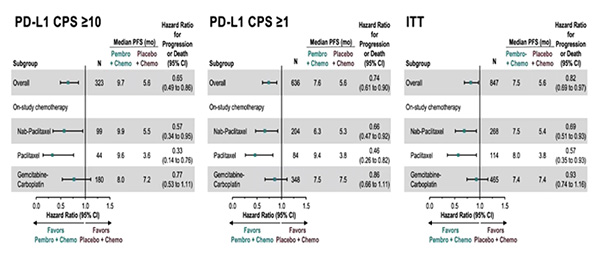
В ходе конгресса были доложены результаты по дополнительным вторичным оценочным конечным точкам исследования KEYNOTE-355 (Rugo H. и соавт.) по изучению применения пембролизумаба в комбинации с ХТ 1-й линии терапии местно-рецидивирующего неоперабельного или метастатического трижды негативного РМЖ (ТНРМЖ) [5]. Ранее при промежуточном анализе данных было отмечено статистически значимое увеличение БПВ при применении пембролизумаба в сочетании с ХТ (наб-паклитаксел / паклитаксел / гемцитабин + карбоплатин) vs только ХТ при экспрессии PD-L1 CPS ≥10 (ОР 0,65; 95% ДИ 0,49-0,86; одностороннее значение P=0,0012, заранее оговоренный статистический критерий альфа = 0,00411). Вторичные конечные точки включали частоту объективных ответов (ОО), частоту контроля над заболеванием (полный регресс + частичный регресс + стабилизация заболевания ≥24 недель), а также длительность ответа.
Результаты по всем вторичным конечным точкам показали преимущество комбинации пембролизумаб + ХТ при наличии PD-L1 экспрессии. Частота ОО при CPS ≥10 составила 53,2% (95% ДИ 46,4-59,9%) vs 39,8% (95% ДИ 30,3-49,9%); при CPS ≥1 – 45,2% (95% ДИ 40,4-50,0%) vs 37,9% (95% ДИ 31,3-44,8%).
При подгрупповом анализе увеличение показателя ВБП в группе пембролизумаб + ХТ наблюдалось вне зависимости от комбинаторного химиотерапевтического препарата. Данные результаты вызывают особый интерес, учитывая негативные результаты в исследовании IMPASSION131, которое показало отсутствие увеличения ВБП и ОВ при назначении атезолизумаба в комбинации с еженедельным паклитакселом (возможно, по причине индуцированной иммуносупрессии, вызванной еженедельным введением дексаметазона с целью премедикации). Однако сравнение эффективности комбинаторных цитостатиков не являлось целью исследования, именно поэтому сделать объективные выводы в настоящий момент не представляется возможным. Также отмечено сравнительное снижение эффективности пембролизумаба в комбинации гемцитабин + карбоплатин, что обусловлено изначально плохим прогнозом в данной группе больных.
При CPS ≥10 выживаемость без прогрессирования в группе больных мТНРМЖ пембролизумаб + ХТ составила 9,7 мес. vs 5,6 мес. в группе плацебо + ХТ (ОР 0,65; 95% ДИ 0,49-0,86); при CPS ≥1 показатели ВБП составили 7,6 мес. vs 5,6 мес. соответственно (ОР 0,74; 95% ДИ 0,61-0,90).
На основании результатов KEYNOTE-355 в улучшении показателей выживаемости без прогрессирования FDA присвоило статус ускоренного одобрения комбинации пембролизумаб + ХТ для лечения больных с местно-рецидивирующим нерезектабельным или метастатическим ТНРМЖ с экспрессией PD-L1 (CPS ≥10). Данные по ОВ ожидаются в 2021 году.
Рисунок 4. Исследование III фазы KEYNOTE-355: пембролизумаб в комбинации с химиотерапией
в 1-й линии терапии неоперабельного или метастатического ТНРМЖ.
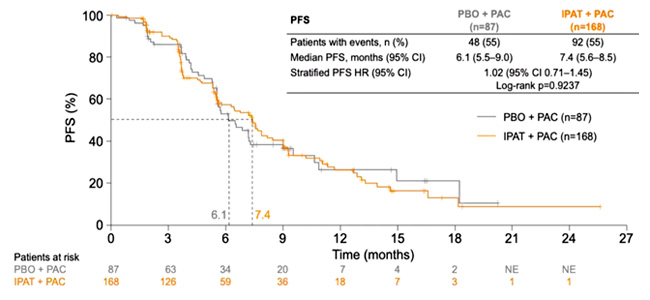
Dent R. et al представили результаты исследования III фазы IPATunity130, анализирующего эффективность комбинации ипатасертиб + паклитаксел при мутациях в сигнальном пути PIK3CA/AKT1/PTEN в качестве 1-й линии терапии местнораспространенного или метастатического ТНРМЖ [6].
Ранее согласно результатам клинического исследования II фазы LOTUS наблюдалось увеличение показателей ВБП в группе больных ТНРМЖ с мутацией в PIK3CA/AKT1/PTEN сигнальном пути (4,9 vs 9,0 мес.; ОР 0,44; 95% ДИ 0,37-0,98).
Известно, что PIK3CA/АКТ сигнальный путь является необходимым для метаболизма, пролиферации и инвазии опухолевых клеток. Ипатасертиб – пероральный высокоспецифичный препарат, предназначенный для таргетного воздействия на все три изоформы АКТ (серин-треониновой протеинкиназы). Ипатасертиб блокирует сигнальный путь PI3K/AKT – ключевой фактор роста и пролиферации опухолевых клеток при РМЖ. Когорта А включала пациентов, у которых была обнаружена мутация в гене PIK3CA или AKT1- и/или PTEN. Пациенты не получали ранее химиотерапию по поводу распространенного ТНРМЖ.
Пациенты были рандомизированы 2:1 и получали ипатасертиб 400 мг или плацебо (день 1-21) в комбинации с паклитакселом 80 мг/м 2 (Д 1, 8, 15). Отмечено отсутствие преимущества в показателях ВБП в группах пациентов, получавших ипатасертиб + паклитаксел vs плацебо + паклитаксел (7,4 vs 6,1 мес.; ОР 1,02; 95% ДИ 0,71-1,45; р=0,9237). Результаты исследования III фазы IPATunity130 отличаются от ранее полученных результатов исследований II фазы АКТ ингибиторов при ТНРМЖ: в исследовании LOTUS по изучению комбинации паклитаксел + ипатасертиб и в исследовании PAKT по изучению комбинации паклитаксел + капивасеритиб. Кроме того, необходимо выделение потенциальных биомаркеров для определения группы пациентов ТНРМЖ, которая может получить преимущество от назначения АКТ ингибиторов, в том числе и ипатасертиба.
Рисунок 5. Исследование III фазы IPATunity130: ипатасертиб + паклитаксел
в 1-й линии терапии нерезектабельного или метастатического ТНРМЖ.
ER+HER2- метастатический РМЖ
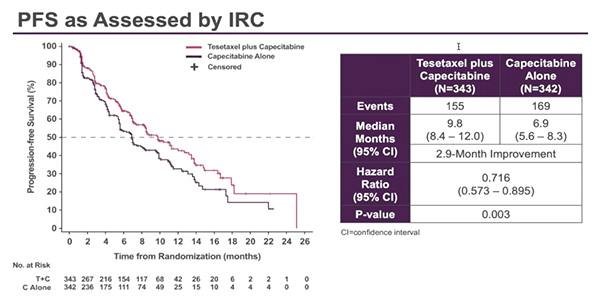
O’Shaughnessy и соавт. представили результаты исследования III фазы CONTESSA по ВБП при применении тезетаксела в комбинации с редуцированной дозой капецитабина (1650 мг/м 2 ) vs стандартная доза капецитабина (2500 мг/м 2 ) в монорежиме для лечения больных с HR+HER2- мРМЖ, ранее получавших препараты таксанового ряда (исследование выполнено совместно с НМИЦ онкологии им. Н.Н. Петрова) [7].
Тезетаксел – новый препарат для приема внутрь таксаного ряда, назначаемый в дозировке 27 мг/м 2 1 раз в 3 недели. В отличие от других препаратов таксанов, тезетаксел обладает более длительным периодом полувыведения и не нуждается в премедикации.
Ранее сообщались обнадеживающие результаты II фазы исследования по применению тезетаксела в монорежиме, ЧОО составила 45% и медиана ВБП – 5,4 мес. (Seidman et al, 2018 ASCO Annual Meeting).
В исследование были включены 685 больных ER+HER2- мРМЖ. Медиана ВБП составила 9,8 мес. в группе тезетаксел + капецитабин vs 6.9 мес. капецитабин в монорежиме (ОР 0,716; 95% ДИ 0,573-0,895; p=0,003). Частота объективных ответов составила 57% vs 41% (p=0,0002). Данные по ОВ ожидаются. Нейтропения была наиболее частым нежелательным явлением ≥3 степени (71,2% vs 8,3%). Отмена терапии в связи с нейтропенией или фебрильной нейтропенией в группе тезетаксел + капецитабин – 4,2%, в группе капецитабина – 1,5%. Частота развития нейропатии ≥3 степени – 5,9% vs 0,9%, алопеции ≥2 степени – 8,0% vs 0,3%. Следовательно, увеличение ВБП, а также удобство дозировки перорального препарата, отсутствие необходимости госпитализации, сравнительно низкая частота развития нейропатии ≥3 степени могут свидетельствовать в пользу применения тезетаксела в комбинации с редуцированной дозой капецитабина для лечения больных HR+HER2- мРМЖ.
Рисунок 6. Исследование III фазы CONTESSA: Эффективность тезетаксела в комбинации
с редуцированной дозой капецитабина (1650 мг/м 2 ) vs стандартная доза капецитабина (2500 мг/м 2 )
в монорежиме для лечения больных HR+HER2- метастатическим РМЖ, ранее получавших таксаны.
Определение циркулирующих опухолевых клеток при метастатическом РМЖ
Janni W. и соавт. доложены результаты метаанализа по изучению определения циркулирующих опухолевых клеток (ЦОК) с целью оценки ответа на лечение при метастатическом РМЖ [8]. В анализ были включены сведения о 3877 случаях с результатами оценки циркулирующих опухолевых клеток до начала лечения и спустя 29 дней после начала лечения. У 772 больных не определялись ЦОК как до, так и после начала терапии (neg/neg), у 286 больных наблюдалось приобретение ЦОК после лечения (neg/pos), у 1054 пациентов была отмечена конверсия из ЦОК+ в ЦОК- (pos/neg) и 1765 больных имели хотя бы одну ЦОК до и после начала терапии (pos/pos).
Медиана ОВ для групп neg/neg, neg/pos, pos/neg и pos/pos была 47,05, 29,67, 32,20, и 17,87 мес. (p