буферный аспирин что это
Некоторые аспекты применения ацетилсалициловой кислоты и клопидогрела у кардиологических больных
Рассмотрены возможности использования ацетилсалициловой кислоты и клопидогрела у больных со стабильными проявлениями атеротромбоза для первичной профилактики сердечно-сосудистых заболеваний и вопросы безопасности антитромбоцитарной терапии.
Possibilities of use of acetylsalicylic acid and clopidogrel in patients with stable implications of atherothrombosis, for primary prevention of cardiovascular diseases and safety questions of antithrombocytic therapy are surveyed.
Признание атеротромбоза основой патогенеза большинства сердечно-сосудистых заболеваний (ССЗ), успехи в изучении молекулярных механизмов тромбообразования оказали влияние на развитие антитромбоцитарной терапии и способствовали появлению новых препаратов [1]. Наиболее изученными и широко применяемыми в клинической практике антитромбоцитарными препаратами в настоящее время являются ацетилсалициловая кислота (АСК) и клопидогрел.
В качестве лекарственного средства АСК известна с 1899 г. Несмотря на более чем 100-летний опыт использования и появление в последние годы новых антиагрегантов, АСК удалось сохранить за собой позиции «золотого» стандарта антитромбоцитарной терапии. В основе антитромбоцитарного действия АСК лежит ее способность необратимо ингибировать фермент циклооксигеназу (ЦОГ) тромбоцитов, вследствие чего снижается образование тромбоксана А2 — мощного стимулятора агрегации тромбоцитов и вазоконстриктора. Циклооксигеназа имеет две изоформы: ЦОГ-1 и ЦОГ-2. Притом, что АСК блокирует обе изоформы, ее активность в отношении ЦОГ-1 в тромбоцитах в 50–100 раз выше, чем влияние на ЦОГ-2 в моноцитах и других клетках воспаления. Поскольку тромбоциты не имеют ядра и поэтому не способны синтезировать белки, необратимое ингибирование ЦОГ-1 приводит к тому, что блокада синтеза тромбоксана А2 под действием АСК сохраняется на протяжении всего периода жизни тромбоцитов (в течение 7–10 дней). Именно способность необратимо блокировать ЦОГ-1 обусловливает стабильный и длительный антитромбоцитарный эффект АСК [2].
Клопидогрел по химической структуре относится к тиенопиридинам. Механизм антитромбоцитарного действия клопидогрела отличается от такового АСК и заключается в селективном и необратимом ингибировании P2Y12-рецепторов тромбоцитов, что, в свою очередь, приводит к угнетению стимуляции аденилатциклазного механизма и блокированию связанного с ним сигнала, направленного на усиление агрегации тромбоцитов [3]. Клопидогрел является пролекарством и метаболизируется в печени в активный метаболит с помощью нескольких изоферментов цитохрома Р450 (CYP). Исследования последних лет показали, что существуют полиморфизмы генов, носительство которых ассоциируется со снижением активности ферментов, участвующих в превращении клопидогрела в активный метаболит [4]. Так, носительство аллеля CYP2C19*1 обеспечивает полностью функционирующий метаболизм, тогда как носительство аллелей CYP2C19*2 и CYP2C19*3 уменьшает функциональную активность ферментов, метаболизирующих клопидогрел. Установлено, что носительство различных аллелей CYP2C19 определяет не только фармакокинетику активного метаболита клопидогрела, но и антитромбоцитарный эффект. По данным ряда исследований [5–10], носительство аллелей CYP2C19*2 и CYP2C19*3 соотносится с меньшим подавлением агрегации тромбоцитов и более высокой частотой неблагоприятных сердечно-сосудистых событий (включая тромбозы внутрикоронарных стентов) у больных, получающих клопидогрел в стандартной дозировке (75 мг/сут).
Важно отметить, что при одновременном применении АСК и клопидогрела антитромбоцитарный эффект усиливается. Предполагают, что это обусловлено синергизмом между двумя препаратами в подавлении агрегации тромбоцитов, индуцированной коллагеном [3, 11].
Ацетилсалициловая кислота, безусловно, является более изученным препаратом, чем клопидогрел, поэтому неудивительно, что спектр ее применения в кардиологии значительно шире. Назначение АСК позволяет уменьшить частоту неблагоприятных исходов у больных стабильной и нестабильной стенокардией, инфарктом миокарда с наличием зубца Q на ЭКГ и без такового, после чрескожных коронарных вмешательств и операции аортокоронарного шунтирования, при цереброваскулярной болезни, а также у пациентов с перемежающейся хромотой атеросклеротического происхождения. Согласно рекомендациям европейских, американских и российских медицинских сообществ при всех вышеперечисленных заболеваниях и состояниях рекомендован неограниченно долгий (пожизненный) прием АСК. В разных рекомендациях при одном и том же заболевании предписано использовать различные дозы АСК (так, например, в Европе поддерживающая доза АСК обычно составляет 75–100 мг/сут, а в США — 81 мг/сут), но предпочтительны все-таки низкие дозы АСК как минимально эффективные.
Клопидогрел рекомендуется использовать в основном в комбинации с АСК (так называемая двойная антитромбоцитарная терапия) при инфаркте миокарда и нестабильной стенокардии, а также у больных, подвергнутых чрескожным коронарным вмешательствам, поскольку, как было показано в многочисленных крупных исследованиях, добавление клопидогрела к АСК в этих ситуациях превосходит по эффективности монотерапию АСК. Монотерапия клопидогрелом как альтернатива монотерапии АСК может быть рекомендована только при атеросклеротическом поражении артерий нижних конечностей [12–14] и в качестве средства вторичной профилактики у больных, перенесших острое нарушение мозгового кровообращения [15–17]. Во всех остальных случаях монотерапия клопидогрелом возможна лишь при непереносимости АСК.
Рассмотрим более подробно некоторые аспекты применения АСК и клопидогрела в кардиологической практике.
Первичная профилактика ССЗ
Н. М. Воробьёва, доктор медицинских наук
ФГБУ РКНПК МЗ РФ, Москва
Проблемы безопасности при использовании препаратов ацетилсалициловой кислоты для профилактики сердечно-сосудистых осложнений
В настоящем обзоре представлены данные о проблемах назначения ацетилсалициловой кислоты в широкой клинической практике. Рассмотрены вопросы, касающиеся возможностей профилактики поражений желудочно-кишечного тракта.
This review present data on problems in using of acetilsalicylic in cardiovascular prevention. The questions concerning opportunities of prevention of defeats of a gastrointestinal path are considered.
Лечение низкими дозами ацетилсалициловой кислоты (АСК) (в монотерапии или в комбинации с другими антитромбоцитарными препаратами) на сегодняшний день является основой вторичной профилактики при ишемической болезни сердца. Длительная терапия низкими дозами АСК рекомендована больным со стабильной ишемической болезнью сердца, у пациентов, перенесших острый коронарный синдром с подъемом и без подъема сегмента ST, после реваскуляризации [1–3].
Применение низких доз АСК в первичной профилактике вызывает больше вопросов. Здесь, при определении показаний к назначению АСК, ключевое значение приобретает соотношение пользы от назначения препарата и риском, связанным с его использованием. В настоящее время рекомендации Европейского общества кардиологов и Европейского общества гипертонии предусматривают назначение АСК больным с высоким риском сердечно-сосудистых осложнений, а также при снижении функции почек при условии хорошего контроля за артериальным давлением (АД) [4]. Выделение именно этих групп больных базируется на результатах субанализа исследования HOT. В этом исследовании участвовало 18 750 больных с артериальной гипертензией (АГ). Одной из задач исследования было оценить эффективность для первичной профилактики терапии АСК в дозе 75 мг/сут. Было показано снижение риска всех сердечно-сосудистых событий на 15% и инфаркта миокарда на 36%. Однако риск кровотечений увеличивался в 1,65 раза. Субанализ показал наиболее значимую эффективность применения АСК у больных с уровнем креатинина выше 1,3 мг/дл, АД выше 180/107 мм рт. ст. и у больных с высоким и очень высоким риском сердечно-сосудистых событий. При этом в этих группах не наблюдается значимого увеличения риска кровотечений [5].
Метаанализ трех основных исследований (JPAD, POPADAD и ETDRS), где АСК использовалась в качестве средства первичной профилактики у больных с сахарным диабетом, показал снижение риска всех сердечно-сосудистых событий на 9%. Именно поэтому применение низких доз АСК у больных с диабетом должно базироваться на индивидуальной оценке риска. Соотношение риск/польза склоняется в сторону большей полезности лишь у больных с высоким дополнительным риском [6].
Хотя применение АСК в первичной профилактике показано только больным высокого риска, АСК остается наиболее часто назначаемым в рутинной практике антитромбоцитарным препаратом. При опросе пациентов двух семейных клиник Канады оказалось, что лица старше 50 лет в 39% случаев регулярно получают АСК, причем 53% пациентов получают АСК для первичной профилактики сердечно-сосудистых и 46% с целью вторичной профилактики. Частота назначения АСК возрастает с возрастом. В возрастной группе 50–59 лет АСК получают 24% пациентов, в возрасте 70–79 лет — 48%. С возрастом возрастает пропорция больных, получающих АСК для вторичной профилактики сердечно-сосудистых осложнений [7]. При анализе 131 050 электронных карт больных, наблюдавшихся врачами общей практики в США, в период с 2008 по 2011 год оказалось, что доля больных, получающих АСК в рамках первичной профилактики осложнений, растет, несмотря на то, что польза от назначения АСК всем больных с АГ, сахарным диабетом, дислипидемией не является доказанной [8]. Широкое применение АСК делает особенно актуальной задачу оценки риска осложнений антитромбоцитарной терапии и поиск возможных путей профилактики этих осложнений.
Влияние антитромбоцитарных препаратов на состояние желудочно-кишечного тракта
Ульцерогенное действие АСК складывается из прямого повреждающего действия кислоты на слизистую оболочку ЖКТ и воздействия на синтез простагландинов. В синтезе простагландинов участвует фермент циклооксигеназа 1-го типа (ЦОГ-1), которую и блокируют нестероидные противоспалительные средства (НПВС), в том числе и АСК. Простагландин Е2 улучшает микроциркуляцию стенки ЖКТ, стимулирует синтез слизи и бикарбонатов, являющихся основным защитным барьером слизистой оболочки, нейтрализующим действие пепсина, желчных кислот и соляной кислоты. В целом при популяционной оценке риска, связанного с приемом НПВС, оказалось, что прием низких доз АСК несет за собой даже несколько меньший риск кровотечений из ЖКТ, чем НПВС (5,5 и 6,1). Нужно отметить, что ульцерогенным эффектом обладают и селективные ингибиторы циклооксигеназы 2-го типа. Это связывают с недостаточной степенью селективности и некоторым остаточным воздействием на ЦОГ-1. АСК в дозах, использующихся в кардиологической практике (325 мг и менее), по ульцерогенному эффекту сопоставима с неселективными НПВС. На большой когорте из почти 3000 больных провели ретроспективную оценку частоты возникновения поражений ЖКТ у больных, получающих низкие дозы АСК, и больных, получающих терапию НПВС. 1103 больных получали лечение АСК, 1856 больных — НПВС. Частота развития поражений ЖКТ составила 2,54% и 0,27% соответственно. При этом более высокая частота развития эрозивно-язвенных поражений при лечении АСК связана, вероятно, с более высокой степенью подавления синтеза простагландинов Е2 при лечении даже низкими дозами ацетилсалициловой кислоты [9].
Наиболее высок риск осложнений в начале антитромбоцитарной терапии. В исследовании на 991 больном с ишемической болезнью сердца (ИБС) оценили риск язвенных кровотечений на фоне терапии низкими дозами АСК. Оказалось, что 45% осложнений приходятся на первый месяц терапии АСК, общая частота осложнений составила 1,5% в год [10].
Показано, что замена АСК на клопидогрель или другие антитромбоцитарные препараты не снижает риска больших кровотечений [11]. По данным некоторых исследований с проведением эндоскопического контроля среди больных, имеющих симптомы диспепсии, на фоне применения клопидогреля тяжесть поражений ЖКТ и выраженность геморрагических проявлений выше, чем у больных, принимающих АСК [12].
Сочетанное применения АСК и НПВС существенно увеличивает риск кровотечений из ЖКТ и язвенных осложнений. Так, показано, что частота госпитализаций увеличивается с 0,6% в год при лечении низкими дозами, а до 1,5 в год при терапии и АСК и другими НПВС. Соответственно возрастает и потребность в применении профилактической терапии. Комбинация низких доз АСК с антикоагулянтами также приводит к 2-кратному увеличению риска осложнений.
Инфекция Helicobacter pylori (Hp) также является наиболее значимым фактором, ассоциированным с развитием осложненных и неосложненных язвенных поражений как желудка, так и двенадцатиперстной кишки. При наличии Нр-инфекции риск кровотечений из верхних отделов ЖКТ возрастает в 4,9 раза и на фоне низких доз АСК и на фоне НПВС [13].
С практической точки зрения выделяют группы с низким, умеренным и высоким риском желудочно-кишечных кровотечений. Больные в возрасте моложе 65 лет и не имеющие дополнительных факторов риска имеют низкую вероятность развития кровотечений. Риск считается умеренным у больных старше 65 лет, при использовании НПВС, антиагрегатнов, бифосфонатов, блокаторов обратного захвата серотонина или кортикостероидов. Высокий риск кровотечений у больных, уже переносивших ЖКК или имеющих пептическую язву в анамнезе, а также у больных, получающих антикоагулянты. У больных с низким риском кровотечений специальной профилактики при использовании низких доз АСК не требуется. Больные умеренного или высокого риска кровотечений требуют дополнительных профилактических мероприятий.
Возможные подходы к профилактике поражений ЖКТ
К мерам профилактики желудочно-кишечных кровотечений и поражений ЖКТ при использовании АСК относится использование рациональных и обоснованных доз антитромбоцитарных препаратов, использование «защищенных» форм АСК, применение антацидов, блокаторов секреции и эрадикационная терапия.
Прием любых дозировок АСК сопровождается увеличением риска поражений ЖКТ, однако повышение риска коррелирует с принимаемой дозой АСК. В одном из исследований проанализировали риск кровотечений у больных, получавших 75 мг, 150 мг и 300 мг АСК. Риск осложнений возрастал в 2,3, 3,3 и 3,9 раза соответственно. Риск кровотечений был максимальным в начале приема АСК. Существенное увеличение риска отмечалось при комбинировании АСК с другими НПВС [14].
В другом исследовании при анализе группы 12 562 больных при проведении анализа безопасности приема разных доз АСК было показано, что только применение дозировок 75–81 мг/сут является более безопасным, чем применение более высоких доз препарата. При этом основной антиагрегантный эффект мало зависит от применяемой дозы АСК [15].
Таким образом, предпочтительным является использование низких доз АСК. При этом доза АСК в 75 мг/сут обладает доказанной эффективностью в предотвращении риска неблагопритяных исходов.
«Защищенные» формы АСК
Другим подходом к профилактике поражений ЖКТ при лечении АСК является использование «защищенных» лекарственных форм АСК. К таким формам относят кишечно-растворимые и буферные, в которых АСК сочетается с невсасывающимися антацидами. Данные об эффективности и безопасности этих форм противоречивы.
АСК адсорбируется из желудка путем пассивной диффузии в негидролизованном виде. Условием этого является сохраненная кислая среда желудка, обеспечивающая низкую скорость гидролиза ацетилсалициловой кислоты. Это обеспечивает биодоступность АСК около 50%. При использовании кишечно-растворимых форм АСК, из которых ацетилсалициловая кислота высвобождается в тонком кишечнике, биодоступность может снижаться за счет гидролиза АСК с участием кишечных гидролаз и щелочной среды кишечника. Следствием этого является сниженная блокада образования тромбоксана А2 при использовании кишечно-растворимых форм по сравнению с обычными [16].
Показано, что применение кишечно-растворимых форм АСК не снижает существенно риск эрозивно-язвенных поражений ЖКТ, а растворимые шипучие формы АСК могут этот риск даже повышать. При эндоскопической оценке воздействия разных форм АСК (АСК с кишечно-растворимой оболочкой или буферных форм АСК) оказалось, что при использовании кишечно-растворимых форм существенно увеличивается частота развития эрозивных и язвенных поражения тонкого кишечника [17].
В исследовании на 1402 больных, получающих низкие дозы АСК, оказалось, что частота кровотечений одинакова, а риск развития анемии несколько выше при использовании кишечно-растворимых форм (2% и 0,3%) [18].
Использование буферных форм, содержащих невсасывающиеся антациды, существенно снижает повреждающий потенциал в отношении слизистой желудка, связанный с приемом препарата [19].
При сравнении влияния буферной и обычной формы АСК на слизистую оболочку желудка на группе из 24 здоровых волонтеров оказалось, что гиперемия и эрозирование слизистой чаще отмечались при использовании небуферной формы. Клиническая симптоматика, связанная с гастропатией, появлялась только в группе с небуферной формой АСК. Интересно, что в исследовании использовались очень высокие дозы АСК (800 мг для буферной формы, 500 мг для обычной) [20]. При сравнении параметров фармакокинентики буферной и простой формы АСК у здоровых добровольцев было показано, что биодоступность АСК существенно не отличается, площадь под кривой концентрации препаратов также оказалась идентичной. Применение буферных форм АСК позволяло быстрее достичь максимальной концентрации препарата в крови [21].
Нужно отметить, что есть и данные об увеличении частоты осложнений со стороны ЖКТ при использовании буферных форм АСК. Так, метаанализ разных форм АСК показал, что относительный риск развития осложнений со стороны ЖКТ при применении обычных, кишечно-растворимых и буферных форм АСК составляет 2,6, 2,4 и 5,3 [22]. Однако следует учесть, что большинство буферных форм содержит высокие дозы АКС.
Особенный интерес представляет собой фармакологическая форма, сочетающая малую дозу АСК (75 мг) и невсасывающийся антацид — гидроокись магния, — Кардиомагнил. Показано, что такая форма АСК не уступает по влиянию на агрегацию тромбоцитов АСК в незащищенных или кишечно-растворимых формах [23]. Частота геморрагических и язвенных поражений верхних отделов ЖКТ при этом на фоне использования Кардиомагнила меньше, чем при использовании кишечно-растворимой формы АСК [24].
Медикаментозная профилактика поражений ЖКТ при терапии АСК
Чаще всего для профилактики медикаментозно обусловленных поражений ЖКТ используются различные блокаторы желудочной секреции, антациды, синтетические аналоги простагландинов.
Наиболее эффективны и широко используются, особенно у больных с высоким риском кровотечений, препараты из группы ингибиторов протонной помпы (ИПП), применение которых эффективно снижает риск кровотечений. В большом когортном исследовании, проведенном в Японии, было показано, что увеличение частоты использования ИПП у больных, получающих НПВС и низкие дозы АСК, приводит к снижению частоты кровотечений из ЖКТ со 160 до 23,2/100 000 населения в год [25].
При проведении фармакоэкономического анализа было показано, что использование АСК в комбинации с ИПП практически в 2 раза уменьшает риск осложнений, связанных с кровотечениями из ЖКТ. Увеличивается продолжительность жизни при этих осложнениях (на 38 дней к году наблюдения, или на 61%). При этом увеличивается приверженность больных к терапии АСК (с 71% до 74%). Все это ведет к уменьшению риска повторных коронарных событий (на 26 в год на 10 000 больных) [26].
Еще один подход к профилактике желудочно-кишечных кровотечений связан с проведением эрадикации Hp-инфекции. Успешная эрадикация снижает риск кровотечений на фоне приема АСК в 5,5 раз [27]. Таким образом, больным с желудочно-кишечным кровотечением в анамнезе, при необходимости проведения антиагрегантной терапии, рекомендуется обследование для выявления Hp-инфекции и проведения эрадикационной терапии.
Таким образом, в настоящее время достаточно хорошо разработаны подходы к профилактике поражений ЖКТ при лечении АСК. Этот антитромбоцитарный препарат является одним из наиболее часто используемых в современной кардиологической и терапевтической практике. При этом особенно важно четко следовать показаниям к назначению АСК, применяя только в тех ситуациях, когда польза от назначения препарата превышает риск связанных с ним осложнений. Наиболее значимым для безопасного использования АСК является использование минимально эффективных доз препарата. Сочетание АСК с небольшими дозами антацидов может сделать применение АСК более безопасным, не влияя существенно на эффективность лекарства. Для больных с высоким риском кровотечений возможно также профилактическое использование блокаторов желудочной секреции, а при наличии показаний — проведение эрадикации Hp-инфекции.
Литература
Л. О. Минушкина, доктор медицинских наук, профессор
ФГБУ УНМЦ УД Президента РФ, Москва
Ацетилсалициловая кислота как антитромбоцитарное средство: какие лекарственные формы препарата предпочтительны с позиций доказательной медицины?
Опубликовано в журнале:
«Кардиоваскулярная терапия и профилактика», 2010; 9(2) с. 61-68
О.В. Аверков
Российский университет дружбы народов. Москва, Россия.
В аналитической статье приведены рассуждения о доказательствах эффективности, плюсах и минусах одного из наиболее изученных антитромбоцитарных средств – ацетилсалициловой кислоты (АСК). Убедительные положительные результаты клинических испытаний и, так называемая, “желудочная токсичность” АСК – Аспирина, вместе с необходимостью длительного применения препарата в качестве антиагреганта, стали основанием появления различных лекарственных форм Аспирина: растворимых, с контролируемым высвобождением, покрытых кишечных, локальных (накожных), буферных, а также комбинированных средств, сочетающих в себе АСК и вещества с антацидным эффектом. К настоящему времени наиболее убедительные доказательства щадящего действия на слизистую желудка получены для покрытых кишечных форм Аспирина. Особенности биодоступности, различия в лабораторных эффектах, желудочно-кишечной переносимости и безопасности различных форм Аспирина не могут быть окончательной мерой при выборе препарата. Финальным критерием целесообразности применения какой-либо из многочисленных форм АСК могут быть, прежде всего, данные о способности снижать риск событий, предотвращению которых должно способствовать назначение препарата. В многочисленной доказательной базе Аспирина, как антитромбоцитарного средства, большая часть информации пришла из результатов исследований, выполненных с обычной АСК. Убедительные аргументы в пользу применения, в т.ч. данные о снижении смертности, есть у покрытых кишечных форм этого препарата. У других “улучшенных” форм Аспирина, включая буферные, растворимые и комбинированные с антацидом, доказательства эффективности подобного уровня отсутствуют и их предлагают использовать лишь на основании схожести лабораторных эффектов и ожидаемой меньшей “желудочной токсичности”.
Ключевые слова: ацетилсалициловая кислота, антиагреганты, вторичная и первичная профилактика.
Acetylsalicylic acid as an anti-platelet agent: what forms should be used, according to evidence-based medicine?
O.V. Averkov
Russian Peoples` Friendship University. Moscow, Russia.
This analytic paper reviews the evidence on effectiveness, benefits and limitations of one of the best-studied anti-platelet agents – acetylsalicylic acid (ASA). The results of clinical trials, together with so called “gastro-toxicity” of ASA, or Aspirin, and a need for long-term anti-platelet therapy, were the basis for development of various Aspirin forms – soluble, with controlled release, enteric-coated, local (cutaneous), buffer, and combined (Aspirin plus antacids). Currently, the minimal gastro-toxicity has been demonstrated for enteric-coated forms. Specifics of bio-availability, laboratory effects, gastro-intestinal tolerability, and safety could not be the main criteria for choosing a medication form. The choice of an ASA form is defined by the evidence on risk reduction by this form. The extensive evidence on Aspirin as an anti-platelet agent has been obtained in clinical trials using standard ASA. For enteric-coated ASA forms, the evidence on end-point reduction, including mortality reduction, is also available. For other “improved” Aspirin forms, such as buffer, soluble and combined, this evidence is lacking; therefore, their choice could be based only on similarity of laboratory effects and expected lower gastro-toxicity.
Key words: Acetylsalicylic acid, anti-aggregants, secondary and primary prevention.
Атеротромбоз по праву считают морфологической основой инфарктов миокарда (ИМ) и мозга, других ишемических и некротических осложнений атеросклероза. Многие из этих событий несут в себе прямую или отсроченную угрозу для жизни больных атеросклерозом. Именно поэтому эффективные антитромботические вмешательства являются обязательным элементом лечения больных с острыми и хроническими проявлениями атеросклероза. Основу подобного лечения составляют антитромбоцитарные препараты, представленные в абсолютном большинстве показаний ацетилсалициловой кислотой (АСК) или комбинацией АСК с другими дезагрегантами.
Требования к эффективному медикаментозному вмешательству в современной доказательной медицине достаточно просты. Предлагаемое средство должно предотвращать события, угрожающие жизни, а его побочные действия, в свою очередь, не должны угрожать жизни и ограничивать переносимость препарата. Окончательной мерой эффективности и безопасности является влияние любого вмешательства на смертность.
В современной медицине объективные доказательства эффективности и безопасности лекарства получают в специально организованных, рандомизированных, плацебо-контролируемых, сравнительных исследованиях. В основе статистического подтверждения “неслучайности” полученных доказательств лежит участие в подобных исследованиях тысяч, а иногда и десятков тысяч больных.
Сам факт существования такого термина как “эра аспирина” указывает на значимое место этого препарата в предотвращении осложнений атеросклероза. Многократно доказанная эффективность АСК привела к тому, что любое средство, предлагаемое в качестве антитромбоцитарных препаратов, в исследованиях по выяснению целесообразности его применения сравнивается не с “контролем”, а с АСК. В последние годы замысел исследований по оценке антитромбоцитарных препаратов все чаще предусматривает сравнение двух групп больных: получающих АСК и получающих АСК в сочетании с новым дезагрегантом. Другими словами, лечение АСК признано бесспорным эталоном в предотвращении осложнений атеросклероза с помощью средств, влияющих на тромбоцитарное звено гемостаза.
200 исследований, включавших > 140 тыс. разных больных высокого риска, добавил к имевшимся ранее показаниям для АТТ острый ИИ, периферический атеросклероз и стабильную стенокардию. При этом АСК так и осталась основным препаратом для большинства клинических состояний, требующих применения антитромбоцитарных препаратов [2]. Главным достоинством АСК оказалась его универсальность. В исследованиях получены основания для ее использования при острых состояниях, вызванных атеротромбозом: ИМ, нестабильной стенокардии (НС), ишемическом инсульте, и для длительного применения в качестве средства вторичной профилактики: после перенесенного ИМ, ишемического инсульта или преходящего нарушения мозгового кровообращения (НМК).
Конец ХХ века и начало XXI прошли под знаком создания многочисленных рекомендательных документов, разработанных группами экспертов и призванных облегчить деятельность практических врачей. Не избежало подобной участи и АТТ, отношение к различным элементам которого сформулировано группой экспертов Европейского Кардиологического общества в 2004г [3]. Подобного рода документы создаются на основании результатов крупных исследований, мета-анализов, объединяющих данные нескольких исследований, а иногда и менее надежных источников. Представленные итоговые таблицы вышеупомянутого документа, показывают, что основу АТТ при всех известных показаниях к подобному лечению по прежнему составляет АСК (таблицы 1 и 2), а изменения, добавленные в таблицы автором статьи, на основании результатов исследований, опубликованных после 2004г, касаются лишь препаратов, которые следует сочетать с Аспирином.
Таблица 1. Рекомендации по использованию антитромбоцитарных средств при различных клинических проявлениях коронарной болезни сердца [3]
| Клиническое проявление | Рекомендовано | Примечания | ||
| Стабильная стенокардия | Аспирин | — | 1А | |
| клопидогрел | как альтернатива Аспирину | 1С | ||
| ОКС без подъема ST | с ЧКВ | Аспирин | — | 1А |
| А + клопидогрел | лучше чем один Аспирин | 1А | ||
| в/в бл. GP IIb/IIIa | перипроцедурное использование | 1А | ||
| ОКС без подъема ST | Без ЧКВ | Аспирин | — | 1А |
| А + клопидогрел | лучше чем один Аспирин | 1B | ||
| в/в бл. GP IIb/IIIa | тирофибан или эптифибатид | 2А | ||
| ОКС с подъемом ST | С ЧКВ | Аспирин | — | 1А |
| А + празугрел + | — | 1B | ||
| в/в бл. GP IIb/IIIa | абциксимаб | 1А | ||
| ОКС с подъемом ST | Без ЧКВ | Аспирин | — | 1А |
| А + клопидогрел | лучше чем один Аспирин | 1А | ||
| После ИМ | Аспирин | — | 1А | |
| клопидогрел | как альтернатива Аспирину | 1А | ||
| После КШ | Аспирин | |||
| Плановое ЧКВ | Аспирин | — | 1А | |
| А + клопидогрел | в случае стентирования | 1А | ||
| А + тиклопидин? | в случае стентирования | 1А | ||
| в/в бл. GP IIb/IIIa | 2 класс у стабильных больных | 2А | ||
Примечание: В правой колонке – класс (цифра) и уровень (буква) доказательств; А – аспирин, КШ – коронарное шунтирование, ЧКВ – чрескожное коронарное вмешательство, бл.GPIIb/IIIa – блокаторы гликопротеиновых IIb/IIIa рецепторов тромбоцитов.
Таблица 2. Рекомендации по использованию антитромбоцитарных средств при различных состояниях, отличных от коронарной болезни сердца [3]
| Клиническое проявление | Рекомендовано | Примечания | |
| Острые НМК или ПНМК | Аспирин | 1А | |
| НМК или ПНМК в прошлом | Аспирин | 1А | |
| клопидогрел | как альтернатива Аспирину | 1А | |
| Периферический атеросклероз | Аспирин | 1С | |
| клопидогрел | как альтернатива Аспирину | 1А | |
| Первичная профилактика: | |||
| Сахарный диабет | Аспирин | 2В | |
| Артериальная гипертония | Аспирин | 2А | |
| Мерцательная аритмия | Аспирин | При промежуточном риске, а при высоком риск только у тех, кто не подходит для лечения варфарином | 1А |
| Болезни клапанов | Аспирин | При ревматическом поражении клапанов у тех, кто не подходит для варфарина | 1В |
| Оперированные клапаны | Аспирин | В сочетании с варфарином при механических клапанах | 2В |
Примечание: В правой колонке – класс (цифра) и уровень (буква) доказательств.
Плюсы и минусы Аспирина
По своим основным характеристикам Аспирин соответствует основным требованиям, предъявляемым к антитромбоцитарному препарату, используемому для предотвращения осложнений атеросклероза. Он прост в применении, в т.ч. длительном, доступен по цене, имеет доказательства бесспорного преобладания ожидаемой пользы над возможным риском и требует минимального, в т.ч. лабораторного, контроля, однако, как и любой эффективный препарат, Аспирин не лишен недостатков. Принято считать, что Аспирин угнетает лишь один из множества (> 90) механизмов активации тромбоцита, а именно тромбоксан-зависимый. Наличие других “свободных” путей активации, по мнению сторонников “усиления” действия Аспирина или его замены на другие антитромбоцитарные препараты, служит одним из объяснений развития ишемических событий на фоне использования Аспирина.
Другим “слабым” местом Аспирина считают так называемую “резистентность” к Аспирину у 15-30% пациентов. Долгое время поводом для дискуссий были косвенные указания на способность Аспирина ослаблять положительное влияние на течение сердечной недостаточности ингибиторов ангиотензин-превращающего фермента (ингибиторов АПФ). Среди других, важных с практической точки зрения, контраргументов Аспирина – свойственные ему желудочно-кишечные побочные действия, прежде всего – увеличение риска кровотечений.
Насколько серьезны “недостатки” Аспирина?
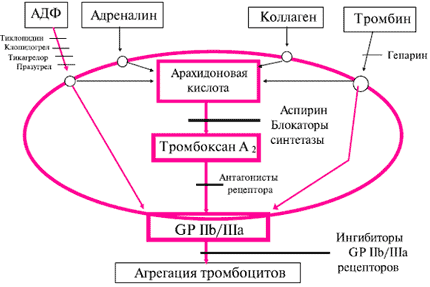
С позиций врача, применяющего Аспирин на практике, принципиально важно следующее. Даже если считать, что Аспирин угнетает всего один путь активации тромбоцита, и это угнетение – единственный механизм действия при атеросклерозе и его осложнениях, существуют доказанные клинические последствия этого угнетения в виде снижения риска смерти, ИМ и ишемического инсульта. Все это заставляет считать циклооксигеназный путь активации тромбоцита одним из важнейших, и подавлять его наиболее изученным средством – Аспирином. Тем не менее, лабораторные эффекты Аспирина, в основном его влияние на агрегацию тромбоцитов (АТр), включают снижение не только АТр, вызванной арахидоновой кислотой, но и уменьшение степени АТр при использовании таких индукторов как коллаген, аденозиндифосфат, малые концентрации тромбина и адреналин. Наиболее простым объяснением участия Аспирина в подавлении АТр, вызванной основными индукторами, является вовлечение циклооксигеназного механизма в различные пути активации тромбоцита (рисунок 1). Не следует забывать о том, что существует достаточно фактов для того, что бы связывать положительный клинический эффект Аспирина не только с его влиянием на активацию тромбоцита, но и с его противовоспалительными свойствами, способностью уменьшать реперфузионное повреждение и влиять на показатели свертываемости крови.
Рис. 1 Механизмы активации тромбоцитов и место действия основных антитромбоцитарных средств.
Активация тромбоцита (по Peterson & Mark с изменениями)
В вышеупомянутом втором мета-анализе [2] было выполнено сравнение частоты неблагоприятных исходов (сумма смертей, ИМ и инсультов) при использовании наиболее изученных антитромбоцитарных препаратов: клопидогрела, тиклопидина, дипиридамола, трифлузала, ридогрела, индобуфена и сульфинпиразона, Аспирина. Оказалось, что единственным средством, способным хотя бы формально рассматриваться в качестве более эффективной альтернативы Аспирину с позиций доказательной медицины можно считать только клопидогрел.
Не следует забывать, что эффективное усиление АТТ (в дополнение к Аспирину) практически невозможно без увеличения риска геморрагических осложнений. В подобных попытках усилить действие Аспирина с помощью новых антитромбоцитарных препаратов основной задачей исследователей становится поиск доз и способов применения этих средств, обеспечивающих приемлемое соотношение эффективность/безопасность. В качестве примеров сравнительно удачного с этой позиции сочетания Аспирин с другим дезагрегантом можно привести использование клопидогрела при острых коронарных синдромах (ОКС) и мерцательной аритмии, парентеральное применение блокаторов тромбоцитарных гликопротеинов IIb/IIIa для профилактики осложнений внутрикоронарных вмешательств и использование высокой дозы дипиридамола в пролонгированной форме при ишемическом инсульте. В примерах с клопидогрелом и блокаторами гликопротеиновых рецепторов увеличение риска геморагических осложнений, включая серьезные кровотечения, при присоединении к Аспирину клопидогрела или БГП IIb/ IIIa было статистически значимым. Оно признано “приемлемой платой” за убедительное снижение риска ишемических осложнений.
Понятие “резистентность к Аспирину” и до настоящего времени продолжает обсуждаться. Этот термин используется для описания нескольких феноменов, среди которых неспособность Аспирина предотвращать тромботические осложнения, увеличивать время кровотечения, оказывать ощутимый эффект на лабораторные показатели функции тромбоцитов. Среди потенциальных причин резистентности к Аспирину С. Patrono предлагает (в порядке значимости): неспособность больных следовать предписанному лечению (noncompliance); конкурентное взаимодействие Аспирина с нестероидными противовоспалительными средствами; наличие внетромбоцитарных источников образования тромбоксана А2 (моноциты и макрофаги). Две из трех возможных перечисленных причин, потенциально предотвратимы. Простейшие мероприятия в виде контроля за приемом препарата и выяснения подробностей сопутствующей терапии способны существенно уменьшить частоту “резистентности к Аспирину).
Касаясь возможного взаимодействии Аспирина и ингибиторов АПФ, следует отметить, что если такое взаимодействие и существует, оно не столь значительно, что бы отказываться от использования Аспирина. С практической точки зрения важно, что влияние Аспирина на синтез простациклина в эндотелии, а, значит и на возможное опосредованное простациклином действие ингибиторов АПФ, является дозозависимым. Следовательно, в случае сочетанного назначения ингибиторов АПФ и Аспирина, последний следует использовать в минимальных эффективных дозах.
Тезис противников Аспирина о неприемлемом профиле безопасности и переносимости этого препарата также нуждается в разъяснении. Основными побочными эффектами Аспирина не без оснований считаются желудочно-кишечные кровотечения (ЖКК). Потенциально опасны желудочные и кишечные кровотечения. Наглядный подход к оценке значения ЖКК, вызванных Аспирином у больных с различным риском ишемических событий, предложен С. Patrono, известным экспертом в области антитромбоцитарных препаратов, и, прежде всего Аспирина. Во главу концепции положены сведения о том, что во взрослой популяции людей, считающихся здоровыми, возникает 1 случай ЖКК на 1 тыс. чел./год. Использование Аспирина риск этого кровотечения удваивает, причем увеличивает его в одинаковой степени у здоровых лиц и больных атеросклерозом. Дальнейшее решение о целесообразности использования Аспирина с профилактической целью определяется риском ишемических осложнений. Там, где риск этих осложнений сравнительно низок – здоровые люди с факторами риска, больные артериальной гипертонией, положительный эффект Аспирина (снижение риска ишемических событий) оказывается сопоставимым с риском кровотечения. В случае более высокого риска – стабильная и нестабильная стенокардия, перенесенный в прошлом ИМ, 1-2 новых случая кровотечения у 1 тыс. больных, принимающих Аспирин, оказываются вполне приемлемой платой за предотвращение десятков новых сосудистых событий. К настоящему времени имеется достаточно информации для сомнений в приписываемой Аспирину “желудочной токсичности”. Дело в том, что значительная часть данных о побочных действиях Аспирина накоплена в тот период, когда для предотвращения осложнений атеросклероза использовались относительно высокие дозы препарата. Собранные к началу 90-х годов прошлого века данные о распространенности его дозозависимых побочных действий, позволяют утверждать, что в случае применения относительно низких доз Аспирина ≤ 325 мг/сут., увеличение риска кровотечений и побочных действий, требующих отмены препарата, оказывается приемлемым для большинства клинических состояний. Косвенное указание на возможность снижения риска кровотечений при назначении Аспирина в рамках рекомендуемых “кардиологических” доз представлено в результатах исследования CURE (Clopidogrel in Unstable angina to prevent Recurrent Events) [4]. У больных с ОКС без подъемов сегмента ST использование Аспирина в дозе 75-100 м/сут. при сравнении с больными, принимавшими препарат в дозе 200-325 мг/сут., частота кровотечений оказалась вдвое меньшей. Эти данные, в сочетании с информацией о сходной эффективности доз Аспирина 75-150 мг/сут. и 160-325 мг/сут., полученной во втором мета-анализе АТТ, позволяют считать, что оптимальная доза Аспирина, способная обеспечить приемлемое соотношение пользы и риска, находится в пределах 75-150 мг/сут. и может считаться вполне безопасной.
Почему понадобились “улучшенные” формы Аспирина?
Так называемая “желудочная токсичность” Аспирина и необходимость длительного применения препарата в качестве антиагреганта стали основанием для фармакологических манипуляций с ним. Следствием этих манипуляций стало появление растворимых форм, форм с контролируемым высвобождением [5], покрытых кишечных (ПК), локальных (накожных) [6] и, так называемых, буферных форм. К применению с профилактической целью предложены комбинированные препараты, сочетающие в себе АСК и антациды (например, гидроокись магния). Ряд изменений (контролируемое высвобождение и накожные формы) призваны уменьшить гастротоксическое действие АСК за счет относительно избирательной блокады синтеза тромбоксана А2 тромбоцитами и минимального влияния на образование сосудистых и желудочных простаноидов. Считается, что препараты АСК, покрытые кишечно-растворимой оболочкой, могут быть менее гастротоксичны из-за ослабления прямого раздражающего действия кислоты на слизистую оболочку желудка. Сходный механизм уменьшения негативного действия Аспирина на желудочно-кишечный тракт (ЖКТ) предложен для обоснования использования комбинации препарата с гидроокисью магния.
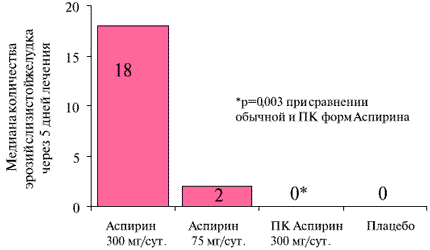
К настоящему времени наиболее убедительные доказательства более щадящего действия на слизистую желудка получены для ПК форм Аспирина. В небольшом эндоскопическом исследовании у бессимптомных больных, длительно принимавших АСК, эрозии на слизистой желудка были отмечены у 90% больных, получавших обычную АСК, и у 60%, принимавших препарат в виде ПК формы [7]. При эндоскопической оценке краткосрочных эффектов обычных и ПК форм Аспирина преимущество последней продемонстрировано в 5 исследованиях [8]. Результаты некоторых подобных исследований выглядят более чем убедительными (рисунок 2) [9].
Рис. 2. Частота эрозий на слизистой желудка при сравнении краткосрочного применения разных форм и доз Аспирина [9].
Очевидно, что подходы, предлагаемые с целью “гастропротекции”, не могут свести на нет негативное влияние Аспирина на слизистую желудка. Возможно поэтому, в большинстве исследований по сравнению ПК и обычной форм Аспирина не удалось обнаружить разницы по частоте ЖКК. Тем не менее, в исследовании, сравнивая ПК таблетки Аспирина (325 мг) с обычными (325 мг), зарегистрирована достоверно меньшая кровопотеря через ЖКТ [10]. “Гастропротективные” свойства ПК форм Аспирина способны в той или иной степени ослабить его ульцерогенное влияние. Объяснение этому в том, что при назначении каждой из этих форм, неизбежно возникает системное ингибирование циклооксигеназы и следующее за этим “ульцерогенное” изменение баланса простаноидов слизистой желудка. Возможно поэтому в большинстве исследований с наиболее изученной ПК формой Аспирина “желудочная токсичность” оказывалась хуже, чем у плацебо [9], а частота ЖКК была сопоставима с таковой при приеме обычных форм препарата [11]. Сомнения в целесообразности ПК форм Аспирина может усилить информация о худшей, чем у обычного Аспирина, биодоступности [12]. Однако это феномен если и существует, то способен повлиять лишь на время наступления эффекта от приема первой дозы препарата. Эту проблему легко решить разжевыванием ПК таблетки Аспирина или использованием для первого приема обычных форм препарата.
Принципиально важно, что даже при допущении о сопоставимой с обычным Аспирином безопасности, “улучшенные”, прежде всего ПК формы препарата, могут иметь преимущество за счет лучшей переносимости, которая в итоге, может повлиять на эффективность, приводя к меньшей частоте прекращения приема препарата. Косвенным доказательством этого предположения служат результаты крупного, проспективного, эпидемиологического исследования с участием 577 немецких врачей [13]. Особенностью исследования была регистрация не только “крупных” (кровотечения), но “малых” (изжога, составляющие синдрома диспепсии) желудочно-кишечных эффектов Аспирина (Аспирин ® Кардио, Байер Шеринг Фарма, Германия), которые определяют переносимость препарата и степень следования предписанному лечению. В исследование были включены 1156 кардиологических больных, изначально получавших ПК форму Аспирина ® Кардио и 1570 больных, у которых Аспирин в обычной форме был заменен на ПК Аспирин ® Кардио. В ходе наблюдения выявлено существенное снижение частоты симптомов диспепсии после замены обычного Аспирина на ПК форму. В начале исследования среди больных, принимавших обычный Аспирин, на изжогу жаловались 37,6% больных, а в дальнейшем, на фоне приема ПК формы Аспирина ® Кардио, число таких больных уменьшилось до 19,1% через 3 мес. и до 10,5% через 2 года лечения.
У какой из “улучшенных” форм Аспирина есть своя “доказательная база”?
Рассуждая об особенностях биодоступности, различных лабораторных (дезагрегантных) эффектах, желудочно-кишечной переносимости и даже безопасности различных форм Аспирина, следует помнить, что окончательным критерием целесообразности применения какой-либо из этих форм могут быть только данные о способности убедительно влиять на риск тех событий, предотвращению которых должно способствовать назначение препарата. Речь идет, прежде всего, о снижении риска развития ИМ и ишемического инсульта, а окончательной мерой пользы препарата, учитывающей и безопасность его применения, может служить статистически значимое снижение смертности. При использовании ПК форм были получены наиболее впечатляющие результаты за всю историю изучения профилактического действия АСК на сердечнососудистую систему.
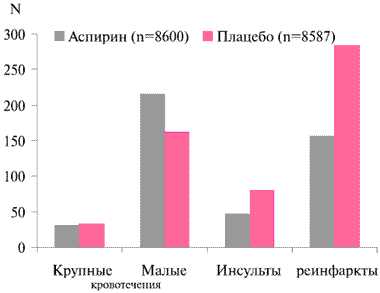
Рис. 3 Кровотечения и несмертельные ишемические события в исследовании ISIS-2. Наблюдение 5 нед. [14]
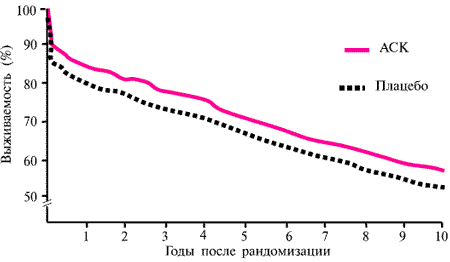
Рис. 4 Выживаемость больных при сравнении АСК и плацебо у больных ИМ в исследовании ISIS-2 (наблюдение до 10 лет, препарат применялся первые 5 нед). [15]
В достаточно многочисленных и во многом успешных попытках доказать необходимость применения Аспирина для первичной профилактики сердечно-сосудистых событий только один раз было зарегистрировано положительное влияние препарата на смертность [16]. В этом исследовании использовалась ПК форма Аспирина ® Кардио. 4495 человек с хотя бы одним из традиционных факторов риска ишемической болезни сердца – возраст > 65 лет, артериальная гипертония, гиперхолестеринемия, сахарный диабет, ожирение, преждевременное развитие ИМ у ближайших родственников, в открытую были рандомизированы к приему 100 мг Аспирина ® Кардио или в группу сравнения. За 3,5 года вмешательства среди 2226, принимавших АСК от сердечно-сосудистых причин умерли 17 человек, а среди 2269 в группе контроля от этих причин умер 31 пациент – снижение риска на 44% (p