высокорезистентный кровоток это что значит
Высокорезистентный кровоток это что значит
Кривые скоростей маточных артерий вне беременности характеризуются высокими показателями резистентности кровотока. Допплерометрические индексы (С/Д, ПИ и ИР) изменяются в зависимости от фазы менструального цикла. Отсутствие кровотока в конце диастолы и ранняя диастолическая выемка более характерны для фолликулиновой фазы.
Аналогичные данные были получены у больных, получавших лечение с помощью экстракорпорального оплодотворения (ЭКО). Те из них, кто имел высокие значения ПИ в день аспирации яйцеклеток, имели более низкую вероятность наступления беременности.
C.V. Steer et al. показали, что среднее значение ПИ больше 3,0 перед переносом эмбрионов прогнозировало 35% случаев неудач имплантации или наступления беременности. Полученные результаты позволили предположить, что допплерометрическое исследование кровотока в маточных артериях может иметь значение для оценки восприимчивости эндометрия в циклах проведения процедуры ЭКО.
Было высказано предположение, что при наличии высоких показателей сосудистого сопротивления следует проводить криоконсервацию эмбрионов до тех пор, пока не нормализуется маточный кровоток.
Маточный кровоток в первом триместре беременности
Поэтому в течение первого триместра межворсинчатого пространства достигает очень ограниченное количество материнской крови и цветовые доппле-ровские сигналы обычно не регистрируются в паренхиме плаценты.
Это было доказано клиническими наблюдениями, показавшими, что образцы ворсин хориона, полученные до 12 нед беременности, редко окрашены кровью по сравнению с образцами, полученными во втором триместре или позже. Визуализация кровотока в межворсинчатом пространстве в течение первого триместра связана с более высокой вероятностью наступления неразвивающейся беременности.
После 12 нед кровоток в паренхиме плаценты может постоянно регистрироваться с помощью ЦДК.
В отличие от цветового картирования КСК из области имплантации могут быть зарегистрированы уже в 5 нед от первого дня последней менструации и характеризуются низкими показателями резистентности кровотока. У них отмечается хорошо выраженный кровоток в фазу диастолы и средние значения ИР находятся пределах от 0,41 ±0,10 (СО) до 0,48 ± 0,08 (СО).
Величина ИР постепенно уменьшается с 6 до 12 нед. Кривые скоростей кровотока в маточных артериях в этот период характеризуются высокими значениями С/Д, низкой конечной диастолической скоростью и наличием выемки в фазу систолического замедления. Резистентность кровотока снижается, как только развитие беременности достигает второго триместра.
М. Coppens et al. выполнили продольное исследование, оценивая в динамике маточно-пла-центарный кровоток у 37 здоровых беременных на ранних сроках. Кровоток в маточных артериях характеризовался высокой систолической и низкой конечной диастолической скоростью, а также имелась выраженная ранняя диастолическая выемка, которая постоянно регистрировалась в сроки 8-14 нед беременности.
Профиль КСК аркуатных артерий также имел диастолическую выемку, но по сравнению с маточными артериями регистрировались более высокие скорости в фазу диастолы. В спиральных артериях обнаруживались наиболее низкие показатели сосудистого сопротивления с относительно высокой скоростью кровотока в диастолу и незначительно выраженной диастолической выемкой, которая исчезала приблизительно в половине случаев к 10 нед и во всех наблюдениях к 13 нед гестации. У 62% пациенток диастолическая выемка в аркуатных артериях переставала регистрироваться через неделю после исчезновения выемки в спиральных артериях.
Плацентарная недостаточность
Большинство женщин знают, что плацента связывает маму и малыша во время беременности и при помощи нее к малышу поступают питательные вещества и кислород.
Бывают ли такие ситуации, когда плацента перестает правильно и полноценно выполнять свою функцию? Можно ли как то предотвратить это?
Какую функцию выполняет плацента
Внутри ворсин течет кровь малыша, а снаружи они омываются кровью матери. Между кровотоком мамы и малыша расположен всего один слой клеток, который и играет роль барьера между организмом матери и ребенка. Благодаря этой мембране кровь матери и плода не смешивается.
Однако в последние годы стало известно, что клетки крови плода все-таки проникают через плацентарный барьер в кровоток матери и благодаря этому стало возможным проведение генетических анализов и определение хромосомных аномалий, резуса фактора и пола плода по крови беременной женщины (неинвазивный пренатальный тест).
В плаценте происходит постоянный обмен веществ между мамой и ребенком. Из материнской крови к плоду поступает кислород и питательные вещества, от плода обратно к матери углекислый газ и продукты обмена, подлежащие выведению из организма.
Важной функцией плаценты является выработка гормонов и биологически активных веществ. В первую очередь это гормоны, важные для успешного вынашивания беременности, например хорионический гонадотропин, плацентарный лактоген, эстрогены и др.
К сожалению, не всегда все складывается вполне благополучно. В силу самых различных причин на разных сроках беременности могут происходить отклонения в развитии и функционировании плаценты. Изменения эти никогда не проходят бесследно для мамы и малыша, а зачастую имеют грозные последствия.
Если плацента перестает выполнять свои функции в полной мере, развивается так называемая плацентарная недостаточность. По сути, она заключается в ухудшении кровообращения в системе мать-плацента-плод.
Виды и причины плацентарной недостаточности
Врачи различают острую и хроническую плацентарную недостаточность:
Острая плацентарная недостаточность
Это состояние, требующее экстренного вмешательства врачей. Она характеризуется стремительным ухудшением плацентарного кровотока. Острая плацентарная недостаточность возникает в основном в результате отслойки плаценты или гибели отдельных участков ткани плаценты например при образовании тромбов в сосудах. Причиной отслойки может послужить травма живота, антифосфолипидный синдром.
Фосфолипиды – это сложные жиры, которые входят в состав оболочек всех клеток организма. В ряде случаев иммунная система организма вырабатывает большое количество антител к некоторым собственным фосфолипидам и белкам, связывающим эти липиды. Они называются антифосфолипидные антитела и при взаимодействии с клетками организма вызывают повреждение клеток и активацию свертывающей системы крови, что приводит к тромбообразованию.
Антифосфолипидный синдром является самой частой причиной тромботических осложнений при беременности, в том числе причиной отслойки плаценты и острой плацентаной недостаточности.
Вызвать отслойку плаценты может также тяжелое течение гестоза – грозного осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Острая плацентарная недостаточность развивается при отслойке более 2/3 поверхности плаценты.
В случае развития острой плацентарной недостаточности необходимо максимально быстро провести операцию кесарева сечения для сохранения жизни малыша и мамы.
Хроническая плацентарная недостаточность
Значительно чаще у беременных женщин встречается хроническая плацентарная недостаточность. В этом случае происходит нарушение формирования и созревания плаценты, уменьшается маточно-плацентарный и плодово-плацентарный кровотоки, ограничивается газообмен и обмен веществ в плаценте, снижается синтез плацентарных гормонов. Все эти изменения определяют недостаточное поступление кислорода и питательных веществ малышу, вызывают задержку роста и развития плода.
Причинами плацентарной недостаточности чаще всего являются перенесенные аборты, особенно хирургический аборт при первой беременности, курение, при этом количество и крепость выкуриваемых сигарет значения не имеют, поскольку на формировании неполноценных сосудов плаценты негативное действие оказывает табачный дым, а не никотин.
В группу риска по развитию плацентарной недостаточности входят также женщины с хроническими заболеваниями, такими как артериальная гипертензия, железодефицитная анемия, пиелонефрит, сахарный диабет, заболевания щитовидной железы.
В последние годы наблюдается значительный рост плацентарной недостаточности, вызванной бактериями, вирусами, грибами. Причиной этого может быть как острая инфекция, перенесенная будущей мамой во время беременности, так и активация хронического инфекционного процесса в организме беременной женщины.
Немаловажное значение в формировании хронической плацентарной недостаточности играет патология матки: эндометриоз, пороки развития матки (седловидная, двурогая). Фактором риска врачи считают также миому матки. Безусловно, целый ряд лекарственных средств оказывает неблагоприятное влияние на формирование плаценты и развитие плода. В настоящее время определен список препаратов, не разрешенных к применению во время беременности.
В некоторых случаях плацентарная недостаточность может быть обусловлена наличием хромосомных нарушений у плода, в частности при синдромах Дауна (наличие дополнительной 21 хромосомы у плода) или синдроме Эдвардса (дополнительная 18 хромосома у плода) уже в ранние сроки беременности диагностируется нарушение функции плаценты.
Следует отметить, что среди осложнений беременности, наиболее часто приводящих к развитию хронической плацентарной недостаточности, существенным фактором является преэклампсия (или поздний гестоз) – это осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Независимо от факторов, способствующих развитию плацентарной недостаточности, в основе ее лежат нарушения кровообращения в маточно-плацентарном комплексе, приводящие к нарушению всех функций плаценты. Следовательно, симптомы хронической плацентарной недостаточности будут обусловлены недостатком поступления кислорода и питательных веществ к плоду.
Это прежде всего, задержка внутриутробного развития плода – отставание размеров плода и замедление темпов его роста. Часто имеют место изменение двигательной активности плода. Сначала может быть некоторое усиление движений, а затем уменьшение. Нарушение защитной функции плаценты приводит к внутриутробному инфицированию плода под действием проникающих через плаценту патогенных (болезнетворных) микроорганизмов. Плод, развитие которого происходит в условиях плацентарной недостаточности, в значительно большей степени подвержен риску травматизации в родах, у них отмечается нарушение адаптации к внеутробной жизни, повышенная заболеваемость в первый год жизни.
По времени возникновения врачи разделяют плацентарную недостаточность на раннюю и позднюю.
Ранняя (или первичная) плацентарная недостаточность
Развивается до 16 недель беременности. Она возникает уже на этапе формирования плаценты и связана с заболеваниями беременной женщины, имеющимися до беременности, к примеру с патологией матки, хронической артериальной гипертензией, эндокринологическими заболеваниями. При этом происходит формированием неполноценных сосудов в плаценте.
Поздняя (или вторичная) плацентарная недостаточность
Возникает после 16 недель беременности и чаще всего связана с заболеваниями, возникшими уже во время беременности. Чаще всего это железодефицитная анемия (то есть снижение концентрации гемоглобина и железа в крови), гестационный сахарный диабет (то есть нарушение усвоения организмом глюкозы, возникшее на фоне беременности), перенесенные вирусные и бактериальные инфекции.
Важным является подразделение плацентарной недостаточности на компенсированную и декомпенсированные формы.
Компенсированная плацентарная недостаточность
Развивается, к примеру, при угрозе прерывания беременности и нетяжелых формах позднего гестоза, в случае, если эти осложнения успешно поддаются медикаментозной коррекции.
Декомпенсированная плацентарная недостаточность
Вызывает развитие задержки развития плода, хронической внутриутробной гипоксии, вплоть до гибели плода.
Диагностика плацентарной недостаточности
Лечить уже развившуюся плацентарную недостаточность практически невозможно, поэтому врачи активно стремятся выявлять беременных женщин, угрожаемых в отношении формирования нарушений функции плаценты. Если плацентарная недостаточность выявляется в 3 триместре беременности, эффективного лечения, к сожалению, не существует. Поэтому очень активно в настоящее время применяются все способы выявления в ранние сроки беременности тех женщин, в формировании плаценты которых произошли нарушения.
В первую очередь, при постановке на учет по беременности выявляют максимально значимые факторы риска – курение, перенесенные аборты, отягощенную наследственность (низкий вес при рождении, склонность к тромбозам), наличие хронических заболеваний сердца, сосудов, сахарного диабета.
Профилактические мероприятия против развития плацентарной недостаточности особенно актуальны и необходимы до 16-17 недель беременности, когда происходит формирование структур плаценты.
Значимую помощь в оценке риска развития плацентарной недостаточности оказывает пренатальный скрининг, который проводится в 11-14 недель беременности. Он проводится для выявления синдромов Дауна, Эдвардса и др. хромосомных болезней у плода. В настоящее время самым актуальным является проведение комплексного ранний скрининг беременной на прогнозирование риска развития плацентарной недостаточности, преэклампсии и внутриутробной задержки развития плода. Поскольку данный вид диагностики относится к самым современным и передовым, к сожалению, он пока не включен в перечень услуг, предоставляемых в женской консультации в рамках ОМС, но доступен всем желающим в центрах пренатальной диагностики.
Определение белков, вырабатываемых плацентой
В первую очередь проводят определение белка РАРР-А, он является также маркером хромосомных аномалий плода. Снижение концентрации РАРР-А в крови в 11-14 недель беременности встречается у беременных женщин, имеющих высокий риск плацентарной недостаточности и задержки развития плода.
Второй гормон плаценты, который помогает в оценке рисков плацентарной недостаточности – PIGF (плацентарный фактор роста). Его концентрация в крови снижается задолго до первых проявлений плацентарной недостаточности. Его определение применяют не настолько широко, как PAPP-A, но тем не менее многие лаборатории уже включили данный белок в пренатальный скрининг 1 триместра. Крайне важное значение при проведении скрининга 1 триместра имеет измерение кровотоков в сосудах матки. Однозначно доказано, что сужение сосудов матки, определяемое при исследовании, свидетельствует о неполноценности формирования плаценты, которое будет ухудшаться с увеличением срока беременности и приведет к снижению питания малыша и снабжения его кислородов, то есть к развитию плацентарной недостаточности и задержки развития плода. При нормальных размерах маточных сосудов в 11-14 недель беременности риск тяжелой плацентарной недостаточности ничтожно мал.
Следующее обязательное скрининговое ультразвуковое исследование проводится в 20-21 неделю беременности. При этом обязательно проводят измерения плода, чтобы оценить, нет ли отставания в росте. Ведь при кислородном голодании замедляются темпы роста плода и размеры его начинают отставать от нормы для каждого срока беременности. Кроме того врач обязательно оценивает состояние и зрелость плаценты. Во время УЗИ проводится также допплерометрия сосудов матки для выявления ранних изменений, предшествующих клиническим проявлениям плацентарной недостаточности.
У пациенток, относящихся к группе высокого риска кроме УЗИ и допплерометрии проводят также суточное мониторирование колебаний артериального давления, определение количества белка в анализе мочи, собранном за сутки, оценивают показатели системы свертывания крови.
Третье УЗИ проводится всем будущим мамам в 30–34 недели беременности. Врач измеряет окружность головы и живота крохи, длину костей его ручек и ножек, и вычисляет предполагаемый вес плода. Эти измерения позволяют доктору убедиться в том, что малыш развивается нормально. Также имеет значение строение плаценты, наличие в ней признаков старения, вследствие чего она обычно перестает полноценно снабжать малыша кровью, а, значит, ему перестает хватать кислорода и питательных веществ и развитие ребенка нарушается. Во время УЗИ оценивается количество и вид околоплодных вод, которые также могут изменяться при внутриутробном страдании плода.
Допплерометрия
Допплерометрия сосудов плаценты и пуповины (метод исследования скоростей кровотоков в этих сосудах) так же позволяет оценить самочувствие малыша. Доктор исследует кровоток в артериях матки, пуповины, сердца и мозга ребенка. Это исследование позволяет определить, хорошо ли работает плацента, нет ли признаков нехватки кислорода у малыша, или развития гестоза у мамы. При снижении скорости кровотока в каком-либо сосуде можно говорить о нарушениях питания плода различной степени тяжести.
Вовремя проведенное обследование позволяет выявить начальные стадии дефицита кровоснабжения. В таких случаях лечение сможет предотвратить грозные осложнения, такие как гипоксия и внутриутробная задержка развития малыша. Допперометрию проводят в 20–21 неделю и в 30-32 недели беременности, при наличии изменений, контроль осуществляют минимум каждые две недели.
Кардиотокография
Это важный метод оценки состояния плода. Проводится КТГ при сроке беременности 33 недели и более, поскольку только на этом этапе внутриутробного развития малыша устанавливается полноценная регуляция деятельности сердечно-сосудистой системы плода центрами спинного и головного мозга. Запись сердцебиений плода проводят в течение 20–40 минут, а при необходимости исследование может быть продлено до 1,5 часов.
Аппарат регистрирует и записывает частоту сердцебиений малыша. Врач акушер-гинеколог оценивает кривую записи сердцебиений, эпизоды урежения и резкого учащения частоты сердечных сокращений плода и на основании этих данных делает заключение о том, насколько комфортно малыш чувствует себя в животе у мамы. К примеру, при снижении концентрации кислорода в крови плода, уменьшается и его поступление к клеткам нервной системы, что в свою очередь отражается на частоте сердечных сокращений. При нормальном течении беременности КТГ проводят после 33 недели 1 раз в 10–14 дней, иногда чаще. В некоторых клиниках в настоящее время предлагается услуга постоянного КТГ-мониторирования, что приобретает актуальность при наличии признаков плацентарной недостаточности. Беременной женщине выдается мониторчик, который регистрирует изменения сердечной деятельности малыша и эти данные по интернету передаются лечащему врачу.
Лечение плацентарной недостаточности
Специфических способов лечения плацентарной недостаточности в настоящее время не существует, поскольку нет лекарственных препаратов, которые избирательно улучшают маточно-плацентарный кровоток. Именно поэтому все меры борьбы с плацентарной недостаточностью направлены на профилактику. Если пациентка относится к группе высокого риска по развитию плацентарной недостаточности, с раннего срока беременности ей назначают лекарственные препараты, эффективность которых хорошо доказана и которые предупреждают раннее развитие выраженных нарушений функции плаценты.
Если во время проведения дополнительных методов оценки состояния плода выявляются начальные нарушения поступления кислорода к малышу, проводится медикаментозное лечение, направленное на увеличение притока крови и кислорода через плаценту и обязательные контрольные обследования на фоне проводимой терапии. Если изменения серьезные и малыш испытывает выраженный дефицит кислорода и питательных веществ, состояние его страдает, то в таких случаях проводится экстренное родоразрешение.
УЗИ сосудов шеи и головы
Дуплексное ангиосканирование магистральных артерий головы
Стоимость дуплексного сканирования магистральных сосудов шеи составляет 400 гривен. В стоимость входит исследование сосудов бассейна сонных и позвоночных артерий, путей венозного оттока и проведение функциональных проб. Подробный отчет об исследовании, печать снимков и запись на электронный носитель.
Цели проведения узи сосудов шеи
Такое исследование сосудов шеи называют дуплексным ангиосканированием, так как применяется одновременно исследование в двумерном режиме и в режиме допплера (цветного и/или спектрального).
Оценка сужения артерий при узи сосудов шеи
Для оценки степени стеноза сонных артерий Американское общество радиологов в 2003 году рекомендовало использовать следующие критерии
Прогностические критерии при узи сосудов шеи
На современных аппаратах с высоким разрешением при узи сосудов шеи оценивают состояние комплекса интима-медиа. Это самый внутренний слой артериальных сосудов, который первым начинает изменяться при атеросклерозе. Изменение толщины и структуры комплекса интима-медиа является очень важным прогностическим признаком при узи сосудов шеи. Считается, что превышение толщины комплекса интима-медиа в общей сонной артерии свыше 0,87 мм, а во внутренней сонной артерии больше,чем 0,9 мм является фактором, который ассоциирован с высоким риском кардиоваскулярных заболеваний (инфаркта миокарда и инсульта). Образно говоря оценка толщины комлекса интим-медиа в сонных артериях является окном, в которое можно заглянуть для диагностики атеросклеротического поражения всех сосудов. Значение предельной толщины этого комплекся колеблется в зависимости от пола, возраста и расы.
Что можно выявить при узи сосудов шеи
Самая частая патология, выявляемая при узи сосудов шеи – наличие атеросклеротических бляшек в просвете сосудов. Так как симптомы нарушения кровообращения, заметные для пациента, развиваются только после перекрытия просвета сосуда более, чем на 60%, процесс образования бляшек и тромбов может протекать длительное время бессимптомно. Бляшки при узи сосудов шеи могут быть различной формы и состава. Задача исследователя – по возможности подробно описать состав бляшки и ее локализацию.
Часто атеросклеротические бляшки распадаются, на них образуются тромбы, которые могут перекрывать полностью просвет артерии или отрываться, вызывая закупорку других, более мелких сосудов. Эти состояния часто заканчиваются развитием инсульта (отмирание участка ткани мозга) вследствие острого нарушения мозгового кровообращения. Инсульт – заболевание сопровождающееся высокой летальностью (около 40%), а более половины людей, перенесших инсульт становятся инвалидами. В последнее время инсульты развиваются у людей во все более молодом возрасте (до 60 лет).
Факторы способствующие развитию мозгового инсульта: курение, сахарный диабет, повышенное артериальное давление, избыточная масса тела, женский пол, наличие подобного заболевания у кровных родственников.
Если такие факторы присутствуют у человека, ему необходимо пройти исследование сосудов шеи как можно раньше. Также исследование сосудов шеи необходимо пройти, если беспокоит головокружение,хронические головные боли, нарушения координации, памяти и речи.
К редким случаям, которые диагностируются при узи сосудов шеи, является диссекция стенки сонной артерии- отслоение ее участка с последующим тромбозом.
Обязательной информацией, получаемой при узи сосудов шеи, является исследование объема крови, который поступает по всем сосуда шеи в головной мозг в единицу времени. Адекватное поступление крови к головному мозгу – главный фактор, который принимается во внимание при оценке патологии мозгового кровообращения. В норме у здорового человека около 15% крови, которое сердце перекачивает за минуту, попадает в сосуды головного мозга. При помощи узи сосудов шеи можно очень точно вычислить сколько именно крови попадает в головной мозг. Для этого складывают объемную скорость кровотока во всех четырех сосудах, питающих головной мозг, а именно во внутренних сонных артериях и в позвоночных артериях с обеих сторон. Корректно проведенное исследование приближается по точности к результатам, полученным при проведении позитронно-эмиссионной томографии.
Подготовка и проведение исследования
Подготовки при проведении узи сосудов шеи не требуется. Нужно только по возможности отказаться от приема лекарств, влияющих на артериальное давление.
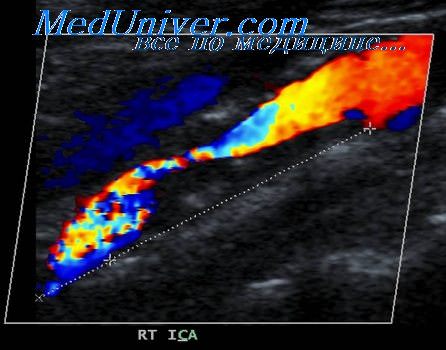
При исследовании пациент не испытывает каких-либо неудобств или болевых ощущений. Исследование сосудов шеи осуществляют в нескольких плоскостях сначала в черно-белом режиме, затем переходят к дуплексному сканированию и к импульсной допплерометрии. При этом оценивают вначале форму сосуда и его геометрию, измеряют линейные размеры и площади при наличии стенозов. Цветовой допплер исползуют прежде всего для диагностики невидимых в черно-белом режиме бляшек. При низких скоростях кровотока, например при почти полной окклюзии сосуда используют энергетический допплер. При помощи импульсного допплера проводят измерения линейной и объемной скорости кровотка.
Очень часто узи сосудов шеи проводят как исследование, предшествующее узи сосудов головного мозга. Связано это с тем, что при поиске причин нарушения мозгового кровообращения вначале логичнее убедиться в том, что по магистральным сосудам поступает достаточное количество крови.
для исследования сосудов шеи
Согласно руководству The American Institute of Ultrasound in Medicine (AIUM), показания к проведению узи сосудов шеи включают в себя:
исследования сосудов шеи в диагностике причин головной боли
Головная боль не является показанием для проведения узи сосудов шеи в большинстве случаев. По крайней мере, как изолированный симптом. Иногда головная боль возникает вследствие повышения внутричерепного венозного давления. При проведении узи сосудов шеи оцениваются также и внутренние яремные вены, затруднение оттока по которым может вызвать повышение внутричерепного венозного давления. Такое может случаться при тромбозе внутренних яремных вен (крайне редко) и при правожелудочковой сердечной недостаточности. Иногда ухудшение оттока крови по правой внутренней яремной вене может происходить на вдохе и улучшаться на выдохе. Из-за анатомических особенностей. При этих состояниях ВСЕГДА есть другие симптомы, которые позволяют заподозрить данную патологию. Узи сосудов шеи в этих случаях является уместным, но не исчерпывающим методом диагностики. Выбрать необходимый метод исследования (например, КТ сосудов с контрастированием или узи сердца) может только врач.
исследования сосудов шеи в диагностике недостаточности крвообращения в вертеб базиллярном отделе
Вертебробазиллярный бассейн включает в себя позвоночные артерии, основную артерию и отходящие от нее задние мозговые артерии. У человека позвоночные артерии отходят от подключичных артерий с обеих сторон, проходят между мышцами шеи и на уровне 6 шейного позвонка впадают в костный канал, образованный отверстиями в поперечных отростках шейных позвонков (сосуды, исследуемые при дуплексном сканировании головы и шеи). 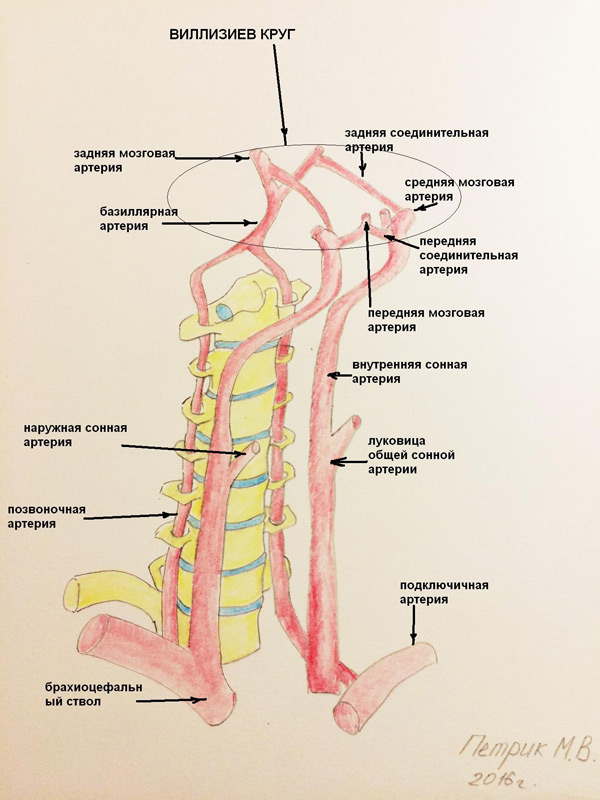
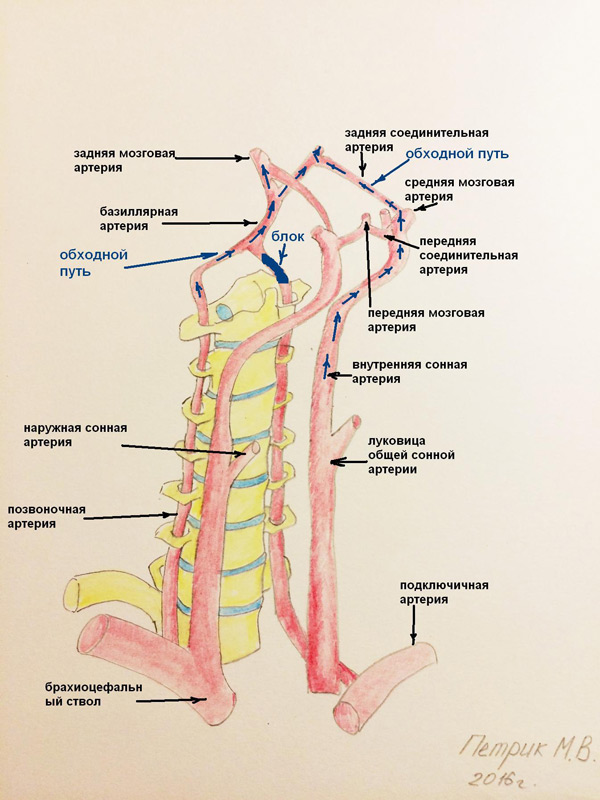
Второе ограничение при проведении поворотных проб при узи сосудов шеи – техническая невозможность моделировать некоторые ситуации, при которых может происходить нарушение кровотока в позвоночных артериях. Иногда просто невозможно достичь визуализации зоны интереса, так как она закрыта структурами, не пропускающими ультразвук.