высокая метаболическая активность что это
Высокая метаболическая активность что это
Актуальность проблемы. В настоящее время большинство онкобольных нуждаются в комбинированном лечении [4,6]. Наблюдаемые у ряда больных неудачи побудили в последнее время шире прибегать к выбору тактики лечения в зависимости от оценки распространенности процесса [3]. Происходит постоянная оптимизация методов для оценки распространения заболевания у пациентов с опухолями пищевода и желудка. Компьютерная томография (КT) представляет стандарт в определении инвазии опухоли. КТ является неинвазивным и наименее дорогостоящим из доступных методов, но имеет серьезные ограничения в плане точной постановки диагноза [5]. Позитронно-эмиссионная томография (ПЭТ) также является неинвазивным, но предоставляет качественно иную информацию по сравнению с КТ, благодаря своей функции участия в метаболическом процессе опухоли, а не только определяя размер опухоли [1]. Многие исследователи показали, что снижение метаболической активности, измеренной значением стандартизированного накопления (SUV) на ПЭТ/КТ, в результате терапии является прогностически значимым критерием [7,9,10]. Следует отметить, что ПЭТ/КТ изображения были изучены у ограниченного количества больных и, согласно другим исследованиям, прогностическая ценность является сомнительной [8,11]. Тем не менее данные ПЭТ/КТ при злокачественных опухолях верхних отделов желудочно-кишечного тракта не были подтверждены [2] и требуют дальнейшего изучения.
Цель работы: выявить зависимость коэффициента максимального поглощения радиофармпрепарата18F-ФДГ от следующих характеристик опухолевого процесса – глубины инвазии опухолевого процесса, гистологической структуры опухоли и степени дифференцировки злокачественной опухоли.
Материалы и методы исследования. В исследование были включены 56 больных с установленным диагнозом или подозрением на злокачественную опухоль верхних отделов желудочно-кишечного тракта, в возрасте от 29 до 89 лет, проходивших обследование на базе отделения радиоизотопной диагностики АО «Республиканского диагностического центра» г. Астана в период с 2010 по 2012 г. Основными критериями включения в исследование явились: наличие или подозрение на злокачественную опухоль желудка или пищевода; проведение позитронно-эмиссионной томографии, совмещенной с компьютерной томографией. Локализация патологического процесса в пищеводе отмечена у 16 больных (28,5%), локализация в желудке – у 40 больных (71,5%). Всем больным проведено ПЭТ/КТ исследование на базе Республиканского Диагностического Центра г. Астана. Позитронно-эмиссионный томограф, совмещенный с 16-срезовым компьютерным томографом GeminiGXL 16 фирмы Philips производства 2008 года. Для проведения ПЭТ/КТ исследования на базе РДЦ создан производственный комплекс, включающий циклотрон «Cyclone 18/9» для производства короткоживущих изотопов, радиохимическая лаборатория для производства радиофармпрепаратов. При проведении ПЭТ/КТ использовался радиофармацевтический препарат «Фтордезоксиглюкоза, 18F, раствор для внутривенного введения». Вводимая доза препарата зависела от площади поверхности тела исследуемого человека. Поверхность тела рассчитывалась по номограмме, исходя из веса и роста больного. Диагностическая доза препарата составляла 220 МБк на 1 м2 поверхности тела пациента; как правило, использовали 300–550 МБк на одно исследование. Препарат вводился внутривенно медленно в объеме 5,0–10,0 мл.
Результаты и их обсуждение. Нами проведен анализ показателя SUVmax в первичной опухоли и определена зависимость коэффициента SUVmax в зависимости от основных характеристик онкологического процесса, таких как глубина инвазии опухолевого процесса, гистологическая структура и дифференцировка опухоли.
Накопление фармпрепарата в первичной опухоли у больных со злокачественными новообразованиями верхних отделов желудочно-кишечного тракта варьировало от 2,1 до 13, в среднем составило 6,25±2,26.
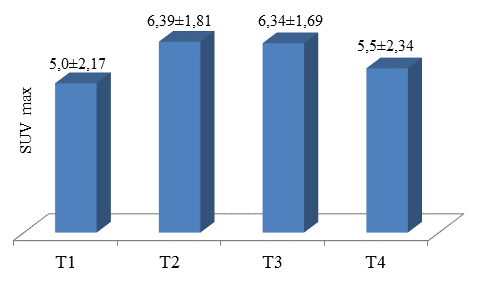
Зависимость максимального накопления радиоизотопа глюкозы от глубины инвазии опухолевого процесса в стенку органа представлена на рисунке 1.
Рисунок 1. Коэффициент SUVmax в зависимости от глубины инвазии опухолевого процесса
Как видно из представленной диаграммы, максимальное накопление радиофармпрепарата не зависело от глубины инвазии стенки органа опухолевым процессом. Наибольшие показатели накопления радиофармпрепарата в первичной опухоли отмечены при прорастании мышечного (Т2, n=27) и серозного (Т3, n=21) слоев. Наиболее низкие показатели отмечены при поражении только слизистого слоя (Т1, n=3) и при прорастании в соседние органы (Т4, n=5). Полученные данные не имели статистически значимых различий (p=0,41).
Проведен анализ содержания радиофармпрепарата ФДГ 18F в зависимости от протяженности поражения органа. Полученные данные представлены в таблице 1.
Таблица 1. Коэффициент SUVmax в зависимости от протяженности поражения органа
Роль позитронно-эмиссионной томографии с 18F-ФДГ в комплексном обследовании пациентов методами лучевой диагностики: достоинства и недостатки
Внедрение в России в клиническую практику позитронно-эмиссионной томографии сопровождалось дискуссиями об актуальности новой методики. До сих пор в научных кругах звучат крайние суждения о ПЭТ как о диагностической панацее с одной стороны, так и о ее крайне низкой целесообразности с другой. Основной причиной разночтений, по нашему мнению, является самостоятельное, оторванное от других методов медицинской визуализации, развитие в России радиоизотопной диагностики в целом и ПЭТ в частности.
Внедрение в России в клиническую практику позитронно-эмиссионной томографии (ПЭТ) сопровождалось дискуссиями об актуальности новой методики. До сих пор в научных кругах звучат крайние суждения о ПЭТ как о диагностической панацее с одной стороны, так и о ее крайне низкой целесообразности с другой.
Основной причиной разночтений, по нашему мнению, является самостоятельное, оторванное от других методов медицинской визуализации, развитие в России радиоизотопной диагностики в целом и ПЭТ в частности.
В федеральном государственном бюджетном учреждении «Клиническая больница №1» Управления делами Президента Российской Федерации (Волынская больница ) два ПЭТ томографа ECAT EXACT 47 фирмы Siemens были инсталлированы в 2001 г.
Таким образом, Волынская больница первой в системе Главного медицинского управления внедрила методику позитронно-эмиссионной томографии и имеет максимальный опыт ее применения.
Все эти годы лаборатория радиоизотопной диагностики и позитронно-эмиссионной томографии функционировала в составе единого отделения лучевой диагностики. Основной идеологией работы отделения является принцип полимодальности. Врач лучевой диагностики на рабочих станциях изучает изображения, полученные при всех ранее проведенных методах медицинской визуализации. Результатом такого подхода являются наиболее достоверные диагностические заключения. Ежедневно в отделении проводится коллегиальное обсуждение результатов с участием рентгенологов, врачей ультразвуковой диагностики, компьютерной и магнитно-резонансной томографии, что дает объективность и преемственность диагностического процесса, расширяет кругозор врачей.
За время работы лаборатории нами было обследовано 3746 пациентов. Из них 85% составили онкологические, 10% неврологические и 5% кардиологические. Такое распределение пациентов соответствует литературным данным, обобщающим опыт работы на ПЭТ с фторглюкозой в других странах.
Волынская больница стала первым учреждением в стране, которое ввиду отсутствия своего циклотрона, отработало, лицензировало и внедрило в практику сателлитный принцип организации ПЭТ лаборатории.
Ввиду отдаленности от циклотрона ФГБУ «Клиническая больница №1» ограничена в выборе РФП и вынуждена использовать только дезоксиглюкозу, меченую 18F, с периодом полураспада в 110 мин. В конце прошлого века за свою универсальность и диагностическую ценность фтордезоксиглюкоза была названа «Молекулой века».
Многолетний опыт работы лаборатории, ретроспективный анализ полученных данных, сравнение результатов ПЭТ с заключениями других методов лучевой диагностики выявил следующие клинические особенности методики.
Первой из них мы назвали бы кажущуюся и обманчивую простоту диагностического процесса. Это обусловлено недостаточно точной привязкой к морфологическим ориентирам, скудностью семиотических признаков и отсутствием строгих количественных критериев накопления ФДГ в различных образованиях.
Проблемы интерпретации результатов ПЭТ исследований иногда связаны с особенностями физиологического выведения ФДГ через мочевыводящую систему, всегда визуализируется чашечно-лоханочная система как очаги гиперфиксации радиофармпрепарата различной степени выраженности.
У пациента Е. при ПЭТ видны множественные очаги гиперфиксации ФДГ в проекции обеих почек. Оценить заинтересованность почек не представляется возможным. При магнитно-резонансной томографии визуализируются пакеты увеличенных лимфоузлов, интимно прилежащих к почкам, без их поражения. Затруднения также вызывает широкая вариабельность физиологического накопления фторглюкозы. Часто визуализируется различной степени гиперфиксация препарата по ходу желудочно-кишечного тракта, а так же в различных группах скелетных мышц при их напряжении.
Так у пациента К. в проекции толстой кишки определяется протяженная гиперфиксация фторглюкозы. Данные ирригоскопии и колоноскопии позволили исключить наличие пораженных участков.
А у пациента Н. выявлялись очаги гиперфиксации фторглюкозы в шейно-надключичной области, подозрительные на пораженные лимфоузлы. При ультразвуковом исследовании подозрение о поражении лимфоузлов было снято.
В некоторых случаях имеют место ложноотрицательные результаты ПЭТ исследований, связанные с одной стороны с относительно низкой разрешающей способностью ПЭТ томографов и с другой стороны с особенностями метаболизма некоторых опухолей, таких как почечно-клеточная карцинома, рак простаты, карциноид и др., часто не поглощающих ФДГ в избыточных количествах. Так же на оценке результатов исследования сказывается уровень глюкозы в крови. При гипергликемии ухудшается качество получаемого изображения и повышается количество ложноотрицательных результатов.
Как пример, при ультразвуковом исследовании почек у пациента Б. было выявлено кистозно-солидное образование в левой почке, которое после проведения компьютерной томографии с внутривенным болюсным контрастным усилением было расценено как доброкачественное.
При ПЭТ исследовании в проекции выявленного объемного образования захвата фторглюкозы не наблюдалось, что тоже говорило в пользу его доброкачественности.
При операции была выявлена умеренно дифференцированная почечно-клеточная карцинома.
Так же встречаются и ложноположительные результаты, связанные с инфекционными и воспалительными процессами, напряжением мышц, состоянием после лучевой и химиотерапии, послеоперационными изменениями и пр.
Так, у пациентки Д. с резекцией левой молочной железы по поводу рака в анамнезе, при ПЭТ исследовании в проекции базальных отделов правого легкого были выявлены очаги гиперфиксации фторглюкозы, подозрительные на метастатический процесс. При проведении компьютерной томографии предположен диагноз туберкулеза правого легкого, который в последующем подтвердили в специализированном учреждении.
Тем не менее, не смотря на вышеперечисленные особенности и ограничения, позитронно-эмиссионная томография заняла достойное место в комплексном обследовании пациентов, так как является методом функциональным и позволяет изучать биохимические процессы организма на молекулярном уровне в томографическом режиме.
Частным примером такого применения является использование позитронно-эмиссионной томографии в неврологии. У пациента М. по клиническим признакам была заподозрена болезнь Альцгеймера. При магнитно-резонансной томографии головного мозга были выявлены только признаки умеренной энцефалопатии, а при ПЭТ исследовании визуализируется двухстороннее уменьшение накопления фторглюкозы в теменной, височной и лобной долях, что характерно для болезни Альцгеймера.
В кардиологии позитронно-эмиссионная томография тоже заняла свою нишу. В мировой практике ПЭТ уже давно является «золотым стандартом» оценки жизнеспособности миокарда в зонах ишемии, определяя целесообразность кардиохирургического вмешательства.
Так, у пациента с зоной выраженного снижения перфузии в задней части перегородки, с гипокинезом и выраженным стенозом правой коронарной артерии при ПЭТ исследовании выявляется сохранный уровень углеводного метаболизма в этой области, что свидетельствует о наличии жизнеспособного миокарда и целесообразности реваскуляризации, после проведения которой функция миокарда восстановилась, состояние пациента улучшилось.
Но наиболее востребована позитронно-эмиссионная томография в онкологической практике. Своевременная диагностика злокачественных опухолевых процессов является одной и актуальных проблем современной медицины. От полноты и объективности оценки первичной опухоли и вторичных изменений зависит определение стадии опухолевого процесса и выбор адекватной тактики лечения.
В отличие от других методов лучевой диагностики (УЗИ, РКТ, МРТ), являющихся анатомо-топографическими, ПЭТ позволяет оценить биологическую активность опухолевой ткани, динамику ее изменений в процессе лечения, определить регионарное и отдаленное метастазирование в организме за одно исследование.
Принцип регистрации опухолей с использованием ФДГ основан на явлении повышенного гликолиза в злокачественных опухолях, причем скорость потребления глюкозы находится в прямой зависимости от степени злокачественности новообразования. Кроме того, злокачественные опухоли характеризуются относительно низкой активностью фосфотазы и высокой активностью гексокиназы. Образующийся в результате биохимических реакций 18F-ФДГ-6-фосфат не вступает в дальнейшие реакции гликолиза и тем самым формируется «метаболическая ловушка», что приводит к повышенному содержанию 18F-ФДГ-6-фосфата в ткани опухоли и способствует ее выявлению.
Так, у пациента с клиникой поражения печени при УЗИ были выявлены изменения диффузного характера. При компьютерной томографии с внутривенным болюсным контрастным усилением выявлено объемное образование печени без четких данных о его характере, а при позитронно-эмиссионной томографии визуализируется огромное злокачественное образование с метастазами в ворота печени и средостение, что позволило правильно скорректировать тактику ведения пациента.
Исходя из возможностей позитронно-эмиссионной томографии, были сформулированы показания к исследованию:
• оценка распространенности опухолевого процесса (стадирование опухолей).
• поиск первичного очага при выявленных метастазах.
• оценка эффективности лечения.
• выявление рецидивов и продолженного роста новообразований.
• первичный поиск при наличии клинических проявлений
• дифференциальная диагностика злокачественных и доброкачественных образований.
Отвечая на поставленные вопросы, позитронно-эмиссионная томография способствует установке более точного диагноза, изменению стадирования опухолевого процесса в сторону повышения или понижения и тем самым позволяя скорректировать проводимую терапию.
Таким образом, можно смело сказать, что позитронно-эмиссионная томография имеет большое значение в диагностическом процессе, является важным диагностическим инструментом и чрезвычайно перспективным методом визуализации злокачественных опухолевых образований.
Зубанов А.Г., Радкевич Л.А., Родченко З.П., Зайцева А.Ю.
Статья добавлена 11 марта 2015 г.
Метаболический синдром: симптомы и диагностика нарушений обмена веществ
Метаболический синдром (МС) – это комплекс патологий, которые увеличивают риск возникновения сердечно-сосудистых заболеваний, инсульта и инфаркта.
Симптомы метаболического синдрома
По сути, метаболический синдром не является самостоятельным заболеванием. Это группа симптомов, которые часто встречаются вместе и увеличивают риск других – еще более тяжелых – нарушений.
Тревожные тенденции
Еще недавно метаболическим синдромом страдали преимущественно пожилые люди (старше 60 лет). Картина существенно изменилась за последние 20 лет. Динамика показала, что эта проблема молодеет и становится актуальной для более юного населения. В ряде стран доля взрослого населения, страдающая от этих симптомов, достигает 25%.
У метаболического синдрома есть еще одно название – «синдром нового мира». Дело в том, что преимущественно от ожирения и связанных с ним патологий страдают люди, ведущие малоподвижный образ жизни (а это касается преобладающего числа жителей больших городов), употребляющие большое количество быстрых углеводов и трансжиров. В результате во всем мире наблюдается всплеск сердечно-сосудистых заболеваний и диабета.
Метаболический синдром затрагивает как развитые страны (где высокотехнологичное производство избавило население от необходимости много двигаться), так и развивающиеся (большому проценту населения которых приходится экономить на продуктах питания и потреблять больше быстрых углеводов – макарон, хлеба, картофеля, кукурузы).
Есть и другая тенденция последних лет. От метаболического синдрома стали страдать женщины репродуктивного возраста. С чем это связано, до конца неясно. Предположительно, могут негативно влиять оральные контрацептивы.
Только представьте: за последние 20 лет число людей с метаболическим синдромом в мире выросло более чем на 100 млн – то есть на треть.
Особенно остро стоит проблема детского ожирения, а с ним и детского МС. Ученые связывают рост детского ожирения с частым отказом от грудного вскармливания. Грудное вскармливание исключает раннее введение прикорма, которое может привести к нездоровому увеличению веса. Потребление белка и общего количества энергии выше у детей, вскармливаемых смесями, что приводит к увеличению массы тела у младенцев. Также кормление смесью несколько увеличивает уровень инсулина, что в свою очередь способствует отложению жира и раннему развитию жировых клеток (адипоцитов).
Таким образом, быстрая прибавка в весе в младенческом возрасте связана с ожирением в детстве. Грудное вскармливание может помочь «запрограммировать» человека на поддержание здорового веса во взрослом возрасте.
В чем причины?
Метаболический синдром имеет наследственную предрасположенность, которая, однако, в большей степени тоже объясняется внешними факторами. Люди, выросшие в одной семье, с большей вероятностью будут иметь схожие пищевые привычки и одинаковое отношение к спорту. Если на родительском столе бывает огромное количество быстрых углеводов и жиров и мало – овощей, зелени и фруктов, у ребенка с детства закладываются нездоровые отношения с едой. Так же и со спортом: ребенок с большей вероятностью будет активным, если у него активные родители.
Факторы риска
Осложнения
Диагностика метаболического синдрома
Диагностика МС состоит из визуального осмотра у врача и лабораторных и инструментальных исследований. В первую очередь врач оценивает абдоминальное ожирение. Но одного лишнего веса для постановки диагноза недостаточно. Оцениваются и другие симптомы и результаты анализов. Также важно обнаружить причину ожирения. Лишний вес может быть следствием эндокринных нарушений, гормональных сбоев или иных патологий.
Другой важный критерий при постановке диагноза – артериальное давление. При метаболическом синдроме оно обычно повышено.
ЭКГ – требуется, чтобы проверить работу сердца и вовремя обнаружить патологии, если заболевание уже запущенно.
Ангиография. Сложное исследование, которое позволяет оценить состояние сосудов. Проводится только по назначению врача.
Диагностика метаболического синдрома – непростая комплексная задача, которая осложняется разнообразием форм заболевания, его причинами и способами коррекции. Также это состояние опасно тем, что долгие годы человек не ощущает себя больным. Самочувствие начинает страдать, когда появляются значительные отклонения в работе организма и развиваются осложнения. Ни один человек не может ощутить повышенный уровень глюкозы в крови или нарушение обмена холестерина. О себе дают знать только уже очень серьезные проблемы, вызванные этими нарушениями, – например, гнойное воспаление пальцев ног или сердечный приступ.
Международная классификация болезней не выделяет метаболический синдром как отдельное заболевание, это целый комплекс заболеваний.
Ни один диагноз нельзя поставить самостоятельно, но любое отклонение в результатах исследований – повод не откладывать поход к врачу.
Лечение
В более запущенных формах может потребоваться применение препаратов, снижающих инсулинорезистентность, и лечащих артериальную гипертонию.
Позитронно Эмиссионная Томографии (ПЭТ)
Главное в онкологии – максимально быстро начать лечение и лучшим считается тот метод визуализации, который обеспечивает быстроту, неинвазивность и точность, поскольку время, потраченное на диагностику, может обернуться значительным ростом опухоли или метастазированием, а лечение заболевания становится более сложным.
Применение таких методов диагностики опухолей даёт возможность клиницистам онкологического центра имени Н.Н. Блохина выработать адекватную стратегию для успешного и своевременного лечения в каждом конкретном случае.
ПОЗИТРОННАЯ ЭМИССИОННАЯ ТОМОГРАФИЯ (ПЭТ) – метод ядерной медицины, основанный на использовании радиофармпрепаратов (РФП), меченных короткоживущими позитрон-излучающими радионуклидами, которые могут быть включены в состав многих естественных биологических веществ, участвующих в метаболизме, без изменения их биохимических свойств. Поэтому ПЭТ с различными РФП позволяет оценить происходящие в организме процессы, обеспечивает информацией о вариабельности различных клеточных и биологических процессов в опухолях и окружающих их тканях. 18 F-ФДГ («ПЭТ с глюкозой») – наиболее распространённый РФР в онкологии. Препараты на основе аминокислот 18 F-ФЭТ («ПЭТ с тирозином») является аналогом 11 С-Метионина («ПЭТ с метионином»), но обладают рядом преимуществ – меньше накапливаются в воспалительных изменениях и имеют более длинный период полураспада. 18 F-Холин («ПЭТ с холином») – препарат, получивший широкое распространение в мире в диагностике рецидивов рака простаты после радикального лечения и оценке отдалённого метастатического поражения.
ПЭТ – это диагностическая процедура, которая практические не имеет побочных эффектов или абсолютных противопоказаний и, в общем, не доставляет неприятных ощущений. Данное обследование может быть показано как взрослым, так и детям, и, как любые другие диагностические исследования, назначается врачом-клиницистом после консультации.
Исследования в нашем центре проводятся в условиях максимального комфорта и конфиденциальности.
Полученная при ПЭТ исследовании информация о характере метаболических процессов в опухолях даёт возможность целенаправленно воздействовать на их жизнедеятельность, повышает избирательность и точность предстоящего лечения.
Уточнение объёма активной опухолевой ткани позволяет максимально сократить отрицательное влияние на здоровые клетки организма при выборе лучевых методов лечения.
ПЭТ позволяет на ранних сроках выявлять рецидивы злокачественных опухолей и дифференцировать их с посттерапевтическими изменениями (в частности, постлучевыми некрозами и фиброзами).
Метаболическая активность опухоли отображается в виде количественной оценки уровня накопления различных РФП и измеряется в единицах SUV (Standardized Uptake Values – стандартизированный уровень накопления, чаще используются максимальные значения). Динамика изменения уровня накопления РФП в опухолях и их метастазах до лечения и в процессе терапии позволяет с высокой достоверностью оценивать эффективность лечения.
Вследствие разнородности метаболических изменений внутри самой опухоли различные участки злокачественных новообразований могут отличаться по уровню включения РФП. Исходя из этого, ПЭТ позволяет выявлять наиболее агрессивные участки опухоли для выбора оптимального места для биопсии.
Полученная информация даст возможность вашему лечащему врачу в кратчайшие сроки установить диагноз и правильно спланировать лечение.
В нашем отделении исследования проводятся на современной аппаратуре в режиме ПЭТ/КТ. Полученные в ходе исследования данные значительно сокращают общее время диагностики и позволяют адекватно корректировать проводимую терапию.
Особенно важное значение метод имеет при раке лёгких, опухолях желудочно-кишечного тракта, раке простаты, нейроэндокринных опухолях, опухолях головного мозга, а также при лимфомах. При солидных опухолях (опухоли в паренхиматозных органах: таких как лёгкие, печень, простата, почки, головной мозг, поджелудочная железа, яичники и др.) результаты ПЭТ могут использоваться для планирования лечения на роботизированной стереотаксической радиохирургической установке, представленной на территории РОНЦ имени Н.Н.Блохина кабинетом «КиберНож».
ГИБРИДНАЯ ТЕХНОЛОГИЯ ПЭТ, СОВМЕЩЁННОЙ С КОМПЬЮТЕРНОЙ ТОМОГРАФИЕЙ (ПЭТ/КТ) облегчает интерпретацию результатов радионуклидного метода за счёт «наложения» анатомической картины, получаемой при КТ. ПЭТ/КТ открывает новые возможности в уточняющей диагностике опухолей и за одну процедуру, кроме более чёткой локализации первичной опухоли, позволяет получать развёрнутую информацию о состоянии других органов и систем (для исключения метастазирования).
Использование комбинированных систем предусматривает коррекцию изображений ПЭТ по данным КТ, и, поскольку, длительность исследования составляет 30-40 минут, для того, чтобы избежать артефактов при реконструкции ПЭТ (мисрегистрации изображений вследствие движения пациента) и обеспечения качества полученных изображений, используются различные приспособления в виде специальных подголовников, фиксирующих подушек и матрацев.
При ПЭТ-исследованиях наиболее стандартный уровень сканирования всего тела — от основания черепа до середины бедра. При необходимости, ПЭТ и ПЭТ/КТ проводят с расширенной зоной сканирования с реальным захватом всего тела – от макушки до стоп.
При проведении ПЭТ-исследования пациенту внутривенно водится радиофармпрепарат (РФП), меченный «короткоживущим» радионуклидом, например, 18F-ФДГ (2-фтор-2-дезокси-D-глюкоза), который используется для оценки активности метаболизма глюкозы (рис. а).
Все радиофармпрепараты (РФП) изготавливаются нами индивидуально для каждого пациента в день исследования с соблюдением всех необходимых норм (по стандартам GMP). В случае любых незначительных отклонений от технологии производства проведение ПЭТ-исследования будет отложено, чтобы гарантировать вашу безопасность.
КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ (КТ) основана на рентгеновском излучении, она позволяет определять анатомическое строение органов и тканей.
В ряде случаев (уточняйте у вашего врача) КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ (КТ) проводится с внутривенным КОНТРАСТИРОВАНИЕМ, которое выполняется посредством болюсного введения контрастного вещества со скоростью 2,5-4 мл/с при помощи автоматического шприца-инжектора. Как правило, используются йодсодержащие рентгеноконтрастные вещества (например, «Омнипак») в объёме от 50 до 100 мл3 – в зависимости от органа или части тела, которые требуется исследовать, а также различные методики КТ (многофазное контрастирование, ангиография, КТ-перфузия).
КТ С ВНУТРИВЕННЫМ КОНТРАСТИРОВАНИЕМ позволяет уточнить природу новообразования, определить границы опухоли, отношение её к окружающим органам и кровеносным сосудам, что имеет немаловажное значение для планировании лечения.
18 F—ФДГ с химической точки зрения является аналогом природной глюкозы и позволяет оценивать гликолитическую активность тканей. При внутривенном введении 18 F—ФДГ интенсивно накапливается в органах и тканях, в которых активно протекает процесс гликолиза (головной мозг, миокард, желудок и кишка, печень, мышцы).
Принцип применения 18 F- ФДГ в онкологии основывается на разнице дифференциальных скоростей метаболизма глюкозы в доброкачественных и злокачественных тканях. Известно, что интенсивность накопления 18 F- ФДГ может быть связана с размером опухоли и может значительно варьироваться при различных типах злокачественных опухолей. NB: накопление РФП также ускоряется при воспалительных процессах, таких как: гранулёмы, абсцессы, что может приводить к возникновению ложно-положительных результатов.
Многие злокачественные опухоли характеризуются повышенным метаболизмом глюкозы, и, следовательно, применение ПЭТ с 18 F—ФДГ у них имеет высокую диагностическую эффективность. Интенсивность накопления 18 F—ФДГ в различных злокачественных опухолях отображает степень их злокачественности и биологическую агрессивность.
В процессе противоопухолевого лечения, объём жизнеспособных злокачественных клеток значительно сокращается, и, следовательно, количественная оценка изменений накопления 18 F-ФДГ в опухолях позволяет использовать этот РФП в качестве чувствительного маркёра эффективности противоопухолевой терапии, что было реализовано в системе критериев оценки эффективности лечения PERCIST (Positron Emission tomography Response Criteria In Solid Tumors).
ПЭТ/КТ с 18 F-ФДГ используется для диагностики, оценки распространённости и динамического наблюдения опухолей молочной железы, колоректального рака, рака пищевода, рака лёгких, лимфом, опухолей головы и шеи, меланомы и ряда других онкологических заболеваний (уточните при записи на исследование). ПЭТ/КТ с 18 F-ФДГ – надёжный способ диагностировать эти опухоли и определить распространённость заболевания, выявлять рецидивы при наличии биомаркёрного рецидива (у бессимптомных пациентов при отсутствии патологических изменений по данным МРТ, КТ или УЗИ), дифференцировать рецидивы от фиброзов и некрозов, и, соответственно, при необходимости корректировать лечение в ходе наблюдения за пациентом.
ПОДГОТОВКА К ИССЛЕДОВАНИЮ:
Этот препарат применяется прежде всего для оценки распространённости, эффективности лечения и диагностики рецидивов РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ, а так же для диагностики ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА, ОПУХОЛЕЙ ПЕЧЕНИ (прежде всего ГЦР ).
Исследование проводится в два этапа (сразу после введения РФП и через 40 минут), строго натощак (при обследовании по поводу рака предстательной железы без водной нагрузки – с утра полностью исключить потребление жидкости).
За 48 часов до исследования необходимо исключить из рациона питания следующие продукты: яйца, субпродукты, бобы, овсяная крупа, шпинат, арахис, апельсиновый сок, капуста, любые витамины (прежде всего группы В).
Чтобы подготовится к исследованию, необходимо выполнить следующие условия:
В настоящее время наиболее прогрессивным и уже зарекомендовавшим себя методом является ПЭТ/КТ, в частности, с использованием 18 F-Холина. Благодаря особенностям метаболизма Холина в клетке рака предстательной железы возможно не только оценить распространённость процесса, но и отличить воспалительные изменения от опухолевых с применением методики двухэтапного исследования, как это показано на представленных снимках – на первом этапе происходит накопление в двух лимфоузлах, указанных красными стрелками. Проведение 2 этапа исследования через 40-50 минут показало, что накопление 18 F-Холина сохраняется только в одном из лимфоузлов (указан красной стрелкой), в то время как изменения в другом лимфоузле (указан зелёной стрелкой) имеют воспалительную природу.
Тактика лечения злокачественных опухолей печени зависит от их внутри- и внеорганной распространённости (метастазы). Хирургическое лечение не показано при множественных метастазах. Поэтому одной из основных задач диагностики является определение распространённости процесса. ПЭТ/КТ обладает высокой чувствительностью при обнаружении рецидивов опухолей после хирургического вмешательства. Так как частота рецидивов при раке печени высока (рецидив заболевания в первый год после операции составляет 20–64%, через 3 года — 57–81%), необходимо как можно раньше выявить изменения, чтобы своевременно начать лечение. Даже при наличии такого высокоточного метода диагностики, как МРТ, нередко возникает проблема дифференцировки объёмного образования в печени. Зачастую, вследствие его малых размеров (менее 1 см), невозможно однозначно высказаться о природе новообразования (доброкачественное или злокачественное). ПЭТ/КТ с 18 F-Холином и 18 F-ФДГ может дать ответ на поставленный вопрос, основываясь на механизмах включения указанных радиофармпрепаратов в опухолевые клетки.
ЦЕЛИ ИССЛЕДОВАНИЯ ПРИ ОПУХОЛЯХ ГОЛОВНОГО МОЗГА:
18 F-ФЭТ отражает уровень активности транспорта аминокислот в клетке и имеет высокую диагностическую точность в определении объёма опухолевого поражения и достоверной оценке границ образования при планировании как хирургического, так и лучевого лечения.
Показания к ПЭТ/КТ исследованию с 18 F-ФЭТ:
Исследование проводится строго натощак. Пить воду можно по желанию (несладкую, негазированную). Необходимо исключить продукты, богатые тирозином: орехи, бобовые, пряности, включая травы, за неделю до исследования.
Для прохождения ПЭТ/КТ исследования вам необходимо взять с собой все документы по заболеванию (выписки, консультации и т.п.), все диски МРТ.
Известно, что большинство опухолей женской репродуктивной системы и молочных желёз гормонозависимы, то есть имеют в структуре рецепторы стероидных гормонов (эстрогена и прогестерона).
18 F-фторэстрадиол ( 18 F-ФЭС) – радиофармпрепарат (РФП), который является аналогом эстрадиола и применяется при опухолях, экспрессирующих рецепторы эстрогенов (РЭ).
В настоящее время исследование ПЭТ/КТ с 18 F-ФЭС наиболее широко применяется у больных раком молочной железы (РМЖ), поскольку в половине случаев опухоль является гормонозависимой.
По ПЭТ гормонозависимая опухоль молочной железы визуализируется в виде «горячего» очага патологического включения 18 F-ФЭС (на фоне нормального физиологического накопления РФП в железистой ткани). Чем больше РЭ в опухолевой ткани (по результатам иммуногистохимического исследования после биопсии опухоли молочной железы – люминальный лип А и В и РЭ должны быть не менее 5 баллов), тем больше чувствительность ПЭТ/КТ с 18 F-ФЭС и выше прогностическая ценность положительного результата в оценке распространённости опухолевого процесса и мониторинга гормональной терапии.
В норме 18 F-ФЭС накапливается в печени, желчевыводящих путях, тонкой кишке и мочевом пузыре, что обусловлено физиологическим выведением 18 F-ФЭС через гепатобилиарную и мочевыделительную системы.
ПЭТ/КТ с 18 F-ФЭС позволяет определить разные биологические подтипы РМЖ, то есть распознавать гормонозависимые формы, что и отличает эти исследования от широко распространённой ПЭТ/КТ с 18 F-фтордезоксиглюкозой ( 18 F-ФДГ).
В оценке распространённости опухолевого процесса при гормонозависимом РМЖ чувствительность и специфичность ПЭТ/КТ с 18 F-ФЭС превосходит таковые при 18 F-ФДГ (другими словами позволяет выявить бόльшее количество опухолевых очагов), что может влиять на тактику лечения.
Применение ПЭТ/КТ с 18 F-ФЭС при раке молочной железы:
Ограничения при проведении ПЭТ/КТ с 18 F-ФЭС у пациентов с гормонозависимой формой РМЖ при гормональной терапии препаратами из группы ингибиторов РЭ (селективных модификаторов эстрогенных рецепторов, например, тамоксифен и фазлодекс). Необходима отмена препарата не менее чем за 30 дней, согласованная с лечащим врачом-онкологом. Гормонотерапия препаратами других групп (к примеру, ингибиторами ароматазы) не влияет на информативность исследования.
Подготовка к исследованию ПЭТ/КТ с 18 F-ФЭС:
Методика проведения исследования ПЭТ/КТ с 18 F-ФЭС (аналогична ПЭТ/КТ с 18 F-ФДГ). В среднем процедура занимает 1,5 часа.
После введения РФП в катетер, предварительно установленный в кубитальной вене (желательно с противоположной стороны от локализации опухоли), пациент проводит в комнате релаксации час, за это время РФП распределяется по организму. Затем проводится ПЭТ/КТ сканирование в течение примерно 20 минут.
Запись на исследование ПЭТ/КТ с 18 F-ФЭС проводится в регистратуре отделения ПЭТ НМИЦ онкологии им. Н.Н. Блохина по рекомендации лечащего врача.
Рак предстательной железы является одним из наиболее распространённых онкологических заболеваний у мужчин.
Простатспецифический мембранный антиген (ПСМА) – мембранный гликопротеин, содержащийся в нормальных эпителиальных клетках предстательной железы. Его уровень увеличивается при раке предстательной железы, особенно при низкой степени дифференцировки, метастатическом процессе или гормон-рефрактерных формах заболевания.
18 F-простатспецифический мембранный антиген-1007 ( 18 F-ПСМА-1007, 18F-PSMA-1007) – радиофармпрепарат (РФП), который является аналогом ПСМА и используется в диагностике опухолей предстательной железы.
В настоящее время ПЭТ/КТ-исследование с 18 F-ПСМА-1007 является перспективным радиофармпрепаратом в диагностике рецидивов рака предстательной железы, так как обладает наиболее высокой чувствительностью, в том числе при уровне ПСА 18 F-ПСМА-1007 накапливается в слёзных и слюнных железах, печени, селезёнке, тонкой кишке и почках.
В отличие от других ПСМА-таргетных трейсеров, 18 F-ПСМА-1007 характеризуется меньшим выведением по мочевыводящим путям, а потому лучшей визуализацией предстательной железы.
Методика проведения исследования ПЭТ/КТ с 18 F-ПСМА-1007 (аналогична ПЭТ/КТ с 18 F-ФДГ). В среднем процедура занимает 1,5-2 часа. После введения РФП в катетер, предварительно установленный в локтевой вене, пациент проводит в комнате релаксации 60-90 минут. За это время РФП распределяется по организму. Затем проводится ПЭТ/КТ сканирование в течение примерно 20-30 минут.
Запись на исследование ПЭТ/КТ с 18 F-ПСМА-1007 проводится в регистратуре отделения ПЭТ НМИЦ онкологии им. Н.Н. Блохина по рекомендации лечащего врача.
На базе НИИ КиЭР в рамках отделения позитронной эмиссионной томографии, лаборатории радиоизотопной диагностики, отделения лучевой топометрии и клинической дозиметрии сформировано направление ТЕРАНОСТИКИ, основанное на комбинированном применении методов радионуклидной диагностики и терапии.
В настоящий момент планируется внедрение препаратов на основе таких изотопов, как 89 Sr, 223 Ra, 177 Lu, применяемых преимущественно для лечения костных метастазов и диссеминированного рака предстательной железы.