вторичная нефропатия что это
Нефропатия
Скидки для друзей из социальных сетей!
Для жителей районов Савеловский, Беговой, Аэропорт, Хорошевский
В этом месяце жителям районов Савеловский, Беговой, Аэропорт, Хорошевский» предоставляется скидка 5% на ВСЕ мед.
Гуляев Сергей Викторович
Врач-ревматолог, терапевт, нефролог
Кандидат медицинских наук
Нефропатией в медицине обозначается поражение почек, лишающее их основной фильтрационной функции в значительной, а при отсутствии своевременного лечения, и в полной степени. Нефропатия – одна из основных причин почечной недостаточности.
Причины и симптомы нефропатии
Нефропатию может вызывать ряд заболеваний, прежде всего, сахарный диабет, эндокринные расстройства, токсические отравления, онкологические заболевания и т.д.
Возникнув на фоне какого-либо заболевания или вследствие того или иного негативного воздействия на здоровье человека, нефропатия может развиваться довольно медленно, первое время не проявляя себя особыми симптомами.
Затем появляются слабость, одышка и утомляемость, головные боли, боли в поясничной области. Человек начинает чаще испытывать жажду.
При дальнейшем развитии нефропатии начинают появляться отёки, возникают проблемы с давлением. Возникает угроза появления хронической почечной недостаточности.
Кроме того, на фоне нефропатии возрастает риск воспалительных заболеваний почек – пиелонефритов.
Консультация нефролога в МедикСити
Консультация нефролога в МедикСити
Консультация нефролога в МедикСити
Диагностика и лечение нефропатии
Чтобы избежать негативных последствий развития нефропатии, необходимо своевременно обращаться к врачу. В тех случаях, когда нефропатия возникает на фоне диабетических или онкологических заболеваний, её появление могут выявить при регулярных обследованиях на основании анализов крови и мочи. Признаками нефропатии являются протеинурия (белок в моче), увеличение плотности мочи и др.
Что же касается тех, кто подвергается риску развития нефропатии вследствие токсических отравлений, радиационного облучения и т.д., то им необходимо помнить о риске возникновения подобных проблем и своевременно обследоваться на предмет выявления возможных негативных последствий.
Беременные женщины также должны следить за своим состоянием – нефропатия может развиться вследствие сильного токсикоза.
Лечение нефропатии осуществляется, как правило, медикаментозным путем в условиях стационара.
Основной задачей при этом является купирование развития почечной недостаточности.
При своевременной медицинской помощи нефропатия полностью излечима, и функции почек могут быть восстановлены.
Важно учитывать, что наиболее эффективным противодействием развитию нефропатии является устранение вызвавших её причин, либо их должная профилактика.
Всё это требует внимания высокопрофессиональных опытных специалистов.
В клинике «МедикСити» к вашим услугам опытные врачи-терапевты, врачи-нефрологи, врачи-иммунологи и другие специалисты, в распоряжении которых первоклассная, оснащённая самым современным оборудованием лечебно-диагностическая база, уникальные методики диагностики и лечения заболеваний урологических, нефрологических и других профилей.
Дисметаболическая нефропатия
Дисметаболические нефропатии – группа заболеваний, которые характеризуются поражением почек вследствие нарушения обмена веществ.
В зависимости от причины развития выделяют первичные и вторичные дисметаболические нефропатии.
Первичные являются наследственно обусловленными заболеваниями, характеризуются прогрессирующим течением, ранним развитиеммочекаменной болезниихронической почечной недостаточности.
Вторичные дисметаболические нефропатии могут быть связаны с повышенным поступлением определенных веществ в организм, нарушением их обмена в связи с поражением других органов и систем (например желудочно-кишечного тракта), лекарственной терапией и др.
Подавляющее большинство дисметаболических нефропатий связаны с нарушением обмена кальция (от 70 до 90%), около 85–90% из них – с избытком солей щавелевой кислоты, оксалатов (в виде оксалата кальция), остальные с избытком фосфатов (фосфаты кальция – 3–10%) или являются смешанными – оксалатно/фосфатно-уратными.
Первичные дисметаболические нефропатии встречаются редко.
Проявления дисметаболических нефропатий
Она наиболее часто встречается в детском возрасте. Ее возникновение может быть связано с нарушением как обмена кальция, так и обмена оксалатов (солей щавелевой кислоты).
Оксалаты попадают в организм с пищей или синтезируются самим организмом.
Причины образования оксалатов:
Это многофакторное заболевание. По данным различных авторов, доля наследственности в развитии оксалатной нефропатии составляет до 70–75%. Помимо генетических, большую роль играют внешние факторы: питание, стресс, экологическая нагрузка и др.
Первые проявления болезни могут развиться в любом возрасте, даже в период новорожденности.
Чаще всего они выявляются в 5–7 лет в виде обнаружения кристаллов оксалатов, небольшим содержанием белка, лейкоцитов и эритроцитов в общем анализе мочи. Характерно повышение удельной плотности мочи.
Общее развитие детей с оксалатной нефропатией, как правило, не страдает; но для них характерныаллергии,ожирение, вегетативно-сосудистая дистония со склонностью к понижению артериального давления (гипотонии), головными болями.
Заболевание обостряется в период полового созревания в возрасте 10–14 лет, что, по-видимому, связано с гормональной перестройкой.
Прогрессирование оксалатной нефропатии может привести к формированию мочекаменной болезни, развитию воспаления почек при наслоении бактериальной инфекции.
Фосфатная нефропатия встречается при заболеваниях, сопровождающихся нарушением фосфорного и кальциевого обмена. Основная причина фосфатурии – хроническая инфекция мочевой системы.
Часто фосфатно-кальциевая нефропатия сопровождает оксалатно-кальциевую, но при этом выражена в меньшей степени.
Нарушения обмена мочевой кислоты (уратная нефропатия)
За сутки в организме образуется 570–1000 мг мочевой кислоты, одна треть количества которой секретируется в кишечник и разрушается там бактериями.
Остальные две трети фильтруются в почках, большая часть всасывается обратно, и только 6–12% от профильтровавшегося количества выделяется с мочой.
Первичные уратные нефропатии обусловлены наследственными нарушениями обмена мочевой кислоты.
Вторичные возникают как осложнения других заболеваний (эритремии,миеломной болезни, хронической гемолитической анемии и др.), являются следствием применения некоторых препаратов (тиазидовых диуретиков, цитостатиков, салицилатов, циклоспорина А и др.) или нарушения функции канальцев почек и физико-химических свойств мочи (при воспалении почек, например).
Кристаллы уратов откладываются в ткани почек – это приводит к развитию воспаления и снижению почечных функций.
Первые признаки заболевания могут выявляться в раннем возрасте, хотя в большинстве случаев наблюдается длительное скрытое течение процесса.
А в общем анализе мочи обнаруживают ураты, небольшое количество белка и эритроцитов. При наличии большого количества уратов моча приобретает кирпичный цвет.
Нарушения обмена цистина
Цистин является продуктом обмена аминокислоты метионина.Можно выделить две основные причины повышения концентрации цистина в моче:
Накопление цистина в клетках происходит в результате генетического дефекта фермента цистинредуктазы. Это нарушение обмена носит системный характер и называется цистинозом.
Внутриклеточное и внеклеточное накопление кристаллов цистина выявляется не только в канальцах и интерстиции почки, но и в печени, селезенке, лимфоузлах, костном мозге, клетках периферической крови, нервной и мышечной ткани, других органах.
Нарушение обратного всасывания цистина в канальцах почек наблюдается вследствие генетически обусловленного дефекта транспорта через клеточную стенку для аминокислот – цистина, аргинина, лизина и орнитина.
По мере прогрессирования заболевания определяются признаки мочекаменной болезни, а при присоединении инфекции – воспаление почек.
Диагностика
Лабораторно-инструментальная диагностика дисметаболической нефропатии основывается на
Выявление кристаллов солей только в общих анализах мочи не является основанием для постановки диагноза дисметаболической нефропатии. Следует иметь в виду, что выделение кристаллов с мочой у детей часто бывает преходящим и оказывается не связанным с нарушением обмена веществ.
Для подтверждения диагноза дисметаболической нефропатии при выявлении кристаллов солей в общем анализе мочи проводится биохимическое исследование мочи.
Тест на кальцифилаксию позволяет выявить нарушения клеточного обмена кальция. Тест на перекиси в моче отражает активность процессов перекисного окисления клеточных мембран.
Изменения, выявляемые при УЗИ почек, как правило, мало специфичны. Возможно выявление в почке микрокамешков или включений.
Лечение дисметаболических нефропатий
Лечение любой дисметаболической нефропатии можно свести к четырем основным принципам:
Прием большого количества жидкости является универсальным способом лечения любой дисметаболической нефропатии, так как способствует уменьшению концентрации растворимых веществ в моче.
Одной из целей лечения является увеличение ночного объема мочеиспускания, что достигается приемом жидкости перед сном. Предпочтение следует отдавать простой или минеральной воде.
Диета позволяет в значительной степени снизить солевую нагрузку на почки.
Специфическая терапия должна быть направлена на предупреждение кристаллообразования, выведение солей, нормализацию обменных процессов.
Лечение оксалатной нефропатии
Рекомендации по питанию
Лекарственная терапия включает мембранотропные препараты и антиоксиданты. Лечение должно быть длительным.
В качестве мембраностабилизаторов используются димефосфон и ксидифон.
Димефосфон применяется в дозе 1 мл 15% раствора на каждые 5 кг веса, 3 приема в сутки. Курс – 1 месяц, 3 раза в год.
Ксидифон предупреждает отложение нерастворимых солей кальция. Назначается в дозе 10 мг/кг/сут. 2% раствора в 3 приема. Курс – 1 месяц, 2 раза в год.
Высокую эффективность имеет цистон, особенно при кристаллурии. Цистон назначается в дозе 1–2 таблетки 2–3 раза в день курсом от 3 до 6 месяцев.
Помимо этого, назначается окись магния, особенно при повышенном содержании оксалатов, в дозе 0,15–0,2 г/сут.
Лечение уратной нефропатии
Для поддержания оптимальной кислотности мочи можно использовать цитратные смеси (уралит-У, блемарен, магурлит, солимок и др.).
При уратной нефропатии важно уменьшить концентрацию мочевой кислоты. Для этого используются средства, снижающие синтез мочевой кислоты – аллопуринол, никотинамид.
Применение в педиатрии аллопуринола ограничено из-за возможных осложнений со стороны кожи, печени, крови.
Под строгим контролем аллопуринол назначают в дозе 0,2–0,3 г/сут. в 2–3 приема в течение 2–3 недель, затем доза снижается. Длительность общего курса – до 6 месяцев.
Никотинамид является более слабым препаратом, чем аллопуринол, но лучше переносится; назначается в дозе 0,005–0,025 г 2–3 раза в сутки по 1–2 месяца повторными курсами.
Мочевую кислоту выводят также оротовая кислота, цистон, этамид, цистенал, фитолизин и др.
Лечение фосфатной нефропатии
Лечение при фосфатной нефропатии должно быть направлено на подкисление мочи (минеральные воды – нарзан, арзни, дзау-суар и др.; препараты – цистенал, аскорбиновая кислота, метионин).
Назначается диета с ограничением продуктов, богатых фосфором (сыр, печень, икра, курица, бобовые, шоколад и др.).
Лечение цистиноза
Лечение цистиноза и цистинурии включает диету, высокожидкостный режим и медикаментозную терапию, направленную на подщелачивание мочи и повышение растворимости цистина.
Цель диетотерапии – предотвратить избыточное поступление в организм ребенка предшественника цистина – метионина и других серосодержащих кислот.
Для этого также исключают (или резко ограничивают) из рациона питания ребенка богатые метионином и серосодержащими аминокислотами продукты – творог, рыбу, яйца, мясо и др.
Поскольку метионин необходим организму ребенка для роста, длительное применение строгой диеты невозможно, поэтому через 4 недели от начала диетотерапии рацион ребенка расширяется и приближается к обычному, но характеризуется строгим исключением рыбы, творога и яиц.
Количество жидкости должно быть не менее 2 л/сут., особенно важно принимать жидкость перед сном.
Для подщелачивания мочи используется цитратная смесь, растворы гидрокарбоната натрия, блемарен, щелочные минеральные воды.
Для повышения растворимости цистина и предупреждения кристаллизации назначается пеницилламин. Он обладает некоторой токсичностью, поэтому в начале терапии назначаются невысокие дозы препарата – 10 мг/кг/сут. в 4–5 приемов, далее доза увеличивается в течение недели до 30 мг/кг/сут., а при цистинозе – до 50 мг/кг/сут.
Лечение пеницилламином должно проводиться под контролем содержания цистина в лейкоцитах и/или цианиднитропруссидного теста (проба на цистин в моче, где концентрация цистина должна составлять до 150–200 мг/л). При достижении этих показателей доза пеницилламина снижается до 10–12 мг/кг/сут.
Лечение пеницилламином проводится длительно, годами. Поскольку пеницилламин инактивирует пиридоксин, параллельно назначается витамин В6 (пиридоксин) в дозе 1–3 мг/кг/сут. в течение 2–3 месяцев с повторными курсами.
Для стабилизации мембран почечных канальцев назначаются витамин А (6600 МЕ/сут) и витамин Е (токоферол, 1 капля на 1 год жизни 5% раствора в сутки) в течение 4–5 недель с повторными курсами.
Имеются данные о положительном эффекте применения вместо пеницилламина менее токсичного его аналога – купренила в уменьшенной дозе в сочетании с ксидифоном и другими мембраностабилизаторами.
Антибактериальная терапия показана при присоединении инфекции.
При цистинозе успешно используется трансплантация почки, которая проводится до развития терминальной стадии хронической почечной недостаточности. Трансплантация почки позволяет значительно увеличить срок жизни больных – до 15–19 лет, однако отложение кристаллов цистина наблюдается и в трансплантате, что в конечном итоге приводит к поражению и пересаженной почки.
Прогноз
Прогноз при дисметаболической нефропатии в целом благоприятен.
В большинстве случаев при соответствующем режиме, диете и лекарственной терапии удается добиться стойкой нормализации соответствующих показателей в моче.
В отсутствие лечения или при его неэффективности наиболее естественным исходом дисметаболической нефропатии является мочекаменная болезнь и воспаление почек.
Самым частым осложнением дисметаболической нефропатии является развитие инфекции мочевой системы, в первую очередь пиелонефрии
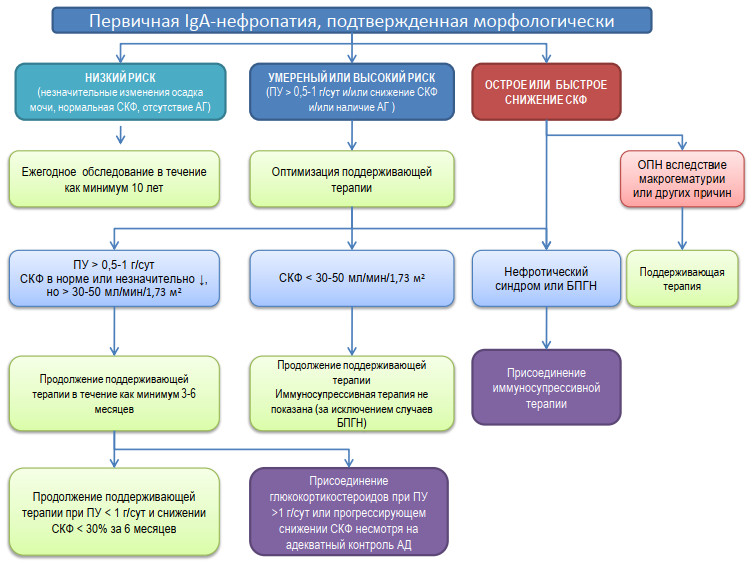
Клинические рекомендации по диагностике и лечению IgA-нефропатии
«Утверждено»
18 декабря 2014 г.
Рабочая группа
Шилов Е.М. Вице-президент НОНР, главный нефролог РФ, зав. кафедрой нефрологии и гемодиализа ИПО ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Министерства здравоохранения РФ, д.м.н., профессор
Бобкова И.Н. Зав. НИО нефрологии НИЦ, профессор кафедры нефрологии и гемодиализа ИПО ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Министерства здравоохранения РФ, д.м.н., ответственный секретарь НОНР
Колина И.Б. Старший научный сотрудник НИО нефрологии НИЦ ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Министерства здравоохранения РФ, к.м.н.
Камышова Е.С. Старший научный сотрудник НИО нефрологии НИЦ ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Министерства здравоохранения РФ, к.м.н.
АННОТАЦИЯ
Представленные рекомендации обобщают принятые в мире подходы к диагностике и лечению одного из наиболее распространенных видов гломерулонефрита – IgA-нефропатии. Они cоставлены в соответствии с современными международными [1] и отечественными [2] рекомендациями по лечению гломерулонефритов, основанными на результатах систематических обзоров и мета-анализов релевантных клинических исследований, а также накопленном на сегодняшний отечественном опыте адаптации международных рекомендаций к условиям Российского здравоохранения.
Данные Рекомендации не следует рассматривать в качестве стандарта оказания медицинской помощи, поскольку в существующей клинической практике объем диагностики и лечения определяется индивидуальными особенностями пациентов, доступностью ра зличных лекарственных средств и спецификой конкретного лечебного учреждения. За уместность применения данных Рекомендаций в конкретной ситуации несет ответственность использующий их врач.
ОЦЕНКА СИЛЫ РЕКОМЕНДАЦИЙ И УРОВНЯ ИХ ДОКАЗАТЕЛЬНОСТИ
Для рекомендаций сила указана как уровень 1, 2 или «нет степени» (табл.1), качество доказательной базы обозначено как А, В, С (табл.2).