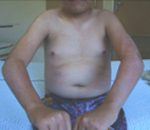
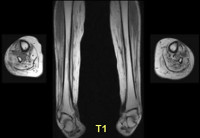
воспалительная миопатия что это
Идиопатические воспалительные миопатии
Общая информация
Краткое описание
Общероссийская общественная организация Ассоциация ревматологов России
Федеральные клинические рекомендации по диагностике и лечению идиопатических воспалительных миопатий
Идиопатические воспалительные миопатии — группа хронических заболеваний, неизвестной этиологии, основным проявлением которых является симметричная мышечная слабость проксимальных отделов конечностей, связанная с воспалением поперечно-полосатой мускулатуры. К ним относятся полимиозит (ПМ), дерматомиозит (ДМ), ювенильный дерматомиозит (ЮДМ); миозит, сочетающийся с системными заболеваниями соединительной ткани (СЗСТ) (перекрестный синдром); миозит, сочетающийся с опухолями; миозит с внутриклеточными включениями и некоторые другие, более редкие заболевания.
Код по МКБ-10:
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
1. Первичный идиопатический полимиозит (ПМ)
2. Первичный идиопатический дерматомиозит (ДМ)
3. Миозит, ассоциированный с другими системными СЗСТ
4. Ювенильный дерматомиозит (ЮДМ)
5. Миозит, сочетающийся со злокачественными опухолями
6. Миозит с включениями (inclusion-body myositis)
7. Гранулематозный миозит
8. Эозинофильный миозит
9. Миозит при васкулитах
10. Орбитальный миозит (глазных мышц)
11. Фокальный (узелковый) миозит
12. Оссифицирующий миозит
Эпидемиология
варьирует в различных популяциях. Согласно эпидемиологическим исследованиям, показатели заболеваемости варьирую от 2,18 до 7,7 случаев в год на миллион населения кавказоидов.
ДМ (реже ПМ), ассоциирующиеся с опухолями, составляют приблизительно 20% всех случаев воспалительных миопатий. Опухоли могут развиваться до появления признаков идиопатического воспалительного миозита, одновременно с ними или после их появления. Частота злокачественных новообразований при ПМ/ДМ в 12 раз выше, чем в популяции. Опухоли могут развиваться до появления признаков ИВМ, одновременно с ними или после их появления. На фоне злокачественных новообразований чаще развивается ДМ, чем ПМ. Соотношение мужчин и женщин составляет 1:1
Диагностика
Диагностика ПМ/ДМ основывается, главным образом, на данных клинического, анамнестичекого обследования, мышечной биопсии, а также, результатах лабораторного и электромиографического (и-ЭМГ) исследования.
Воспалительная миопатия может быть заподозрена у пациентов с симметричной проксимальной мышечной слабостью в сочетании с кожной сыпью или без кожной сыпи.
Диагностические критерии ПМ/ДМ, АСС и миозита с включениями
| Классический ПМ/ДМ | АСС | Миозит с включениями |
| Bohan, Peter 1975 | (предварительные критерии) Solomon, 2011 | Askanas R.C., Di Mauro 1995 [7] |
| 1. Симметричная проксимальная слабость мышц плечевого и тазового пояса, нарастающая в течение от нескольких недель до нескольких месяцев 2. Характерные кожные изменения 3. первично-мышечные изменения по И-ЭМГ 4. Гистологические изменения (некроз и воспалительная инфильтрация мышечных волокон) 5. Повышение уровня «мышечных» ферментов КФК, миоглобина, альдолазы, ЛДГ, АСТ, АЛТ Достоверный ПМ =4 критерия п.1-4. ДостоверныйДМ=4 критерия, включая п.5. Вероятный ПМ.= 3 критерия п.1-4 Вероятный ДМ= 3 критерия, включая п.5. Возможный ПМ=2 критерия п1-4. Возможный ДМ=2 критерия, включая п.5. | Большие критерии: 1. ИПЛ, не связанное с влиянием окружающей среды, профессиональной деятельностью, приемом лекарств 2. Полимиозит или дерматомиозит, согласно критериям Bohan и Peter |
Малые критерии:
1. Артриты
2. Феномен Рейно.
3. «Рука механика»
2. Лабораторные: незначительное повышение КФК;
3. Морфологические: инвазия мононуклеарными воспалительными клетками ненекротизированных мышечных волокон, вакуолизированные мышечные волокна или внутриклеточные депозиты амилоида или 15-18 нмтубулофиламенты на электронной микроскопии;
4. Электромиографические: признаки воспалительной миопатии, но возможно наличие увеличенных по неврогенному типу потенциалов
Лабораторно- инструментальные методы исследования
Увеличение КФК, АЛТ, АСТ, ЛДГ.
Аутоантитела обнаруживаются в сыворотке пациентов 50% ПМ/ДМ. Присутствие миозит-ассоциированных антител наблюдается и при других ревматических заболеваниях. К ним относятся: антинуклеарные антитела (АНА), анти-U1 рибонуклеопротеидные (анти-U1-RNP) антитела, которые при ПМ/ДМ обнаруживаются в 52%, 12% и 11%, соответственно. Anti-PM/Scl антитела определяются у около 8% пациентов с заболеванием, представленном фенотипическими чертами полимиозита и системной склеродермии.
Миозит-специфические антитела выявляются только при ИВМ и маркеруют клинические фенотипы. К ним относятся анти-Мi-2, Anti-SRP и др. Позитивность по антисинтетазным антителам (анти-Jо-1, антитела PL-7, анти-PL-12, анти- KS, анти-OJ, анти-EJ, анти-Zo, антитела к тирозил – т-РНК – синтетазе) и сопряжена с симтомокомплексом, называемым АСС.
И-ЭМГ –выявление локализацию поражения, определение степени выраженности нарушенных функций, стадии и характера патологического процесса. Является, также, необходимым методом для контроля за эффективностью терапии.
Методы оценки мышечной силы.
Мануальное тестирование силы проксимальных и аксиальных мышц проводится согласно рекомендациям IMACS и оценивается по 10-и бальной шкале:
| баллы | Выполняемые движения |
| Нет движения | |
| 0 | Нет никакого сокращения мышцы |
| Движение в горизонтальной плоскости | |
| 1 | Частичный объем движения в горизонтальной плоскости |
| 2 | Полный объем движения в горизонтальной плоскости |
| Движение против гравитации | |
| 3 | Частичное движение против гравитации |
| 4 | Полное движение с постепенным непроизвольным опусканием конечности |
| 5 | Больной удерживает позицию без постороннего давления |
| 6 | Больной удерживает позицию против легкого давления |
| 7 | Больной удерживает позицию при давлении врача от легко до умеренного |
| 8 | Больной удерживает конечность при умеренном давлении врача |
| 9 | Больной удерживает позицию при давлении врача от умеренного до сильного |
| 10 | Больной удерживает позицию против сильного давления врача |
Дифференциальный диагноз
Алгоритм диагностического поиска и дифференциальный диагноз
Патологические состояния, клинически проявляющиеся болью в мышцах или мышечной слабостью, могут быть следствием широкого спектра различных нервно-мышечных заболеваний, в которых имеет место как повреждение непосредственно мышечной ткани, так и нервной системы или нервно-мышечного синапса.
Алгоритм диагностического поиска и дифференциальный диагноз у пациентов с мышечной слабостью (не получающих ГК):
Лечение
Лечение ПМ/ДМ
Основные цели фармакотерапии ПМ/ДМ
· достижение полного клинического ответа (отсутствия клинико-лабораторной активности в течение, не менее чем 6 месяцев на фоне терапии) или ремиссии (отсутствия клинико-лабораторной активности в течение, не менее чем 6 месяцев на фоне отмены терапии) (уровень доказательности В),
· снижение риска комарбидных инфекций ГК) (уровень доказательности С)
· выявление и своевременное лечение пациентов с наибольшим риском ИПЛ
Общие рекомендации по лечению
· Лечение пациентов ПМ/ДМ должно проводиться врачами-ревматологами.
· В случае наличия ИПЛ с ФА при АСС – с привлечением пульмонологов и основываться на тесном взаимодействии врача и пациента
· Следует рекомендовать пациентам избегать факторов, которые могут спровоцировать обострение болезни: отказаться от пребывания на солнце, от курения, от контактов и инфекционными больными, избегать физических и психо-эмоциональных перегрузок.
· Следует рекомендовать пациентам исключить факторы, повышающие риск развития побочных эффектов терапии ГК: не употреблять в пищу сладкие продукты, включая мед и сладкие фрукты, повышающие риск развития стероидного сахарного диабета, также, исключение острой пищи, применение гастропротекторов с целью предотвращения язвенных осложнений (уровень доказательности С)
· Все пациенты нуждаются в активной профилактике и лечении глюкокортикоидного остеопороза. Подбор антиостеопоретической терапии зависит от результатов денситометрического исследования и оценки дополнительных факторов риска остеопороза (менопауза, эндокринные заболевания). В зависимости от исходных данных минеральной плотности костной ткани назначаются препараты кальция в сочетании с витамином Д, или эти же препараты в сочетании с бисфосфанатами.
· У пациентов ПМ/ДМ следует избегать внутримышечных инъекций, проведение которых, затрагивая мышечную ткань, может способствовать как формированию постинъекционных кальцинатов, так быть причиной ложноположительных результатов уровня креатинфосфокиназы (КФК).
Пульс-терапия ГК у взрослых пациентов не является основополагающей при ПМ/ДМ и не служит поводом для применения меньших (не адекватных) доз ГК назначаемых внутрь, как в острый период болезни, так и при ее обострении.
Потенциальные показания к подключению иммуносупрессивной терапии
· Принадлежность больных к клинико-иммунологическим подтипам ПМ/ДМ, особенностью которых является заведомо «плохой ответ» на терапию ГК: АСС c ФА, у пациентов антител к SRP
· Язвенно-некротический васкулит
· Обострение заболевания при снижении дозы ГК
· Стероидрезистентность у больных, ране получавших неадекватно малые дозы ГК
· Неэффективность ГК в течение 3-х месяцев
· Тяжелые побочные эффекты ГК, лимитирующие назначение адекватной дозы ГК (неконтролируемые сахарный диабет или артериальная гипертензия, острая язва желудка, множественные остеопоретические переломы)
Дисфагия
· Дисфагия является фактором риска аспирационной пневмонии, течение и терапия которой осложняется иммуноскомпроментированностью пациентов, связанной с терапией высокими дозами ГК и цитостатиков.
· Рекомендовано проведение пульс-терапии ГК (метипред 1000мг) N 3 в сочетании с пероральным приемом ГК в адекватной дозе.
· Тяжелая дисфагия является потенциальным показанием ВВИГ.
Наличие дисфагии у больных ПМ/ДМ служит поводом для проведения более активного онкопоиска (уровень доказательности Д).
Язвенно-некротический васкулит
Наличие язвенно-некротического васкулита является показанием для проведения пульс-терапии циклофосфамидом в дозе 600-800-1000 мг в месяц в сочетании метилпреднизолоном 500-1000мг.
Кожный синдром при ДМ в сочетании с проксимальной мышечной слабостью отражает активность болезни и, как правило, контролируется ГК в адекватных дозах в острый период болезни.
При резистентном кожном синдроме, сохраняющемся на фоне восстановления мышечной силы, рекомендуется применение антималярийных препаратов (гидроксихлорохин по 200–400 мг/сут), ММФ, топических стероидов.
Наличие резистентного кожного синдрома и/или язвенно-некротического васкулита у больных ПМ/ДМ служит поводом для проведения более активного онкопоиска (уровень доказательности С).
Лихорадка или субфебрилитет встречаются редко, главным образом при АСС с острым началам болезни.
· Контролируется ГК и не требует дополнительной терапии (уровень доказательности В).
При появлении субфебрилитета (или лихорадки) у пациентов на фоне лечения ГК в период клинико-лабораторной положительной динамики – исключение присоединения сопутствующей инфекции. Необходимо учитывать атипизм течения инфекционных осложнений на фоне иммуносупрессивной терапии.
Поражение суставов
· Наличие артрита при ПМ/ДМ может присутствовать в начале болезни. Артриты входят в состав симптомокомплекса АСС, хорошо контролируются ГК и не требуют дополнительного лечения.
· Сгибательные контрактуры, как правило, локтевых, реже коленных суставов, развиваются в острый период ПМ/ДМ и обусловлены воспалительным поражением мышечной ткани, а не непосредственным поражением суставов. Дополнительного медикаментозного лечения не требуется (уровень доказательности С).
Кальциноз мягких тканей
· Кальциноз мягких тканей наиболее часто присутствует (и более агрессивен) при ЮДМ
· Появление множественных кальцинатов, как правило, сопутствует острому течению ПМ/ДМ. Кальцинаты сохраняются на фоне снижения активности болезни, даже при достижении клинико-лабораторной ремиссии и наиболее выражении при ЮДМ.
· При ЮДМ, с целью снижения риска развития кальциноза и его распространенности применяется пульс-терапия ГК в дозе 1-2 мг/кг/сут.
· Хирургическое лечение малоэффективно, поскольку повышает риск присоединения вторичной инфекции и может спровоцировать появление новых кальцинатов.
· В качестве медикаментозной терапии применяютт бисфосфонаты (ксидифон, фосамакс, фосаванс и др.), однако полного контроля над процессом гетеротопического кальцийобразования не достигается.
· Для лечения кальциноза применяется, также динатриевая соль этилендиаминотетрауксусной кислоты (Na2ЭДТА), образующей комплексные соединения с различными катионами, в т.ч.с ионами Са 2+ и способствует выделению их с мочой.
· Имеются данные об эффективном предотвращении прогрессирования кальциноза при применении ВВИГ в течение 2 дней каждый месяц в сочетании с метилпреднизолоном (уровень доказательности С).
Традиционные иммуносупрессивные препараты, применяемые в лечении ПМ/ДМ
· Метотрексат по 7,5–25 мг/нед внутрь или внутривенно (при недостаточной эффективности или плохой переносимости перорального приема препарата, особенно в высоких дозах).
· Азатиоприн по 2–3 мг/кг/сут (100–200 мг/сут)
· Циклоспорин А по 2,5–5.,0 мг/кг/cутки назначают пациентам с резистентными к ГК формами заболевания, в т.ч. при хроническом течении болезни, связанной с неадекватно малой инициальной дозой ГК (уровень доказательности С).
· ММФ. Имеются данные об эффективности ММФ при ИПЛ и резистентном кожном синдроме. Прием начинают с дозы 1000 мг/сут (в 2 приема), постепенно титруя дозу до 2000 мг/сут под контролем показателей общего и биохимического анализов крови (уровень доказательности С).
Общие принципы лечения иммуносупрессивными препаратами:
— титрование дозы: назначение с небольшой дозы и постепенное ее повышение под контролем переносимости.
— контроль переносимости: оценка уровня гемоглобина, числа лейкоцитов, тромбоцитов, азота мочевины, креатинина, активности АСТ, АЛТ. При уменьшении числа лейкоцитов менее 2,5х10 9 /л и/или тромбоцитов – менее 100 х 10 9 /л и повышении концентрации АСТ, АЛТ более чем в 3 раза от верхней границы нормы, лечение необходимо прекратить до устранения симптомов токсичности.
— при присоединении интеркурренотой инфекции, в т.ч. герпетической – временная отмена иммуносупрессивных препаратов до исчезновения ее признаков.
Применение ВВИГ 2 г/кг 1 раз в месяц в течение 3 месяцев является эффективным методом лечения ПМ/ДМ (особенно ЮДМ), резистентного к стандартной терапии. Потенциальным показанием для ВВИГ является тяжелая дисфагия. (уровень доказательности В)
Плазмаферез следует использовать главным образом у больных с тяжёлым, резистентным к другим метода лечения ПМ/ДМ в сочетании с ГК и цитотоксическими препаратами.
Новые направления терапии ПМ/ДМ. Биологические препараты
В настоящее время активно изучается роль и место биологической терапии в терапии ПМ/ДМ.
— Применение в терапии ПМ/ДМ ингибиторов фактора некроза опухоли α TNF-a (инфликсимаба) не принесло желаемых результатов: поскольку он не способен контролировать активность болезни, в том числе ИПЛ, а также, увеличивают риск оппортунистических инфекций [10, 44].
— Имеются данные об успешном применении этанерцепта в качестве стероидсберегающей терапии. (Уровень доказательности Д)
— Применение блокаторов ко-стимуляции Т-лимфоцитов (абатацепта) в сочетании с тиосульфат натрия при ЮДМ с язвенно-некротичнским васкулитом и прогрессирующим кальцинозом оказало положительный эффект в виде нарастания мышечной силы, восстановления целостности кожный покровов, снижения прогрессирования кальциноза, что позволило снизить поддерживающую дозу ГК. (Уровень доказательности Д)
— Особое место среди биологических препаратов, на сегодняшний день, применяемых при ПМ/ДМ, занимает использование анти В-клеточной терапии. Накоплен положительный опыт по применению РТМ у пациентов с тяжелым мышечным поражением и при АСС с СФА, резистентных к ГК и применяемой ранее традиционной цитостатической терапии (уровень доказательности Д)
Практически все авторы описывают высокую эффективность РТМ при ПМ/ДМ. Так, на фоне терапии РТМ (в сочетании с ГК) наблюдается положительная клинико-лабораторная динамика (уменьшение выраженности кожного синдрома, нарастание мышечной силы).
— В случае применения РТМ при АСС с СФА, позитивный эффект наблюдался более, чем у 70% больных в виде увеличения показателей функции внешнего дыхания: увеличения показателей ЖЕЛ и DLCO, а также уменьшения инфильтратов по КТ грудной клетки.
— Максимальный эффект развивался через 12 недель после первой инфузии и коррелировал со снижением CD 20 + В клеток.
Профилактика ГК- остеопороза
Препараты кальция в сочетание с витамином Д3, бисфосфанаты.
Профилактика язвенных осложнений
Гастропротекторы (миозпростол, ранитидин, омепразол).
Профилактика стероидного диабета
Строгое исключение потребления продуктов, содержащих глюкозу, в т.ч., сладких фруктов, соков и йогуртов.
Предосторожности: Исключение контакта с инфекционными больными – во избежание присоединения вторичной инфекции.
Избегание физических перегрузок (в острый период ЛФК противопоказана, только пассивные движения).
Информация
Источники и литература
Информация
Список сокращений:
Методология
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций является глубина публикаций вошедших в Кохрановскую библиотеку, базы данных EMBASE и MEDLINE. Глубина поиска составляла 10 лет.
Методы, использованные для оценки качества и глубины доказательств:
· Консенсус экспертов
· Оценка значимости в соответствии с рейтиноговой схемой
Рейтиноговая схема для оценки силы рекомендаций
| сила | описание |
| А | По меньшей мере, один метаанализ, систематический обзор, или РКИ напрямую примененные к целевой популяции и демонстрирующий устойчивость результатов |
| В | Группа доказательств, включающих результаты исследований, напрямую применимые к целевой популяции и демонстрирующих общую устойчивость результатов |
| С | Хорошо проведенные исследования случай-контроль или когортные исследования со средней вероятностью причинной взаимосвязи |
| D | Небольшие пилотные исследования, описание случаев, мнение экспертов |
Описание метода валидизации рекомендаций
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами по доступности для понимания врачей ревматологов, врачей первичного звена и участковых терапевтов, оценки их важности для повседневной практики.
Комментарии, полученные от экспертов систематизировались и обсуждались председателем и членами рабочей группы, регистрировались изменения каждого пункта рекомендаций. Предварительные рекомендации были представлены для дискуссии на Конференции ФГБУ НИИР РАМН, на совещании Экспертного Совета Ассоциации ревматологов России и выставлены для широкого обсуждения на сайте ФГБУ НИИР РАМН и АРР.
Рабочая группа
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключении, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок сведен к минимуму.
Основные рекомендации
Сила рекомендаций (А-D) приводятся при изложении текста рекомендаций.
Воспалительная миопатия
Воспалительная миопатия — воспалительный процесс, возникающий преимущественно в скелетных мышцах и приводящий к их дегенеративным изменениям. Воспалительная миопатия характеризуется мышечной слабостью, болями в мышцах, резким снижением объема активных движений, развитием контрактур, уплотнением и отечностью мышц. Из методов диагностики воспалительной миопатии наиболее информативно определение уровня КФК и миоглобина, электромиография и биопсия мышц. Лечение воспалительной миопатии осуществляется высокими дозами глюкокортикостероидов с последующей поддерживающей терапией. Однако достаточно часто встречаются резистентные к кортикостероидам формы заболевания.
МКБ-10
Общие сведения
Воспалительные миопатии представляют собой целую группу заболеваний, в которую входят как системные поражение мышечной ткани, так и локальные воспалительные процессы в отдельных мышцах. Воспалительная миопатия системного характера представлена дерматомиозитом, полимиозитом, эозинофильным миозитом, миозитом с включениями, ревматической полимиалгией и миопатиями при системных заболеваниях. Примером локальной воспалительной миопатии может быть миозит глазных мышц, псевдотромбофлебит мышц голени и др. Кроме того, воспалительная миопатия может наблюдаться при некоторых инфекционных заболеваниях.
Возраст пациентов, наиболее подверженных заболеваемости, различается в зависимости от вида воспалительной миопатии. Так, полимиозит обычно возникает у лиц старше 30 лет. Дерматомиозит наблюдается как у взрослых, так и в детском возрасте. А миозит с включениями чаще встречается после 40 лет и является наиболее распространенной формой воспалительной миопатии в пожилом возрасте.
Причины возникновения воспалительной миопатии
В некоторых случаях воспалительная миопатия напрямую связана с инфекционным процессом. Агентами, вызывающими инфекционно-воспалительно поражение мышц, могут быть вирусы (краснуха, грипп, ВИЧ-инфекция, энтеровирусы и пр.), бактерии (чаще стрептококковые инфекции), паразитарные инвазии (цистицеркоз, токсоплазмоз, трихинеллез). При этом заболевание классифицируется как инфекционная воспалительная миопатия.
В тех случаях, когда прямая связь миопатии с инфекцией не прослеживается, говорят об идиопатической миопатии. К ней относятся: миозит с включениями, полимиозит, дерматомиозит, миопатии при системных заболеваниях (системной красной волчанке, склеродермии, синдроме Шегрена, системных васкулитах, ревматоидном артрите). Наиболее распространенным как в неврологии, так и в ревматологии является мнение, что идиопатическая воспалительная миопатия имеет аутоиммунный механизм развития. Однако до сих пор не выделен антиген, который запускает лежащую в ее основе аутоиммунную реакцию. В отдельных случаях воспалительная миопатия имеет семейный характер, свидетельствующий о ее генетическом происхождении.
Симптомы воспалительной миопатии
Воспалительная миопатия клинически проявляется болями в мышцах, прогрессирующей мышечной слабостью и тугоподвижностью в пораженных отделах конечностей. Болевой синдром (миалгия) возникает не только в период двигательной активности, но и при прощупывании мышц, а иногда и в состоянии полного покоя. Мышечная слабость, как правило, начинает проявляться затруднением при удерживании предметов в руках. По мере ее прогрессирования для пациента становится невозможным поднять руку или ногу, сесть, встать. Воспалительная миопатия распространенного характера часто приводит к значительному сокращению объема активных движений, которые может выполнять больной, а иногда и к полной обездвиженности.
Воспалительная миопатия протекает с отеком и уплотнением пораженных мышц. В результате воспаления в них происходят атрофические изменения, развивается миофиброз — замещение мышечных волокон на соединительнотканные, возможен кальциноз. Образующиеся мышечные контрактуры приводят к тугоподвижности суставов. Зачастую воспалительная миопатия имеет длительное ремиттирующее течение. В некоторых случаях, чаще у детей, наблюдается полное выздоровление после перенесенного острого приступа воспалительной миопатии.
Наиболее тяжело воспалительная миопатия протекает при вовлечении в воспалительный процесс мышц гортани и дыхательной мускулатуры, что ведет к развитию миопатического пареза гортани и дыхательной недостаточности. Слабость дыхательных мышц приводит к снижению легочной вентиляции и возникновению застойной пневмонии. Слабость мышц глотки является причиной дисфагии (расстройств глотания), при которой возможно попадание пищи в дыхательные пути и возникновение аспирационной пневмонии. Если воспалительная миопатия распространяется на глазодвигательные мышцы, то возникает косоглазие и опущение верхнего века. Поражение мимических мышц приводит к маскообразному выражению лица. Системная воспалительная миопатия, например, дерматомиозит и полимиозит, может сопровождаться поражением сердечной мышцы с клиникой миокардита, кардиомиопатии и сердечной недостаточности.
Полимиозит проявляется типичным для воспалительной миопатии мышечным синдромом, который захватывает мышцы проксимальных отделов конечностей, в первую очередь плечевого и тазового пояса. В большинстве случаев наблюдается также поражение внутренних органов: ЖКТ (диарея, запор, кишечная непроходимость, язва желудка с перфорацией или желудочно-кишечным кровотечением), сердца и сосудов (артериальная гипотония, аритмия, кардиомиопатия и др), легких (очаговая или долевая пневмония). В 15% случаев эта воспалительная миопатия сопровождается суставным синдромом в виде артритов суставов кисти, реже — других суставов конечностей.
Дерматомиозит имеет сходную с полимиозитом клиническую картину. Отличительной чертой является наличие кожных проявлений: эритематозных пятен, участков гипо- и гиперпигментации, очагов гиперкератоза. Возможно поражение слизистых оболочек с развитием стоматита, гингивита, конъюнктивита.
Миозит с включениями характеризуется ранним поражением мускулатуры дистальных отделов рук: сгибателей пальцев и мышц предплечья. В ногах воспалительная миопатия распространяется как на дистальные, так и на проксимальные мышечные группы. Типично поражение разгибателей стопы и четырехглавой мышцы.
Диагностика воспалительной миопатии
К диагностике воспалительной миопатии помимо неврологов могут привлекаться ревматологи, кардиологи, пульмонологи, дерматологи, иммунологи и др. специалисты. К сожалению, на сегодняшний день воспалительная миопатия не имеет четких диагностических критериев. Определенное значение имеет обнаружение в биохимическом анализе крови повышения уровня креатинфосфокиназы (КФК), а также лактатдегидрогеназы и альдолазы, что свидетельствует о повреждении мышечной ткани. Зачастую воспалительная миопатия сопровождается повышением миоглобина. Однако уровень этих показателей не коррелирует с тяжестью клинических проявлений. По этой причине единственным достоверным критерием прогрессирования миопатии могут быть лишь результате исследования мышечной силы (эргометрии) в динамике. Следует также отметить, что повышение КФК и миоглобина наблюдается далеко не при всех видах воспалительной миопатии. Например, при миозите с включениями уровень КФК и миоглобина часто находится в пределах нормы.
Важное диагностическое значение имеют данные электромиографии. При дерматомиозите и полимиозите наблюдается снижение продолжительности и амплитуды потенциалов двигательных единиц, повышенная электровозбудимость. При миозите с включениями наряду с типичными для миопатии низкоамплитудными и кратковременными потенциалами отмечаются высокоамплитудные и длительные потенциалы, характеризующие нейрогенное поражение.
Уточнить характер поражения мышц и определить его распространенность позволяет биопсия мышц. Морфологическое исследование биоптата выявляет наличие воспалительных инфильтратов, атрофические изменения и некроз мышечных волокон, их замещение соединительной тканью.
Диагностика сопутствующих поражений внутренних органов осуществляется при помощи рентгенографии легких, ЭКГ, Эхо-КГ, гастроскопии, УЗИ органов брюшной полости.
Лечение воспалительной миопатии
Общепринятым методом лечения воспалительной миопатии является терапия глюкокортикостероидами. Суточная доза преднизолона составляет 80-100 мг. При достижении клинического эффекта лечения в виде увеличения мышечной силы производят постепенное снижение суточной дозы до поддерживающего уровня — 15 мг/сут. В тяжелых случаях воспалительная миопатия лечится пульс-терапией метилпреднизолоном. Сложности применения длительного лечения глюкокортикоидами состоит в их побочных эффектах, из-за которых подобная терапия противопоказана пациентам с язвенной болезнью и язвой желудка, артериальной гипертензией, остеопорозом, катарактой и глаукомой. Отсутствие увеличения мышечной силы в течение 3 месяцев с момента начала лечения кортикостероидами говорит о стероидной резистентности воспалительной миопатии.
Альтернативными препаратами в лечении воспалительной миопатии являются цитостатики (азатиоприн, метотрексат, циклоспорин, циклофосфамид). Они применяются вместо кортикостероидов при наличии стероидной резистентности или в комбинации с ними для уменьшения дозы глюкокортикостероидов во избежание их побочных эффектов.
Поскольку системная воспалительная миопатия обычно имеет аутоиммунный характер, то в ее лечении зачастую применяется плазмаферез, позволяющий снизить количество ЦИК в крови.