вобэнзим или креон что лучше при панкреатите
Современные возможности терапии хронического панкреатита
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатит
Хронический панкреатит — длительно протекающее воспалительное заболевание поджелудочной железы, проявляющееся необратимыми морфологическими изменениями, которые вызывают боль и/или стойкое снижение функции поджелудочной железы. При хроническом панкреатите морфологические изменения поджелудочной железы сохраняются после прекращения воздействия этиологического агента. В настоящее время распространенность хронического панкреатита, по данным аутопсий, составляет от 0,01 до 5,4%, в среднем — 0,3-0,4%, при этом за последние 40 лет заболеваемость выросла примерно в два раза, что связывают с тем, что население стало употреблять больше алкогольных напитков, а также с воздействием вредных факторов окружающей среды (см. диаграмму 1).
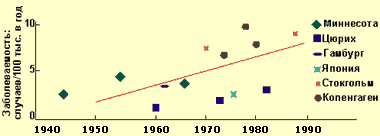 |
| Диаграмма 1. Заболеваемость ХП в 1945—1985 гг. (Worning H., 1990) |
В патогенезе хронического панкреатита важную роль играют несколько факторов. Одним из основных является обструкция главного панкреатического протока при конкрементах, воспалительном стенозе или опухолях. При алкогольном панкреатите повреждение поджелудочной железы связано с повышением содержания белка
в панкреатическом секрете, что приводит к возникновению белковых пробок и обструкции мелких протоков железы. Другим фактором, влияющим на патогенез алкогольного панкреатита, является изменение тонуса сфинктера Одди: его спазм вызывает внутрипротоковую гипертензию, а релаксация способствует рефлюксу дуоденального содержимого и внутрипротоковой активации панкреатических ферментов.
Разрушение экзокринной части поджелудочной железы вызывает прогрессирующее снижение секреции бикарбонатов и ферментов, однако клинические проявления нарушения переваривания пищи развиваются лишь при деструкции более 90% паренхимы органа. В первую очередь возникают проявления недостаточности липазы в виде нарушения всасывания жиров, жирорастворимых витаминов: A, D, E и K, что нечасто проявляется поражением костей, расстройствами свертывания крови. У 10–30% больных хроническим панкреатитом развивается сахарный диабет, обычно на поздних стадиях заболевания, нарушение толерантности в глюкозе наблюдается гораздо чаще. Для таких больных характерно развитие гипогликемических реакций на инсулин, недостаточное питание или злоупотребление алкоголем. Кетоацидоз развивается редко, что связано с одновременным снижением продукции инсулина и глюкагона.
Приступ хронического панкреатита проявляется иррадиирующими в спину болями в верхней половине живота, развивающимися после приема пищи, которые могут продолжаться в течение многих часов или нескольких дней. Нередко наблюдается тошнота, рвота, у 30–52% пациентов — снижение веса, у 16–33% — желтуха. Преходящая желтуха возникает вследствие отека железы при обострениях хронического панкреатита, постоянная — связана с обструкцией общего желчного протока вследствие фиброза головки поджелудочной железы. При разрывах протоков поджелудочной железы, на месте предыдущего некроза ткани происходит скопление секрета, что приводит к формированию псевдокист. Кисты могут быть бессимптомными или вызывать боли в верхней половине живота. При длительном течении заболевания, при уменьшении объема функционирующей паренхимы до 10% от нормы появляются признаки мальабсорбции (полифекалия, жирный стул, похудание).
В течении хронического панкреатита можно выделить несколько стадий (Lankisch P.G., Moessner Y.), умение различать которые важно для правильного подбора терапии. Так, на первой стадии заболевания клиническая симптоматика отсутствует: в этот период характерные для ХП изменения данных КТ или ЭРХПГ выявляются лишь при случайном обследовании.
На второй стадии возникают начальные проявления, характеризующиеся частыми эпизодами обострения ХП (которые могут быть ошибочно расценены как острый панкреатит). Заболевание видоизменяется от повторных приступов боли в животе до постоянных умеренных болей и похудания. С течением времени рецидивы становятся менее тяжелыми, но симптоматика сохраняется в периоды между приступами. На этой стадии может существенно ухудшаться качество жизни. Вторая стадия обычно продолжается на протяжении четырех—семи лет. Иногда заболевание быстро прогрессирует, развивается атрофия ПЖ, и нарушается функция органа.
У больных на третьей стадии постоянно присутствует симптоматика ХП, прежде всего — абдоминальная боль. Пациенты могут стать зависимыми от анальгетиков, значительно сокращают объем принимаемой пищи из-за опасения усиления боли. Появляются признаки экзокринной и эндокринной панкреатической недостаточности.
Особенность панкреатита на четвертой стадии — это атрофия ПЖ, развитие экзокринной и эндокринной недостаточности, что проявляется стеатореей, похуданием и сахарным диабетом. Снижается интенсивность боли, прекращаются острые приступы заболевания, могут развиваться тяжелые системные осложнения ХП и аденокарцинома поджелудочной железы.
Терапия панкреатита проводится по нескольким направлениям: отказ от употребления алкоголя; соблюдение диеты с низким содержанием жира (до 50–75 г/сут) и частым приемом небольших количеств пищи; купирование боли; ферментная заместительная терапия, борьба с витаминной недостаточностью; лечение эндокринных нарушений.
Лечение приступа хронического панкреатита, а также острого панкреатита проводиться по аналогичной схеме. Обязательные компоненты терапии: внутривенное введение растворов электролитов и коллоидов, голодная диета (полное голодание до двух дней) и анальгезия (например, меперидин). Рекомендуется введение свежезамороженной плазмы или альбумина. Диуретики не показаны большинству больных: олигурия разрешается при исчезновении гиповолемии и нормализации перфузии почек. Для облегчения рвоты, купирования пареза желудочно-кишечного тракта и уменьшения стимуляции поджелудочной железы может быть использована аспирация содержимого желудка через назогастральный зонд. Коагулопатия, возникающая при панкреатите, обычно требует назначения гепарина, свежей плазмы. В последние годы при остром панкреатите показана эффективность антагониста тромбоцит-активирующего фактора лексипафанта (60–100 мг/сут), однако его действие при хроническом панкреатите еще нуждается в уточнении.
Применение ингибиторов протеолитических ферментов (например, апротинина, габексата) является спорным. Исследования показывают, что при остром панкреатите не наблюдается дефицита ингибиторов протеаз, кроме того, проведенные клинические исследования не выявили преимуществ этих препаратов по сравнению с плацебо. Однако существуют данные, что габексат, низкомолекулярный ингибитор трипсина, эффективно используется для профилактики развития острого панкреатита, связанного с ЭРХПГ.
Ингибиторы секреции поджелудочной железы: глюкагон, соматостатин, кальцитонин, ингибиторы карбоангидразы, вазопрессин, изопреналин, также было предложено применять для лечения острого панкреатита, однако их эффективность к настоящему времени не получила достаточного подтверждения. Препараты пищеварительных ферментов можно использовать для лечения как в разгар заболевания с целью подавления панкреатической секреции, так и в период выздоровления, когда пациент снова получает возможность принимать пищу орально.
При билиарном обструктивном панкреатите должна быть проведена своевременная эндоскопическая декомпрессия желчных путей. Выполняется папиллосфинктеротомия, дилатация или стентирование панкреатического протока. Хирургическое лечение обструктивного панкреатита, безусловно, является основным методом, в то же время целесообразность проведения вмешательства в первые сутки после развития тяжелого приступа должна быть признана спорной. После стихания остроты воспаления целесообразно проведение холецистэктомии.
Схему длительной терапии при хроническом панкреатите можно разделить на две основные части, в соответствии с ведущими клиническими синдромами (см. диаграмму 2).
Боль могут облегчить большие дозы панкреатических ферментов. Попадание ферментов поджелудочной железы (прежде всего — трипсина) в двенадцатиперстную кишку по механизму отрицательной обратной связи вызывает снижение панкреатической секреции, снижение внутрипротокового давления и уменьшает боль. Традиционно для этой цели использовались порошок или таблетированные препараты панкреатина.
Если болевой синдром резистентен к терапии, при расширении главного протока более 8 мм, у 70–80% пациентов облегчение может принести латеральная панкреатоеюностомия. В случаях, когда панкреатический проток не расширен, показано проведение дистальной панкреатэктомии (при преимущественном поражении хвоста железы) или операция Уиппла (Whipple) (при поражении в основном головки железы). Альтернативой операции является чрезкожная денервация солнечного сплетения введением алкоголя, однако эффект этой процедуры сохраняется лишь в течение нескольких месяцев. Весьма перспективно эндоскопическое лечение под контролем эндоскопического УЗИ (дренирование псевдокист, невролиз солнечного сплетения).
Показаниями для заместительной терапии экзокринной панкреатической недостаточности являются исключительно клинические показатели: похудание, стеаторея, метеоризм. Классическая рекомендация, предусматривающая определение содержания жира в кале перед назначением лечения, в настоящее время потеряла свое значение из-за трудоемкости и низкой чувствительности данного метода. Для купирования внешнесекреторной панкреатической недостаточности используют различные препараты экстрактов поджелудочной железы (см. таблицу 1).
При выборе препарата для заместительной терапии следует учитывать следующие показатели:
Способность препарата активироваться только в щелочной среде — очень важное свойство, которое резко повышает эффективность ферментов; так, при использовании препарата, имеющего энтеросолюбильную оболочку, всасывание жиров повышается в среднем на 20% по сравнению с такой же дозой обычного средства. Однако при хроническом панкреатите происходит значительное снижение продукции бикарбонатов, что приводит к нарушению щелочной среды в двенадцатиперстной кишке. Это создает несколько проблем. Первая касается нарушения активации частиц ферментного препарата, покрытых энтеросолюбильной оболочкой. Вторая проблема заключается в том, что в кислой среде происходит преципитация желчных солей и нарушение эмульгации жира, что делает его малодоступным для расщепления липазой. Поэтому эффективность ферментной терапии (см. рисунок 1) может быть повышена благодаря одновременному назначению антацидов за 30 мин до и через 1 ч после еды или антисекреторных препаратов (Н2-блокаторы, омепразол), но необходимо помнить, что антациды, содержащие кальций или магний, ослабляют действие ферментных препаратов. Возможно использование препаратов, содержащих протеолитические ферменты растительного происхождения, которые сохраняют активность в гораздо более кислой среде, чем животные.
Значительное снижение качества жизни больного панкреатитом связано с такой проблемой, о которой обычно забывают, как стойкое вздутие живота. Нередко вздутие не купируется даже при приведении заместительной терапии высокими дозами ферментов. В этом случае к проводимой терапии необходимо добавить адсорбенты (симетикон, диметикон) или использовать комбинированные ферментные препараты, содержащие адсорбирующие вещества.
Разовая доза ферментов, которая рекомендуется для лечения внешнесекреторной панкреатической недостаточности, должна содержать не менее 20–40 тыс. ед. липазы. Обычно пациенту назначают две—четыре капсулы препарата (по 20—25 тыс. ед. липазы) при основных приемах пищи и по одной-две капсуле (по 8—10 тыс. ед. липазы) или таблетки панкреатина при употреблении небольшого количества пищи. При клинически выраженной панкреатической недостаточности обычно не удается полностью устранить стеаторею даже с помощью высоких доз препаратов, поэтому критериями адекватности подобранной дозы пищеварительных ферментов являются: прибавка веса, нормализация стула (менее трех раз в день), снижение вздутия живота.
Причины неэффективности заместительной терапии могут быть связаны как с неточной диагностикой заболевания, так и с неадекватным назначением терапии больному (см. рисунок 2).
Побочные эффекты ферментной терапии (см. рисунок 3) обычно не носят тяжелого характера, наиболее известный опасный побочный эффект — развитие фиброзирующей колопатии — возникает при длительном приеме очень высоких доз ферментов в виде микротаблеток: более 50 тыс. ед. липолитической активности на 1 кг веса тела в сутки.
Таким образом, терапия хронического панкреатита должна проводиться дифференцированно, в зависимости от ведущего клинического синдрома и стадии заболевания. Заболевание, которое удается обнаружить на первой стадии, как правило, не требует медикаментозной коррекции, в этом случае обычно достаточно изменения образа жизни и диетотерапии. Лечение ХП на второй стадии включает назначение таблетированного панкреатина, антисекреторных препаратов и спазмолитиков. Третья стадия обычно требует использования всего арсенала средств, которые имеются у врача для купирования панкреатической боли: микрогранулы панкреатина, антисекреторные препараты, октреотид, спазмолитики, мощные анальгетики, психотропные препараты. На последней, четвертой, стадии лечение основывается, прежде всего, на использовании микрогранул панкреатина в высокой дозе с целью проведения заместительной терапии.
По вопросам литературы обращайтесь в редакцию
А. В. Охлобыстин, кандидат медицинских наук
Э. Р. Буклис, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
Как выбрать пробиотики для кишечника: список препаратов
Правильное, сбалансированное содержание белков, жиров и углеводов является ключом к здоровью на долгие годы. Продукты не способны в полной мере обеспечить организм человека всем необходимым. Есть целый перечень лекарств, которые помогают держать себя в хорошей форме и не болеть от легкого дуновения ветра.
Предлагаем список лучших пробиотиков. Перед началом терапии рекомендуется проконсультироваться с врачом, чтобы исключить наличие противопоказаний и правильно рассчитать дозировку.
Полезные свойства
Пробиотики – живые микроорганизмы, которые могут принести пользу человеку. В большинстве случаев это бактерии, но могут быть и другие представители микробов (например, дрожжи). Пробиотики несут пользу для кишечника, нормализуя микрофлору и устраняя дисбактериоз.
Нормы и различные вариации
Пробиотики колонизируют кишечник полезными бактериями, противодействуют патогенной (вредной) флоре, вызывающей запор или диарею, повышают иммунитет.
Основную массу бактерий – пробиотиков можно разделить на 2 вида: лакто- и бифидобактерии. В каждом из них существует значительное количество подвидов. Они оказывают то или иное благотворное влияние на организм человека.
Отклонения от нормы
Чем отличаются пробиотики от пребиотиков?
Могут ли навредить пробиотики?
Пробиотики практически не имеют противопоказания. Не рекомендуется принимать при онкологических заболеваниях, поражении лимфатический и кровеносной системы, ВИЧ. С осторожностью рекомендуется принимать в период беременности и лактации. Маленьким детям допустимо давать только те препараты, которые не имеют возрастных ограничений.
Как выбрать пробиотики для кишечника?
Лучшие пробиотики для восстановления кишечника может посоветовать только врач. Должны быть учтены основные критерии: возраст пациента, состояние организма, характер дисфункций, противопоказания и пр. Самолечение может не дать должного результата и привести к развитию проблем со здоровьем.
В список препаратов включены лучшие пробиотики для восстановления микрофлоры кишечника. Рейтинг основан на эффективности, безопасности и соотношении цена-качество.
№1 – «Нормофлорин-Д» (Бифилюкс, Россия)
Биологически активная добавка разработана на основе лактобактерий и их метаболитов. Используется в комплексном лечении язвы двенадцатиперстной кишки и желудка, при ожирении и метаболическом синдроме. Назначается после антибактериальной терапии для восстановления нарушенного микробиоценоза.
Производитель: Бифилюкс, Россия
№2 – «Бифиформ» (Ferrosan, Дания)
Противодиарейный препарат регулирует равновесие микрофлоры кишечника. Содержит Bifidobacterium longum и Enterococcus faecium. МИБП-эубиотик назначается при непереносимости лактозы, для восстановления микрофлоры кишечника и для лечения хеликобактерной инфекции в составе комплексной терапии.
Производитель: Ferrosan [Ферросан], Дания
№3 – «Линекс» (Lek d. d., Словения)
Находится в первых рядах списка пробиотиков для кишечника. Основные активные компоненты этого препарата стимулируют изменение рН путем брожения лактозы. Это тормозит развитие патогенных и условно-патогенных микроорганизмов и создает благоприятные условия для пищеварительных ферментов.
Активные вещества, входящие в «Линекс» устойчивы к антибиотикам. Они оказывают влияние не только на нижние отделы кишечника, но и на верхние (этими свойствами обладают далеко не все пробиотики). Многокомпонентное средство, пригодно практически для всех пациентов, включая детей (даже тех, кто находится на искусственном питании).
Производитель: Lek d. d. [Лек д.д.], Словения
№4 – «Хилак Форте» (Merckle, Германия)
Комбинированный препарат для нормализации кислотности желудка в соответствии с физиологической нормой. Биологически восстанавливает микрофлору кишечника. Таким образом, создает неблагоприятную среду для жизнедеятельности патогенных и условно-патогенных бактерий.
Производитель: Merckle [Меркле], Германия
№5 – «Линекс Форте» (Sandoz, Словения)
Пробиотик регулирует равновесие микрофлоры кишечника. Разработан на основе молочнокислых живых бактерий, которые представляют собой составляющие естественной микрофлору. Широко используется при дисбактериоза, запорах и хеликобактериозе у детей и взрослых.
Производитель: Sandoz [Сандоз], Словения
№6 – «Бифидумбактерин» (Ланафарм, Россия)
Лучший пробиотик для восстановления микрофлоры, который устойчив ко многим лекарственным средствам и антибиотикам. «Бифидумбактерин» является антагонистом достаточно широкого спектра болезнетворных и условно болезнетворных микроорганизмов. Выпускается в форме ректальных суппозиториев и капсул.
Эффективность препарата обусловлена сильной концентрацией бифидобактерий. Быстро нормализует микрофлору кишечника, которая, будучи естественной, накапливает токсические вещества (как поступающие в организм извне, так и находящиеся в нем) и разлагает их на нетоксичные компоненты. Нельзя давать детям, страдающим непереносимостью молочных продуктов.
Производитель: Ланафарм, Россия
№7 – «Бак-Сет Форте» (Probiotics International, Великобритания)
Мульти-пробиотик нового поколения, который включает в состав 14 видов пробиотических живых бактерий. Они дополняют действие друг друга, устраняя проблемы с пищеварением у детей от 3-х летнего возраста и у взрослых. Усовершенствованная микрокапсулированная технология способствует сохранению полезных свойств бактерий на протяжении всего срока хранения препарата.
Производитель: Probiotics International [Пробиотикс Интернейшенал], Великобритания
№8 – «Бифиформ Баланс» (Pfizer, Россия)
Один из лучших пробиотиков для восстановления микрофлоры кишечника. разработан на основе лакто- и бифидобактерий. Биологически активная добавка к пище назначается для лечения дисбактериоза различной этиологии и поддерживает микрофлору кишечника. Способствует коррекции функциональных нарушений желудочно-кишечного тракта.
Производитель: Pfizer [Пфайзер], Россия
№9 – «Флорин Форте» (Партнер, Россия)
Лакто- и бифидобактерии, входящие в состав, принимают участие в процессах синтеза аскорбиновой кислоты, калия, витаминов группы В. В результате повышается устойчивость к агрессивным воздействиям окружающей среды. Также действующие компоненты участвуют в обменных процессах желчных кислот и пигментов. В их присутствии происходит синтез веществ, оказывающих антибактериальное действие. Также препарат повышает иммунную-реактивность человеческого организма.
Производитель: Партнер, Россия
№10 – «Бактериофаг» (Микроген НПО, Россия)
Стафилококковый раствор входит в список лучших пробиотиков для кишечника для взрослых и детей. Используется преимущественно в составе комплексной терапии с антибактериальными препаратами и другими лекарственными средствами.
Производитель: Микроген НПО, Россия
№11 – «Секстафаг» (Микроген НПО, Россия)
Завершает список препаратов пробиотиков для кишечника. Иммунобиологический препарат специфически лизирует бактерии стрептококков и стафилококков, протеи, кишечной и синегнойной палочки. Назначается при энтеральных и гнойно-воспалительных заболеваниях. При необходимости может быть использован в составе комплексной терапии.
Производитель: Микроген НПО, Россия
Пробиотические средства нормализуют процессы пищеварения, активируя перистальтику кишечника и восстанавливая микрофлору. Препараты способствуют синтезу полиаминов, укрепляют клеточный цитоскелет и регенерируют кишечный эпителий, повышая защитные функции организма. Они не только уменьшают газообразование, н и тормозят рост вредоносных микроорганизмов.
Какие пробиотики принимать в том или ином случае может посоветовать врач. Специалист отталкивается от показаний и общего состояния организма пациента, исключая развитие передозировки или побочных реакций.
Применение ферментных препаратов при нарушениях пищеварения у детей
Пищеварение является единым, целостным процессом благодаря тесным взаимосвязям между деятельностью различных отделов пищеварительного тракта. Нарушение функций одного из отделов желудочно-кишечного тракта, как правило, приводит к расстройству функции д
Пищеварение является единым, целостным процессом благодаря тесным взаимосвязям между деятельностью различных отделов пищеварительного тракта. Нарушение функций одного из отделов желудочно-кишечного тракта, как правило, приводит к расстройству функции других органов. В разных отделах пищеварительного тракта протекают различные процессы усвоения пищевых веществ. В желудке — расщепление белка, секреция внутреннего фактора, окисление ионов железа; у новорожденных — расщепление жиров (образование диглицеридов под действием желудочной липазы). В двенадцатиперстной кишке — поступление желчных кислот, эмульгация жира, расщепление триглицеридов, образование моно- и диглицеридов, расщепление крахмала и дисахаридов, расщепление белка, всасывание моносахаров, аминокислот, железа, кальция, цинка, магния. В тощей кишке — расщепление дисахаридов; всасывание моносахаров, моноглицеридов, желчных кислот, жирорастворимых витаминов, фолата, кальция, железа, магния, цинка, витамина В12. В подвздошной кишке — всасывание желчных солей, воды, натрия, основного количества витамина В12. В толстой кишке — всасывание воды, калия, натрия, кальция, желчных солей.
Важным органом пищеварения в организме является поджелудочная железа (ПЖ), выполняющая экзокринную функцию. При поступлении пищи в желудочно-кишечный тракт ПЖ секретирует в тонкую кишку не только панкреатические ферменты, но и бикарбонаты, нейтрализующие соляную кислоту и поддерживающие щелочную среду в двенадцатиперстной кишке, необходимую для нормального функционирования панкреатических ферментов. В физиологических условиях ПЖ образует в сутки от 50 до 2500 мл секрета — в зависимости от возраста человека и характера поступающей пищи. Панкреатический сок представляет собой бесцветную жидкость щелочной реакции (рН 7,8–8,4). Он содержит органические вещества (белки) и неорганические компоненты (бикарбонаты, электролиты, микроэлементы), а также слизь выводящих протоков. Ферментная часть секрета образуется в ацинарных клетках, а жидкая (водно-электролитная) — муцин и бикарбонаты — протоковым эпителием. С помощью панкреатических ферментов (липазы, амилазы и протеаз), играющих ключевую роль во внешнесекреторной функции ПЖ, происходит расщепление пищевых веществ. Большинство из них находятся в неактивной форме — это проэнзимы, которые активируются в двенадцатиперстной кишке энтерокиназой. В активной форме секретируются липаза, амилаза и рибонуклеаза. Указанный механизм обусловливает активность панкреатического сока в полости кишечника, что, в свою очередь, предохраняет ткань ПЖ от аутолиза.
Пищеварительные ферменты ПЖ имеют свои мишени: амилаза — α-1,4-гликозидные связи крахмала, гликогена; липаза — триглицериды (образование ди-моноглицеридов и жирных кислот); фосфолипаза А — фосфатидилхолин (образование лизофосфатидил-холина и жирных кислот); карбоксилэстераза — эфиры холестерина, эфиры жирорастворимых витаминов, три-, ди-, моноглицеридов; трипсин — внутренние связи белка (основные аминокислоты); химотрипсин — внутренние связи белка (ароматические аминокислоты, лейцин, глутамин, метионин); эластаза — внутренние связи белков (нейтральные аминокислоты); карбоксипептидаза А и В — наружные связи белков, включая ароматические и нейтральные алифатические аминокислоты (А) и основные (В) аминокислоты с карбоксильного конца.
Последние четыре фермента секретируются ПЖ в неактивной форме (проферменты) и активируются в двенадцатиперстной кишке.
Экзокринная дисфункция ПЖ наблюдается при различных наследственных и приобретенных заболеваниях и может быть обусловлена нарушением образования ферментов ПЖ или их активацией в тонкой кишке. Вследствие дисфункции ПЖ, сопровождающейся дефицитом ферментов, развивается нарушение переваривания пищи (мальдигестия) и всасывания пищевых веществ (мальабсорбция) в кишечнике.
Мальдигестия у детей обусловлена рядом нарушений.
Причиной мальабсорбции служит нарушение активности секреции кишечных энзимов, обусловленное дисахаридазной недостаточностью, гастроинтестинальной формой пищевой аллергии, нарушением внутриклеточного пищеварения (целиакия, болезнь Крона, энтериты и т. д.), нарушением транспорта всосавшихся веществ (экссудативная энтеропатия, лимфома, опухоли, туберкулез).
Известно, что ПЖ обладает большими компенсаторными возможностями, и нарушения панкреатической секреции проявляются лишь при тяжелом поражении железы. Существует мнение, что выраженная стеаторея и креаторея у взрослых развиваются в тех случаях, когда секреция панкреатической липазы и трипсина снижается более чем на 90%. Однако у детей такой порог не установлен.
Причины и механизмы развития внешнесекреторной недостаточности ПЖ разнообразны. Выделяют абсолютную панкреатическую недостаточность, обусловленную уменьшением объема функционирующей паренхимы ПЖ, и относительную, которая может быть связана с различными заболеваниями желудочно-кишечного тракта.
При выявлении симптомов, свидетельствующих об экзокринной недостаточности ПЖ, необходимо как можно раньше, до того как начала развиваться мальабсорбция, начать заместительную терапию панкреатическими ферментами.
Клиническими признаками внешнесекреторной недостаточности ПЖ являются:
Существует достаточно большое количество методов оценки переваривающей способности желудочно-кишечного тракта.
При нарушении пищеварения выявляют следующие симптомы: стеаторея — наличие в каловых массах нейтрального жира (стеаторея 1-го типа); жирных кислот, мыла (стеаторея 2-го типа); того и другого (стеаторея 3-го типа); креаторея — может быть признаком нарушения внешнесекреторной функции ПЖ. В норме мышечных волокон в каловых массах очень мало; амилорея — наличие в испражнениях большого количества крахмальных зерен — свидетельствует о нарушении расщепления углеводов; выявляется у больных с панкреатической недостаточностью редко, так как гидролиз крахмала практически не нарушается ввиду высокой активности кишечной амилазы. Наиболее ранним признаком экзокринной панкреатической недостаточности является стеаторея, креаторея появляется несколько позже. Амилорея редко наблюдается при внешнесекреторной недостаточности ПЖ.
Впервые ферментные препараты в гастроэнтерологической практике стали использоваться около 100 лет назад. Пищеварительные ферменты в настоящее время широко применяются при различной гастроэнтерологической патологии. Несмотря на многообразие проявлений ферментативных нарушений пищеварения, основным направлением терапии таких больных является заместительная ферментная терапия. В настоящее время в клинической практике используется большое число ферментных препаратов, характеризующихся различной комбинацией компонентов, энзимной активностью, способом производства и формой выпуска. При выборе ферментного препарата в каждом конкретном случае врач прежде всего должен обращать внимание на его состав и активность его компонентов.
Выделяют два направления действия ферментных препаратов:
Показаниями для назначения ферментной терапии являются:
Классификация ферментных препаратов
Различают следующие группы ферментных препаратов.
Несмотря на то что в арсенале врача в настоящее время существует много ферментных препаратов ПЖ, до сих пор не всегда удается подобрать адекватную заместительную терапию ферментами у больных с тяжелыми формами панкреатической недостаточности. Серьезной проблемой остается неустойчивость многих ферментов в кислой среде.
Средства, содержащие панкреатин, включают липазу, амилазу, протеазы. Сырьем для приготовления этих препаратов служит поджелудочная железа свиней, крупного рогатого скота. При выборе ферментных препаратов необходимо учитывать уровень входящих в их состав ферментов (табл. 1).
Препараты, содержащие панкреатические ферменты, могут применяться как постоянно, в качестве заместительной терапии, так и однократно, при высокой пищевой нагрузке. Доза подбирается индивидуально и зависит от степени выраженности клинико-лабораторных показателей экзокринной функции ПЖ. Об эффективности дозы судят по клиническим (исчезновение болей в животе, нормализация частоты и характера стула) и лабораторным показателям (исчезновение стеатореи и креатореи в копрограмме, нормализация триглицеридов в липидограмме стула).
Ферментосодержащие препараты наряду с панкреатином могут содержать желчные кислоты, гемицеллюлазу, растительные желчегонные компоненты (куркума), симетикон и др. (табл. 2). Основным показанием к применению препаратов этой группы у детей является дисфункция билиарного тракта (гипомоторная дискинезия). Желчные кислоты и соли повышают сократительную функцию желчного пузыря, нормализуют биохимические свойства желчи, а также регулируют моторику толстого кишечника у детей с запорами. Их следует применять во время или сразу после приема пищи (не разжевывая) 3–4 раза в день курсами до 2 мес. Ферменты этой группы не используются при панкреатите, так как они содержат компоненты желчи, способствующие усилению перистальтики кишечника.
Желчные кислоты, входящие в состав препаратов, усиливают панкреатическую секрецию, холерез; стимулируют моторику кишечника и желчного пузыря.
В условиях микробной контаминации кишечника происходит деконъюгация желчных кислот, при этом активируется циклический аденозинмонофосфат энтероцитов с развитием осмотической и секреторной диареи. Желчные кислоты вступают в энтеропатическую циркуляцию, метаболизируются в печени, увеличивая на нее нагрузку. Кроме того, желчные кислоты способны оказывать прямое повреждающее действие на слизистую кишечника.
Гемицеллюлаза обеспечивает расщепление полисахаридов растительного происхождения (перевариваемой клетчатки), уменьшает газообразование.
Противопоказания к назначению ферментных препаратов, содержащих компоненты желчи:
Ферментные препараты растительного происхождения, содержащие папаин, экстракт рисового грибка и другие компоненты, могут использоваться для коррекции экзокринной недостаточности ПЖ. Они производятся из растительного сырья.
В группу ферментных препаратов растительного происхождения входят:
Препараты пепфиз, юниэнзим, вобэнзим, меркэнзим и флогэнзим содержат бромелаин — концентрированную смесь протеолитических ферментов из экстракта свежих плодов ананаса и его ветвей. Эффективность бромелаинов не зависит от количества соляной кислоты в желудке (pH 3-8,0).
Все перечисленные ферментные препараты растительного происхождения противопоказаны больным с грибковой и бытовой сенсибилизацией, при бронхиальной астме (А. А. Корсунский, 2000). Солизим и сомилазу нельзя назначать при аллергии к антибиотикам пенициллинового ряда.
Ферменты на основе растительного сырья могут использоваться для коррекции экзокринной недостаточности ПЖ, особенно в тех случаях, когда пациент не переносит панкреатических энзимов (аллергия к свинине, говядине).
Следует отметить, что в литературе появились данные, свидетельствующие о низкой ферментативной активности ферментов растительного и грибкового происхождения (в 75 раз менее эффективных, чем препараты животного происхождения), в связи с чем они не нашли широкого применения в детской практике.
Простые ферменты (бетаин, абомин) не относятся к группе панкреатических ферментов. В настоящее время зарегистрированы следующие препараты, обладающие протеолитической активностью:
Получают эти препараты из слизистой оболочки желудка свиней, телят или ягнят. Наличие в препаратах пепсина, катепсина, пептидаз, аминокислот способствует высвобождению гастрина, являющегося регуляторным полипептидом, в связи с чем препараты этой группы могут назначаться при функциональных нарушениях желудочно-кишечного тракта, при гастритах с секреторной недостаточностью, которые у детей старшего возраста встречаются сравнительно редко. Назначаются эти препараты внутрь во время еды.
Не следует назначать эти препараты при экзокринной недостаточности ПЖ.
Успех терапии внешнесекреторной недостаточности ПЖ зависит от многих причин. Последние исследования не выявили существенных различий в эффективности при почасовом приеме ферментных препаратов и применении их во время еды. Однако наиболее удобным и физиологическим для пациента является прием ферментных препаратов во время еды.
В случае адекватно подобранной дозы и формы ферментного препарата, наступает значительное улучшение состояния больного. Критериями эффективности лечения является исчезновение полифекалии, уменьшение или ликвидация диареи, нарастание массы тела, исчезновение стеатореи, амилореи и креатореи. Первой обычно на фоне терапии ферментами исчезает креаторея. Это может быть связано с тем, что секреция панкреатической протеазы сохраняется несколько дольше, чем липазы.
Доза ферментного препарата подбирается индивидуально в течение первой недели лечения, в зависимости от выраженности экзокринной недостаточности ПЖ. Дозу ферментного препарата целесообразно рассчитывать по липазе начинать следует с небольших дозировок (1000 ЕД липазы на кг массы в сутки). В случае отсутствия эффекта доза препарата постепенно увеличивается под контролем копрологических исследований. При тяжелой экзокринной недостаточности используется 4000–5000 ЕД липазы на кг массы в сутки в 3–4 приема. Длительность терапии определяется индивидуально. Прием ферментов прекращают в случае исчезновения клинических и копрологических признаков мальдигестии и мальабсорбции.
Причины отсутствия эффекта при терапии ферментами:
Несмотря на то что с помощью ферментных препаратов можно значительно уменьшить степень стеатореи, полного и стойкого ее исчезновения удается достичь не всегда.
Факторы, препятствующие исчезновению стеатореи:
Способы, позволяющие преодолеть инактивацию фермента желудочным соком:
Противопоказания к назначению ферментных препаратов:
В настоящее время, благодаря большому выбору ферментных препаратов ПЖ, появилась реальная возможность индивидуальной коррекции нарушений пищеварения у детей с экзокринной недостаточностью ПЖ, функциональными нарушениями желудка, желчевыводящих путей. Назначение ферментных препаратов требует от врача дифференцированного подхода в каждом конкретном случае — необходимо учитывать механизмы развития заболевания, приведшего к нарушению процессов пищеварения.
Н. А. Коровина, доктор медицинских наук, профессор
И. Н. Захарова, доктор медицинских наук, профессор
РМАПО, Москва
















