вместо эутирокса что можно принимать
Особенности лечения гипотиреоза у лиц пожилого возраста
Гипотиреоз — самое распространенное заболевание щитовидной железы у пожилых. Проведена оценка результатов и адекватности лечения больных первичным явным гипотиреозом пожилого и старческого возраста, даны подходы к оптимизации заместительной терапии пациен
Hypothyroidism is the most wide-spread thyroid gland disease in elderly people. Assessment of results and relevance of treatment of patients suffering from primal open hypothyroidism of elderly and old age was done, some approaches to replacement therapy optimization for the patients and to increase of their quality of life were suggested.
Глобальное прогрессирующее старение населения во всем мире, в том числе и в России, сопровождается ростом возрастных патологий и различных заболеваний эндокринной системы. По суммарной частоте встречаемости в популяции заболевания щитовидной железы занимают первое место среди эндокринной патологии, что связано с ухудшением экологической обстановки, увеличением частоты аутоиммунных заболеваний, недостаточным потреблением йода и, несомненно, с улучшением диагностики.
Одним из самых распространенных заболеваний щитовидной железы у лиц пожилого и старческого возраста является гипотиреоз. Гипотиреоз — это синдром, характеризующийся стойким недостатком тиреоидных гормонов в организме или их биологического эффекта на уровне периферических тканей. Гипотиреоз может развиться вследствие поражения самой щитовидной железы (первичный гипотиреоз) или системы, регулирующей ее функцию (вторичный — гипофизарный гипотиреоз и третичный — гипоталамический гипотиреоз) или нарушения метаболизма тиреоидных гормонов на уровне периферических тканей (так называемый периферический, тканевой или транспортный гипотиреоз) [1, 2].
У лиц пожилого возраста, как правило, встречается первичный гипотиреоз (более 99% случаев), вызываемый в основном аутоиммунным тиреоидитом или хирургическими вмешательствами на щитовидной железе. Причиной развития первичного гипотиреоза могут быть также недостаточное поступление в организм йода, белка и селена, а также прием различных препаратов с антитиреоидным действием (тиреостатики, йодсодержащие, препараты сульфанилмочевины, препараты лития, интерферон-альфа, нейролептики, транквилизаторы и многие другие). Клинически по степеням тяжести выделяют субклинический и явный гипотиреоз. Субклинический гипотиреоз характеризуется стертым клиническим течением и устанавливается на основании повышения уровня тиреотропного гормона (ТТГ) (в пределах 4–10 мМЕ/л) при нормальном уровне свободного тироксина (св. Т4). При явном гипотиреозе имеются характерная для гипотиреоза клиническая картина, повышение содержания ТТГ в крови выше 10 мМЕ/л и снижение уровня св. Т4.
Эпидемиологические исследования указывают на нарастание частоты гипотиреоза с возрастом. Bemben D. и др. выявили у 14,6% женщин и 15,4% мужчин старше 60 лет субклинический гипотиреоз. В Колорадском исследовании, в которое были включены 25 862 человека, повышенный уровень ТТГ был установлен у 9,5% обследованных, при этом распространенность гипотиреоза в зависимости от возраста варьировала от 4% до 21% у женщин и от 3% до 16% у мужчин [3]. Аналогичная тенденция наблюдается и в России. Установлено, что при отсутствии лечения в течение года у 5–15% лиц субклинический гипотиреоз переходит в явный, причем при наличии антитиреоидных антител значительно быстрее (через 4 года у 80% лиц старше 65 лет) [4].
Патогенез гипотиреоза вызван длительным снижением эффекта тиреоидных гормонов на уровне практически всех органов и тканей со снижением скорости всех обменных и окислительных процессов с накоплением гликозамингликанов в соединительной ткани различных органов.
Следует указать на особенности развития гипотиреоза у пожилых лиц, что сказывается на своевременной диагностике заболевания, задерживая назначение адекватной заместительной терапии. Заболевание обычно развивается медленно, постепенно и незаметно, часто симптомы гипотиреоза имеют сходство с обычными признаками старения, могут длительно не распознаваться и протекать под «масками» других заболеваний [4]. Стертость клинической картины, полиморбидность с атипичностью течения и нередко отсутствие жалоб (у 25% лиц при явном и у 35% лиц при субклиническом гипотиреозе по данным Колорадского исследования) являются причиной поздней диагностики заболевания. В связи с особенностями проявления гипотиреоза у пожилых лиц такие больные годами наблюдаются по поводу различных заболеваний: ишемической болезни сердца (ИБС), анемии различного генеза, паркинсонизма, атеросклероза и др. С другой стороны, наличие у 15% популяции типичных, характерных для гипотиреоза жалоб, в состоянии эутиреоза (по данным Колорадского исследования) и отсутствие осведомленности практических врачей о влиянии на уровень ТТГ различных лекарств и состояний могут быть причиной гипердиагностики гипотиреоза и необоснованного назначения тиреоидных гормонов.
Проблема лечения гипотиреоза у лиц пожилого и старческого возраста и подбора адекватной дозы тиреоидных гормонов, необходимой для компенсации нарушений метаболизма, а также сохранения высокого качества жизни этих больных, остается одной из актуальных задач тиреодологии. Общие принципы заместительной терапии гипотиреоза сформулированы в международных и отечественных руководствах по эндокринологии и тиреодологии, в монографиях [1–2, 4–5, 8–14]. Цель заместительной терапии первичного гипотиреоза заключается в устранении симптомов гипотиреоза, нормализации и поддержании уровня ТТГ в пределах 0,5–1,5 мМЕ/л и предотвращении развития осложнений.
«Золотым стандартом» для заместительной терапии гипотиреоза считаются препараты левотироксина натрия в индивидуально подобранных адекватных дозах, так как современные синтетические препараты тироксина по сути не отличаются от тироксина человека и позволяют удержать стойкий эутиреоз на фоне их приема 1 раз в сутки. Небольшое увеличение уровня св. Т4, наблюдаемое через несколько часов после приема тироксина, не имеет клинического значения [1]. Однако в терапии гипотиреоза у пожилых лиц имеются особенности: в отличие от молодых и лиц среднего возраста, которым можно назначить сразу полную заместительную дозу из расчета 1,6–1,8 мкг/кг в сутки, пожилым пациентам с сопутствующими заболеваниями лечение рекомендуют начинать с 12,5–25 мкг левотироксина натрия. В связи со снижением потребности в заместительной терапии с возрастом некоторые пожилые люди могут получать левотироксин натрия менее 1 мкг/кг в сутки.
Следует отметить, что вопрос о целесобразности назначения заместительной терапии тироксином при субклиническом гипотиреозе, особенно у пациентов с сердечно-сосудистыми заболеваниями и аритмиями сердца, остается дискутабельным в связи с большим риском получения осложнений. Большинство зарубежных ученых и эндокринологов [14–18], несмотря на некоторую положительную динамику от применения тироксина при субклиническом гипотиреозе, рекомендуют лишь наблюдение за больными и контроль уровня ТТГ 1–2 раза в год. В то же время Российская ассоциация эндокринологов, исходя из того, что восстановление функции щитовидной железы у пожилых лиц наблюдается реже по сравнению с молодыми и что при субклиническом гипотиреозе, особенно при наличии антител к тиреоидной пероксидазе, имеется поражение различных органов, рекомендует назначение тироксина при стойком субклиническом гипотиреозе, когда при двукратном определении уровень ТТГ находится в пределах 5–10 мМЕ/л. Кроме того, имеются данные, что раннее применение тиреоидных гормонов задерживает переход субклинического гипотиреоза в более тяжелый явный [4]. Следует отметить, что в настоящее время проблема терапии субклинического гипотиреоза у лиц пожилого и старческого возраста находится в стадии изучения в некоторых странах Европы и Северной Америки.
В данной статье мы остановимся на особенностях терапии первичного явного гипотиреоза у пожилых лиц.
Известно, что терапия тиреоидными гормонами в первую очередь сказывается на состоянии сердечно-сосудистой и центральной нервной систем, наиболее чувствительных к изменению концентрации тиреоидных гормонов в крови. Нередко при очередном повышении дозы тироксина для достижения компенсации гипотиреоза у больных пожилого и старческого возраста, страдающих кардиальной патологией, нейроциркуляторной дистонией и другими заболеваниями, появляются жалобы и симптомы, требующие исключения ухудшения работы сердечно-сосудистой системы и препятствующие обеспечению адекватной заместительной терапии.
Цель: оценка результатов и адекватности лечения больных первичным явным гипотиреозом пожилого и старческого возраста для оптимизации заместительной терапии и повышения качества их жизни.
Материалы и методы
Проведена оценка адекватности терапии явного гипотиреоза 544 больных первичным гипотиреозом в возрасте 60–87 лет (средний возраст 64,7 ± 5,8 года) при обращении в Медицинский центр «Профессор» и 112 пациентов, поступивших в эндокринологическое отделение больницы № 46 в «Центре для жителей блокадного Ленинграда» с 2001 по 2011 гг. Давность гипотиреоза у больных составила 2–25 лет. Диагноз явного гипотиреоза у пациентов был установлен общепринятыми лабораторными методами. Все больные получали заместительную терапию Эутироксом или L-Тироксином. В процессе наблюдения у всех больных определяли св. Т4, ТТГ, холестерин исходно и через 3 и 6 месяцев после первого обращения, однократно — антитела к тиреоглобулину и тиреоидной пероксидазе и УЗИ щитовидной железы. Всем больным выполнялось ЭКГ, эхокардиография и осмотр кардиолога — по показаниям.
Результаты и их обсуждение
Адекватная терапия гипотиреоза у пожилых лиц часто трудная задача. Назначаемые тиреоидные гормоны, оказывая положительное хроно- и инотропное действие на миокард, увеличивая количество катехоламиновых рецепторов в миокарде и их чувствительность, повышают потребность миокарда в кислороде. Это может спровоцировать ухудшение работы сердечно-сосудистой системы вплоть до развития нарушений сердечного ритма и правожелудочковой недостаточности. Поэтому у пожилых больных рекомендуются меньшие дозы тиреоидных гормонов (из расчета 0,9 мкг/кг массы тела), при титрации дозы определение уровня ТТГ и св. Т4 и контроль ЭКГ — 1 раз в 2 месяца. При наличии ожирения расчет дозы тиреоидных гормонов ведется на 1 кг «идеальной» массы тела. Целью терапии гипотиреоза у пожилых лиц является устранение (если это возможно) всех клинических симптомов гипотиреоза, при этом допускается ведение больных при более высоком уровне ТТГ — 0,5–4,0 мМЕ/л, в отличие от лиц молодого возраста. При невозможности идеально компенсировать гипотиреоз у пожилых уровень ТТГ можно поддержать в пределах 10 мМЕ/л. Тиреоидные гормоны назначаются утром натощак 1 раз в сутки за 30 минут до приема пищи. Причем прием лекарственных препаратов, витаминов и пищи, содержащих соевые продукты, кальций, железо или другие соединения, влияющих на процесс всасывания из желудочно-кишечного тракта, рекомендуется через 4 часа после приема тиреоидных гормонов. Пациентам, получающим подобранную дозу, рекомендуют ежегодно исследовать уровень ТТГ. Ниже мы приводим список ситуаций и лекарственных препаратов, требующих изменения дозы тиреоидных гормонов, из Национального руководства по эндокринологии, 2008 г. (табл. 1).
Противопоказанием к назначению тиреоидных гормонов являются декомпенсированный тиреотоксикоз, нелеченная надпочечниковая недостаточность и острый инфаркт миокарда. Относительные противопоказания включают нарушения ритма сердца, нестабильную стенокардию и миокардиты. При перечисленных состояниях лечение явного гипотиреоза может проводиться только на фоне адекватной терапии сердечной патологии.
Побочные эффекты, как правило, при использовании малых и средних доз тиреоидных гормонов почти не встречаются. Однако при передозировке или слишком быстром увеличении дозы наблюдаются симптомы тиреотоксикоза, а при длительной передозировке — снижение минеральной плотности костной ткани, особенно у женщин в постменопаузе. У больных ИБС тиреоидные гормоны, особенно лиотиронин, могут провоцировать учащение приступов стенокардии, поэтому таким пациентам рекомендуется начинать лечение с малых доз (12,5–25 мкг) и повышение дозы проводить постепенно с интервалом в 6–8 нед под контролем ЭКГ. Известно, что многие лекарственные средства взаимодействуют с тиреоидными гормонами и влияют на функцию щитовидной железы (табл. 1), однако лишь некоторые взаимодействия имеют значение в клинической практике, когда они либо требуют изменить дозу тиреоидных гормонов, либо влияют на интерпретацию результатов диагностических исследований.
При опросе пациентов было установлено, что наши больные получали L-Тироксин или Эутирокс в дозе 25–125 мкг один раз в сутки утром натощак (средняя доза 87,5 ± 2,5 мкг), непостоянно, редко посещали эндокринолога, многие из них самостоятельно меняли дозу тиреоидных гормонов, редко определяли уровень гормонов (1 раз в 1–3 года) и не соблюдали рекомендации эндокринологов.
Нами клинически и лабораторно эутиреоз был установлен у 436 из 656 больных (табл. 2): средний уровень ТТГ у них составил 2,05 ± 0,7 мМЕ/л и св. Т4 — 14,7 ± 0,3 нмоль/л. У 105 больных был установлен лекарственный тиреотоксикоз (ТТГ ниже 0,3 мМЕ/л), а у 115 лиц гипотиреоз был декомпенсирован: средний уровень ТТГ в этой группе составил 16,4 ± 0,8 мМЕ/л.
Следует отметить, что похожая картина наблюдается и в США (табл. 3). По данным Колорадского исследования лишь 60% больных из 1525 лиц, получающих тиреоидные гормоны, имели эутиреоз. Декомпенсация гипотиреоза, связанная с применением низких доз или отсутствием приема препаратов, имелась у 18% лиц. В то же время у 22% лиц уровень ТТГ был очень низким или не определялся, что указывало на передозировку тироксина [3].
На основании этих данных Cooper D. пришел к выводу, что из 2,6 млн человек старше 60 лет, получающих тиреоидные гормоны в США, у 22% (580 000 лиц) мог быть субклинический и явный гипертиреоз, вызванный избытком тиреоидных гормонов, и справедливо отметил, что у 28% лиц этой группы могла развиться фибрилляция предсердий в течение ближайших 10 лет [5].
В связи с вышеизложенным требуется применение тироксина у пожилых лиц с большой осторожностью, под контролем артериального давления, частоты сердечных сокращений и ЭКГ, а также необходимо учитывать возможное усиление действия антикоагулянтов под их влиянием. При наличии тахикардии, артериальной гипертензии, аритмиях рекомендуется назначение бета-адреноблокаторов для уменьшения потребности миокарда в кислороде. Для снижения риска осложнений со стороны сердечно-сосудистой системы имеются также рекомендации прерывистого назначения тиреоидных гормонов и уменьшения их дозы в летнее время года [6]. При ухудшении работы сердца, показателей ЭКГ или развитии инфаркта миокарда рекомендуется отмена тиреоидных препаратов на несколько дней с последующим назначением их в меньшей дозе.
У 105 больных с передозировкой тиреоидных гормонов нами была проведена коррекция дозы (уменьшение дозы на 25–50 мкг), что сопровождалось значительным улучшением самочувствия и нормализацией уровня ТТГ и св. Т4, при последующем обследовании через 3 и 6 месяцев.
У 115 больных c декомпенсированным гипотиреозом была проведена титрация с повышением дозы тиреоидных гормонов, в результате чего имело место улучшение самочувствия, устранение жалоб и снижение среднего уровня ТТГ до 3,6 ± 1,0 мМЕ/л (р
Э. Г. Гаспарян*, **, ***, доктор медицинских наук, профессор
Г. А. Осташко***
А. А. Гаспарян**
С. Е. Дымнова***
*ГБОУ ВПО СЗГМУ им. И. И. Мечникова,
**Медицинский центр «Профессор»,
***ГУЗ ГКБ № 46 Святой Евгении, Санкт-Петербург
Инструкция по применению: лекарства и их дженерики (5)
Среди препаратов, используемых для лечения нарушений функции щитовидной железы, основную группу составляют гормональные средства. Выбор их на фарм. рынке России, к сожалению, не велик. А в последние годы ещё и сократился.
Сегодня я хочу остановиться на препаратах для лечения гипотиреоза, сниженной функции щитовидной железы. Эта группа препаратов состоит из 3 подгрупп, если их так разделить условно. Препараты тироксина (Т4) – замещающие гормон Т4, более известный, как Л-тироксин, о нём позже будет отдельный разговор.
Если с препаратами Т4 на фарм. рынке ещё всё нормально, препарат есть, а главное, в разных дозах. То с препаратами Т3 всё хуже – их просто нет. Несколько лет в нашей стране препараты Т3 не продавались. Часть таблеток не прошла процедуру перерегистрации препарата на территории России в контролирующих организациях, а другие вообще сняли с производства.
В эти годы у небольшого процента пациентов стала наблюдаться нечувствительность к Т4, и соответственно, стойкий гипотиреоз, который в том числе требовал замещения дополнительно и препаратами, содержащими Т3. Учитывая огромную распространенность тиреоидной патологии, общее количество нуждающихся в Т3 людей оказалось достаточно большим.
Также Т3 может использоваться в комплексном лечении диффузного нетоксического зоба и многоузлового зоба с размером узлов менее 2 см, после операций на щитовидной железе, при АИТе в сочетании с гипотиреозом, при гипертрофической форме или многоузловой форме.
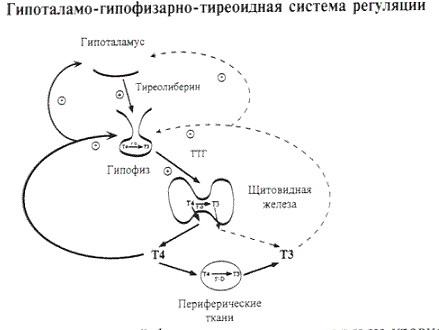
Чтобы понять важность Т3 в организме, привожу ниже облегчённую схему образования гормонов щитовидной железе.
По схеме видно, что Т3 образуется в организме путём перехода из Т4, он является более активным, и непосредственно «работает» на уровне тканей и органов-мишеней, ещё и за счёт того, что соотношение Т4 и Т3 в организме 1:10, то есть триойдтиронина в 10 раз должно быть больше, что учитывается при лечении.
Вот почему при полной заместительной дозе Т4 при гипотиреозе и «нормальном» уровне ТТГ, сохраняется недомогание – вялость, слабость, плохо снижается вес, рассеянно внимание, то есть в организме не хватает Т3.
Есть препараты, позволяющие восполнить дефицит Т3 в организме
Самостоятельно таблетированный трийодтиронин не применяется (для этого есть «узкие» показания), в лечении заболеваний щитовидной железы обычно подбирается комбинация Т4 и Т3 в соотношении, их подбирает только лечащий врач.
Современные принципы лечения диффузного эутиреоидного зоба
Выбор правильной тактики лечения пациента с диффузным эутиреоидным зобом (ДЭЗ) является одним из самых актуальных вопросов тиреидологии. Это связано с тем, что данная патология щитовидной железы (ЩЖ) занимает внушительное место среди всех тиреоидных забол
Выбор правильной тактики лечения пациента с диффузным эутиреоидным зобом (ДЭЗ) является одним из самых актуальных вопросов тиреидологии. Это связано с тем, что данная патология щитовидной железы (ЩЖ) занимает внушительное место среди всех тиреоидных заболеваний. Консервативное лечение ДЭЗ остается единственным научно обоснованным методом, позволяющим реально уменьшить прогрессирование заболевания и, как следствие, снизить частоту формирования в ЩЖ коллоидных узлов.
Несмотря на то, что терапевтические алгоритмы, используемые при ДЭЗ, известны и определены, существуют проблемы, с которыми практический врач-эндокринолог сталкивается ежедневно, а именно:
Единых подходов к решению этих вопросов в настоящее время не существует. Тем не менее, разработка оптимальных подходов к консервативному лечению ДЭЗ должна быть направлена прежде всего на излечение и/или улучшение прогноза заболевания для каждого конкретного пациента.
Доказано, что хронический дефицит йода приводит к формированию сначала диффузного, а затем и узлового коллоидного зоба. При эутиреоидном зобе существует определенная совокупность морфологических изменений в ЩЖ, итогом которых является увеличение тиреоидного объема и нередко формирование узловых образований. Принимая во внимание полиморфность причин, приводящих к развитию зоба, бывает непросто судить о том, какая именно привела к развитию этого заболевания у конкретного больного. Однако главным звеном патогенеза ДЭЗ служит относительный недостаток тиреоидных гормонов, возникающий в условиях йодного дефицита и приводящий к гиперпродукции тиреотропного гормона (ТТГ) гипофизом с последующей пролиферацией тиреоцитов и накоплением коллоида. В подобной ситуации устанавливается баланс равновесия при повышенной стимуляции ЩЖ ТТГ с сохранением ее гормонпродуцирующей функции и формированием зоба.
Йод играет центральную роль в физиологии ЩЖ. Этот микроэлемент является не только незаменимым субстратом для синтеза тиреоидных гормонов, но также регулятором гормоногенеза и пролиферации тиреоцитов. ЩЖ способна избирательно поглощать йод против градиента концентрации. Движущей силой йодного «насоса» является трансмембранная разность потенциалов за счет различной концентрации ионов Na, создаваемая и удерживаемая К/Na-АТФазой. Йодный насос является по сути натриево-йодным котранспортером.
Все этапы метаболизма йода в ЩЖ регулируются тиреотропным гормоном. Под влиянием ТТГ усиливается захват йода, а также все этапы его органификации: увеличивается активность тиреоидной пероксидазы, ускоряются процессы пиноцитоза, протеолиза, синтеза и секреции тиреоглобулина.
Существуют следующие факторы, в разной степени ответственные за усиление клеточной пролиферации в условиях хронического дефицита поступления йода:
При разработке подходов к лечению ДЭЗ были изучены эффективность различных методов терапии и их влияние на концентрацию йода в ЩЖ.
На сегодняшний день существует три варианта консервативной терапии ДЭЗ:
Монотерапия препаратами йода является этиотропной терапией. В работах последних 10–15 лет показано, что повышение продукции ТТГ или повышение к нему чувствительности тиреоцитов имеет лишь второстепенное значение в патогенезе йоддефицитного зоба. При недостаточном поступлении йода в железу снижается количество йодированных липидов (основных ингибиторов факторов роста), что оказывает мощное стимулирующее воздействие на рост тиреоцитов.
Назначение 100–150 мкг йода хорошо зарекомендовало себя для лечения зоба у детей. Лечебные дозы йода при ДЭЗ у взрослых почти не отличаются от профилактических и составляют 150–200 мкг в сутки, однако эффект терапии препаратом йода у взрослых не всегда является оптимальным.
Наиболее привлекательным с точки зрения достижения быстрого клинического эффекта (уменьшение объема ЩЖ) методом лечения ДЭЗ у взрослых является назначение Эутирокса в дозе, позволяющей достичь целевого уровня ТТГ 0,1–0,4 мМЕ/л. Монотерапия Эутироксом ДЭЗ эффективна, но высока вероятность рецидива зоба после отмены препарата. Существует риск осложнений медикаментозного тиреотоксикоза, есть необходимость подбора дозы, необходимы достаточно частые гормональные исследования.
Тем не менее, назначение тиреоидных гормонов подавляет по принципу обратной связи уровень ТТГ, который является мощным фактором, стимулирующим гипертрофию и гиперплазию тиреоцитов, и оказывает, таким образом, антипролиферативный эффект. Опыт многих клинических наблюдений за пациентами с ДЭЗ, вообще не получавшими лечения, показывает, что естественный ход событий представляет собой продолжающийся более или менее постоянный рост зоба.
В литературе активно обсуждается вопрос о неблагоприятном влиянии терапии тироксином на интратиреоидную концентрацию йода. Известно, что за счет подавления уровня ТТГ происходит снижение захвата йода тиреоцитами. Снижение интратиреоидной концентрации йода на фоне отмены тироксина приводит к быстрому увеличению объема ЩЖ.
Т. е. применение Эутирокса при ДЭЗ ограничено по срокам из-за возможных побочных эффектов, а отмена препарата часто сопровождается дальнейшим ростом объема ЩЖ.
Исходя из этого длительность терапии Эутироксом должна ограничиваться годом, а после отмены препарата в обязательном порядке требуется назначение монотерапии йодидом калия (Йодбаланс).
Целый ряд исследований, в которых сравнивались результаты лечения ДЭЗ йодом, тироксином и их комбинацией, показали, что назначение либо монотерапии препаратом йода (Йодбаланс), либо комбинированное лечение (Йодтирокс) также эффективно позволяют добиться сокращения объема щитовидной железы, как и монотерапия тироксином.
Преимущества комбинированной терапии тироксином и йодом (Йодтирокс) состоят в том, что Йодтирокс воздействует на все патогенетические механизмы формирования зоба. Уменьшение объема зоба более выражено на комбинированной, чем на монотерапии Эутироксом. Реже развивается синдром отмены в отличие от монотерапии Эутироксом.
Таким образом, использование комбинированных препаратов (Йодтирокс), содержащих помимо тиреоидных гормонов определенное количество йода, в виде «стартового препарата» в лечении ДЭЗ вполне оправдано. На фоне применения комбинированных препаратов, в отличие от монотерапии тироксином, не происходит снижения интратиреоидной концентрации йода. Однако в условиях йодного дефицита не произойдет также и повышения концентрации йода в ЩЖ, поскольку уровень ТТГ, который является основным фактором, стимулирующим захват йода тиреоцитами, подавлен в результате назначения тироксина.
Хорошо известно, что высокая частота ДЭЗ среди населения России связана с йодным дефицитом. Назначение профилактических доз йода после отмены базовой терапии Эутироксом или Йодтироксом может предотвратить «синдром отмены», связанный со снижением концентрации йода в ЩЖ.
Напомним, что суточная потребность взрослого человека в йоде составляет 150–200 мкг. Среднее потребление йода в йододефицитных регионах России составляет около 40–80 мкг, а ежедневный дефицит поступления йода в йоддефицитных регионах равен 100–200 мкг.
Подводя итог вышесказанного, можно сделать вывод, что основной целью в лечении йоддефицитного зоба является не только снижение объема ЩЖ, но и поддержание достигнутого результата. Для этого также подойдут препараты йода как в виде монотерапии (Йодбаланс), так и в составе комбинированной терапии с тироксином (Йодтирокс).
Остается вопрос, что же назначать в первую очередь. Исходя из того, что интратиреоидная концентрация йода достоверно сильнее повышается при первоначальном приеме препаратов йода, чем комбинированных с тироксином препаратов, становится понятной целесообразность начала лечения именно с назначения йодидов (Йодбаланс). Тем не менее, при исходно больших размерах зоба (более 40 мл) препаратом выбора для начала лечения может быть Йодтирокс.
Алгоритм терапии диффузного эутиреоидного зоба
При достижении желаемого эффекта от лечения — нормализации объема ЩЖ, лекарственный препарат можно отменить, но рекомендовать обязательное использование в питании йодированной соли и дальнейшее динамическое наблюдение (ежегодное УЗИ ЩЖ).
Литература
Е. А. Трошина, доктор медицинских наук, профессор
ФГУ ЭНЦ, Москва
.gif)
.gif)