вирус эпштейн барра чем лечить у детей
Эпштейна–Барр-вирусная инфекция у детей: клиническая характеристика, современные аспекты диагностики, дифференцированный подход к лечению

В статье изложены современные представления о проблеме Эпштейна–Барр-вирусной инфекции (ЭБВИ) у детей. Представлены особенности возможного клинического течения как острой ЭБВИ, чаще протекающей как инфекционный мононуклеоз, так и хронических форм, которые
The article presents modern ideas of the issue of Epstein-Barr viral infection (EBVI) in children. Features of possible clinical course both of acute EBVI, which more often manifests as infectious mononucleosis, and of chronic forms, which, in recent years, are taking special role among persistent infections, were presented. The modern schemes of the therapeutic approach were given, including rehabilitation therapy and dispensary observation.
Эпштейна–Барр-вирусная инфекция (ЭБВИ), наряду с остальными инфекционными заболеваниями, встречающимися среди детского населения, остается одной из наиболее актуальных в современной педиатрии. Свою популярность вирус получил не только из-за повсеместного распространения среди всех возрастных групп, но еще и потому, что сам по себе вирус обладает тропизмом к различным клеткам организма, о чем свидетельствует многообразие клинической картины. Кроме того, ЭБВИ может стать причиной аутоиммунной, онкологической, соматической патологии, что, в свою очередь, связано с отсутствием эффективных методов лечения и реабилитации.
Частота заболеваемости в различных странах составляет от 4 до 68 на 100 тыс. населения.
Это не весь текст статьи. Статья входит в раздел Premium и доступна только
зарегистрированным пользователям.
Вирус Эпштейна-Барр: что это и как лечить
Чем лечить вирус Эпштейна-Барр.
25 августа, 2021 год
Содержание
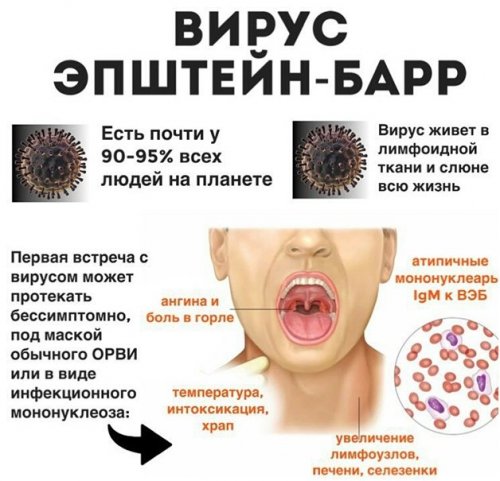
У большинства людей вирус Эпштейна-Барр (ВЭБ) пожизненно сохраняется в организме после контакта с инфекцией. ВЭБ часто запускает развитие различных заболеваний, а первый контакт с вирусом обычно происходит в первые 10 лет жизни ребенка, вызывая вялотекущее инфекционное заболевание. В раннем возрасте симптомы ВЭБ практически отсутствуют либо смазаны. При встрече с вирусом до 10-летнего возраста у ребенка в 40 % случаев развиваются респираторные заболевания, а у 10-25% – инфекционный мононуклеоз.
Вирус Эпштейна-Барр – представитель герпесвирусов, он способен заражать разные клетки, в том числе В-клетки иммунной системы (это лейкоциты) и клетки эпителия слизистых оболочек.
Почему возникают заболевания на фоне вируса Эпштейна-Барр
Передается ВЭБ воздушно-капельным путем. Именно поэтому инфекционный мононуклеоз, который развивается на фоне вируса, называют «болезнью поцелуев».
Еще один способ заражения вирусом Эпштейна-Барр – контактно-бытовой (посуда, зубная щетка, полотенце и т. д.). Также ВЭБ передается через сперму и кровь.
Размножается вирус Эпштейна-Барр в клетках эпителия и в В-лимфоцитах, поэтому проявления этого заражения очень многообразны. Особенность ВЭБ в том, что он атакует клетки иммунной системы – они начинают клонировать ДНК вируса. В организме развивается воспалительный процесс, вызывая различную симптоматику.
Как классифицируют ВЭБ
Поскольку единой классификации вируса Эпштейна-Барр официально не существует, на практике его классификация выглядит так:
Симптомы вируса Эпштейна-Барр
Вирус Эпштейна-Барр вызывает такие заболевания:
Как диагностировать вирус Эпштейна-Барр
Чтобы выявить в организме ВЭБ, врач собирает эпидемиологический анамнез, учитывает клиническую картину заболевания и направляет пациента на определенные анализы. Обычно лабораторная диагностика ВЭБ включает в себя такие маркеры:
Только врач может сказать, какие анализы из вышеперечисленных нужно сдать пациенту с подозрением на вирус Эпштейна-Барр. Диагностикой и лечением должны заниматься терапевт, педиатр или инфекционист. Если у пациента увеличен один или несколько лимфоузлов, он постоянно чувствует усталость, длительно кашляет, живот увеличен в объеме, есть боли в животе или костях, нужна консультация гематолога, онколога и других специалистов.
Как лечить вирус Эпштейна-Барр
Определенного лечения ВЭБ не существует. Обычно лечение вируса Эпштейна-Барр заключается в устранении симптомов. Пациенту нужно пить достаточно жидкости, принимать жаропонижающие и болеутоляющие препараты, интерфероны, противовирусные препараты, антибиотики (только если есть вирусная ангина или бактериальные осложнения), кортикостероиды. Нужно много отдыхать и уменьшить физическую нагрузку. Если у человека тяжелая форма ВЭБ, врачи назначают препараты против герпетической инфекции.
Осложнения при вирусе Эпштейна-Барр
Иногда при вирусе Эпштейна-Барр могут возникать осложнения: анемия, разрыв селезенки, снижение уровня тромбоцитов, гепатит, миокардит, энцефалит, менингит, синдром Гийена–Барре (при котором поражается нервная система.
Профилактика вируса Эпштейна-Барр
На сегодняшний день нет ни препаратов для профилактики ВЭБ, ни вакцин. Основные правила профилактики заболевания – это соблюдение правил личной гигиены, подвижный образ жизни, борьба с вредными привычками, полноценное питание, а также контроль хронических болезней.
Чем лечить вирус Эпштейна-Барр
Обычно для лечения вируса Эпштейна-Барр назначаются иммуномодулирующие, противовирусные препараты («Гропринозин», «Изопринозин»), а также средства на основе интерферона («Лаферобион» и т. д.).
Гропринозин
Противовирусный препарат с иммуномодулирующими свойствами «Гропринозин» назначают пациентам с вирусными инфекциями: герпес 1 и 2 типа, цитомегаловирус, ветряная оспа, вирус Эпштейна-Барр, вирус паротита и кори и т. д. Препарат стимулирует работу иммунной системы, если она снижена, уменьшает симптомы вирусных заболеваний, ускоряет выздоровление и помогает снизить количество рецидивов вирусных инфекций. Дозировку препарата определяет врач, исходя из веса и возраста пациента. Среди побочных эффектов – повышение уровня мочевой кислоты в плазме крови и моче, общее недомогание. Купить «Гропринозин» можно в таблетках и сиропе.
Гропринозин
Gedeon Richter (Гедеон Рихтер), Венгрия
Протефлазид
Это противовирусное средство эффективно при вирусе герпеса 1 и 2 типа, гепатитах, папилломавирусе, ВИЧ-инфекции, гриппе и ОРВИ. «Протефлазид» стимулирует местный иммунитет, защищая слизистые оболочки. Назначают препарат при вирусе Эпштейна-Барр, для профилактики и лечения герпеса (в том числе опоясывающего), при ветряной оспе, цитомегаловирусе. Среди побочных эффектов – боль в животе, головная боль, общая слабость, незначительное повышение температуры. Противопоказания – язва желудка и двенадцатиперстной кишки, повышенная чувствительность к компонентам лекарства. Купить «Протефлазид» можно в виде капель и суппозиториев.
Протефлазид
ЧАО Фитофарм, Украина; Фитофарм НЦ, Россия; ЗАО «ЭкоФармПлюс», Россия
В состав препарата Протефлазид входят флавоноиды диких злаков Calamagrostis epigeios L. и Deschampsia caespitosa L., способные ингибировать ДНК-полимеразу и тимидинкиназу (специфические ферменты вирусов), в клетках, которые инфицированы вирусом. Угнетение этих ферментов приводит к прекращению репликации ДНК вируса, что делает невозможным размножение вируса. Кроме того Протефлазид улучшает неспецифический иммунитет, повышая уровень эндогенного интерферона, что улучшает резистентность организма не только к вирусам, но и к бактериям. Препарат обладает антиоксидантными свойствами, предупреждая накопление продуктов перекисного окисления липидов.
Новирин
В «Новирине» увеличено содержание интерферона, поэтому он имеет прямой противовирусный эффект. Купить «Новирин» можно в сиропе и в таблетках. Назначается «Новирин» при гриппе, аденовирусах, паротите, кори, вирусных бронхитах, герпесе, вирусе Эпштейна-Барр, гепатите В, папилломавирусе и цитомегаловирусе. «Новирин» также показан при инфекциях мочевыводящих путей. Среди противопоказаний – почечная недостаточность, мочекаменная болезнь, подагра. Не подходит «Новирин» для лечения детей до года, беременных и кормящих грудью.
Новирин
ПАТ «Київський вітамінний завод», Украина
Новирин – противовирусный препарат прямого действия. Новирин содержит инозина пранобекс (сложный молекулярный комплекс инозин; N,N-диметиламино-2-пропанол; п-ацетамидобензойная кислота в соотношении 1:3:3), который обладает выраженным иммуномодулирующим и противовирусным действием. Новирин оказывает прямое противовирусное действие, которое обусловлено связыванием активного вещества с рибосомами зараженных клеток, вследствие чего замедляются процессы синтеза вирусной и-РНК, репликация РНК- и ДНК-геномных вирусов.
Лаферобион
Противовирусный и иммуномодулирующий препарат «Лаферобион» назначают взрослым и детям при ОРВИ, гепатите В (остром и хроническом), при хроническом гепатите С, вирусных, бактериальных инфекциях, септических поражениях, при герпесе, папилломатозе гортани, рассеянном склерозе, вирусе Эпштейна-Барр, почечно-клеточной карциноме, грибовидном микозе и т. д. Противопоказания: серьезные проблемы с сердечно-сосудистой системой, почками и печенью, эпилепсия и другие заболевания ЦНС, цирроз печени и т. д. При приеме «Лаферобиона» возможны хроническая усталость, боли в мышцах, повышение температуры. Купить «Лаферобион» можно в виде суппозиториев, порошка, назального спрея.
Лаферобион
ЧАО «Биофарма», Украина
Препарат Лаферобион противовирусное средство, повышает иммунитет от вирусных заболеваний, оказывает противоопухолевое и иммуномодулирующее действие. Лаферобион повышает иммуномодулирующую активность, подавляет пролиферации и рост вирусов в зараженных клетках.
Эпштейна-Барра вирусная инфекция у детей: современные подходы к диагностике и лечению
Эпштейна-Барр вирусная инфекция (ЭБВИ) относится к наиболее распространенным инфекционным заболеваниям человека. Антитела (Ат) к вирусу Эпштейна-Барр (ВЭБ) обнаруживают у 60% детей первых двух лет жизни и у 80–100% взрослых [3, 13]. Заболеваемость острой формой ЭБВИ (ОЭБВИ) в различных регионах мира колеблется от 40 до 80 случаев на 100 тыс. населения [2]. Хроническая форма ЭБВИ (ХЭБВИ) развивается у 15–25% лиц после ОЭБВИ [1, 5, 15]. Установлена роль ВЭБ в развитии злокачественных новообразований, аутоиммунных заболеваний и синдрома хронической усталости [3, 5, 14, 15]. Все это свидетельствует об актуальности проблемы ЭБВИ.
Источник заражения ВЭБ — больные манифестными и бессимптомными формами. 70–90% лиц, перенесших ОЭБВИ, выделяют вирус в последующие 1–18 мес. Пути передачи ВЭБ: воздушно-капельный, контактно-бытовой, парентеральный, половой, вертикальный. ОЭБВИ характеризуется эпидемическими подъемами 1 раз в 6–7 лет, чаще регистрируется в возрасте от 1 до 5 лет, в организованных коллективах [4, 7, 9].
Входные ворота для ВЭБ — слизистая оболочка верхних дыхательных путей: вирус проникает в лимфоидную ткань, инфицирует В-лимфоциты, развивается поликлональная активация В-лимфоцитов, диссеминация возбудителя в составе В-лимфоцитов, синтез антител (Ат) в ответ на антигенную стимуляцию снижен. В первую очередь ВЭБ поражает лимфоидные органы (миндалины, печень, селезенку).
Следующий этап — образование клона сенсибилизированных цитотоксических CD8-клеток, последовательный синтез Ат к VCA-, EA- и EBNA-антигенам вируса. Вследствие нарушения иммунного ответа, функциональной активности факторов врожденной резистентности (нейтрофилов, макрофагов, NK-клеток, системы интерферона) формируется вторичное ИДС [2–4, 12].
Иммунный статус 109 больных ОЭБВИ в возрасте от 5 до 14 лет в нашей работе выявил признаки активации Т-клеточного звена иммунной системы — повышение количества Т-лимфоцитов (CD3), цитотоксических Т-лимфоцитов (CD8), клеток с маркерами поздней активации (HLA-DR); поликлональную активацию В-лимфоцитов — увеличение количества CD20-клеток, иммуноглобулинов (Ig) IgA, IgM, IgG, циркулирующих иммунных комплексов (ЦИК). Обнаружены признаки угнетения иммунной системы: нормальное содержание Т-хелперов (CD4), снижение иммунорегуляторного индекса CD4/CD8, количества естественных киллерных клеток NK (CD16), повышение готовности иммунокомпетентных клеток к апоптозу (CD95). Наблюдалась активация кислородзависимого метаболизма нейтрофилов и редукция его адаптационных возможностей.
У трети обследованных детей (33,9%) ОЭБВИ протекала в форме микст-инфекции с цитомегаловирусами (ЦМВ), вирусами простого герпеса 1 и 2 типов (ВПГ-1, ВПГ-2). При бактериологическом исследовании мазков из ротоглотки у 41,3% пациентов выделены Streptococcus (S.) viridans, у 11,9% — Candida albicans, у 8,2% — Staphilococcus (Staph.) epidermidis, у 6,4% — S. pyogenes, у 2,7% — Klebsiella (Kl.) pneumoniae, у 41,3% — ассоциация бактерий. У 43,1% пациентов — серологические маркеры активной формы хламидийной инфекции, у 30,3% — микоплазмоза.
Возможны следующие исходы ОЭБВИ: латентная инфекция, ХЭБВИ, ИДС, онкологические, аутоиммунные заболевания, синдром хронической усталости [5, 8, 10, 11]. Переход в ХЭБВИ связан с комплексом неблагоприятных факторов в анте-, интра- и постнатальном периодах, нарушением нейроиммунноэндокринной регуляции, генетической предрасположенностью.
Проведенное нами обследование 60 детей в возрасте от 5 до 14 лет с ХЭБВИ показало, что в этой группе у 86,7% матерей имел место отягощенный акушерский анамнез; у 83,3% детей обнаружены перинатальная и постнатальная патология ЦНС, ЛОР-органов и др.
В иммунном статусе больных ХЭБВИ выявлено увеличение содержания антагониста интерлейкина-1 (ИЛ-1RA), недостаточная активация иммунокомпетентных клеток (уменьшение HLA-DR) и повышение их готовности к апоптозу (увеличение CD95). Отмечалось нарушение функциональной активности Т-хелперов 1 типа (Th1) (снижение содержания интерферона γ (ИФН γ)); уменьшение общего пула Т-клеток (CD3), количества лимфоцитов с рецепторами к ИЛ-2 (CD25) и NK-клеток (CD16); содержание цитотоксических CD8-лимфоцитов было повышено. Сохранение маркеров репликации ВЭБ на протяжении длительного времени в этой группе свидетельствовало о нарушении элиминации вируса; при этом отмечались повышение функциональной активности Th2, поликлональная активация В-лимфоцитов (CD20), повышение содержания IgA, IgM, IgG, ЦИК, снижение уровня хемотаксического фактора нейтрофилов (ИЛ-8), изменение их метаболизма.
Нарушения иммунного статуса приводили к активации условно-патогенной микрофлоры, вирусных и грибковых инфекций. В микробном спектре слизистой ротоглотки пациентов с ХЭБВИ выделены S. Viridans (30%), Candida albicans (28,3%), Staph. Epidermidis (25%), S. Pyogenes (20%), Kl. Pneumoniae (8,4%), ассоциация бактерий (41,7%); у 28,3% — серологические маркеры активной формы хламидиоза, у 26,7% — микоплазмоза. У 90% пациентов заболевание протекало в форме микст-инфекции с участием герпес-вирусов: ВЭБ + ЦМВ, ВЭБ + ВПГ-1, ВПГ-2.
Классификация. Общепринятая классификация заболевания отсутствует; рекомендуем использовать разработанную нами рабочую классификацию ЭБВИ.
Примеры оформления диагноза:
Клиническая картина острой ЭБВИ впервые была описана Н. Ф. Филатовым (1885) и Е. Пфейфером (1889). Инкубационный период длится от 4-х дней до 7 нед. Полный симптомокомплекс формируется к 4–10-му дням болезни [4, 7].
Нами обследованы 109 детей с ОЭБВИ. У большинства пациентов заболевание начинается остро, с повышения температуры тела и появления симптомов интоксикации; реже отмечается постепенное начало: несколько дней наблюдается недомогание, слабость, вялость, снижение аппетита. Температура тела субфебрильная или нормальная. Ко 2–4-му дням болезни температура достигает 39–40 °С; лихорадка и симптомы интоксикации могут сохраняться в течение 2–3 и более недель.
Генерализованная лимфаденопатия относится к патогномоничным симптомам ЭБВИ и с первых дней болезни проявляется в виде системного поражения 5–6 групп лимфоузлов (ЛУ), с преимущественным увеличением до 1–3 см в диаметре передне- и заднешейных, подчелюстных ЛУ. ЛУ слегка болезненны при пальпации, не спаяны между собой и окружающими тканями, располагаются в виде «цепочки», «пакета»; видны при повороте головы, придают шее «фестончатые» очертания. Иногда отмечается пастозность мягких тканей над увеличенными ЛУ.
Тонзиллит — наиболее частый и ранний симптом ОЭБВИ, сопровождается увеличением миндалин до II-III степени. Лакунарный рисунок подчеркнут за счет инфильтрации ткани миндалин или сглажен из-за лимфостаза. На миндалинах — налеты желтовато-белого или грязно-серого цвета в виде островков, полосок. Они исходят из лакун, имеют шероховатую поверхность (напоминают кружево), легко снимаются без кровоточивости, растираются, не тонут в воде. Характерно несоответствие размера налета и степени увеличения регионарных ЛУ. При фибринозно-некротическом характере налетов в случае их распространения за пределы миндалин необходим дифференциальный диагноз с дифтерией. Налеты на миндалинах исчезают, как правило, через 5–10 дней.
Признаки аденоидита обнаруживают у подавляющего большинства больных. Отмечаются заложенность носа, затруднение носового дыхания, храпящее дыхание с открытым ртом, особенно во сне. Лицо больного приобретает «аденоидный» вид: одутловатость, пастозность век, переносицы, дыхание через открытый рот, сухость губ.
Гепатомегалия может быть обнаружена с первых дней болезни, однако чаще выявляется на второй неделе. Нормализация размеров печени происходит в течение полугода. У 15–20% больных в качестве осложнения развивается гепатит.
Спленомегалия относится к поздним симптомам, встречается у большинства больных. Нормализация размеров селезенки происходит в течение 1–3 нед.
Экзантема при ОЭБВИ появляется на 3–14-й дни болезни, имеет полиморфный характер — пятнистая, папулезная, пятнисто-папулезная, розеолезная, мелкоточечная, геморрагическая. Определенной локализации нет. Сыпь наблюдается в течение 4–10 дней, иногда оставляет пигментацию. У детей, получавших ампициллин или амоксициллин, сыпь появляется чаще (90–100%).
Гематологические изменения включают лейкоцитоз (10–30 х 10 9 /л), нейтропению с палочкоядерным сдвигом влево, увеличение количества лимфоцитов, моноцитов, атипичных мононуклеаров до 50–80%, повышение СОЭ до 20–30 мм/час. Характерный гематологический признак — атипичные мононуклеары в количестве 10–50%: они появляются к концу первой недели заболевания, сохраняются в течение 1–3 нед.
Хроническая ЭБВИ является исходом ОЭБВИ или развивается как первично-хроническая форма [2, 5, 8, 10, 11, 15]. Нами обследовано 60 детей с ХЭБВИ, клиника которой включала хронический мононуклеозоподобный синдром и полиорганную патологию. У всех пациентов обнаружены лимфопролиферативный синдром (генерализованная лимфаденопатия, гипертрофия небных и глоточной миндалин, увеличение печени и селезенки) и признаки хронической интоксикации (длительный субфебрилитет, слабость, снижение аппетита и др.). Вследствие развития ИДС наблюдались острые инфекции респираторного тракта и ЛОР-органов с обострениями до 6–11 раз в год: ринофарингиты (28,3%), фаринготонзиллиты (91,7%), аденоидиты (56,7%), отиты (11,7%), синуситы (20%), ларинготрахеиты (18,3%), бронхиты (38,3%), пневмонии (25%). Обращала внимание высокая частота полиорганной патологии, обусловленная длительной репликацией ВЭБ, вторичным ИДС, аутоиммунными реакциями (патология ЦНС; хронический гастрит, дискинезия желчевыводящих путей; кардиальный синдром, артралгии).
В последние годы описана врожденная ЭБВИ. Установлено, что риск ее при первичной ЭБВИ во время беременности составляет 67%, при реактивации — 22%. Клиника врожденной ЭБВИ сходна с ЦМВИ.
Установлена роль ВЭБ в развитии онкологических заболеваний и паранеопластических процессов — лимфомы Беркетта, назофарингеальной карциномы, лимфогранулематоза, опухолей желудка, кишечника, слюнных желез, матки, лейкоплакии языка и слизистой ротовой полости, а также ряда аутоиммунных заболеваний — системной красной волчанки, ревматоидного артрита, синдрома Шегрена, лимфоидного интерстициального пневмонита, хронического гепатита, увеита и др. [3, 5, 14, 15]. ВЭБ, наряду с вирусами герпеса человека 6 и 7 типов, является этиологическим фактором синдрома хронической усталости и наиболее частой причиной (15%) развития длительной лихорадки неясного генеза.
Диагностика ЭБВИ основана на учете групп риска, ведущих клинических синдромов и данных лабораторного исследования [8–11]. К группам риска у матери относят отягощенный анамнез, маркеры герпес-вирусных инфекций и др., у ребенка — перинатальное поражение ЦНС, аллергический фенотип, ИДС, маркеры герпес-вирусных инфекций и др. Ведущими клиническими синдромами ЭБВИ являются мононуклеозоподобный, общеинфекционный синдромы, экзантема, синдром полиорганной патологии.
В обязательный стандарт диагностики ЭБВИ входят клинический анализ крови, общий анализ мочи, биохимическое исследование крови, бактериологическое исследование слизи ротоглотки и носа, серологические маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм, УЗИ органов брюшной полости, консультация ЛОР-врача, по показаниям — рентгенография придаточных пазух носа, органов грудной клетки, ЭКГ. Дополнительный стандарт диагностики (в специализированном лечебно-профилактическом учреждении): маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм методом полимеразной цепной реакции (ПЦР), иммунограмма второго уровня, консультация иммунолога, по показаниям — коагулограмма, морфологическая картина стернальной пункции, консультация гематолога, онколога.
Методом иммуноферментного анализа (ИФА) определяют Ат к антигенам ВЭБ, что позволяет осуществить лабораторную диагностику ЭБВИ и определить период инфекционного процесса.
Ат класса IgM к VCA появляются одновременно с клиникой ОЭБВИ, сохраняются в течение 2–3 мес, повторно синтезируются при реактивации ВЭБ. Длительная персистенция высоких титров этих Ат характерна для ХЭБВИ, ВЭБ-индуцированных опухолей, аутоиммунных заболеваний, ИДС.
Ат класса IgG к EA достигают высокого титра на 3–4-й нед ОЭБВИ, исчезают через 2–6 мес. Они появляются при реактивации, отсутствуют при атипичной форме ЭБВИ. Высокие титры Ат данного класса выявляют при ХЭБВИ, ВЭБ-индуцированных онкологических и аутоиммунных заболеваниях, ИДС.
Ат класса IgG к EBNA появляются через 1–6 мес после первичной инфекции. Затем их титр уменьшается и сохраняется в течение всей жизни. При реактивации ЭБВИ происходит повторное увеличение их титра.
Большое значение имеет исследование авидности Ат класса IgG (прочности связывания антигена с Ат). При первичной инфекции сначала синтезируются Ат с низкой авидностью (индекс авидности (ИА) менее 30%). Для поздней стадии первичной инфекции характерны Ат со средней авидностью (ИА — 30–49%). Высокоавидные Ат (ИА — более 50%) образуются через 1–7 мес после инфицирования ВЭБ.
Серологическими маркерами активной фазы ЭБВИ являются Ат IgM к VCA и Ат IgG к EA, низкая и средняя авидность Ат IgG к маркерам неактивной фазы, Ат IgG к EBNA.
Материалом для ПЦР служат кровь, ликвор, слюна, мазки со слизистой ротоглотки, биоптаты органов и др. Чувствительность ПЦР при ЭБВИ (70–75%) ниже, чем при других герпесвирусных инфекциях (95–100%). Это связано с появлением ВЭБ в биологических жидкостях лишь при иммуноопосредованном лизисе инфицированных В-лимфоцитов.
Лечение. Принципами терапии ЭБВИ являются комплексный характер, применение этиотропных препаратов, непрерывность, длительность и преемственность лечебных мероприятий на этапах «стационар → поликлиника → реабилитационный центр», контроль клинико-лабораторных показателей.
На основании опыта лечения 169 детей с ЭБВИ нами разработан стандарт лечения этого заболевания.
Базисная терапия: охранительный режим; лечебное питание; противовирусные препараты: вироцидные препараты — инозин пранобекс (Изопринозин), аномальные нуклеозиды (Валтрекс, Ацикловир), Арбидол; препараты ИФН — рекомбинантный ИФН α-2β (Виферон), Кипферон, Реаферон-ЕС-Липинт, интерфероны для в/м введения (Реаферон-EC, Реальдирон, Интрон А, Роферон А и др.); индукторы ИФН — Амиксин, сверхмалые дозы антител к γ-ИФН (Анаферон), Циклоферон, Неовир. По показаниям: локальные антибактериальные препараты (Биопарокс, Лизобакт, Стопангин и др.); системные антибактериальные препараты (цефалоспорины, макролиды, карбапенемы); иммуноглобулины для внутривенного введения (Иммуновенин, Габриглобин, Интраглобин, Пентаглобин и др.); витаминно-минеральные комплексы — Мульти-табс, Вибовит, Санасол, Киндер Биовиталь гель и др.
Интенсификация базисной терапии по показаниям:
Иммунокорригирующая терапия под контролем иммунограммы — иммуномодуляторы (Полиоксидоний, Ликопид, Рибомунил, ИРС-19, Имудон, Деринат и др.), цитокины (Ронколейкин, Лейкинферон); пробиотики (Бифиформ, Аципол и др.); препараты метаболической реабилитации (Актовегин, Солкосерил, Элькар и др.); энтеросорбенты (Смекта, Фильтрум, Энтеросгель, Полифепан и др.); антигистаминные препараты второго поколения (Кларитин, Зиртек, Фенистил и др.); гепатопротекторы (Хофитол, Галстена и др.); глюкокортикостероиды (преднизолон, дексаметазон); ингибиторы протеаз (Контрикал, Гордокс); нейро- и ангиопротекторы (Энцефабол, Глиатилин, Инстенон и др.); «кардиотропные» препараты (Рибоксин, Кокарбоксилаза, Цитохром С и др.); гомеопатические и антигомотоксические средства (Оциллококцинум, Афлубин, Лимфомиозот, Тонзилла композитум и др.); немедикаментозные методы (лазеротерапия, магнитотерапия, иглорефлексотерапия, массаж, лечебная физкультура и др.)
Симптоматическая терапия.
При лихорадке — жаропонижающие препараты (парацетамол, ибупрофен и др.); при затруднении носового дыхания — назальные препараты (Изофра, Полидекса, Називин, Виброцил, Адрианол и др.); при сухом кашле — противокашлевые препараты (Глаувент, Либексин), при влажном кашле — отхаркивающие и муколитические препараты (АмброГЕКСАЛ, бромгексин, ацетилцистеин и др.).
 |
| Рис. 1. Схема комплексной терапии Эпштейна-Барр вирусной инфекции у детей |
В течение нескольких лет для лечения ЭБВИ мы с успехом применяем схему комбинированной этапной этиотропной терапии, в которую входят инозин пранобекс (Изопринозин) и рекомбинантный интерферон α-2β (Виферон) (рис. 1, 2). Инозин пранобекс (Изопринозин) подавляет синтез вирусных белков и тормозит репликацию широкого спектра ДНК- и РНК-содержащих вирусов, в том числе ВЭБ [3]. Препарат обладает иммунокорригирующей активностью — модулирует иммунный ответ по клеточному типу, стимулирует продукцию Ат, цитокинов, ИФН, повышает функциональную активность макрофагов, нейтрофилов и NK-клеток; предохраняет пораженные клетки от поствирусного снижения синтеза белка. Инозин пранобекс (Изопринозин) назначался по 50–100 мг/кг/сут внутрь в 3–4 приема. Проводили три курса лечения по 10 дней с интервалом 10 дней. Рекомбинантный ИФН α-2β (Виферон) тормозит репликацию вирусов за счет активации эндонуклеазы, разрушения вирусной матричной РНК [6]. Препарат модулирует иммунный ответ, способствует дифференцировке В-лимфоцитов, стимулирует выработку цитокинов, повышает функциональную активность макрофагов, нейтрофилов и NK-клеток. Входящие в его состав природные антиоксиданты (витамины Е и С) стабилизируют клеточные мембраны. Препарат назначали по пролонгированной схеме (В. В. Малиновской и соавт., 2006) [6].
Эффективность этиотропной терапии ОЭБВИ оценена в двух группах больных. Пациенты 1-й группы (52 человека) получали инозин пранобекс (Изопринозин) в сочетании с рекомбинантным ИФН α-2β (Вифероном), больные 2-й группы (57 детей) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Клинико-серологические показатели до начала лечения и через 3 мес терапии представлены в табл. 1. У пациентов обеих групп в динамике отмечалось достоверное уменьшение таких симптомов, как генерализованная лимфаденопатия, тонзиллит, аденоидит, гепатомегалия и спленомегалия. Вместе с тем на фоне комбинированной терапии, положительная динамика клинических показателей была более значительной; острые респираторные инфекции (ОРИ) лишь у 19,2% больных 1-й группы и у 40,3% больных 2-й группы (p Рис. 2. Механизмы этиопатогенетического действия комбинации инозина пранобекса (Изопринозина) и рекомбинантного интерферона α-βb (Виферона) при Эпштейна-Барр вирусной инфекции у детей
Комбинированная терапия при ОЭБВИ способствовала модуляции иммунного ответа по клеточному типу (увеличение CD3-, CD4-, CD8-, CD16- и HLA-DRT-лимфоцитов). Снижалась готовность иммунокомпетентных клеток к апоптозу (CD95). Отмечались стимуляция выработки IgA, переключение синтеза Ат с IgM на IgG, снижение содержания ЦИК, улучшались показатели метаболизма нейтрофилов.
Эффективность этиотропной терапии исследована у 60 больных ХЭБВИ. Пациенты 1-й группы (30 детей) получали инозина пранобекс (Изопринозин) и рекомбинантный ИФН α-2β (Виферон), 2-я группа (30 человек) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Независимо от схемы лечения через 3 мес после начала терапии отмечалось достоверное уменьшение частоты генерализованной лимфаденопатии, гипертрофии небных и глоточной миндалин, спленомегалии, интоксикационного, инфекционного и вегето-висцерального синдромов (табл. 2). Комбинация инозина пранобекса (Изопринозина) с рекомбинантным ИФН α-2β (Вифероном) способствовало более существенной динамике клинических показателей. Количество эпизодов ОРИ снизилось с 6–11 (7,9 ± 1,1) до 4–6 (5,2 ± 1,2) в год на фоне монотерапии рекомбинантным ИФН α-2β (Вифероном), и до 2–4 (2,5 ± 1,4) в год на фоне комбинированной терапии (p
Э. Н. Симованьян, доктор медицинских наук, профессор
В. Б. Денисенко, кандидат медицинских наук
Л. Ф. Бовтало, кандидат медицинских наук
А. В. Григорян
Ростовский ГМУ, Ростов-на-Дону