в чем растворяется ртуть
О ртути
Ртуть: общие понятия
Консультация оперативного дежурного: +7(812)309-13-43
Химические свойства ртути
Ртуть – единственный из всех существующих в природе металлов, который остается жидким при комнатной температуре. В этих условиях на воздухе она не окисляется, в воде и щелочах не растворяется. Растворяется в холодной азотной кислоте и нагретой концентрированной серной. В обычных условиях активно испаряется, и скорость этого процесса прямо пропорциональна температуре и площади поверхности испарения. Пары ртути не имеют ни запаха, ни цвета, обнаружить их в воздухе можно только с помощью специальных приборов
Физические свойства ртути
Для ртути характерны низкая вязкость и высокое поверхностное натяжение. Эти свойства становятся причиной двух негативных с точки зрения ртутного загрязнения среды процессов:
Пары ртути отличает очень высокая летучесть, и слой воды или иной жидкости не представляет для них реальной преграды. То же самое можно сказать и о многих строительных материалах, таких как бетон, кирпич, лакокрасочное покрытие, линолеум или плитка. Ртутные пары равномерно пропитывают их на всю толщину, а также легко сорбируются из воздуха деревом, коврами и тканями. При повышении температуры или при механическом воздействии происходит обратная десорбция ртути в воздух помещения.
Чистая металлическая ртуть хорошо растворяет многие металлы, снижая тем самым прочность металлических конструкций, и образует непрочные соединения как с неорганическими, так и с органическими веществами.
Воздействие ртути на человека и животных
Основные пути попадания ртути в организм – это вдыхание ее паров с воздухом либо употребление с пищей или водой. Организм человека выводит не более 20% попавшей в него ртути, и она накапливается в почках и мозге, поражает плод, если женщина беременна, содержится в крови и грудном молоке. При концентрации паров ртути более 0,1 мг/м3 наступает острое отравление, признаки которого:
Следствием длительного воздействия малых доз ртути является хроническое отравление, которое может проявиться с задержкой на несколько лет. Все это время в организме накапливаются необратимые нарушения с такими внешними признаками:
Мнение эксперта:
Алена Парецкая, врач — педиатр
Пролитая ртуть: как с ней бороться
Существуют как природные (месторождения), так и техногенные (места добычи, горнорудные и предприятия цветной металлургии, специальные полигоны-хранилища, отходы сжигания нефтепродуктов и т. д.) источники ртути, загрязняющей воздух, воду и почву. Бытовые и производственные помещения загрязняются ртутью при неправильной эксплуатации ртутных приборов и устройств, таких как термометры, манометры, выпрямители электрического тока. Статистика утверждает, что 80% всех работ МЧС в Санкт-Петербурге источники паров ртути. Если не принимать во внимание злоумышленные проливы ртути, то наиболее частая причина их существования – разбитый ртутный термометр и преступно халатное отношение к последствиям этого события
Ликвидация розлива ртути: +7(812)309-13-43
ОЧЕНЬ ВАЖНО!
Если у Вас в семье есть ребёнок, заранее объясните ему, что если он нечаянно
разобьёт термометр, его никто не будет за это ругать. В противном случае ваше чадо, испугавшись наказания за разбитый градусник, спрячет его остатки куда-нибудь под кровать или шкаф и ничего Вам не скажет – в итоге вся Ваша семья долгое время будет дышать ядовитыми парами ртути.
При прохождении теста нужно помнить: Предельно допустимая концентрация ртути 300нг/м3
Ртуть
(молярная масса)
(первый электрон)
Содержание
История
Ртуть известна с древних времён. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом природной киновари. Древние греки и римляне использовали ртуть для очистки золота (амальгамирование), знали о токсичности самой ртути и её соединений, в частности сулемы. Много веков алхимики считали ртуть главной составной частью всех металлов и полагали, что если жидкой ртути возвратить твёрдость при помощи серы или мышьяка, то получится золото. Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 году. Для представления элемента как у алхимиков, так и в настоящее время используется символ планеты Меркурий. Но принадлежность ртути к металлам была доказана только трудами Ломоносова и Брауна, которые в декабре 1759 года смогли заморозить ртуть и установить её металлические свойства в твёрдом состоянии: ковкость, электропроводность и др.
Происхождение названия
Нахождение в природе
Ртуть — относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе — рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути — 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — тиманит (HgSe) и онофрит (смесь тиманита и сфалерита).
Ртуть является одним из наиболее чувствительных индикаторов скрытого оруденения не только ртутных, но и различных сульфидных месторождений, поэтому ореолы ртути обычно выявляются над всеми скрытыми сульфидными залежами и вдоль дорудных разрывных нарушений. Эта особенность, а также незначительное содержание ртути в породах, объясняются высокой упругостью паров ртути, возрастающей с увеличением температуры и определяющей высокую миграцию этого элемента в газовой фазе.
В обычных условиях киноварь и металлическая ртуть не растворимы в воде, но в присутствии некоторых веществ (Fe2(SO4)3, озон, пероксид водорода) растворимость в воде этих минералов достигает десятков мг/л. Особенно хорошо растворяется ртуть в сульфидах щелочных металлов с образованием, например, комплекса HgS•nNa2S. Ртуть легко сорбируется глинами, гидроксидами железа и марганца, глинистыми сланцами и углями.
В природе известно около 20 минералов ртути, но главное промышленное значение имеет киноварь HgS (86,2 % Hg). В редких случаях предметом добычи является самородная ртуть, метациннабарит HgS и блёклая руда — шватцит (до 17 % Hg). На единственном месторождении Гуитцуко (Мексика) главным рудным минералом является ливингстонит HgSb4S7. В зоне окисления ртутных месторождений образуются вторичные минералы ртути. К ним относятся, прежде всего, самородная ртуть, реже метациннабарит, отличающиеся от таких же первичных минералов большей чистотой состава. Относительно распространена каломель Hg2Cl2. На месторождении Терлингуа (Техас) распространены и другие гипергенные галоидные соединения — терлингуаит Hg2ClO, эглестонит Hg4Cl.
Месторождения
Ртуть считается редким металлом.
Одно из крупнейших в мире ртутных месторождений находится в Испании (Альмаден). Известны месторождения ртути на Кавказе (Дагестан, Армения), в Таджикистане, Словении, Киргизии (Хайдаркан — Айдаркен), Донбассе (Горловка, Никитовский ртутный комбинат).
В России находятся 23 месторождения ртути, промышленные запасы составляют 15,6 тыс. тонн (на 2002 год), из них крупнейшие разведаны на Чукотке — Западно-Палянское и Тамватнейское.
В окружающей среде
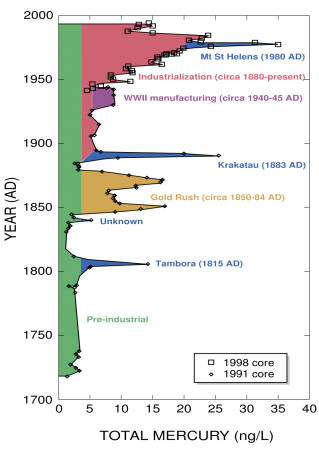
До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограммов на 1 кубический дециметр льда. Природные источники, такие, как вулканы, составляют примерно половину всех выбросов атмосферной ртути. Причиной появления остальной половины является деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля (главным образом в тепловых электростанциях) — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6,8 %, производство цемента — 6,4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1,4 %, ртути (в основном для батареек) — 1,1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1956 году, что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата.
Изотопы
Природная ртуть состоит из смеси 7 стабильных изотопов: 196 Hg (распространённость 0,155 %), 198 Hg (10,04 %), 199 Hg (16,94 %), 200 Hg (23,14 %), 201 Hg (13,17 %), 202 Hg (29,74 %), 204 Hg (6,82 %). Искусственным путём получены радиоактивные изотопы ртути с массовыми числами 171—210.
Получение
Ртуть получают обжигом киновари (сульфида ртути II) или металлотермическим методом:
HgS + O2 ⟶ Hg + SO2↑ HgS + Fe ⟶ FeS↓ + Hg
Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности.
На протяжении многих столетий в Европе основным и единственным месторождением ртути был Альмаден в Испании. В Новое время с ним стала конкурировать Идрия во владениях Габсбургов (современная Словения). Там же появилась первая лечебница для поражённых отравлением парами ртути рудокопов. В 2012 г. ЮНЕСКО объявило промышленную инфраструктуру Альмадена и Идрии памятником Всемирного наследия человечества.
В надписях во дворце древнеперсидских царей Ахеменидов (VI—IV века до н. э.) в Сузах упоминается, что ртутную киноварь доставляли сюда с Зеравшанских гор и использовали в качестве краски.
Как можно нейтрализовать ртуть

В подобных ситуациях знания об обезвреживании ртути очень пригодятся, ведь сделав все правильно, вы сохраните здоровье себе и своей семье, возможно, даже спасете жизнь.
Что такое ртуть и чем она опасна
Ртуть — один из элементов таблицы Менделеева (металл группы цинка). Этому веществу присвоена первая степень опасности. Оно представляет угрозу для здоровья и жизни человека.
Опасна ртуть непосредственно своими испарениями, которые при попадании в человеческий организм через дыхательные пути, вызывают отравление, тяжесть которого напрямую зависит от того, как долго и в каких количествах вдыхались испарения.
В открытом пространстве, например, если разбить градусник, ртуть принимает форму шариков разной величины, которые остаются на поверхности и практически не впитываются в какие-либо материалы. Шарики имеют серебристо-серый цвет, при нажатии могут распадаться на еще более мелкие частицы.
Попадая в открытое пространство из разбившегося градусника, вещество начинает испаряться. Причем, испарения появляются уже при температуре воздуха в 18 °C.
Испаряясь, частицы этого металла не имеют ни запаха, ни цвета. То есть обнаружить ртуть можно только увидев ее шарики. Если вы не заметили хотя бы 1 шарик из разбившегося термометра, он может незаметно испаряться месяцами, нанося колоссальный вред здоровью.
Как обнаружить ртуть
Чтобы обезопасить помещение и всех находящихся в нем людей, после того как разбился ртутный градусник, необходимо проверить, вся ли ртуть была собрана. Но из-за того, что пары ее невидимы, сделать это тяжело.
Однако существует способ обнаружения испарений ртути в воздухе, для этого необходимо изготовить импровизированный индикатор:
Для обнаружения испарений ртути разложите получившиеся «индикаторы» в комнате.
Если в воздухе присутствуют пары ртути, полоски бумаги окрасятся в розовый. В этом случае либо попробуйте найти шарики самостоятельно, либо вызывайте МЧС, сотрудники службы опечатают помещение, займутся сбором ртути и ее нейтрализацией.
Помните, непродолжительное вдыхание воздуха с парами ртути не принесет организму серьезного ущерба, то есть собрать ее можно самостоятельно. Однако длительное нахождение в загрязненном помещении губительно для здоровья, испарения наносят тяжелый вред органам и приводят к страшным последствиям.
Первые шаги
Если ртуть вытекла из градусника, можно попробовать собрать ее самостоятельно. При этом важно соблюдать все необходимые правила безопасности, а также соответствующие рекомендации:
Утилизация ртути из лопнувшего градусника, при условии отсутствия утечки, проводится аналогично. Его полностью помещают в стеклянную банку, закупоривают и отдают в МЧС.
Принципы нейтрализации
Процесс нейтрализации ртути в домашних условиях предполагает скорейший сбор этого металла с соблюдением нескольких правил.
Собранную ртуть ни в коем случае нельзя выбрасывать в мусоропровод, смывать химикат в раковину или унитаз. Банку со ртутью плотно закрывают, оборачивают 1-2 пакетами для исключения утечки и отвозят в МЧС, где ее утилизируют.
Также стоит понимать, что в зависимости от того, где был разбит ртутный термометр, и на какую поверхность попала ртуть, методы ее сбора будут разительно отличаться.
Ртуть
Ртуть — элемент побочной подгруппы второй группы, шестого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 80. Обозначается символом Hg (лат. Hydrargyrum). Простое вещество ртуть (CAS-номер: 7439-97-6) — переходный металл, при комнатной температуре представляет собой тяжёлую серебристо-белую заметно летучую жидкость, пары которой чрезвычайно ядовиты. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй элемент — бром). В природе находится как в самородном виде, так и образует ряд минералов. Чаще всего ртуть получают путём восстановления из её наиболее распространённого минерала — киновари. Применяется для изготовления измерительных приборов, вакуумных насосов, источников света и в других областях науки и техники.
В XIX веке врачи лечили ртутью раны и венерические болезни.
Происхождение названия
Русское название ртути, по одной из версий, — это заимствование из арабского (через тюркские языки); по другой версии, «ртуть» связана с литовским ritu — качу, катаю, происшедшим от индоевропейского рет (х) — бежать, катиться.
Соединения ртути
Ртуть и её соединения применяются в технике, химической промышленности, медицине. Желтый оксид ртути (II) входит в состав глазной мази и мазей для лечения кожных заболеваний. Красный оксид ртути (II) применяется для получения красок.
Хлорид ртути (I), который называется каломель, используется в пиротехнике, а также в качестве фунгицида.
В ряде стран каломель используется в качестве слабительного. Токсическое действие каломели проявляется особенно тогда, когда после приема её внутрь не наступает слабительное действие и организм долгое время не освобождается от этого препарата. Хлорид ртути (II), который называется сулема, является очень токсичным. Сулема применялась в медицине как дезинфицирующее средство, в технике она используется для обработки дерева, получения некоторых видов чернил, травления и чернения стали.
В сельском хозяйстве сулема применяется как фунгицид. Амидохлорид ртути (белый преципитат ртути) входит в состав некоторых мазей. В ветеринарии амидохлорид ртути применяется как средство против паразитарных заболеваний кожи. Нитрат ртути (II) применяется для отделки меха и получения других соединений этого металла. Токсичность нитрата ртути (II) примерно такая же, как и токсичность сулемы. Многие органические соединения ртути используются в качестве пестицидов и средств для обработки семян. Отдельные органические соединения ртути применяются как диуретические средства.
Распространённость в природе
Ртуть относительно редкий элемент в Земной коре со средней концентрацией 0.08 частей на миллион. Однако в виду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2.5 % ртути. Иногда ртуть даже встречается в самородном виде.
В окружающей среде
До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограмма на литр льда. Природные источники, такие как вулканы, составляют примерно половину всех выбросов атмосферной ртути. За оставшуюся половину ответственна деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля главным образом в тепловых электростанциях — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6.8 %, производство цемента — 6.4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1.4 %, ртути (в основном для батареек) — 1.1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1956 году, что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата.
Получение
Ртуть получают сжиганием киновари (Сульфида ртути (II)). Этот способ применяли алхимики древности. Уравнение реакции горения киновари: HgS+O2→Hg+SO2
В России известны 23 месторождения ртути, промышленные запасы составляют 15,6 тыс.тонн (на 2002 год).
Физические свойства
Химические свойства
Ртуть — малоактивный металл (см. ряд напряжений).
При нагревании до 300 °C ртуть вступает в реакцию с кислородом: 2Hg + O2 → 2HgO Образуется оксид ртути(II) красного цвета. Эта реакция обратима: при нагревании выше 340 °C оксид разлагается до простых веществ. Реакция разложения оксида ртути исторически является одним из первых способов получения кислорода.
При нагревании ртути с серой образуется сульфид ртути(II).
Ртуть не растворяется в растворах кислот, не обладающих окислительными свойствами, но растворяется в царской водке и азотной кислоте, образуя соли двухвалентной ртути. При растворении избытка ртути в азотной кислоте на холоде образуется нитрат Hg2(NO3)2.
Из элементов IIБ группы именно у ртути появляется возможность разрушения очень устойчивой 6d 10 — электронной оболочки, что приводит к возможности существования соединений ртути (+4). Так, кроме малорастворимого Hg2F2 и разлагающегося водой HgF2 существует и HgF4, получаемый при взаимодействии атомов ртути и смеси неона и фтора при температуре 4К.
Применение
Ртуть применяется в изготовлении термометров, парами ртути наполняются ртутно-кварцевые и люминесцентные лампы. Ртутные контакты служат датчиками положения. Кроме того, металлическая ртуть применяется для получения целого ряда важнейших сплавов.
Ранее различные амальгамы металлов, особенно амальгамы золота и серебра, широко использовались в ювелирном деле, в производстве зеркал и зубных пломб. В технике ртуть широко применялась для барометров и манометров. Соединения ртути использовались как антисептик (сулема), слабительное (каломель), в шляпном производстве и т.д., но в связи с её высокой токсичностью к концу XX века были практически вытеснены из этих сфер (замена амальгамирования на напыление и электроосаждение металлов, полимерные пломбы в стоматологии).
Сплав ртути с таллием используется для низкотемпературных термометров.
Металлическая ртуть служит катодом для электролитического получения ряда активных металлов, хлора и щелочей, в некоторых химических источниках тока (например, ртутно-цинковых — тип РЦ), в эталонных источниках напряжения (Вестона элемент). Ртутно-цинковый элемент (эдс 1,35 Вольт) обладает очень высокой энергией по объёму и массе (130 Вт/час/кг, 550 Вт/час/дм).
Ртуть используется для переработки вторичного алюминия и добычи золота (см. амальгамная металлургия).
Ртуть используется в качестве балласта в подводных лодках и регулирования крена и дифферента некоторых аппаратов. [источник не указан 236 дней] Перспективно использование ртути в сплавах с цезием в качестве высокоэффективного рабочего тела в ионных двигателях.
Ртуть входит в состав некоторых биоцидных красок для предотвращения обрастания корпуса судов в морской воде.
Ртуть-203 (T1/2 = 53 сек) используется в радиофармакологии.
Также используются и соли ртути:
Иодид ртути используется как полупроводниковый детектор радиоактивного излучения.
Фульминат ртути («Гремучая ртуть») издавна применяется в качестве инициирующего ВВ (Детонаторы).
Бромид ртути применяется при термохимическом разложении воды на водород и кислород (атомно-водородная энергетика).
Некоторые соединения ртути применяются как лекарства (например, мертиолят для консервации вакцин), но в основном из-за токсичности ртуть была вытеснена из медицины (сулема, оксицианид ртути — антисептики, каломель — слабительное и др.) в середине-конце XX века.
Токсикология ртути
Пары́ ртути, а также металлическая ртуть очень ядовиты, могут вызвать тяжёлое отравление. Ртуть и её соединения (сулема, каломель, цианид ртути) поражают нервную систему, печень, почки, желудочно-кишечный тракт, при вдыхании — дыхательные пути (а проникновение ртути в организм чаще происходит именно при вдыхании её паров, не имеющих запаха). По классу опасности ртуть относится к первому классу (чрезвычайно опасное химическое вещество). Опасный загрязнитель окружающей среды, особенно опасны выбросы в воду, поскольку в результате деятельности населяющих дно микроорганизмов происходит образованием растворимой в воде и токсичной метилртути.
Подробнее смотрите статью отравление ртутью.