в чем причина существования двойного электрического слоя мицеллы
Строение мицеллы. Двойной электрический слой (ДЭС), современные представления о строении ДЭС. Факторы, определяющие величину дзета-потенциала.



Мицелла –сложное структурное образование, состоящее из агрегата, потенциалопределяющих ионов и противоионов.
Агрегат вместе с потенциалопределяющими ионами составляет
ядро мицеллы. Ядро мицеллы, обладающее большим зарядом, притягивает ионы противоположного заряда –противоионы(ПИ) из раствора.
Часть противоионов находится в непосредственной близости от ядра, прочно связана с ним за счет адсорбционных и электростатических сил, и образует плотную часть двойного электрического слоя (адсорбционный слой).
Ядро с противоионами плотной части двойного электрического слоя образуют гранулуиликоллоидную частицу. Знак заряда коллоидной частицы определяется знаком заряда потенциалопределяющих ионов.
Коллоидную частицу (гранулу) окружают противоионы диффузного слоя – остальная часть противоионов, подвергающихся броуновскому движению и менее прочно связанная с ядром. В целом образуется мицелла. Мицелла в отличие от коллоидной частицы электронейтральна.
ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ
Из строения мицеллы следует, что у неё на границе раздела двух фаз (твёрдой и жидкой) возникает тонкий поверхностный слой из пространственно разделённых электрических зарядов противополжного знака, который и носит название двойного электрического слоя (ДЭС).
Современные представления о строении ДЭС следующие:
1. ДЭС образован потенциалопределяющими ионами, находящимися на поверхности твердой частицы и эквивалентным количеством противоионов, находящихся в дисперсионной среде вблизи поверхности твердой частицы.
2. Потенциалопределяющие ионы прочно связаны с твердой частицей и равномерно распределены по её поверхности.
3. Противоионы имеют конечные размеры и, следовательно, не могут подходить к твердой поверхности ближе, чем на расстояние одного ионного радиуса.
4. Слой противоионов, компенсирующих заряд твердой поверхности, имеет сложное строение и состоит из двух частей: плотного слоя (адсорбционного слоя или слоя Гельмгольца) и диффузного слоя (слоя Гуи).
5. Адсорбционный слой противоионов примыкает к заряженной поверхности твердой частицы и имеет толщину порядка диаметра гидратированного противоинаd. Те противоионы, которые находятся в этом пространстве, называются адсорбционными противоионами. Они связаны с заряженной твердой частицей двумя видами сил – адсорбционными и электростатическим. Эта связь является настолько прочной, что противоионы адсорбционного слоя перемещаются с твердой частицей, не отрываются от неё, образуя с ней единое кинетическое целое – коллоидную частицу.Противоионы адсорбционного слоя равномерно распределены в слое, поэтому падение потенциала происходит линейно и равно φd.
6. Диффузный слой имеет толщину δ, его образуют те противоины, которые находятся от заряженной поверхности на расстоянии, большем d, но в пределах расстояния δ. Эти противоины притягиваются к частице только электростатическими силами, следовательно, менее прочно, чем противоионы адсорбционного слоя. При движении твердой частицы они от неё отрываются. На противоионы диффузного слоя большое влияние оказывает тепловое движение, которое стремится распределить их равномерно по всему объему системы. Его действие тем сильнее, чем дальше от заряженной поверхности находятся противоионы. Это приводит к установлению динамического равновесия в диффузном слое. Так как противоионы в диффузном слое распределены неравномерно, то падение потенциала в нем (φδ) происходит также неравномерно – по какой-то криволинейной зависимости.
7. Полное падение потенциала ДЭС называется термодинамическим потенциалом φ0:
Таким образом, в ДЭС происходит полная компенсация суммарного заряда твердой поверхности суммарным зарядом противоионов и на границе ДЭС с дисперсионной средой потенциал равен нулю.
Потенциал на плоскости скольжения называется ЭЛЕКТРОКИНЕТИЧЕСКИМ ПОТЕНЦИАЛОМ (или дзета-потенциалом).
В самом термине «электрокинетический потенциал» отражено то, что потенциал существует только в связи с движением, он очень чувствителен к изменению ширины двойного электрического слоя, к изменению распределения ионов в ДЭС. Вместе с тем, дзета-потенциал генетически связан с полным потенциалом (φ0) на границе фаз и обычно составляет часть его. Чем больше размыт двойной слой, тем больше и дзета-потенциал. Если слой предельно сжат, то дзета-потенциал равен 0. Это соответствует изоэлектрическому состоянию, и система не реагирует на электрический ток, тогда как φ0 – потенциал остаётся практически неизменным.
Величина дзета-потенциала определяется:
¨ Величиной термодинамического потенциала φ0 и характером падения потенциала в ДЭС;
¨ Характером движения жидкости вблизи твердой поверхности (он определяет местонахождение плоскости скольжения), который зависит, главным образом, от вязкости среды.
Двойной электрический слой (ДЭС) мицеллы



ДЭС – это слой, возникающийй на границе твердой и жидкой фазы мицеллы, состоящей из пространственно разделенных электрических зарядов противоположного знака. Электрические свойства коллоидных систем определяются наличием ДЭС.
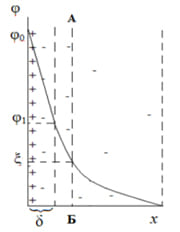
Падение (изменение) электрических потенциалов мицеллы:
АО (φ) – полный (максимальный ) электрический потенциал на границе ядра мицеллы.
АВ (φ1) –падение потенциала в адсорбционном слое.
ВС – падение дэета-потенциала в диффузном слое.
1. От размера ДЭС. Чем больше размыт ДЭС, тем больше дзета-потенциал. Если ДЭС предельно сжат, то ξ = 0. Это отвечает изоэлектрическому состоянию коллоидной частицы, то есть коллоидная частица электронейтральна и не реагирует на электрический ток. При этом электродинамический потенциал φ остается неизменным.
2. От концентрации электролита-стабилизатора – чем ор больше, тем меньше дзета-потенциал
3. От заряда противоиона – чем он больше, тем больше дзета-потенциал.
Устойчивость коллоидных систем падает с понижением дзета-потенциала. Электрокинетические свойства коллоидных частиц играют большую роль в живых организмах. Например, при движении крови в артериях возникает потенциал течения (1-2мВ). Одна из кривой электрокардиограммы связана с ним. При восприятии звука органами слуха также возникает такой потенциал.
Электрокинетические явления
Электрокинетические явления классифицируют на:
1. Электрокинетические явления I-рода – относительное перемещение фазы под действием приложенного напряжения. К ним относятся:
— электрофорез – движение частиц дисперсной фазы в неподвижной дисперсной среде.
— Электроосмос – движение жидкости относительно неподвижной твердой поверхности пористых мембран.
— потенциал оседания (эффект Дорна) – возникновение разности потенциалов при движении частиц в неподвижной жидкости.
— потенциал протекания (эффект Квинке) – возникновение разности потенциалов, при движении жидкости относительно неподвижной твердой поверхности.
Причина электрокинетических явлений – образование двойного электрического слоя на границе раздела дисперсной среды и, как следствие, наличие электрического заряда как у частиц дисперсной фазы, так и у дисперсной среды.
Лекция №5
План лекции:
ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ
На поверхности твердого тела при его контакте с жидкостью самопроизвольно возникает избыточный электрический заряд, который компенсируется противоионами. В результате, на границе Ж-Т возникает ДЭС. Образование ДЭС происходит самопроизвольно, вследствие стремления поверхностной энергии к минимуму и в связи с особыми свойствами границы раздела.
Возникновение на границе электрических зарядов характерно, прежде всего, для золей и суспензий, дисперсная фаза которых формируется из твердых частиц.


ОБРАЗОВАНИЕ ДЭС
Поверхность твердого тела приобретает ионы определенного знака. Эти ионы называют потенциалоопределяющими. К твердой поверхности из жидкой среды притягиваются ионы противоположного знака, их называют противоионами. Возникает ДЭС.
Было предложено несколько теорий образования ДЭС.
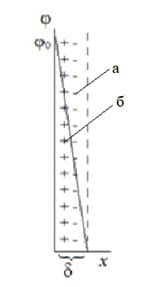
Простейшей из них является модель плоского конденсатора Гельмгольца (5.1.а), согласно которой потенциалоопределяющие ионы и противоионы находятся на молекулярном расстоянии друг от друга, взаимодействие между ними осуществляется только за счет электростатических сил, а падение потенциала между слоями происходит линейно.
Дальнейшее развитие теория ДЭС получила в работах Гуи и Чепмена на основе сопоставления электростатического взаимодействия противоионов с энергией их теплового движения. Согласно модели Гуи и Чепмена противоионы рассматриваются как точечные заряды, не имеющие собственных размеров, расположенные в диффузном слое (5.1.б), а потенциал экспотенциально снижается по мере удаления от поверхности.
ДЭС может возникнуть на частицах, находящихся в полярной среде, и в отсутствии электролитов, вследствие ориентации диполей, а также частичной поверхностной диссоциации полярных частиц, если в жидкой среде присутствуют хотя бы следы воды.
ТЕРМОДИНАМИЧЕСКИЕ СООТНОШЕНИЯ МЕЖДУ ПОВЕРХНОСТНЫМ НАТЯЖЕНИЕМ И ЭЛЕКТРИЧЕСКИМ ПОТЕНЦИАЛОМ ДЭС.
Образование ДЭС происходит самопроизвольно, в результате стремления
системы уменьшить энергию Гиббса поверхностного слоя.
Тогда, в соответствии с обобщенным уравнением первого и второго начал термодинамики (без учета химической энергии), изменение энергии Гиббса на поверхности можно записать следующим образом:
dG = s dS + j d q (5.3)
Полный дифференциал энергии Гиббса :
dG = s dS +S d s + j d q + q d j
Вычитая это уравнение из 5.3, получим:
S d s + q d j = 0 (5.4)
Разделим 5.4 на S (площадь межфазной поверхности) и обозначим q / S через qS (плотность заряда), получим:

I уравнение Липпмана
Если знаки потенциала и заряда совпадают, то поверхностное натяжение уменьшается с увеличением потенциала, если их знаки противоположны, то с увеличением потенциала увеличивается поверхностное натяжение.
Дифференциальная емкость ДЭС, как и любого конденсатора, определяется соотношением:

Дифференцируем 5.5 по j и подставляем в него соотношение 5.6, получаем второе уравнение Липпмана:

II уравнение Липпмана
Это уравнение показывает возможность определения емкости ДЭС, если известна зависимость поверхностного натяжения от потенциала.
Если ДЭС возникает вследствие перераспределения ионов, то для описания адсорбции ионов можно воспользоваться адсорбционным уравнением Гиббса. Если на поверхности адсорбируется катионы:
Поверхностная плотность заряда:
Подставляем это выражение в уравнение Липпмана:
сравниваем 5.8 и 5.9:

Полученное уравнение называется уравнением электродного потенциала Нернста. Приведенный вывод указывает на связь между уравнениями Гиббса и Липпмана и показывает, что потенциалоопределяющие ионы, адсорбируясь, изменяют поверхностное натяжение.
СПЕЦИФИЧЕСКАЯ АДСОРБЦИЯ ИОНОВ
Штерн попытался учесть влияние специфической адсорбции ионов на электрический потенциал, обусловленный действием ковалентных сил дополнительно к электростатическим силам. Так как радиус действия сил такой адсорбции соизмерим с размером ионов, это дает основание учитывать ковалентные силы только для ионов, входящих в плотный слой Гельмгольца.
Плотность поверхностного заряда противоионов можно разделить на две части: плотность заряда qr, обусловленную слоем Гельмгольца и q d диффузного слоя Гуи.
Общая поверхностная плотность заряда ДЭС:
Штерн предположил, что поверхность имеет определенное число адсорбционных центров, каждый из которых взаимодействует с одним противоионом.
Константа такой квазихимической реакции равна фактору Больцмана, в котором общий адсорбционный потенциал составляет сумму адсорбционных потенциалов электростатического и специфического взаимодействия:

Такой подход позволил Штерну получить уравнение для плотности поверхностного заряда в слое Гельмгольца:

При малых концентрациях электролита можно пренебречь единицей в знаменателе.
Теория Штерна позволяет рассчитать заряд в плотном и диффузном слоях.
Из теории Ш. следует, что лучше адсорбируются и ближе подходят к Пв менее гидратированные ионы.
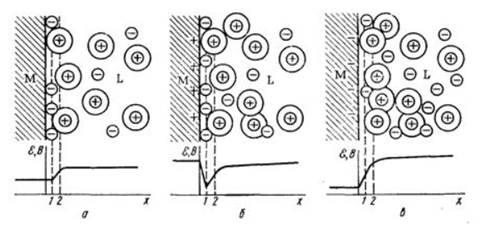
Сильно адсорбирующиеся ионы в плотном слое способны создать избыточный заряд со знаком заряда противоионов. Это явление называется перезарядкой. (рис. 5.2)
Рис. 5.2. Изменение потенциала поверхности при ее перезарядке.
При перезарядке j o и j d имеют разные знаки. Общую поверхностную плотность заряда можно представить в виде разности между величинами адсорбции потенциалоопределяющих ионов разного знака :
Пример:
n-число потенциалопределяющих ионов
x-число противоионов в диффузной части
В результате преобладающей адсорбции одного и этих ионов поверхность оксида приобретает соответствующий знак заряда поверхности. Например: SiO2 обладает кислотными свойствами, поэтому его поверхность заряжена отрицательно:
FeO имеет основные свойства, его поверхность будет заряжена положительно:
В дисперсионных системах ДЭС возникает на поверхности частиц.
Частицу дисперсной фазы в гетерогенно-дисперсной системе вместе с ДЭС называют мицеллой.
Строение мицеллы можно показать той же формулой, что и строение ДЭС.
Агрегат + потенциалопределяющие ионы = ядро.
Ядро + противоионы = гранула.
Гранулу окружают противоионы диффузного слоя. Вся мицелла электронейтральна.
В чем причина существования двойного электрического слоя мицеллы
ФИЗИЧЕСКАЯ И КОЛЛОИДНАЯ ХИМИЯ
Конспект лекций для студентов биофака ЮФУ (РГУ)
4.2 КОЛЛОИДНЫЕ СИСТЕМЫ
4.2.4 Двойной электрический слой и электрокинетические явления
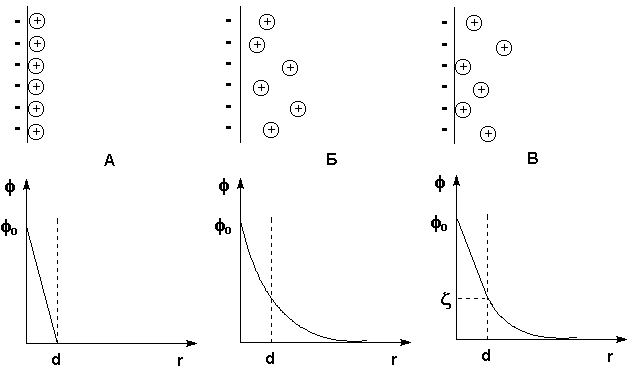
При рассмотрении строения мицеллы было показано, что на поверхности лиофобных коллоидов образуется двойной электрический слой. Первая теория строения ДЭС была развита Гельмгольцем и Перреном; в их представлении двойной электрический слой подобен плоскому конденсатору, внутренняя обкладка которого находится в твердой фазе, а внешняя – в жидкости параллельно поверхности ядра на расстоянии порядка диаметра иона. Потенциал электрического поля внутри ДЭС φ в этом случае линейно уменьшается с увеличением расстояния от поверхности r (рис. 4.12а).
Рис. 4.12 Строение ДЭС: а) – по Гельмгольцу и Перрену, б) – по Гуи и Чепмену, в) – по Штерну. Вверху – схема расположения противоионов, внизу – зависимость потенциала от расстояния
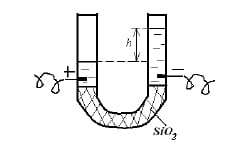
Рис. 4.13 Схема опыта по электрофорезу
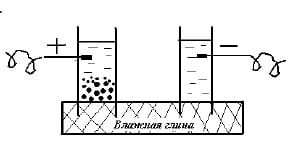
Рис. 4.14 Схема опыта по электроосмосу
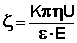
Обратные электрофорезу и электроосмосу электрокинетические явления (т.н. электрокинетические явления второго рода) называются соответственно потенциал седиментации и потенциал протекания. Потенциал седиментации (эффект Дорна) – возникновение разности потенциалов при вынужденном движении дисперсной фазы относительно неподвижной дисперсионной среды (например, под действием силы тяжести). Потенциал протекания (эффект Квинке) есть явление возникновения разности потенциалов при движении дисперсионной среды относительно неподвижной дисперсной фазы (например, при продавливании электролита через пористое тело).
Двойной электрический слой (ДЭС): понятие и теории строения
Содержание:
1. Электрокинетические явления.
В начале XIX века Рейс, проводя электролиз воды, обнаружил явления электрокинетики.
В одном из опытов Рейсс заметил, что если дно U-образной трубки наполнить кварцем, то при наложении разности потенциалов на систему совершается смещение столба воды в область «-» электрода. Явление получило название электроосмос.
После этого Рейс сделал схему из двух стеклянных трубок, заполненных водой и опущенных концами в мокрую глину. Под действием электрического тока глина передвигалась к электроду, имеющему заряд «+», что получило название «электрофорез».
В 1879 г. Дорном был открыт потенциал седиментации. Разность потенциалов возникала, когда частички кварца свободно осаждались в столбе жидкости.
Итак, различают электрокинетические явления двух родов:
• I рода, в которых происходит взаимное перемещение фаз при воздействии электрического поля;
• II рода, в которых разность потенциалов возникает за счет перемещения двух фаз.
Присутствие одноименно заряженных частиц на поверхности дисперсной фазы и противоположно заряженных частиц на поверхности дисперсной среды и есть причина возникновения электрокинетических явлений. Совокупность же всех зарядов, сконцентрированных на границе раздела фаз, образует структуру, называемую двойным электрическим слоем (ДЭС).
2. Механизмы образования ДЭС.
Формирование ДЭС происходит в результате стремления системы уменьшить энергию Гиббса межфазного слоя. Межфазный слой – это слой, в котором происходит взаимодействие двух различных фаз, в результате соприкосновения которых свойства поверхности каждой фазы станут отличаться от их индивидуальных свойств.
Различают два типа ДЭС, в которых:
ДЭС будет играть весомую роль при:
Выделяют несколько механизмов образования ДЭС:
а) Формирование ДЭС при наступлении электрохимического равновесия, посредством прохода заряженных частиц между фазами. Основные разновидности этого механизма формирования ДЭС:
• Переход заряженных частиц на границе металл – газ. В этом варианте происходит переход электронов с поверхности металла в газовую фазу, из-за чего поверхность металла заряжается положительно, а со стороны газовой фазы образуется электронное облако. Появляется препятствие для дальнейшего перехода электронов (положительный заряд поверхности металла), в результате чего наступает равновесное состояние.
• В системе «малорастворимое соединение – жидкость» переход заряженных частиц будет происходить в результате поверхностного растворения частицы малорастворимого соединения, при чем в жидкую фазу преимущественно будет выполняться переход тех ионов, электрохимический потенциал которых выше. В данном случае равновесие будет выражаться электрохимическими потенциалами:
При установлении равновесия происходит переход ионов из фазы с большим электрохимическим потенциалом, в фазу с меньшим потенциалом. При этом возникает межфазный скачок потенциалов, который препятствует дальнейшему переходу ионов. В результате этого равновесие будет выражаться уравнением
б) ДЭС может формироваться за счет адсорбции ионов из раствора, этот механизм формирования можно разделить на несколько вариантов:
• В соответствии с правилом Фаянса – Панета ионы могут адсорбироваться на поверхности частиц, сообщая им соответствующий заряд, если эти ионы входят в состав кристаллической структуры этих частиц. Около заряженной поверхности будут концентрироваться противоположно заряженные ионы (противоионы).
• Заряд поверхности может образовываться за счет избирательной адсорбции ионов из растворов, не входящих в состав твердой фазы. В пример можно привести раствор хлорида натрия, в котором на металлах адсорбируются хлорид-ионы и придают его поверхности «-» заряд, а ионы натрия, в свою очередь, являются противоионами создавая с хлорид-ионами ДЭС
в) ДЭС может создаваться в том случае, если поверхность образована двумя фазами, молекулы которых не могут диссоциировать, но обладают дипольными моментами. Согласно правилу Кёна, из двух соприкасающихся фаз, не способных обмениваться зарядами, положительно заряжается та фаза, которая имеет большую диэлектрическую проницаемость.
3. Модели строения двойного электрического слоя.
Авторы моделей придерживались следующих положений:
Основное различие между моделями строения ДЭС заключается в постепенном усложнении представлений о структуре слоя противоионов.
3.1 Модель Гельмгольца – Перрена.
В конце XIX века Г. Гельмгольц предложил первую модель строения ДЭС, далее ее развивал Ж.Б. Перрен, но уже в 1904 г.
Модель Гельмгольца – Перрена основывалась на представлении ДЭС как плоского конденсатора, в котором обкладки представлялись как два ряда ионов (потенциалопределяющих ионов и противоионов) (рисунок 1). Потенциал в ДЭС линейно уменьшался с расстоянием, как в плоском конденсаторе, а плотность заряда на поверхности η0 определялась уравнением:
где:
δ – толщина ДЭС;
ε0ε – диэлектрическая проницаемость среды между обкладками конденсатора;
(ε0ε /δ)= С – емкость плоского конденсатора;
φ0 – потенциал поверхности относительно объема раствора.
Рисунок 1. Схема строения двойного электрического слоя по модели Гельмгольца – Перрена: а) слой потенциалопределяющих ионов, б) слой противоионов.
Модель Гельмгольца – Перрена подтверждена несколькими экспериментальными фактами:
У этой модели есть и ряд недостатков:
3.2 Модель Гуи – Чапмена.
В начале XX века Л. Гуи и С. Чампен (Чэпмен) предположили более сложную структуру ДЭС (рисунок 2), предположив, что слой противоионов имеет диффузное строение и обусловлен противоположно направленным действием двух факторов:
По закону Больцмана концентрация противоионовв диффузном слое изменяется, за счет установления динамического равновесия:
где:
ciX – концентрация i-иона в ДЭС на расстоянии xот поверхности;
ci0 – концентрация i-иона за пределами ДЭС;
Z – заряд иона;
F – число Фарадея (96500);
φ – потенциал на расстоянии x от поверхности;
R – универсальная газовая постоянная (8,31);
Е – абсолютная температура.
Если взять в пример плоский конденсатор (модель Гельмгольца – Перрена), то все противоионы будут располагаться около поверхности (при температуре близкой к абсолютному нулю), так как диффузность слоя будет определяться тепловым движением ионов.
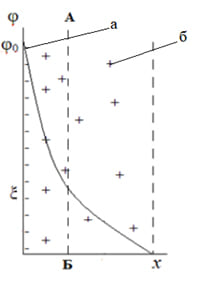
Вторая представленная модель позволила описать явления электрокинетики. При перемещении твердой и жидкой фаз относительно друг друга плоскость скольжения (АБ) лежит внутри двойного слоя, поэтому на границе скольжения φ≠0. Потенциал в плоскости скольжения соответствует той доле заряда поверхности, которая нескомпенсирована противоионами и вызывает перемещение фаз при наложении электрического поля. Часть общего скачка потенциала в двойном электрическом слое, которая приходится на границу скольжения и проявляется в электрокинетических явлениях, называется электрокинетическим, или ξ – потенциалом.
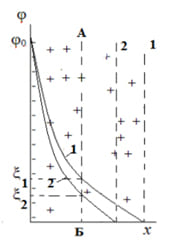
Можно описать изменение структуры ДЭС при повышении концентрации индифферентного электролита (рисунок 3). Введение индифферентного электролита повышает концентрацию противоионов в диффузном слое. Но, так как на компенсацию поверхностных зарядов потенциалопределяющих ионов необходимо то же количество противоионов, что и до введения электролита, часть противоионов окажется в избытке и это приведет к таким изменениям как:
или, с учетом уравнения Больцмана (2):
Если ДЭС считать плоским и учитывать изменение потенциала только по одной координате, х, то:
Подставив (4) в уравнение (5), получим уравнение Пуассона – Больцмана:
В основе данной модели лежит уравнение (6), так как из него можно получить уравнение, выражающее зависимость потенциала от свойств и концентрации электролита:
При двойном интегрировании уравнения (6) в пределах от 0 до х и от φ0 до φх, получаем:
С увеличением расстояния потенциал ДЭС уменьшается по кривой, это определяется уравнением (8).
Емкость ДЭС разделяют на:
Недостатки модели Гуи-Чапмена:
Все эти недостатки были учтены в теории Штерна, которая стала новым этапом в развитии представлений о двойном электрическом слое.
3.3 Модель Штерна.
Дальнейшее изучение строения ДЭС проводил физик О.Штерн, который ввел два условия о его структуре:
В своей схеме Штерн объединил две прошлые модели и ввел представления о плотном и диффузионном слое (рисунок 4). Часть противоионов, притягиваясь к заряженной потенциалопределяющими ионами поверхности электростатическими и адсорбционными силами, образует с потенциалопределяющими ионами плотный слой – плоский конденсатор. В плотном слое потенциал падает с расстоянием от поверхности практически по прямой, как в плоском конденсаторе. Остальные противоионы, в количестве необходимом для полной компенсации поверхностного заряда, образуют диффузный слой, в котором потенциал падает по экспоненте от φ1 до φ=0. Плоскость скольжения АБ расположена в диффузной части ДЭС.
Уравнения (3) – (6) так же применимы и для модели Штерна, но возникает еще одно условие: функция расстояния х= δ описывает распределение противоионов.
После интегрирования уравнения Пуассона – Больцмана в этом случае справедливо уравнение:
Данные уравнения не берут во внимание адсорбционные силы, а выражение (9) называется уравнением Гуи. И если расстояние отсчитывать от начала диффузионного слоя ДЭС, то уравнение (8) преобразуется в:
С ростом температуры растет энергия теплового движения, а с увеличением диэлектрической проницаемости среды усиливается диссоциация электролитов. Оба фактора увеличивают толщину ДЭС.
В отсутствии электрического поля происходит перенос ионов на поверхность под влиянием адсорбционных сил, такое явление Штерн назвал адсорбционным потенциалом иона (Фi). Это считается главным достижением данной модели.
По модели Штерна плотный слой заряжается за счет заряда ионов при адсорбции:
При учете этих факторов Штерн вывел уравнение для плотного слоя Гельмгольца:
Таким образом, модель Штерна позволяет рассчитать заряд как в плотном, так и в диффузионном слое.
Модель Штерна позволила решить ряд вопросов, ответы на которые не смогли дать предыдущие теории строения ДЭС:
Зависимость структуры двойного слоя за счет введения не- и индифферентных электролитов;
3.4 Модель Грэма.
Грэм развил предыдущие модели и выделил три части в ДЭС (рисунок 5):
В первой плоскости Гельмгольца находятся только специфически адсорбирующиеся анионы, причем их поверхностная концентрация растет при переходе от незаряженной поверхности (рисунок 5, а) к заряженной положительно (рисунок 5, б). При достаточно отрицательном заряде поверхности (рисунок 5, в) во внутреннем слое Гельмгольца остается лишь растворитель, и заряд его становится равным нулю. В этих условиях ДЭС электрически равен двум последовательно включенным конденсаторам.
Грэм разработал метод расчета кривых емкости ДЭС, где dη0/dφ0 при различных концентрациях электролита, так как он посчитал, что данная ёмкость будет зависеть не от концентрации раствора.
Таким образом модель Грэма может рассматриваться как модель, отражающая основные черты и особенности структуры ДЭС «металл – электролит».
3.5 Модель Фрумкина при адсорбции органических веществ.
Модель Фрумкина была разработана в 1926 году, она была рассмотрена в целях определения формы электрокаппилярных кривых и влияния органических веществ на ДЭС.
Адсорбцию органических соединений можно рассматривать как замену в двойном слое воды на органическое вещество. Так как размеры органических молекул больше, чем молекул воды, то, как это следует из теории плоского конденсатора, удельная емкость воды будет больше емкости исходного вещества в растворе, такая замена вызывает необходимость отвода заряда с обкладок конденсатора.
В случае перехода от исходного раствора к раствору с органическим веществом возникает разность потенциала равная сдвигу потенциала на электрокаппилярной кривой. Все это происходит так как молекулы органического вещества обладают дипольным моментом.
По версии Фрумкина в данном случае двойной слой напоминает два параллельно присоединенных конденсатора (это является одним из его исходных положений). В одном из конденсаторов будет находиться вода, между обкладками, а у другого – органические вещества. Другое положение теории связано с выбором изотермы адсорбции.
В качестве еще одного исходного предположения Фрумкин допускает, что адсорбция органического вещества подчиняется уравнению Ленгмюра:
В согласии с законом распределения Больцмана, можно записать в виде:
Из основного уравнения электрокаппилярности следует, что снижение пограничного натяжения σ под влиянием адсорбции органического вещества при данном δ равно:
Из данных уравнений Фрумкин вывел уравнение новой изотермы:
а – константа аттракционного взаимодействия.
Полученное уравнение назвали изотермой Фрумкина.
3.6 Модель Алексеева–Попова–Колотыркина (АПК).
На случай смешанных растворов была разработана модель Алексеева – Попова – Колотыркина типа:
В 60-х годах ХХ века Пейн сделал открытие, которое не описывалось ни одним физическим явлением. В системах типа нитрата калия зависимость энергии от заряда носила линейный характер, но, если рассмотреть границу Hg/H2О (xM NH4NO3 + (1–x)M NH4F), то можно было увидеть, что эта зависимость приобретала параболический вид.
После 20 лет попыток решения этой проблемы был дан ответ. В смешенных растворах выделяют скачок потенциала, а не заряд электрода. Это легло в основу модели АПК.
В смешанных растворах с постоянной ионной силой типа:
При значениях m выше m≤0.2, отсутствуют экспериментальные данные для количественного определения адсорбции ионов.
При использовании модели АПК некоторые параметры находят из экспериментальных данных. При этом она очень хорошо описывает некоторые свойства ДЭС при специфической адсорбции, но только на идеально поляризуемых электродах.
4. Влияние различных факторов на структуру ДЭС.
4.1 Влияние индифферентных и неиндифферентных электролитов.
Влияние концентрации индифферентного электролита на структуру ДЭС показано в разделе 3.2. При увеличении концентрации электролита увеличивается заряд противоионов, это приводит к уменьшению ξпотенциала. Учитывая все это уравнение (9) преобразуется в:
Уравнение (17) показывает, что при неизменном заряде поверхности η0 увеличение концентрации индифферентного электролита с и заряда противоионов z приводит к снижению потенциала φ1. При этом происходит уменьшение диффузионного слоя, снижение ξ-потенциала.
Неиндифферентным электролитом называют электролит, в котором хотя бы один ион может влиять на потенциал поверхности φ0, то такой ион будет называться потенциалопределяющим. При увеличении заряда поверхности η0, то также повышается и ξ-потенциал. Появление этих двух факторов приводит к зависимости ξ-потенциала от с: при малых с главным фактором является рост адсорбции потенциалопределяющих ионов, η0 и ξ-потенциал растут, затем наступает насыщение поверхности, рост заряда прекращается и главным фактором выступает сжатие диффузного слоя за счет повышения концентрации противоионов, ξ-потенциал уменьшается.
4.2 Явление перезарядки ДЭС под влиянием многозарядных противоионов.
Явление перезарядки ДЭС возникает в плотном слое посредством того, что многозарядные анионы могут превысить заряд потенциалопределяющих ионов. Так как происходит перезарядка, то потенциалы в двух слоях ДЭС приобретают отличные друг от друга знаки. Так как происходит смена знаков потенциалов, то изменяется и ξ-потенциал. Вследствие этого явления изменяется направление движения частиц дисперсной фазы.
4.3 Влияние температуры, рН и других факторов.
Увеличение температуры приведет к нескольким факторам:
5. Заключение.
Первой теорией строения ДЭС была теория Гельмгольца – Перрена: ДЭС состоит из двух плоских зарядов и взаимодействующих между собой только за счет электростатических сил притяжения. Структура подобна плоскому конденсатору, падение потенциала между слоями происходит линейно.
Модель Гуи – Чэпмена предполагала диффузное расположение противоионов, находящихся под воздействием сил, действующих в противоположных направлениях: электростатических сил притяжения и сил теплового движения ионов, приводящих к диффузии и размыванию внешнего слоя. Теория вводит понятие диффузионного слоя, ионы рассматриваются как точечные заряды, не имеющие собственных размеров.
Грэм усовершенствовал модель Штерна и разделил ДЭС на три части: внутренний плотный слой, или же внутренняя плоскость Гельмгольца, внешний плотный слой и диффузионный слой. В этом случае ДЭС представляется в виде двух последовательно соединенных конденсаторов.
Фрумкин изучал строение ДЭС при адсорбции органических соединений. В этом случае ДЭС представлял собой два параллельно подсоединенных между собой конденсатора, в одном из них между обкладками находятся молекулы воды, в другом – молекулы органического вещества.