в чем причина различного поведения спиртов в воде
Характеристика спиртов
Опыт 1. Растворимость спиртов в воде.
Условия выполнения работы:
В две пробирки налили примерно по 2 мл этилового и изоамилового спиртов. Добавили в каждую из пробирок по 3 мл воды и взболтали. Наблюдаем, что этиловый спирт растворился, а изоамиловый нет, и при стоянии образует верхний маслянистый слой, так как его плотность меньше плотности воды (0,8 г/мл). Причиной различного поведения спиртов в воде является природа веществ.
Опыт 2. Получение глицерата меди.
Условия выполнения работы:
В пробирку налили 1 мл 10%-го раствора сульфата меди (II) и добавили немного 10%-го раствора гидроксида натрия. Наблюдаем выпадение голубого осадка Cu(OH)2. К полученному осадку добавили по каплям глицерин, смесь взболтали. Наблюдаем растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнения реакции взаимодействия сульфата меди (ΙΙ) с гидроксидом натрия:
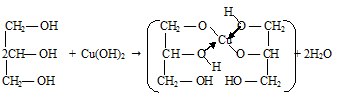
Качественной реакцией на многоатомные спирты является реакция с гидроксидом меди (ΙΙ). Например, при действии глицерина на осадок гидроксида меди (ΙΙ) н аблюдается растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнение реакции имеет вид:
Этиловый и изоамиловый спирты не будут реагировать с Cu(OH)2, так как это качественная реакция на многоатомные спирты.
Опыт 3. Окисление этилового спирта хромовой смесью.
Условия выполнения работы:
Налили в пробирку 2 мл 5%-го раствора дихромата калия, 1 мл 20%-го раствора серной кислоты и 0,5 мл этилового спирта, получили смесь оранжевого цвета. Пробирку нагрели. Наблюдаем изменение цвета раствора на зелёный и чувствуем характерный запах уксусного альдегида.
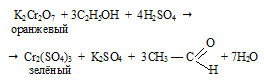
В данной реакции применяют серную кислоту, а не соляную, потому что соляная кислота может окислиться.
Характеристика спиртов
Опыт 1. Растворимость спиртов в воде.
Условия выполнения работы:
В две пробирки налили примерно по 2 мл этилового и изоамилового спиртов. Добавили в каждую из пробирок по 3 мл воды и взболтали. Наблюдаем, что этиловый спирт растворился, а изоамиловый нет, и при стоянии образует верхний маслянистый слой, так как его плотность меньше плотности воды (0,8 г/мл). Причиной различного поведения спиртов в воде является природа веществ.
Опыт 2. Получение глицерата меди.
Условия выполнения работы:
В пробирку налили 1 мл 10%-го раствора сульфата меди (II) и добавили немного 10%-го раствора гидроксида натрия. Наблюдаем выпадение голубого осадка Cu(OH)2. К полученному осадку добавили по каплям глицерин, смесь взболтали. Наблюдаем растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнения реакции взаимодействия сульфата меди (ΙΙ) с гидроксидом натрия:
Качественной реакцией на многоатомные спирты является реакция с гидроксидом меди (ΙΙ). Например, при действии глицерина на осадок гидроксида меди (ΙΙ) н аблюдается растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнение реакции имеет вид:
Этиловый и изоамиловый спирты не будут реагировать с Cu(OH)2, так как это качественная реакция на многоатомные спирты.
Опыт 3. Окисление этилового спирта хромовой смесью.
Условия выполнения работы:
Налили в пробирку 2 мл 5%-го раствора дихромата калия, 1 мл 20%-го раствора серной кислоты и 0,5 мл этилового спирта, получили смесь оранжевого цвета. Пробирку нагрели. Наблюдаем изменение цвета раствора на зелёный и чувствуем характерный запах уксусного альдегида.
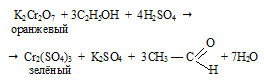
В данной реакции применяют серную кислоту, а не соляную, потому что соляная кислота может окислиться.
Т 1: Реакция серебряного зеркала
Практическая работа № 4
Спирты
Т 1: Растворимость спиртов в воде
Приборы и материалы:пробирки химические,этиловый спирт 
вода
Ход работы:
1. В определённые пробирки наливаем 1-2 мл/г этилового спирта, во вторую пробирку наливаем другого спирта.
2. К ним добавляем 2-3 мл/г воды и взбалтываем.
3. Отмечаем, что этиловый спирт полностью растворился в воде, а изоамиловый спирт отделяется при отстаивании в виде масляного слоя над водой.
Вопросы:
1. В чём причина различного «поведения» спиртов в воде?
2. Почему изоамиловый спирт отслаивается над водой?
3. Какие органические жидкие вещества при смешивании с водой будут отслаиваться над водой?
Ответы на вопросы:
1. Причина различного «поведения» спиртов в воде зависит от особенности химической природы спиртов, прежде всего проявляется в строении молекул.
2. Причина в том, что при увеличении числа метиловых групп реакции окисления замедляются.
3. Бутиловый спирт, изоамиловый спирт, пропиловый спирт, цетиловый спирт, амиловый спирт, пропаргиловый спирт.
Т 2: Получение глицерата меди
Приборы и материалы:пробирки химические, 10% раствор сульфата меди


глицирин
Ход работы:
1. В пробирку наливаем около 1 мл/г 10% раствора судьфата меди, сюда же добавляем 1 мл/г 10% раствора гидроксида натрия до образования голубого осадка гидроксида меди.
2. К полученному осадку добавили по каплям глицерин, взболтали смесь.
3. Отмечаем превращение голубуго осадка в растворе тёмно-синего цвета.
Вопросы:
1. Какая реакция лежит в основе получения гидроксида меди? Напишите уравнение реакции.
2. Почему при добавлении глицерина к осадку гидроксида меди осадок растворяется? С чем связано интенсивное окрашивание раствора? Напишите уравнение взаимодействия глицерина с гидроксидом меди.
3. Будут ли этиловый и изоамиловый спирты реагировать с гидроксидом меди?
Ответы на вопросы:
1.
2. Глицерин как многоатомный спирт образовывает растворимые в воде ярко-синие комплексные соединения при взаимодействии со свеже-полученным осадком 

| 


3. Нет, не будут, потому что свеже-осаждённый гидроксид меди реагирует только с многоатомными спиртами.
Т 3: Окисление этилового спирта дихроматом калия
Приборы и материалы:пробирка химическая, 5% раствор дихромата
калия, 20% раствор серной кислоты, спиртовая
Ход работы:
1. В пробирке смешиваем 2 мл/г 5% раствора дихромата калия, 1 мл/г 20% раствора серной кислоты, 0,5% мл/г этилового спирта.
2. Отмечаем цвет раствора.
3. Осторожно нагреваем смесь на пламени спиртовой горелки до начала изменения цвета, при этом ощущается запах уксусного альдегида, образовавшийся в результате реакции.
Вопросы:
1. Почему цвет раствора меняется с оранжевого до синевато-зелёного? Напишите уравнение окисления этилового спирта.
2. Можно ли заменить серную кислоту в данной реакции на соляную?
Ответы на вопросы:
1.
2. Да, я считаю, что можно заменить серную кислоту на соляную.
Практическая работа № 5
Альдегиды и Кетоны
Т 1: Реакция серебряного зеркала
Приборы и материалы:пробирка химическая ПХ-16, формалин
(формальдегид), аммиачный раствор оксида
серебра, спиртовая горелка
Ход работы:
1. В пробирку с 1 мл/г формальна добавляем несколько капель аммиачного раствора оксида серебра.
2. Пробирку слегка нагреваем, выделяющееся серебро выпадает или в виде чёрного осадка или в виде блестящего зеркального налёта.
Вопросы:
1. Что наблюдается в пробирке?
2. Почему поверхность стекла становится зеркальной?
Ответы на вопросы:
1. Наблюдается выделение газа и образование «зеркала».
2. Потому что на ней оседает металлическое серебро.
В чём причина различного поведения спиртов в воде?
Спирты по сути своей гидрофобны.
Поведение спирта при попадании в воду обусловлено по большей части водородной связью.
У спиртов в основном молекулярная масса на довольно высоком уровне.
Чтобы понять принцип поведения определенного спирта в воде достаточно добавить несколько капель спирта сверху и подождать.
Прежде, чем покупать водку, обязательно надо обращать внимание, еще и на внешний вид бутылки, этикетка не должна отклеиваться, не должно быть осадка и розоватого цвета.
Прогресс не стоит на месте и в скором будущем, наверное, стоит ожидать появления Наносамогонщиков.
Если бы все многочисленные виды водки содержали только спирт и чистую воду в определенной пропорции, то не было бы никакой разницы во вкусе разных видов водки. Однако знатоки утверждают, что это далеко не так. А это значит, что в водке присутствуют, хотя и в небольших количествах, и другие компоненты. Судя по справочнику
в 100 г водки содержится 0,1 г «золы» (в других справочника- 0,01 г; вероятно, это неорганические вещества, а не та зола, которая в печке), а также 0,4 г углеводов, как правило, в виде сахара. Также в 100 г водки содержится 1 мг (0,001%) калия, 1 мг кальция, 10 мг натрия, 5 мг фосфора. А также очень малые (следовые) количества витаминов В1 и В2..
Урок по химии на тему » Практическая работа. Спирты.» (10 класс)
Выбранный для просмотра документ Пр. р. спирты.docx
Практическая работа (УМК О.С. Габриелян)
Цель работы: изучить свойства одноатомных и многоатомных спиртов на примере этанола и глицерина: Инструкция по технике безопасности
Работать с этанолом, глицерином необходимо так, чтобы не допустить попадания их на кожу, так как они могут вызвать ожоги.
Щёлочь (гидроксид натрия) – едкое вещество. Работать с ним необходимо аккуратно.
Зажжённую спиртовку нельзя переносить с места на место, нельзя также зажигать одну спиртовку непосредственно от другой. Для зажигания спиртовки пользуйтесь спичками.
Гасить спиртовку можно только одним способом – накрыть пламя фитиля колпачком. Колпачок должен находиться всегда под рукой.
Начнём оформление работы. Запишите название работы. Какую проблему вам необходимо решить, выполняя данную работу? Запишите.
Какую гипотезу вы выдвигаете? Запишите.
Задачи работы:… Запишите
Начертите и заполните таблицу 1.
Уравнение реакции и выводы
Реактивы: этанол, изоамиловый спирт, вода.
Опыт 2. Окисление этилового спирта оксидом меди(II).
Реактивы: этанол, медная проволока.
Оборудование: пробирка, спиртовка, спички.
Методика. В чистую пробирку налейте 1мл этанола, раскалите на спиртовке медную проволоку, погрузите в этанол медную проволоку. Повторите процедуру несколько раз. Какой ощущается запах?
При опускании раскалённой медной проволоки в этанол происходит реакция дегидрирования и спирт превращается в этаналь.
Опыт 3. Окисление этилового спирта хромовой смесью
Реактивы: 5%-го раствор дихромата калия, этиловый спирт, серная кислота.
Методика. Налили в пробирку 2 мл 5%-го раствора дихромата калия, 1 мл 20%-го раствора серной кислоты и 0,5 мл этилового спирта, получили смесь оранжевого цвета. Пробирку нагрели. Наблюдаем изменение цвета раствора на зеленый и чувствуем характерный запах уксусного альдегида.
Опыт 4. Получение глицерата меди Качественная реакция на глицерин
Заключение. В результате работы я решил(а) следующую проблему…, доказав что…