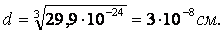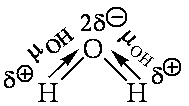в чем измеряется энергия связи
В чем измеряется энергия связи
Масса ядра измеряется в атомных единицах массы (а.е.м). За одну атомную единицу массы принимается 1/12 часть массы нейтрального атома углерода 12 С:
А.е.м. выражается через энергетические единицы:
Масса ядра всегда меньше суммы масс составляющих его нуклонов.
Избыток масс Δ связан с массой атома Mат(A,Z) и массовым числом A соотношением:
Энергия связи ядра Eсв(A,Z) это минимальная энергия, необходимая, чтобы развалить ядро на отдельные, составляющие его нуклоны.
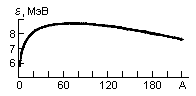
Рис. 1
Удельная энергия связи ядра ε(A, Z) это энергия связи, приходящаяся на один нуклон
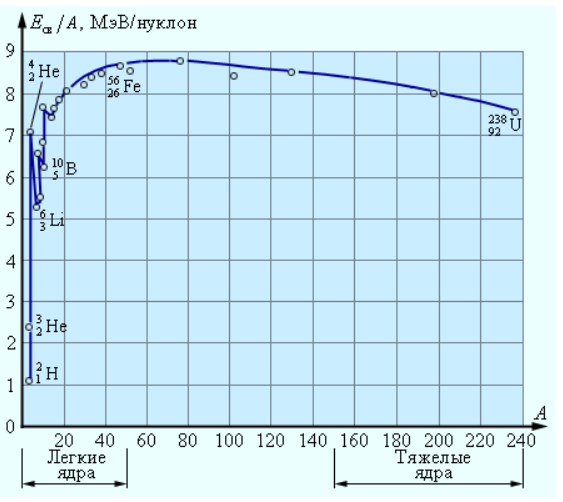
На рис. 1 показана зависимость удельной энергии связи ядра ε от числа нуклонов A. Видно, что наиболее сильно связаны ядра в районе железа и никеля (A
55-60). Такой ход зависимости ε(A) показывает, что для легких ядер энергетически выгодны реакции синтеза более тяжелых ядер, а тяжелых − деление на более легкие осколки.
Используется также понятие энергия связи (отделения) частицы в ядре
Энергия отделения нейтрона
Энергия отделения протона
Энергия отделения α-частицы
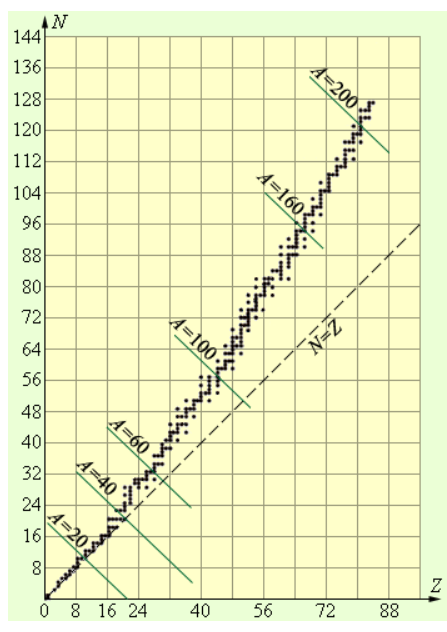
Наиболее устойчивы ядра, у которых магическое число протонов или нейтронов.
n
p
Подробно о массовых формулах см. Н.Н. Колесников. Массы ядер и массовые формулы.
Энергия связи ядер
Устойчивость атомных ядер основывается на действии неких колоссальных многократно превосходящих силы кулоновского отталкивания протонов сил, удерживающих нейтроны и протоны внутри ядра.
Приведенные выше силы, удерживающие нуклоны в ядре, носят название ядерных. Они представляют собой проявление самого интенсивного из всех известных в физике видов взаимодействия, то есть, так называемого сильного взаимодействия.
Основываясь на опытных данных, можно заявить, что протоны в ядре в отношении сильного взаимодействия ведут себя ровно так же, как и нейтроны. Из этого факта исходит вывод о том, что ядерные силы не имеют зависимости от наличия или отсутствия у частиц электрического заряда.
Дефект массы
Важнейшее место в ядерной физике занимает понятие энергии связи ядра.
Энергия связи атомного ядра эквивалентна минимальной необходимой для полного расщепления ядра на отдельные частицы энергии. Опираясь на закон сохранения энергии, можно сказать, что энергия связи равняется выделяющейся в процессе образования ядра из отдельных частиц энергии.
Энергия связи каждого ядра может быть определена при помощи точного измерения его массы. В наше время физики обладают знаниями, позволяющими им измерять массы частиц, будь то электроны, протоны, нейтроны, ядра или что-то подобное, с чрезвычайно высокой точностью.
Такие измерения доказывают, что масса каждого конкретного ядра M я в любом случае меньше совокупности масс входящих в его состав протонов и нейтронов:
Следующее выражение разности масс:
Носит название дефекта массы.
Ядерные превращения
Оба приведенных процесса выделяют колоссальное количество энергии. В условиях современной физики, как деление тяжелых ядер на более легкие, так и слияние легких в тяжелые осуществлены на практике: реакции деления и термоядерные реакции.
Стоит отметить, что в сравнении с делением тяжелых элементов синтез легких провоцирует излучение энергии на один нуклон большее примерно в шесть раз.
В чем измеряется энергия связи
Ковалентная химическая связь имеет определенные качественные или количественные характеристики. К ним относятся:
4.1. Насыщаемость ковалентной связи
Атом не может образовать бесконечное число ковалентных связей, оно вполне определенное. Максимальное число связей, которое может образовать атом, определяется числом его валентных электронных орбиталей. Это и определяет насыщаемость ковалентной связи.
4.2. Энергия связи
Энергия связи – это энергия, которая выделяется при образовании молекулы из одиночных атомов. Энергия связи отличается от ΔHобр. Теплота образования – это энергия, которая выделяется или поглощается при образовании молекул из простых веществ. Так:
Энергии связей в молекулах, состоящих из одинаковых атомов, уменьшаются по группам сверху вниз (табл. 4.1).
По периоду энергии связей растут. В этом же направлении возрастает и сродство к электрону
Энергии связей некоторых двухатомных молекул
Cs2
Если в молекуле соединяются более двух различных атомов, то средняя энергия связи не совпадает с величиной энергии диссоциации молекулы. Если в молекуле представлены различные типы связи, то каждому из них можно приближенно приписать определенное значение Е. Это позволяет оценить энергию образования молекулы из атомов. Например, энергию образования молекулы пентана из атомов углерода и водорода можно вычислить по уравнению:
В табл. 4.2 рассматривается взаимосвязь между энергией химической связи и свойствами веществ.
Взаимосвязь между энергией химической связи и свойствами веществ
Энергия связи, кДж/моль
Высокие твердость, прочность, температуры кипения и плавления
Высокая пластичность
Низкие твердость, прочность, температуры кипения и плавления
4.3. Длина связи
Длина связи – это расстояние между ядрами взаимодействующих атомов. Ориентировочно оценить длину связи можно, исходя из атомных или ионных радиусов, или из результатов определения размеров молекул с помощью числа Авогадро. Так, объем, приходящийся на одну молекулу воды: 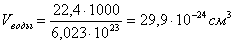
С помощью различных методов физико-химических исследований (например электронографии) определяют d более точно. Исследование длин связей показало, что для данной пары атомов в различных (сходных) соединениях длина связи остается величиной постоянной.
Из длин связей между атомами в молекуле можно вычислить ковалентные радиусы атомов. Если рассмотреть гомоядерные двухатомные молекулы с простой связью, такие как F 2 или С l 2, атомам F и С l можно приписать ковалентные радиусы простых связей, равные половине межъядерного расстояния в соответствующих молекулах. Для элементов, которые не могут образовать двухатомные молекулы с простыми связями, используют другие методы определения радиусов. Так, поскольку расстояние С—С в алмазе и множестве органических молекул найдено равным 1,54+0,01 Å, то ковалентный радиус атома углерода принимают равным 0,77. Чтобы получить ковалентный радиус атома азота, вычитают 0,77 из расстояния С—N в молекуле Н3С— NH 2, при этом получают 0,70. Этим способом можно составить таблицу ковалентных радиусов простых связей (табл. 4.3).
Некоторые ковалентные радиусы простых связей
Ковалентный радиус, Å
Ковалентный радиус, Å
Также можно получить и радиусы кратных связей. Например, для тройной связи радиусы атомов углерода и азота можно вычислить из длин связей в Н—С º С—Н и N º N ; они равны 0,60 и 0,55, причем для длины связи C º N они дают величину 1,15 по сравнению с 1,16, полученной экспериментально. Можно сделать вывод, что чем выше порядок связи между атомами, тем она короче (см. табл. 4.4).
4.4. Кратность связи
Кратность связи определяется количеством электронных пар, участвующих в связи между атомами. Химическая связь обусловлена перекрыванием электронных облаков. Если это перекрывание происходит вдоль линии, соединяющей ядра атомов, то такая связь называется σ-связью. Она может быть образована за счет s – s электронов, р – р электронов, s – р электронов. Химическая связь, осуществляемая одной электронной парой, называется одинарной.
Если связь образуется более чем одной парой электронов, то она называется кратной.
Кратная связь образуется в тех случаях, когда имеется слишком мало электронов и связывающихся атомов, чтобы каждая пригодная для образования связи валентная орбиталь центрального атома могла перекрыться с какой-либо орбиталью окружающего атома.
Поскольку р-орбитали строго ориентированы в пространстве, то они могут перекрываться только в том случае, если перпендикулярные межъядерной оси р-орбитали каждого атома будут параллельны друг другу. Это означает, что в молекулах с кратной связью отсутствует вращение вокруг связи.
4.5. Полярность связи
Если двухатомная молекула состоит из атомов одного элемента, как, например, молекулы Н2, N2, Cl 2 и т. п., то каждое электронное облако, образованное общей парой электронов и осуществляющее ковалентную связь, распределяется в пространстве симметрично относительно ядер обоих атомов. В подобном случае ковалентная связь называется неполярной или гомеополярной. Если же двухатомная молекула состоит из атомов различных элементов, то общее электронное облако смещено в сторону одного из атомов, так что возникает асимметрия в распределении заряда. В таких случаях ковалентная связь называется полярной или гетерополярной.
Для оценки способности атома данного элемента оттягивать к себе общую электронную пару пользуются величиной относительной электроотрицательности. Чем больше электроотрицательность атома, тем сильнее притягивает он общую электронную пару. Иначе говоря, при образовании ковалентной связи между двумя атомами разных элементов общее электронное облако смещается к более электроотрицательному атому, и в тем большей степени, чем больше различаются электроотрицательности взаимодействующих атомов. Значения электроотрицательности атомов некоторых элементов по отношению к электроотрицательности фтора, которая принята равной 4, приведены в табл. 4.5.
У элементов одной и той же подгруппы электроотрицательность с ростом заряда ядра проявляет тенденцию к уменьшению. Таким образом, чем более типичным металлом является элемент, тем ниже его электроотрицательность; чем более типичным неметаллом является элемент, тем выше его электроотрицательность.
Относительная электроотрицательность элементов
Так, в молекуле хлористого водорода общая электронная пара смещена в сторону более электроотрицательного атома хлора, что приводит к появлению у атома хлора эффективного отрицательного заряда, равного 0,17 заряда электрона, а у атома водорода такого же по абсолютной величине эффективного положительного заряда. Следовательно, молекула НС1 является полярной молекулой. Ее можно рассматривать как систему из двух равных по абсолютной величине, но противоположных по знаку зарядов, расположенных на определенном расстоянии друг от друга.
4.6. Типы ковалентных молекул
Электрический момент диполя молекулы представляет собой векторную сумму моментов всех связей и несвязывающих электронных пар в молекуле. Результат сложения зависит от структуры молекулы.
Многоатомные молекулы также могут быть неполярными при симметричном распределении зарядов, или полярными – при асимметричном распределении зарядов. В последнем случае дипольный момент молекулы будет отличаться от нуля. Каждой связи в многоатомной молекуле можно приписать определенный дипольный момент, характеризующий ее полярность; при этом следует принимать во внимание не только величину дипольного момента, но и его направление, т. е. рассматривать дипольный момент каждой связи как вектор. Тогда суммарный дипольный момент молекулы в целом можно считать равным векторной сумме дипольных моментов отдельных связей. Дипольный момент обычно принято считать направленным от положительного конца диполя к отрицательному.
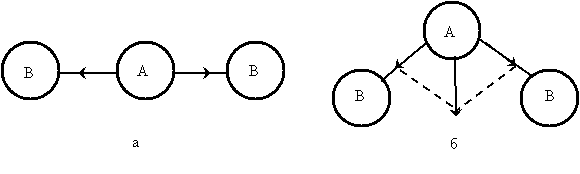
Рис. 4.1. Дипольные моменты отдельных связей в молекулах типа АВ2 различного строения: а – линейное строение, б – угловое строение
На рис. 4.1 изображены схемы возможного строения молекулы типа АВ2; векторы дипольных моментов отдельных связей А—В показаны стрелками, направленными от А к В. При линейном строении (рис. 4.1, а) равные по величине дипольные моменты двух связей А—В противоположны по направлению. Следовательно, дипольный момент такой молекулы будет равен нулю. В случае углового строения (рис. 4.1, б) векторная сумма дипольных моментов двух связей А—В отличается от нуля; такая молекула обладает дипольным моментом и является полярной. Поэтому наличие или отсутствие дипольного момента у молекулы типа АВ2 позволяет сделать вывод о ее геометрическом строении.
Например, молекула СО2 имеет симметричное линейное строение:
Полярность молекул оказывает заметное влияние на свойства образуемых ими веществ. Полярные молекулы стремятся ориентироваться по отношению друг к другу разноименно заряженными концами. Следствием такого диполь-дипольного взаимодействия является взаимное притяжение полярных молекул и упрочнение связей между ними. Поэтому вещества, образованные полярными молекулами, обладают, как правило, более высокими температурами плавления и кипения, чем вещества, молекулы которых неполярны.
Строение и ожидаемая полярность молекул
Пространственная конфигурация
Примеры
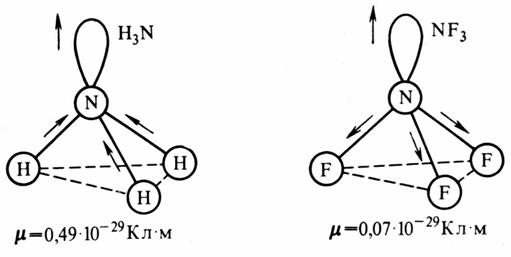
Рис. 4.2. Сложение электрических моментов диполя связывающей и несвязывающей электронных пар молекул H 3 N и NF 3
Это объясняется тем, что в Н3 N направление электрического момента диполя связывающей N—Н и несвязывающей электронной пары совпадает и при векторном сложении обусловливает большой электрический момент диполя. Наоборот, в NF 3 моменты связей N—F и электронной пары направлены в противоположные стороны, поэтому при сложении они частично компенсируются (рис. 4.2). Значения электрических моментов диполя некоторых молекул приведены в табл. 4.7.
Электрический момент диполя
4.7. Вопросы и задания
4.7.14. Вычислите среднюю энергию связи Н— Se и Н—Те для соединений H 2 Se и Н2Те, если стандартные теплоты образования этих соединений соответственно равны 85,77 и 154,39 кДж/моль. Энергия диссоциации H 2 равна 435,9 кДж/моль.
4.7.17. К каким атомам смещены связывающие электронные облака в следующих молекулах: а) НС1; б) НВг; в) HI ; г) NaH ; д) КН; е) ВеО; ж) N0; з) BN ; и) C 1 F ; к) ClBr ; л) MgS ; м) BeCl 2; н) ВВ r 3; о) СО2; п) OF 2; р) MgF 2; с) А1С13?
4.7.18. Рассчитайте эффективные заряды на атомах следующих молекул: a ) BrCl ; б) BrF ; в) C 1 F ; г) НС1; д) НВ r ; е) HI ; ж) LiBr ; з) LiF ; и) NaCl ; к) Nal ; л) NO ; м) Н2О ( NH 3 ( HNH = 107°).
4.7.19. Как изменяется полярность в ряду молекул: а) HF ; НС1; НВ r ; HI ; б) NH 3; РН3; А sH 3?
4.7.27. Какая молекула, аммиак или арсин имеет больший дипольный момент? Почему?
4.7.28. Почему молекула CCl 4 неполярная, а CH 3 Cl – полярная?