гематоэнцефалический барьер что пропускает
Анатомически, BBB представляет собой обширную сеть микрокапилляров протяженностью
650 км, каждый из которых имеет диаметр просвета
На целостность и функцию ВВВ оказывает сильное влияние то, что сейчас называют «расширенной нейрососудистой единицей или блоком» (“extended neurovascular unit”), которая включает в себя не только микрососудистые эндотелиальные клетки и смежные перициты, астроциты и нейроны, но также соседние клетки гладкой мускулатуры и микроглии в мозге, а также клетки крови, находящиеся в капиллярном просвете, например, таких как полиморфноядерные клетки, лимфоциты и моноциты. У
P-гликопротеин (ABCB1 / MDR1) является выдающимся молекулярным открытием доставки лекарственного средства в ЦНС через ВВВ. Стратегически обогащенный на мембране церебральных микрососудистых эндотелиальных клеток, P-гликопротеин использует энергию от АТФ-гидролиза, чтобы вытеснить лекарства обратно в микрокапиллярный просвет против крутых градиентов концентрации.
Кодеиновая анальгезия опосредованно централизована, что требует ее накопления в головном мозге, что и происходит при пассивной парацеллюлярной диффузии. Неконтролируемое увеличение потребления мозгом кодеина во время периферической воспалительной боли из-за патологического увеличения парацеллюлярной проницаемости может привести к значительным побочным эффектам ЦНС, связанным с опиоидами, такими как угнетение дыхания, зависимость и повышенная толерантность.
Гематоэнцефалический барьер (ВВВ) представляет собой физический и метаболический барьер, который отделяет ЦНС от периферического кровообращения. Доставка лекарств в ЦНС (CNS) через BBB является сложной задачей, в первую очередь из-за физического ограничения парацеллюлярной диффузии между эндотелиальными клетками, которые содержат микрососуды ВВВ, и активности транспортеров оттока, которые быстро вытесняют обратно в капиллярный просвет широкий спектр ксенобиотиков. В заключении отметим, что терапевтическое манипулирование трафиком P-гликопротеинов представляет собой относительно недорогой и неспецифический подход для усиления доставки лекарств в ЦНС (множества лекарств) и выбора оптимальных комбинаций лекарственных средств. Субстратами, влияющими на активность Р-гликопротеиновой транспортной системы, являются дигоксин, циметидин, такролимус, нифедипин, кетоконазол и амитриптилин.
Гематоэнцефалический барьер что пропускает
Гематоэнцефалический барьер разграничивает нервную систему от общего кровотока, обеспечивая постоянную и оптимальную по химическому составу среду для ее функционирования.
Межклеточная жидкость занимает 15 % общего объема мозга и окружает нейроны и нейроглию. Схема межклеточных пространств представлена на рисунке ниже. Секретируемая сосудистыми сплетениями спинномозговая жидкость циркулирует в системе желудочков и субарахноидальном пространстве и через пахионовы грануляции проникает в синусы твердой мозговой оболочки.
Затем спинномозговая жидкость путем пассивного транспорта через выстилающую стенки желудочков эпендимоглиальную мембрану проходит во внеклеточные пространства мозга, где смешивается с межклеточной жидкостью, продуцируемой клетками капилляров, и в процессе клеточного метаболизма распространяется через пиаглиальную мембрану в субарахноидальное пространство. «Стекание» спинномозговой жидкости компенсирует отсутствие лимфатических сосудов в ЦНС.
Единственная составляющая спинномозговой жидкости, которая не проникает через гематоэнцефалический барьер,— метаболическая жидкость. В ее состав входят нейромедиаторы, высвобожденные нейронами и не подвергнувшиеся обратному захвату, что обусловливает наличие неспособных преодолеть гематоэнцефалический барьер медиаторов и их метаболитов в субарахноидальном пространстве.
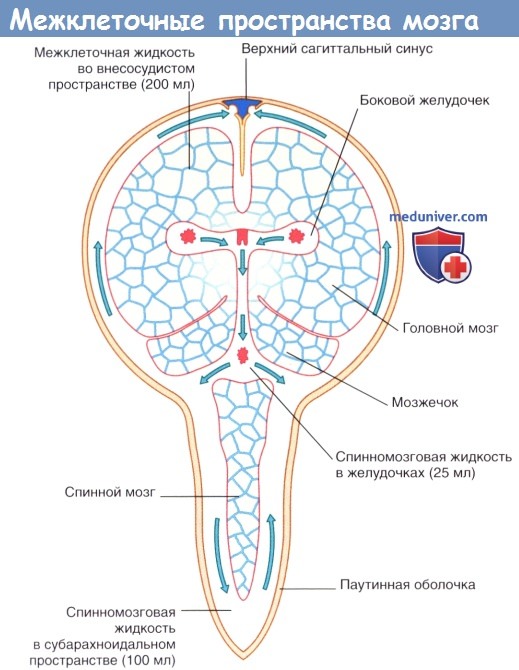
Стрелками показаны направления циркуляции спинномозговой жидкости.
Компоненты спинномозговой жидкости распределены следующим образом (по результатам поясничной пункции):
• жидкость, продуцированная клетками сосудистых сплетений, — 60 %;
• жидкость, продуцированная клетками капилляров, — 30 %;
• метаболическая жидкость — 10%.
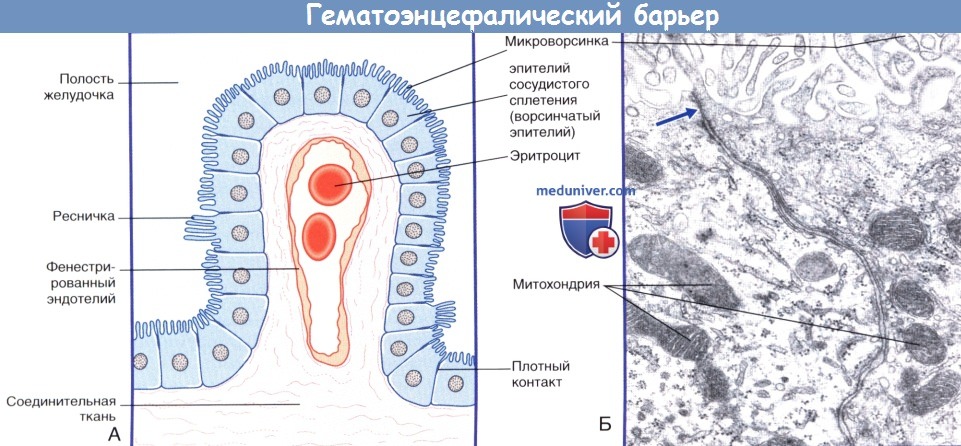
(Б) Ультраструктура эпителия сосудистого сплетения. В эпителиальных клетках расположены множество митохондрий и гранулярная эндоплазматическая сеть.
Клетки соединены плотными контактами в апикальной части.
Гематоэнцефалический барьер состоит из двух компонентов. Первый представлен барьером между кровью и спинномозговой жидкостью на уровне сосудистых сплетений, а второй — барьером между кровью и межклеточной жидкостью на уровне капилляров ЦНС.
а) Барьер между кровью и спинномозговой жидкостью. Барьер между кровью и спинномозговой жидкостью представлен эпендимальным эпителием сосудистых сплетений, который характеризуется следующими особенностями строения.
1. Практически все реснички замещены микроворсинками.
2. Клетки образуют плотные контакты. Именно эти места плотного соединения мембран клеток разграничивают кровь и спинномозговую жидкость.
3. Клетки эпителия содержат ферменты, обеспечивающие транспорт ионов и продуктов метаболизма.
б) Барьер между кровью и межклеточной жидкостью. Барьер между кровью и межклеточной жидкостью представлен эндотелием капилляров ЦНС, который характеризуется следующими особенностями строения.
1. Эндотелиоциты образуют плотные контакты.
2. В состав клеток входит небольшое количество пиноцитозных пузырьков, а также отсутствуют фенестрации.
3. Транспортные системы в клетках аналогичны таковым в эпителии сосудистых сплетений.
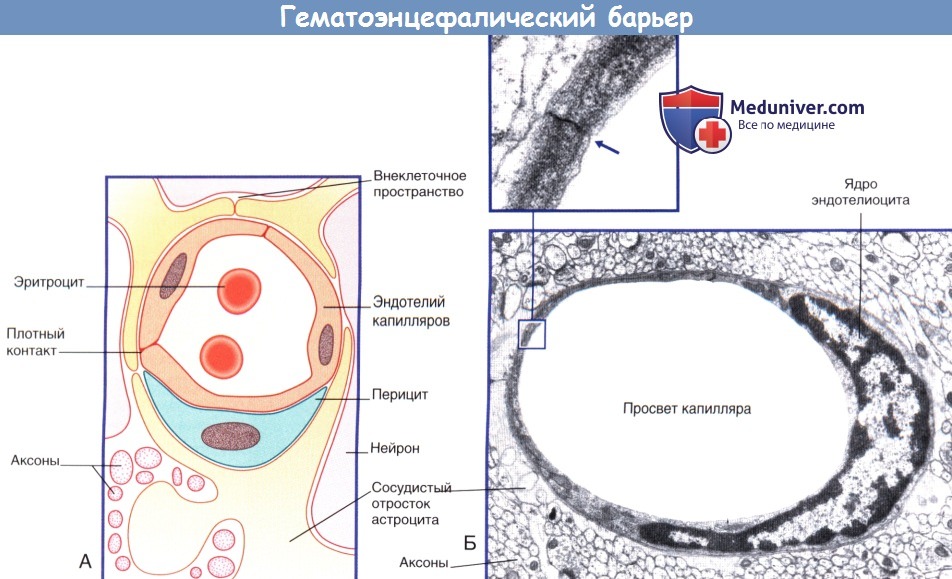
(Б) Капилляр центральной нервной системы. На поперечном срезе показан одиночный эндотелиоцит, полностью окружающий просвет сосуда.
Края эндотелиоцитов образуют плотный контакт. Эндотелиоцит окружен базальной мембраной. Капилляр окружен отростками астроцитов.
в) Функции перицитов капиллярного русла. Перициты и клетки эндотелия связаны с помощью щелевидных контактов. В ходе исследований культур клеток было достоверно доказано, что перициты играют ключевую роль в ангиогенезе капилляров, а также в формировании и поддержании плотных контактов между эндотелиоцитами.
Перициты принимают участие в саморегуляции мозгового кровотока за счет того, что на их поверхности экспрессируются рецепторы к вазоактивным медиаторам: норадреналину, вазопрессину, ангиотензину II. При хронической артериальной гипертензии развиваются гипертрофия и гиперплазия перицитов, а также происходит внутриклеточная продукция цитоплазматических сократительных филаментов, что обеспечивает компенсаторное расширение капилляров.
Поверхность клеточной стенки перицитов способна обеспечивать связывание протромбинового комплекса, за счет чего перициты могут принимать участие в процессе свертывания крови.
Кроме того, перициты обладают способностью к фагоцитозу и свойствами иммунорегуляторных цитокинов.
Общая площадь капиллярного русла головного мозга соответствует размерам теннисного корта! Наличие такой огромной поверхности объясняет тот факт, что мозг потребляет 20 % поступающего кислорода. Плотность капилляров коры головного мозга можно оценить на изображении латексного слепк.
г) Функции гематоэнцефалического барьера:
• Контроль проникновения метаболических веществ. Основной источник питания нейронов — глюкоза. При повышении уровня глюкозы в крови специфический белок-переносчик связывает ее, а при низком уровне — обеспечивает более активный захват.
• Предотвращение поступления в мозг токсических веществ и периферических нейромедиаторов, выделяемых вегетативными нервными окончаниями в системный кровоток.
Корковые капилляры имеют вид извилистых белесоватых нитей.
д) Состояния, связанные с нарушением гематоэнцефалического барьера:
1. Пациенты с артериальной гипертензией подвержены приступам гипертонической энцефалопатии в связи с тем, что степень повышения давления превосходит компенсаторные способности стенок артериол. Вследствие такого повышения давления может произойти нарушение плотных межклеточных контактов эндотелия капилляров, что приводит к отеку мозга за счет быстрого выхода плазмы. Клинически эта ситуация проявляется сильной головной болью, рвотой и, в некоторых случаях, появлением судорог и развитием комы.
2. У пациентов с повышенным содержанием углекислого газа в крови (при заболеваниях дыхательной или сердечно-сосудистой системы, а также после хирургических вмешательств) причиной отека мозга даже при нормальном уровне артериального давления может стать расслабление мышечного слоя артериол. Данная ситуация клинически проявляется спутанностью сознания и сонливостью, в дальнейшем переходящими в кому.
3. Повреждения мозга (травмы или спонтанные кровоизлияния) приводят к отеку мозга вследствие осмотического повреждения тканей мозга (и других факторов).
4. Инфекционные заболевания мозга или его оболочек сопровождаются нарушением гематоэнцефалического барьера, предположительно из-за усиленного перемещения лейкоцитов в капиллярном русле мозга. Несостоятельность гематоэнцефалического барьера играет и положительную роль: стенки капилляров проницаемы для жирорастворимых антибиотиков.
Кроме того, капилляры опухолей мозга характеризуются наличием фенестраций, что позволяет идентифицировать злокачественное новообразование при помощи рентгеноконтрастного вещества, неспособного пройти через капилляры непораженных отделов мозга.
Редактор: Искандер Милевски. Дата публикации: 10.11.2018
Открыть ворота гематоэнцефалического барьера
Оксана Семячкина-Глушковская,
доктор биологических наук, Саратовский государственный университет им. Н. Г. Чернышевского
«Наука и жизнь» №7, 2015
В последнее десятилетие всё чаще врачи сталкиваются с инсультом новорождённых, но лечить его пока не очень получается. Трудности связаны с гематоэнцефалическим барьером — одной из самых загадочных систем мозга, «перегородкой» между кровью, циркулирующей в теле, и мозгом. Именно он решает, что допустить в мозг, а что — нет. Сегодня тема преодоления гематоэнцефалического барьера нужными лекарствами стала одной из горячих и «денежных» в нейрофизиологии.
130 лет назад человечеству приоткрылся один из механизмов работы мозга: была обнаружена «перегородка» между мозгом и кровеносной системой тела — гематоэнцефалический барьер. Он состоит из нескольких слоёв: со стороны тела кровеносный капилляр мозга выложен клетками эндотелия на базальной мембране. Со стороны ткани мозга находится слой нейронов, так что они переплетаются в трёхмерную сеть. Такая структура позволяет регулировать проникновение из крови в мозг биологически активных веществ, метаболитов, но препятствует поступлению в мозг чужеродных веществ, микроорганизмов, токсинов
Гематоэнцефалический барьер — тонкая физиологическая организация — оставался вне поля зрения учёных до тех пор, пока не стало очевидно, что именно он тормозит успехи современной медицины и именно в его работе скрыты ресурсы для новой эпохи в фармакологии. За последние 20 лет в мире было синтезировано более 40 новых препаратов, из которых всего два — для лечения болезней мозга. Гематоэнцефалический барьер создаёт для некоторых веществ «зелёный» коридор, но для целого ряда препаратов он остаётся непроницаемым, и потому врачи безоружны в борьбе со многими неврологическими патологиями, такими, например, как инсульт мозга. Задача проницаемости барьера встала, когда было признано, что у новорождённых это заболевание встречается так же часто, как у взрослых.
Десять лет назад диагноз «инсульт» детям ставили крайне редко. Сегодня прогресс в развитии безопасных технологий для внутреннего исследования мозга (визуализация) позволил исследователям увидеть серьёзность проблемы. Особенность детского инсульта в том, что он проходит зачастую бессимптомно или «маскируется» под другие заболевания. Последствия катастрофичны для ребёнка. У большинства маленьких пациентов возникают серьёзные нарушения: задержка умственного и речевого развития, гиперреактивность, затруднения в концентрации внимания, у них страдают логика и адаптация к стрессам, что не сразу и не очевидно проявляется в первые дни жизни.
Но диагностика инсульта мозга у новорождённых — лишь первый этап. Главный вопрос — как лечить и как предупредить это заболевание. Детский и взрослый инсульты — разные! Мы знаем, какие факторы провоцируют развитие инсульта у взрослых — к примеру, гипертензия. Но для малышей эти факторы не так актуальны, и даже такие очевидные на первый взгляд причины, как родовые травмы, не вошли в лидирующую десятку провокаторов инсульта у детей.
Почему инсульты мозга у новорождённых и взрослых так различаются? После появления на свет мозг ребёнка ещё продолжает развиваться, причём особенно интенсивно в первые дни после рождения. В настоящий момент не существует тактики лечения инсульта мозга у новорождённых. Мало зная об этом заболевании у младенцев, врачи вынуждены применять к ним терапию, показанную для взрослых. Она оказывается неэффективной, а иногда даже мешает выздоровлению. Успех в лечении таких детей — зачастую случайность, а не результат заранее спланированной тактики врача.
Возникло предположение, что многие препараты, которые существуют в арсенале врача для лечения инсульта, просто не доходят до мозга новорождённого из-за капризного гематоэнцефалического барьера, который закрывается и не даёт поработать препаратам.
Несмотря на прорывные технологии в визуализации структур мозга, решения проблем детского инсульта не было, потому что не хватало подходящего инструментария для исследования «ворот», пропускающих лекарства в гематоэнцефалическом барьере.
В экспериментальной медицине платформа для изучения любых болезней — моделирование патологии на животных. Среди существующих на сегодняшний день моделей инсульта ни одна не пригодна для новорождённых.
Есть два типа инсульта — ишемический, когда сосуды мозга сужаются, что ограничивает его питание и кровоснабжение, и геморрагический, когда сосуды рвутся без явных на то причин. У новорождённых преобладает второй тип инсульта. Однако модели, традиционно применяемые для изучения геморрагического инсульта, работают по принципу механического введения крови в мозг экспериментальных животных, что сильно ограничивает исследовательские возможности.
На биологическом факультете Саратовского государственного университета им. Н. Г. Чернышевского разработали модель инсульта, с помощью которой можно увидеть, как сосуды мозга разрываются самостоятельно, без дополнительных вмешательств. Для этого используется звуковой стресс (120 дБ, 7 Гц). Звуковые волны за счёт способности глубоко проникать в мозг нарушают центры регуляции его кровотока.
Сосудистые «катастрофы» у новорождённых случаются не сразу, а через два-три дня после рождения. Аналогичные изменения происходят с сосудами лабораторных животных после влияния звукового стресса. И хотя звук — это неадекватный провоцирующий фактор для детского инсульта, на сегодняшний день это единственная модель, которая позволяет изучать развитие данной патологии без инвазивных вмешательств, запуская внутренние патологические процессы, максимально приближенные к естественному ходу событий.
Однако для взрослых животных простого стресса недостаточно, чтобы вызвать инсульт головного мозга. Для них требуется наличие хронически высокого артериального давления, изнашивающего сосуды и делающего их стресс-неустойчивыми. Для того чтобы изучать, как работает «барьер» на первых этапах жизни и на последующих этапах развития, мы вооружились современными методами флуоресцентного обнаружения белков окклудин и клаудин-5, работающих «таможенниками» на границе между мозгом и кровью. Воспользовались и старым методом изучения прохождения барьера красителем Evans blue (голубой Эванса), связывающимся с белками крови. Именно этот краситель в 1885 году помог открыть гематоэнцефалический барьер немецкому нейрофизиологу Паулю Эрлиху. Когда он ввёл краситель в кровь, то обнаружил, что все внутренние органы окрасились, а мозг нет. Позже опыты повторил его ученик Эдвин Голдман, но он вводил краситель уже непосредственно в спинномозговой канал лабораторного животного. Мозг становился синим, при этом вся краска оставалась в нём, не проникая на периферию. И по сей день краситель Evans blue — надёжный способ проверки работы гематоэнцефалического барьера. Конечно, появились и другие, более точные способы тестирования проницаемости барьера, например светящиеся метки, закреплённые на полисахаридах — декстранах разной массы (3 кДа и 70 кДа).
Появление голубого окрашивания тканей мозга у взрослой (справа) и у новорождённой (слева) крыс на фоне развития инсульта и введения красителя Evans blue
А теперь посмотрим, как работает гематоэнцефалический барьер при развитии геморрагического инсульта и как эти процессы отличаются друг от друга в первые дни после рождения лабораторного животного и в последующем его развитии.
Оказалось, внутривенное введение красителя крысам на фоне развития инсульта сопровождается появлением голубой окраски тканей мозга только у взрослых, но не у новорождённых особей.
Мы исследовали, какие вещества проходят через гематоэнцефалический барьер в условиях, когда организму необходимо бороться с инсультом. Для этого использовали флуоресцентные метки — лёгкие (декстран 3 кДа) и тяжёлые (декстран 70 кДа), которые своим свечением подсказывают нам их местонахождение и помогают определить путь движения.
Лёгкие флуоресцентные метки (декстран 3 кДа) распределены по-разному: у взрослой крысы (слева) — распределение по всему мозгу, а у новорождённой (справа) — концентрирование в сосуде на фоне развития инсульта мозга
Как оказалось, у взрослых крыс мозг при инсульте как решето: пропускает даже высокомолекулярные соединения (декстран 70 кДа). А у новорождённых декстрановые флуоресцентные метки застревают в сосудах: барьер закрывается так плотно, что даже низкомолекулярные соединения (декстран 3 кДа) остаются в пределах сосудов и не попадают в мозг.
Используя метод иммуноблоттинга (метод определения специфических белков), удалось увидеть белки, которые и делают барьер непроницаемым. Мы наблюдали за двумя критически важными белками — клаудином-5 и окклудином. У новорождённых крыс этих белков в разы больше, чем у взрослых. Вот почему краситель Evans blue и флуоресцентные метки у новорождённых особей «застревают» в барьере, в то время как у взрослых он становится более «лояльным» — проницаемым для веществ, которые в обычных условиях в мозг не попадают.
Экспрессия структурных белков гематоэнцефалического барьера — окклудина и клаудина-5 у новорождённых и взрослых крыс (более тёмные полоски отражают более высокую экспрессию)
Возможно ли найти объяснение разного поведения мозга в момент его начального развития и когда статус организма уже сформировался? Мозг развивается по принципу избыточности. Он старается иметь сразу всё и много и только потом разбирается, что с этим делать. Часть его структур, к примеру адренергические нейроны, у которых медиаторами служат норадреналин и адреналин, образуется задолго до рождения, но созревает только к двум годам жизни. Другие структуры, альфа2-адренорецепторы, наоборот, созревают до рождения в огромном количестве, а после их плотность заметно снижается. Но так или иначе, многие молекулярные структуры мозга, равно как и его биохимия, формируются заведомо с избытком. Возможно, это одна из причин, почему у новорождённых наблюдается повышенная экспрессия «барьерных» белков, препятствующих проникновению многих «взрослых» препаратов, которые применяют при лечении инсульта мозга.
Тайна гематоэнцефалического барьера — как грань между небом, землёй и воздухом. Его можно «увидеть», но трудно постичь. Нужны бойцы-невидимки, которые могли бы обмануть строгих стражей барьера, пронести необходимую «гуманитарную помощь» страдающему мозгу маленького пациента и помочь ему в борьбе с инсультом. Такими помощниками могут стать транспортные системы — липосомы, капсулы, углеродные нанотрубки, которые активно разрабатываются с этой целью во всём мире.
Исследования проводились на биологическом факультете Саратовского государственного университета им. Н. Г. Чернышевского в рамках проекта Российского научного фонда (№14-15-00128) и гранта Президента РФ (МД-2216.2014.4).
Гематоэнцефалический барьер и лекарства
Поделиться:
Нормальная деятельность головного мозга возможна лишь в условиях биохимического и электролитного гомеостаза (равновесия). Поэтому жизненно необходимо, чтобы мозг был надежно защищен от попадания веществ, способных изменить работу центральной нервной системы. Для этого и существует гематоэнцефалический барьер, или сокращенно ГЭБ.
Для чего нам нужен ГЭБ
ГЭБ — это полупроницаемая мембрана, которая отделяет мозг от кровеносного русла. Этот барьер состоит из эндотелиальных клеток, астроцитов и перицитов. Мембрана имеет особо «плотное» расположение капилляров, что и является основой барьера, предохраняющего мозг от проникновения большинства веществ, циркулирующих в крови.
ГЭБ сохраняет специфическую внеклеточную среду вокруг нейронов, поддерживая концентрацию аминокислот, аскорбиновой и фолиевой кислот даже при снижении их концентрации в сыворотке крови.
Читайте также:
Инновации в нейронауках
Кроме того, абсолютно необходимо, чтобы никакие патогенные микробы не могли попасть в головной мозг. Иначе наступает катастрофа. Типичный пример: микроб менингита, так называемый менингококк, вполне мирно может проживать в носоглотке, но при ослаблении защитных сил (и нарушении проницаемости ГЭБ) менингококк попадает в центральную нервную систему, поражая оболочки головного мозга и вызывая потенциально смертельную болезнь — гнойный менингит.
Повышение проницаемости ГЭБ также характерно и для других заболеваний нервной системы. Например, при рассеянном склерозе активированные Т-лимфоциты легко преодолевают ГЭБ и вызывают поражение мозга.
Как ГЭБ работает на практике
Проницаемость гематоэнцефалического барьера напрямую зависит от величины молекул. Маленькие молекулы кислорода, углекислого газа проходят вообще без проблем. Но чем крупнее молекула вещества, тем труднее ей пробраться. Впрочем, существуют способы облегчить эту задачу. Например, давно замечено, что жирорастворимые вещества диффундируют через барьер на ура. Это свойство используется при создании некоторых лекарств, например снотворных барбитуратов.
Интересна ситуация с таким важным веществом, как глюкоза. Пониженный ее уровень — гипогликемия мозга — проявляет себя в виде головной боли, нарушений внимания, спутанности сознания и эпилептических приступов. При этом концентрация сахара в крови может оставаться нормальной (!). Тут «заупрямился» ГЭБ и возникли нарушения в системе переноса глюкозы.
Кстати, все больше и больше свидетельств, что классическая эпилепсия, происхождение которой в известной мере остается загадкой для врачей, является «болезнью ГЭБ», когда нарушен транспорт глюкозы в тканях мозга.
ГЭБ и фармакология
Давайте сразу уясним, что большинству лекарств незачем преодолевать этот барьер. К примеру, средство от расстройства желудка должно держаться подальше от мозга и заниматься своим прямым делом в пищеварительном тракте. Но если возникло серьезное поражение центральной нервной системы, «тогда мы идем к вам!».
Антибиотикам желательно добраться до мозга при инфекционных поражениях, противоконвульсивным препаратам — для лечения судорог и, уж конечно, нейролептикам — для купирования острых психозов. Эффективность вышеперечисленных препаратов напрямую зависит от проницаемости ГЭБ.
А вот при болезни Паркинсона, для которой характерен недостаток допамина в мозге, не удастся восполнить этот дефицит ни таблетками, ни уколами, потому что допамин через ГЭБ, к сожалению, не проходит. Хотя, например, предшественник допамина — Л-допа — способен преодолеть ГЭБ. Но все-таки это не совсем то, что нужно.
Кстати, похожая ситуация при депрессиях, в патогенезе которых большую роль играет глютамат. Глютамат также не проникает через через ГЭБ. Поэтому глотать его бессмысленно.
Когда ГЭБ может рухнуть?
Существует ряд ситуаций, при которых страдает ГЭБ и мозг остается незащищенным. Это может случиться при высоком артериальном давлении, поэтому стоит держать его под контролем. Внутривенное введение гиперосмолярных растворов также несет в себе угрозу нарушения барьера. Длительное воздействие микроволнового излучения и радиации доказанно считается причинами нарушений ГЭБ. Инфекции центральной нервной системы типично дают сбои в работе барьера. Также нарушения возможны при травмах мозга, его ишемии, воспалении и инсультах.
А если ГЭБ не пускает, но нам очень нужно?
Существует ряд заболеваний головного мозга, когда жизненно важно пропихнуть лекарство в определенный участок мозга. Чаще всего это онкология. Для этого используется метод «локального открытия ГЭБ». Лучше всего работают маннитол и его аналоги, которые вводятся в артерию мозга под контролем компьютерного томографа.
Маннитол открывает ГЭБ примерно на час, и за это время опухоль подвергается воздействию химиотерапии. С уходом маннитола дверь в мозг закрывается. И правильно — нельзя оставлять мозг без защиты.
Подобным эффектом открытия ГЭБ обладают Лейкотриен С4 и брадикинин. В определенной дозе ГЭБ открывает и гистамин. Кстати, «закрыть дверь» за гистамином можно его антиподом — цимедином. Имейте в виду, что все эти препараты вводятся прицельно в надлежащий кровеносный сосуд. Если принимать их в виде таблеток или инъекций, результата не будет.
Информация для простого пациента
Не ведитесь на рекламу деятелей «народной медицины», утверждающих, что нашли средства, улучшающие состояние психики. Далеко не всякая таблетка, вами проглоченная, вообще доберется до головы. На страже вашего мозга стоит ГЭБ, и чаще всего это только на пользу.





 Читайте также:
Читайте также: 

