гексализ или лизобакт что эффективнее при фарингите
Оценка эффективности препарата гексализ в лечении острого фарингита
Опубликовано:
Вестник оториноларингологии, 6, 2011
Проф. Н.А. Арефьева, асп. А.А. Васяева, д.м.н. Л.Ф. Азнабаева
Кафедра оториноларингологии ФГУ ВПО «Башкирский государственный медицинский университет» Росздрава (зав. кафедрой — проф., д.м.н. Н.А. Арефьева)
The estimation of the efficacy of Hexalyse used for the treatment of acute pharyngitis
N.A. Arefieva, A.A. Vasyaeva, L.F. Aznabaeva Изучение взаимосвязи между активностью интерфероновой системы на местном уровне и частотой развития рецидивов острого воспаления слизистой оболочки глотки, а также оценка необходимости, возможности и эффективности коррекции выявленных нарушений местного иммунного ответа с помощью препаратов, обладающих иммунонаправленным действием. Обследованы 45 пациентов с острым фарингитом. Группу 1 составили 25 пациентов, которые получали комбинированный препарат для местного применения гексализ, группу 2 — препарат стрепсилс. Проводились общее обследование, оториноларингологический осмотр, оценивалась активность интерфероновой продукции на местном уровне путем определения иммуноферментным методом содержания α-ИНФ в слюне до начала лечения и на 3-й и 5-й дни терапии. Установлено, что адаптационные механизмы слизистой оболочки глотки при остром воспалении реализуются активацией интерфероновой системы, купирование воспалительного процесса при этом сопровождается нормализацией уровня α-ИНФ в слюне и не зависит от вида лечения. У 1/3 больных острым фарингитом отмечается интерфероновая недостаточность. Включение в схему лечения таких пациентов на ранних стадиях заболевания препарата с иммунонаправленным действием (гексализ) способствует активации синтеза α-ИНФ и клинически проявляется снижением частоты рецидивов заболевания. На основании изучения взаимосвязи между содержанием в слюне α-ИНФ, длительности заболевания на момент обращения и частотой развития рецидивов определены практические рекомендации к применению препарата гексализ в лечении пациентов с острым фарингитом.
Ключевые слова: фарингит, гексализ, альфа-интерферон.
The objective of the present study was to elucidate the relationship between the activity of the interferon system at the local level and the frequency of the development of relapses of acute inflammation of pharyngeal mucosa. The secondary objective was to estimate the possibility, necessity, and efficacy of the correction of the abnormal local immune response with the use of immunomodulatory agents. A total of 45 patients presenting with acute pharyngitis were available for the examination. They were allocated to two groups comprised of 25 and 20 patients respectively. Those in group 1 were given Hexalyse, a composite preparation for the local application. The patients of group 2 were treated with Strepsils. The study included general and specialized otorhinological examination as well as the evaluation of interferon production at the local level by measuring (using immunoenzyme assay) the concentration of interferon-alpha in the saliva before and on days 3 and 5 after the initiation of therapy. It was shown that the adaptive mechanisms of pharyngeal mucosa in acute pharyngitis are realized through activation of the interferon system. Elimination of the inflammatory process was accompanied by normalization of interferon-alpha level in the saliva regardless of the therapeutic modality used. One third of the patients presenting with acute pharyngitis suffered insufficiency of interferon production. It is concluded that the inclusion of an immunomodulatory agent, such as Hexalyse, in the combined treatment of such patients activates biosynthesis of interferon-alpha and leads to the reduction in the frequency of relapses of the disease. The results of the study of the relationship between the concentration of interferon-alpha in the saliva, the duration of acute pharyngitis, and the frequency of its post-treatment relapses were used to develop the practical recommendations for the prescription of Hexalyse for the treatment of patients with this pathology.
Key words: pharyngitis, hexalyse, interferon-alpha.
Лечение рецидивирующих воспалительных заболеваний слизистой оболочки глотки (СОГ) остается проблемой оториноларингологии [1—4]. В настоящее время в лечении острого фарингита (ОФ) и профилактике его рецидивов активно используются препараты, обладающие иммунонаправленным действием [5, 6]. В работах отечественных исследователей были показаны пути реализации иммунного ответа через активацию синтеза иммуноглобулина А, лизоцима, стимуляцию фагоцитоза [5, 7]. Вместе с тем клиническая эффективность многих подобных препаратов, например бактериальных лизатов, заключается в профилактике вторичных бактериальных осложнений. Однако в 70% случаев причиной являются вирусы, что необходимо учитывать при выборе алгоритма лечения [7—9].
Как известно возможны два варианта течения вирусной инфекции: репликативное — продуктивная реакция организма на патоген, ведущая к гибели зараженных клеток, и персистентное — стабилизация вируса внутри клетки в отсутствие эффективного иммунного ответа на раздражитель, что лежит в основе хронической вирусной патологии и ее обострений [2, 10]. Среди цитокинов, обеспечивающих при острой вирусной инфекции быстрое формирование защитного барьера на пути патогенного фактора, ведущее место занимает альфа-интерферон (α-ИНФ), активность которого состоит в подавлении белкового синтеза и репликации вирусов и в активации натуральных клеток-киллеров. Во время острой фазы вирусных инфекций уровень α-ИНФ значительно возрастает у подавляющего большинства пациентов, что следует считать адекватной реакцией местных механизмов врожденного иммунного ответа на внедрение патогена [5, 7, 11].
Цель исследования — изучение взаимосвязи между активностью интерфероновой системы на местном уровне и частотой развития рецидивов острого воспаления слизистой оболочки глотки, а также оценка необходимости, возможности и эффективности коррекции выявленных нарушений местного иммунного ответа с помощью препаратов, обладающих иммунонаправленным действием.
Материал и методы
Для исследования были отобраны 45 пациентов с острым фарингитом, которые были разделены на 2 группы. 1-ю группу составили 25 пациентов, которые получали комбинированный препарат для местного применения гексализ («Бушара Рекордати», Франция). Действующие вещества препарата: биклотимол, лизоцим, эноксолон. Гексализ оказывает антисептическое (биклотимол) и противовоспалительное (эноксолон, лизоцим), а также иммунонаправленное (эноксолон, лизоцим) действие. Пациенты 2-й группы также получали препарат комбинированного действия (антисептическое, противовоспалительное) для местного применения стрепсилс («Бутс Хелскэр», Великобритания), действующие вещества: 2,4-дихлорбензиловый спирт, амилметакрезол, мед, масло мяты перечной, масло лимонное.
В исследование не включались пациенты с нелеченным кариесом и периодонтитом, хроническим тонзиллитом, гипертрофией небных миндалин, заболеваниями внутренних органов в стадии субкомпенсации или декомпенсации, а также женщины в период беременности и лактации. Из исследования были исключены пациенты, выкуривающие по меньшей мере одну сигарету в день, злоупотребляющие алкоголем, работающие в условиях повышенной запыленности и загазованности воздуха, а также получавшие предшествовавшее обращению лечение настоящего заболевания.
Обследование пациентов включало в себя сбор жалоб (боль в горле, глоточные парестезии — першение, саднение, сухость), сбор анамнеза (длительность заболевания, частота эпизодов острого фарингита за предшествующие пять лет), термометрию и оториноларингологический осмотр (гиперемия, отек, гипо- или гиперсекреция слизистой оболочки глотки). Данные регистрировали до начала лечения и на 3-й и 5-й дни терапии.
Для оценки активности интерфероновой продукции на местном уровне определяли содержание α-ИНФ в слюне пациентов. Взятие материала (около 2,0 мл слюны в стеклянную посуду, после полоскания полости рта водой) производили до начала лечения и на 3-й и 5-й дни терапии. Концентрацию α-ИНФ определяли методом иммуноферментного анализа, наборами реагентов ЗАО «Вектор-Бест» (Россия). Полученные результаты сравнивали с показателями 30 практически здоровых лиц.
Статистическая обработка полученных результатов выполнялась с использованием пакета прикладных программ для статистической обработки данных Microsoft Excel XP, раздел программы «Анализ данных» на персональном компьютере. Достоверность различий между сравниваемыми группами оценивалась по критериям Стьюдента. Различия между сравниваемыми величинами признавали статистически достоверными при уровне значимости p
Боль в горле
В данной публикации мы представляем пример тематической разработки из издания «Консультируем и рекомендуем» (выпуск 1) серии «Аптечный практикум». Боль в горле входит в TOP3 наиболее частых обращений клиентов в аптеки*, при этом 15% из них запрашивают конкретный препарат, а 85% просто называют симптом. Поэтому нами рассмотрены как рецептурные, так и безрецептурные препараты, применяемые при этом недуге.
Причины: чаще всего боль в горле появляется как один из симптомов инфекционного заболевания. Наиболее часто ее вызывают две группы возбудителей:
В то же время боль в горле может иметь неинфекционное происхождение, например, вследствие химического раздражения слизистых оболочек ротовой полости, перегрузок голосовых связок.
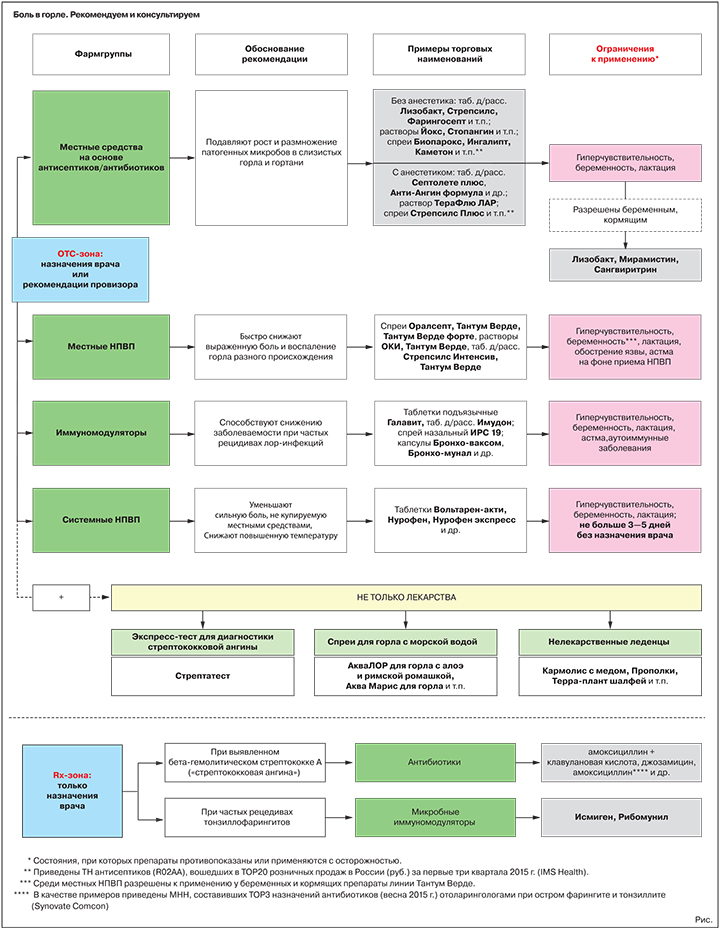
Симптомы: при всем разнообразии проявлений можно выделить основные признаки, отличающие бактериальную инфекцию от инфекций, вызванных другими возбудителями (табл. 1).
Rх-зона
К рецептурным препаратам, которые могут назначаться врачами при тяжелом течении инфекционно-воспалительных заболеваний горла, относятся различные противомикробные средства системного действия.
Антибиотики системного действия
Цель применения: этиологическое лечение острых и хронических инфекционно-воспалительных заболеваний горла бактериального происхождения.
Принцип действия: подавление роста или размножения бактериальной флоры или ее уничтожение.
На заметку провизору
Микробные иммуномодуляторы
Цель применения: лечение и профилактика рецидивирующих инфекций горла, в т.ч. у часто болеющих детей.
Принцип действия: стимуляция неспецифического и специфического иммунитета (усиление выработки антител IgA) в ответ на введение лизатов или структурных фрагментов бактерий, чаще других вызывающих лор-инфекции.
Представители группы: лизаты бактерий (Исмиген), рибосомально-протеогликановые фрагменты бактерий (Рибомунил).
На заметку провизору
OTC-зона
К безрецептурному сегменту лекарственных препаратов, применяемых в комплексном лечении инфекционно-воспалительных заболеваний горла, относятся многочисленные средства местного действия. Именно они могут быть рекомендованы первостольником при непосредственной жалобе клиента на боль в горле.
Местные средства на основе антисептиков/антибиотиков
Обоснование рекомендации: подавляют рост и размножение патогенных микробов в слизистых оболочках горла и гортани, способствуют снятию воспаления и боли за счет содержания дополнительных компонентов.
На заметку провизору
Местные НПВП
Обоснование рекомендации: благодаря выраженному местному противовоспалительному действию помогают быстро облегчить боль в горле любого происхождения.
Варианты предложения: бензидамин — спрей Оралсепт, спрей/раствор/таблетки для рассасывания Тантум Верде; кетопрофен — раствор ОКИ; флурбипрофен — таблетки для рассасывания Стрепсилс Интенсив.
На заметку провизору
Иммуномодуляторы
Обоснование рекомендации: усиливают специфический и неспецифический противоинфекционный иммунитет к возбудителям лор-инфекций, применяются для профилактики и комплексного лечения часто повторяющихся инфекционных заболеваний горла.
На заметку провизору
Системные НПВП
Обоснование рекомендации: обладают выраженным обезболивающим и противовоспалительным действием. Могут применяться, если боль в горле не купируется местными средствами или сопровождается выраженным подъемом температуры (ангина, грипп и др.).
На заметку провизору
Нелекарственный ассортимент
Экспресс-тест для диагностики стрептококковой ангины
Обоснование рекомендации: применяется для домашней самодиагностики заболеваний, вызванных β-гемолитическим стрептококком группы А.
Варианты предложения: Стрептатест.
На заметку провизору
Устройство может пригодиться пациенту с болью в горле перед визитом в поликлинику. Врачи при инфекционно-воспалительных заболеваниях горла нередко назначают антибиотики эмпирически — без предварительного исследования патогенной флоры. Отрицательные результаты теста на стрептококк могут освободить пациента от ненужного и потенциально опасного приема антибиотиков.
Местные средства для горла с морской солью
Обоснование рекомендации: очищают слизистые оболочки горла и гортани от микробов, поддерживают их нормальное физиологическое состояние, способствуют уменьшению воспаления. Применяются как дополнение к местным лекарственным средствам.
Варианты предложения: спреи АкваЛОР для горла с алоэ и римской ромашкой, Аква Марис для горла и др.
На заметку провизору
Данные средства могут пригодиться покупателю и для профилактики новых эпизодов инфекционных заболеваний горла.
Нелекарственные леденцы для горла
Обоснование рекомендации: обладают смягчающим действием на слизистую оболочку горла, способствуют уменьшению воспаления. Могут применяться в течение всего дня в дополнение к лекарствам.
Варианты предложения: леденцы и пастилки Доктор Тайсс Швейцарские травы с медом и витамином С, Кармолис с медом, Прополки, Терра-плант шалфей и др.
––––––––––––––––––––––––––––––
* Synovate Comcon (Pharma-Q, HealthIndex, мнение провизоров — весна 2015 г.).
** Synovate Comcon, по весенним волнам исследования PrIndex по 5 городам: Москва, С.-Петербург, Екатеринбург, Новосибирск и Н.Новгород.
Лизобакт : инструкция по применению
Состав
Одна таблетка содержит:
вспомогательные вещества: лактоза моногидрат, камедь трагакантовая, магния стеарат, натрия сахаринат, ванилин.
Описание
Таблетки белого или желтовато-белого цвета, круглые, с риской. Возможны включения в виде черных точек.
Фармакотерапевтическая группа
Средства для лечения заболеваний гортани и глотки. Антисептики.
Показания для применения
Лечение инфекционно-воспалительных заболеваний слизистой оболочки полости рта, десен и гортани, включая афтозные изъязвления слизистой оболочки полости рта.
Примечание: когда присутствуют общие признаки бактериальной инфекции, необходимо рассмотреть системную антибактериальную терапию.
Способы применения и дозировка
Лекарственное средство применяется местно. Таблетки следует медленно рассасывать, не разжевывая, задерживая растаявшую массу таблетки в полости рта как можно дольше, до полного растворения.
Курс лечения 5 дней.
Побочное действие
Лекарственное средство обычно хорошо переносится и побочные явления при его приеме встречаются редко. В отдельных случаях возможны аллергические реакции.
Нарушения со стороны иммунной системы: анафилактический шок, анафилактические реакции, отек Квинке.
Нарушения со стороны кожи и подкожных тканей: крапивница, зуд, фотосенсибилизация.
Противопоказания
Гиперчувствительность к компонентам лекарственного средства (включая гиперчувствительность к белку куриного яйца).
Детский возраст до 6 лет.
Передозировка
Случаев острой передозировки лекарственным средством Лизобакт® не отмечено.
Использование высоких доз пиридоксина, значительно превышающих терапевтические (>200 мг/сут) в течение длительного периода времени (несколько месяцев или лет) может вызвать симптомы сенсорной нейропатии, которая чувством онемения, ощущением покалывания, а также потерей чувствительности в области верхних и нижних конечностей. Эти симптомы обратимы и исчезают после прекращения лечения.
Лечение: отмена лекарственного средства, обильное питье (форсированный диурез).
При появлении других симптомов (сильной боли в горле, головной боли, тошноты, рвоты) или связанной с ними лихорадки, следует пересмотреть тактику лечения.
Данный препарат не следует применять длительно.
Использование высоких доз пиридоксина, значительно превышающих терапевтические (>200 мг/сут) в течение длительного периода времени (несколько месяцев или лет) может вызвать симптомы сенсорной нейропатии, которая чувством онемения, ощущением покалывания, а также потерей чувствительности в области верхних и нижних конечностей. Эти симптомы обратимы и исчезают после прекращения лечения.
Данный препарат содержит лактозу. Поэтому его применение противопоказано пациентам, страдающим непереносимостью галактозы, недостаточностью лактазы или синдромом мальабсорбции глюкозы или галактозы (редкие наследственные заболевания).
Взаимодействие с другими лекарственными средствами
Лизоцим усиливает действие антибиотиков, в том числе пенициллина, хлорамфеникола, нитрофурантоина.
Применение в период беременности и лактации
Лизобакт® может применяться во время беременности и в период кормления грудью.
Влияние на способность управлять автомобилем и работу с движущими механизмами
Не влияет на способность к вождению автотранспорта и управлению механизмами.
Упаковка
По 10 таблеток в контурной ячейковой упаковке из пленки ПВХ и фольги алюминиевой.
По 1,2,3 или 5 контурных ячейковых упаковок вместе с листком-вкладышем помещают в пачку из картона.
Условия хранения
Хранить при температуре не выше ЗО°С.
Хранить в недоступном для детей месте.
Срок годности
5 лет. Лекарственное средство не должно применяться по истечении срока годности.
Информация о производителе (заявителе)
Острые тонзиллофарингиты — взгляд инфекциониста
Рассмотрены подходы к терапии острых тонзиллофарингитов в зависимости от этиологии заболевания. Уделено внимание местным средствам лечения острых тонзиллофарингитов. Приведены клинические случаи.
Approaches to the therapy of acute tonsillopharyngitis, depending on the etiology of the disease, were considered. Special attention was paid to topical remedies for treatment of acute tonsillopharyngitis. Clinical cases were given.
Острые инфекции верхних дыхательных путей относятся к наиболее распространенным инфекционным заболеваниям человека. В 2017 г. общая заболеваемость острыми респираторными инфекциями (ОРИ) составила 21738,0 случаев заболевания на 100 тысяч человек, что на 0,2% больше, чем по данным за 2016 г. При этом 73,1% среди всех зарегистрированных случаев ОРИ приходится на детей в возрасте до 17 лет, у которых регистрируется 81056,75 случая на 100 тысяч населения — на каждые 5 детей приходится 4 случая заболевания [1].
Одним из ведущих клинических проявлений ОРИ является развитие воспалительного процесса в тканях глотки и миндалин, что в медицинской литературе описывается терминами «острый фарингит» и «тонзиллит». Общность этиологии и клинических проявлений острых тонзиллита и фарингита позволяет объединить оба термина в один — «острый тонзиллофарингит», который в настоящее время становится наиболее часто используемым в медицинском сообществе, несмотря на его отсутствие в Международной классификации болезней 10-го пересмотра (МКБ-10). Он более точно отражает распространенность воспалительных изменений глоточного кольца [2]. В этой связи согласно МКБ-10 классифицировать диагнозы острых тонзиллита и фарингита можно следующим образом:
В обсуждаемой в настоящее время Международной классификации болезней 11-го пересмотра сохраняется дифференциация диагнозов на острые тонзиллит и фарингит [4].
Наиболее частыми этиологическими факторами острых тонзиллофарингитов являются респираторные вирусы (аденовирус, вирус парагриппа, респираторно-синтициальный вирус, риновирус), вирусы герпеса (Эпштейна–Барр (ВЭБ), цитомегаловирус), энтеровирусы (вирусы Коксаки). К значимым бактериальным возбудителям относится бета-гемолитический стрептококк группы А (БГСА). Однако определенное место в этиологической структуре острых тонзиллофарингитов занимают стрептококки других групп (С, G), пневмококк, Mycoplasma pneumonia и Chlamydophila pneumoniae [5].
Фарингоскопическая классификация острых тонзиллофарингитов Б. С. Преображенского сохраняет свою актуальность при описании status loсalis и включает в себя катаральную, фолликулярную, лакунарную, фибринозную, герпетическую, флегмонозную (интратонзиллярный абсцесс), язвенно-некротическую и смешанную формы [6].
Острые тонзиллофарингиты могут быть самостоятельным заболеванием (первичные) или клиническим проявлением других заболеваний — инфекционных (скарлатина, дифтерия и т. д.), гематологических (агранулоцитоз, гемобластоз) [7, 8].
Общность клинических проявлений острых тонзиллофарингитов различной этиологии (боль в горле, лихорадка, симптомы интоксикации, реакция регионарных лимфатических узлов) в дебюте заболевания нередко создает определенные диагностические трудности. Данный факт наглядно демонстрирует клинический пример 1.
Клинический пример 1
Пациентка (В.О.В., 16 лет) поступила в инфекционное отделение 31 июля 2016 г. с направляющим диагнозом «острый тонзиллит неуточненный, левосторонний подчелюстной лимфаденит» и жалобами на повышение температуры тела, боль в горле, вялость, слабость.
Anamnesis morbi. Острое начало заболевания за сутки до поступления в стационар с повышения температуры до 39,6 °С, появления вялости, слабости, болей в горле, отека подкожно-жировой клетчатки лица и шеи слева.
Status praesens. Состояние при поступлении тяжелое. Выраженный интоксикационный синдром. Температура тела 39,1 °С. Выраженный двухсторонний отек лица и шеи, безболезненный при пальпации, тестоватой консистенции, в течение 2 суток спустившийся на верхнюю часть грудной клетки. Тоны сердца несколько приглушены, ритмичные. ЧСС 94 уд./мин, АД 110/60 мм рт. ст. В легких дыхание везикулярное, проводится во все отделы. Хрипов нет. ЧДД 20 в минуту. Живот мягкий, доступен глубокой пальпации, безболезненный. Печень у края реберной дуги по среднеключичной линии, безболезненная. Селезенка не пальпируется. Моча светлая. Стул в отделении оформленный.
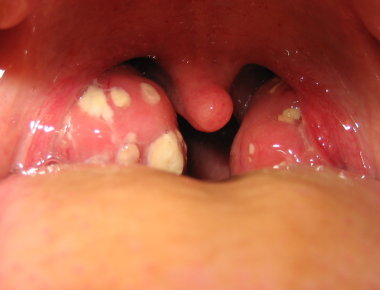
Status localis. Односторонние налеты на миндалинах пленчатого характера серовато-белесоватого цвета, при отделении не дающие кровоточащую поверхность, клинические признаки острого фарингита (рис. 1). Гипертрофический гингивит (рис. 2).
Лабораторное обследование при поступлении: гемоглобин 159 г/л, лейкоциты 16,4 × 10 9 /мл, лейкоцитарная формула: метамиелоциты 1%, п/я 21%, с/я 60%, моноциты 2%, лимфоциты 15%, эозинофилы 1%, СОЭ 24 мм/час.
Детальный анализ эпидемиологического анамнеза — пациент доставлен из очага массового падежа скота (олени), за 3–5 дней до заболевания со слов больной «вытягивала зубами жилы» из туши погибшего животного с целью приготовления нитей для шитья, а также проведенная этиологическая диагностика (исключение таких инфекционных заболеваний, как дифтерия, туляремия, обнаружение методом ПЦР антигена Bacillus anthracis (мазок со слизистых полости рта)) позволили поставить диагноз: «сибирская язва, орофарингеальная форма, тяжелая форма».
Наиболее часто этиологическими факторами острых тонзиллофарингитов являются вирусы: вирус Эпштейна–Барр, респираторно-синцитиальный вирус, вирусы Коксаки, аденовирусы, герпесвирусы [9].
Клиническая картина вирусных острых тонзиллофарингитов характеризуется непатогномоничными общими симптомами: лихорадка (от субфебрильной до гипертермии), интоксикационным синдромом (общая слабость, головная боль, снижение аппетита и др.), болью в горле, увеличением шейных лимфоузлов. В status localis отмечаются гиперемия зева, отечность миндалин. Отличительными особенностями клинической картины острых тонзиллофарингитов вирусной этиологии является наличие катарального синдрома, конъюнктивита и катаральный характер налетов на миндалинах [10].
ВЭБ-инфекция является одной из наиболее значимых в этиологической структуре острых тонзиллофарингитов, особенно у детей и лиц молодого возраста. Особенности клинических проявлений данной инфекции наглядно демонстрирует клинический пример 2.
Клинический пример 2
Пациент (В.А.А., 6 лет, пол мужской) поступает с жалобами на повышение температуры тела до 39,8 °С, боль в горле и при глотании, слабость, выраженное затруднение носового дыхания. На фоне лихорадки отмечались кратковременные судороги, сопровождавшиеся развитием спутанного сознания.
Anamnesis vitae. Ребенок от первой беременности, протекавшей без патологии. Первых срочных родов. Родился доношенный массой тела 3150 г. Грудное вскармливание продолжалось до 8 месяцев. Отклонений в темпах роста и развития зафиксировано не было. Перенесенные заболевания: острые респираторные инфекции (2–3 раза в год). На учете у специалистов не состоит.
Anamnesis morbi. Заболел остро за сутки до поступления с появления слабости, снижения аппетита, повышения температуры тела до 38,0 °С. В течение суток лихорадка возросла, снижалась незначительно при назначении НПВС, присоединились боли в горле, затруднение носового дыхания. Осмотрен участковым врачом, обнаружены налеты на миндалинах фибринового характера, выраженная лимфаденопатия шейных лимфоузлов, увеличение подмышечных и паховых лимфоузлов. На догоспитальном этапе назначен амоксициллин с клавулановой кислотой. Доставлен в стационар в связи с развитием фебрильных судорог.
Status praesens. Состояние ребенка при поступлении средней тяжести. Отмечается выраженная слабость, вялость. Температура тела 39,5 °С, ЧСС 118 уд./мин, АД 100/60 мм рт. ст., ЧДД 24 в минуту. Кожные покровы умеренной бледности, влажность удовлетворительная, сыпи нет. Носовое дыхание значительно затруднено, отделяемого из носа нет. Зев гиперемирован, миндалины увеличены, смыкаются, налеты нитевидные фибриновые. Лимфоузлы подчелюстные, передние шейные, подмышечные, паховые увеличены. Тоны сердца ясные, ритмичные. В легких дыхание проводится во все отделы. Хрипов нет. Живот мягкий, доступен глубокой пальпации, болезненный в мезогастрии. Печень у края реберной дуги по среднеключичной линии, безболезненная. Селезенка не пальпируется. Моча светлая. Стул в отделении однократно, оформленный.
Лабораторная этиологическая диагностика. ПЦР (кровь, мазок из ротоглотки) — обнаружены ВЭБ и вирус герпеса человека (ВГЧ) VI типа.
Диагноз: сочетанные ВЭБ и ВГЧ VI инфекции.
При Эпштейна–Барр острых тонзиллофарингитах, как и при тонзиллофарингитах другой этиологии, отмечается острое начало, фебрильная лихорадка, выраженный интоксикационный синдром. Отличительными особенностями являются наличие затруднения носового дыхания без отделяемого из носовых ходов за счет отека лимфоидной ткани, увеличение всех групп шейных лимфоузлов, поверхностный фибриновый налет на миндалинах, гепатоспленомегалия (которая развивается постепенно и в первые сутки заболевания может не определяться). При лабораторном обследовании могут быть лейкоцитоз или лейкопения, характерны лимфоцитоз, моноцитоз, однако наличие атипичных мононуклеаров диагностируется только у 83% больных и также может не определяться в дебюте инфекции. В приведенном выше клиническом примере участковым врачом в дебюте инфекции не было учтено наличие у пациента выраженной заложенности носа без отделяемого, лимфаденопатии и характерных изменений миндалин, что привело к необоснованному назначению антибактериальной терапии. Развитие у пациента судорожного синдрома можно объяснить сочетанным течением инфекций — ВЭБ и ВГЧ VI [11].
Энтеровирусные инфекции нередко становятся причиной обращения к врачу с жалобами на боли в горле, что требует проведения дифференциальной диагностики с острыми тонзиллофарингитами другой этиологии. Для энтеровирусной инфекции характерны острый подъем температуры тела до 39 °С и более, наличие дисфагии, болей в горле, повышенной саливации и поражение ЖКТ (боли в животе, тошнота, рвота, диарея). В status localis отмечаются характерные изменения — герпангина — проявляющиеся высыпаниями на передних дужках неба, миндалинах, язычке и задней стенке глотки в виде мелких папул 1–2 мм с красным венчиком, трансформирующиеся в несливающиеся между собой везикулы с прозрачным содержимым, которые в течение 24–48 ч вскрываются с образованием эрозий. Данная инфекция более характерна для детей раннего возраста [12].
Наличие сыпи на коже и слизистых оболочках у пациента требует исключения таких инфекционных заболеваний, как корь, скарлатина, краснуха, при которых одним из клинических проявлений является острый тонзиллофарингит [13].
Среди бактериальных инфекций в этиологии острых тонзиллофарингитов наиболее значимыми являются вызванные БГСА [2].
Клиническими особенностями БГСА острого тонзиллофарингита (БГСА-ТФ) являются острое начало с лихорадкой и головной болью, выраженная боль в горле, яркая гиперемия миндалин и задней стенки глотки, на миндалинах отмечаются гнойные налеты на фоне отечности миндалин и язычка. Не характерны для данной инфекции наличие ринита, кашля, симптомов ларингита, конъюнктивита, стоматита, диареи [10].
Верификация БГСА-ТФ важна в дебюте инфекции, так как диктует необходимость решения вопроса назначения системной антибактериальной терапии, важность своевременного назначения которой демонстрирует клинический пример 3.
Клинический пример 3
Пациент (4 года, пол женский) поступает с жалобами на гиперкинезы, статокоординационные нарушения.
Anamnesis vitae. Ребенок от первой беременности, протекавшей без патологии. Первых срочных родов. Родилась доношенной. Искусственное вскармливание с возраста 1 месяц (адаптированная молочная смесь). Рост и развитие соответствовали возрасту. На учете у специалистов не состоит.
Anamnesis morbi. Со слов родителей, за 3 недели до появления настоящих жалоб ребенок перенес острый тонзиллофарингит. За медицинской помощью не обращались. Этиологическая диагностика не осуществлялась. Системная антибактериальная терапия не проводилась. В лечении использовались средства фитотерапии и симптоматические лекарственные средства.
Status praesens. Состояние ребенка при поступлении средней тяжести. Отмечаются умеренные слабость, вялость. Температура тела 37,0 °С, ЧСС 100 уд./мин, АД 90/60 мм рт. ст, ЧДД 24 в минуту. Кожные покровы обычного цвета, влажность удовлетворительная, сыпи нет. Носовое дыхание свободное, отделяемого из носа нет. Миндалины не увеличены, налетов нет. Видимые слизистые полости рта без патологии. Язык: чистый, налетов нет. Лимфоузлы подчелюстные незначительно увеличены, безболезненны при пальпации, не спаяны между собой и окружающими тканями; передние шейные, подмышечные, паховые лимфоузлы не увеличены. Тоны сердца ясные, звучные, ритмичные. В легких дыхание везикулярное, проводится во все отделы, хрипов нет. Живот мягкий, доступен глубокой пальпации, безболезненный. Печень не увеличена, безболезненная при пальпации. Селезенка не пальпируется. У ребенка отмечается избыточная масса тела (87-й процентиль). Моча светлая. Стул оформленный (со слов родителей).
В неврологическом статусе: сознание ясное. Менингеальные симптомы отсутствуют. При одевании, приеме пищи, игре и ходьбе у ребенка отмечаются хаотичные, непроизвольные, не стереотипные, нерегулярные, быстрые движения, захватывающие преимущественно проксимальные отделы конечностей, затрудняющие координацию действий пациента, усиливающиеся во время эмоционального напряжения. Неустойчивость в пробе Ромберга. Выполнение пальце-носовой и пяточно-коленной проб затруднено из-за гиперкинезов. Болевая, температурная, тактильная, проприоцептивная чувствительность не нарушена. Рефлексы снижены и неравномерны, наблюдается положительный симптом Гордона-2 (при вызывании коленного рефлекса наблюдается более продолжительное, чем у здорового, разгибание голени).
Лабораторная диагностика: повышение титров антистрептолизина-О (280 ЕД/мл, норма до 100 ЕД/мл), СОЭ (22 мм/ч), С-реактивного белка (10 мг/л), лейкоцитоз (19 × 10 9 /л).
Диагноз: «Ревматическая хорея без вовлечения сердца (I02.9). Избыточная масса тела, конституционально-алиментарная форма».
Развитие постинфекционной ревматической хореи у данного пациента было связано с отсутствием этиотропной терапии острого тонзиллофарингита, вызванного БГСА, что подчеркивает значимость ранней диагностики данной инфекции.
В этой связи можно использовать клинические и лабораторные методы верификации диагноза. Клинически ранее широко использовалась таблица Centor [14], однако ввиду низкой специфичности и чувствительности в настоящее время международным сообществом рекомендованы критерии W. J. McIsaac [15]. Согласно данной шкале оценивается наличие любого из следующих критериев:
Наличие каждого из симптомов соответствует 1 баллу, 3 и более баллов свидетельствуют о высокой вероятности БГС-ТФ. По мнению ряда авторов данная шкала у взрослых пациентов может помочь в принятии решения о назначении противомикробных препаратов, но не помогает в диагностике БГС-ТФ [2]. В этой связи актуальным для практического врача является возможность проведения лабораторной диагностики у постели больного, что можно реализовать с помощью стрептотеста [16].
При наличии локализованного безболезненного эрозивного образования, имеющего гладкую блестящую поверхность, ярко-красную окраску, округлую или овальную форму с невыраженным уплотнением у основания, необходимо исключать первичный период сифилиса. Лихорадочная реакция, интоксикационный синдром и реакция регионарных лимфатических узлов у таких больных могут отсутствовать.
Несмотря на то, что в 2017 г. в Российской Федерации случаев дифтерии зарегистрировано не было [1], рассматривая дифференциальную диагностику острых тонзиллофарингитов, необходимо исключать данную инфекцию, особенно учитывая текущую эпидемиологическую ситуацию в ряде стран [17]. Для дифтерии характерна лихорадка, выраженные симптомы интоксикации, наличие тахикардии, боль в горле при глотании. При осмотре определяются запах ацетона изо рта, значительное увеличение шейных лимфоузлов и отек подкожной клетчатки шеи. Миндалины гиперемированы, отечны, покрыты сероватыми, сливными, плохо снимающимися налетами, которые распространяются на небные дужки и мягкое небо, а при удалении оставляют кровоточащую поверхность [18].
При развитии острого тонзиллофарингита чрезвычайно важно провести дифференциальный диагноз между бактериальной, в первую очередь стрептококковой, и вирусной инфекцией. В случае развития последней системная антибактериальная терапия не показана, а при бактериальных тонзиллитах вопрос назначения антибактериальных препаратов решается индивидуально, в зависимости от вероятности риска инфекции, вызванной БГСА. В случае доказанной или с высокой долей вероятности подозреваемой стрептококковой этиологии острого тонзиллофарингита у детей необходимо назначать системную антибактериальную терапию [19].
Рекомендации Национального института охраны здоровья и совершенствования медицинской помощи Великобритании (National Institute of Health and Care Excellence, NICE) включают в себя показания к назначению антибактериальных препаратов в случае развития системной бактериальной инфекции, при наличии осложнений (перитонзиллярный абсцесс), а также в случае наличия сопутствующих заболеваний, повышающих риск развития осложнений [20].
Антибиотиками первого ряда при острых тонзиллофарингитах являются β-лактамные антибиотики: пенициллины и цефалоспорины, так как отличаются высокой чувствительностью к ним БГСА и отсутствием резистентности (табл.) [21].
В настоящее время БГСА являются этиологической причиной острых тонзиллофарингитов от 5% до 15% во взрослой популяции и 20–30% — у детей [22]. В большинстве случаев наблюдается острый тонзиллофарингит не-БГСА-этиологии. Наиболее распространенной является вирусная этиология острого тонзиллофарингита, по данным ряда авторов она составляет от 70% до 90% [23–26].
Зачастую врачи общей практики, терапевты, педиатры назначают системные антибиотики широкого спектра еще до получения результатов бактериологического исследования. На практике такая гипердиагностика приводит к избыточному назначению антибиотиков — до 98% случаев (!) [27].
Следует особо подчеркнуть, что назначение антибактериальных препаратов требует рационального подхода и обязательного проведения дифференциальной диагностики. Неадекватно подобранная терапия острого инфекционно-воспалительного процесса респираторного тракта приводит к дисбиозу верхних дыхательных путей, нарушению колонизационной резистентности биотопа, а в результате — к подавлению топического иммунитета, хронизации тонзиллитов и фарингитов, появлению очень трудных для лечения форм заболеваний [28]. Необоснованное применение системных антимикробных препаратов способствует развитию токсико-аллергических реакций, в частности при ВЭБ-инфекции, обусловливает рост числа антибиотикорезистентных штаммов и их распространение в популяции. Назначение системных антибиотиков всегда должно быть клинически оправданным и ограничено строгими медицинскими показаниями [29].
В случаях нестрептококковой этиологии острого тонзиллофарингита, а также при БГСА-инфекционных процессах комплексно с системной антибактериальной терапией возможно топическое применение антимикробных препаратов. Целью местной терапии является быстрое уменьшение выраженности болевого синдрома и других воспалительных явлений, а также профилактика вторичного инфицирования поврежденной слизистой оболочки.
В этой связи оправдано применение местной терапии в виде антисептических и антибактериальных средств для топического применения в полости рта и глотке [30].
Препараты для местной антимикробной терапии представлены на российском рынке в достаточно большом количестве и различных фармакологических формах (таблетки и леденцы для рассасывания, спреи, растворы для обработки слизистых).
Главными требованиями к наносимым на слизистую оболочку препаратам являются:
Действующими веществами в данных препаратах являются различные антисептические средства (грамицидин С, хлоргексидин, гексетидин, бензидамин, тимол и его производные, спирты, препараты йода и др.), в том числе в сочетании с местными анестетиками (лидокаин, тетракаин, ментол), препараты на основе растительного сырья (экстракт ромашки и др.), а также содержащие факторы неспецифической противоинфекционной защиты (лизоцим) и бактериальные лизаты. Каждая из лекарственных форм имеет свою терапевтическую нишу, однако практическому врачу необходимо учитывать токсичность некоторых соединений (например, хлоргексидина), что диктует необходимость активного контроля схем применения препаратов пациентами [31]. Также при выборе местной терапии необходимо учитывать риски развития аллергических реакций (препараты на основе растительного сырья и продуктов пчеловодства), раздражающего действия (средства, содержащие йод) [32, 33].
Значимым для практического здравоохранения является наличие у местных средств лечения острых тонзиллофарингитов бактерицидного действия и влияния на биопленки микроорганизмов. Одними из средств, отвечающих всем требованиям, предъявляемым к наносимым на слизистую оболочку препаратам, и эффективно справляющихся с микроорганизмами в составе биопленок, являются препараты серии Граммидин: Граммидин нео, Граммидин детский, Граммидин нео с анестетиком, Граммидин спрей и Граммидин спрей детский.
Действующими веществами являются грамицидин C и цетилпиридиния хлорид. Грамицидин С является пептидным антибиотиком тиротрициновой группы. Он был выделен в 1942 г. Г. Ф. Гаузе и М. Г. Бражниковой из штамма Bacillus brevis. Отличительной особенностью грамицидина С является циклическая структура белка, содержащая пять различных аминокислот. Спектр противомикробной активности включает грамположительные бактерии, в том числе стрептококки и стафилококки, некоторые грамотрицательные бактерии, грибковую микрофлору, а также возбудителей анаэробной инфекции. Микроорганизмы не развивают устойчивость к данному антибиотику [34, 35]. Механизм антибактериального действия грамицидина С заключается в образовании сети каналов в липидном бислое мембраны, что повышает проницаемость мембран микробной клетки и в конечном итоге приводит к ее гибели [36, 37].
Входящий в состав Граммидина цетилперидиния хлорид представляет собой катионовый сурфактант, оказывающий дестабилизирующее действие на мембраны микробной клетки. Для него доказано выраженное дестабилизирующее действие на биопленки патогенных микроорганизмов, что потенциирует антибактериальное действие грамицидина C. В исследованиях было показано, что обработка биопленки раствором цетилперидиния хлорида в концентрациях 0,05–0,5% приводит к гибели 90% бактерий и уменьшению толщины биопленки на 34,5–43,0% [38]. В Граммидин нео с анестетиком входит анестетик местного действия — оксибупрокаина гидрохлорид.
Таким образом, острые тонзиллофарингиты требуют от врача исключения целого спектра инфекционных заболеваний и дифференцированного в зависимости от этиологии подхода к терапии.
Литература
А. А. Плоскирева, доктор медицинских наук, профессор
ФБУН ЦНИИЭ Роспотребнадзора, Москва
Острые тонзиллофарингиты – взгляд инфекциониста/ А. А. Плоскирева
Для цитирования: Лечащий врач № 10/2018; Номера страниц в выпуске: 7-12
Теги: глотка, миндалины, воспаление, инфекция

.png)
_575.gif)