газ cf4 что это
Тетрафторид углерода
| Тетрафторид углерода | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | фторид углерода(IV), тетрафторид углерода |
| Сокращения | R14 |
| Традиционные названия | тетрафторметан, перфторметан, метфоран, углерод четырехфтористый, углерода тетрафторид, фреон 14, хладон 14 |
| Химическая формула | CF4 |
| Физические свойства | |
| Состояние (ст. усл.) | бесцветный газ без запаха |
| Молярная масса | 88.0043 г/моль |
| Плотность | 3.72 г/см³ |
| Термические свойства | |
| Температура плавления | −183.6 °C |
| Температура кипения | −127.8 °C |
| Температура вспышки | негорюч °C |
| Температура самовоспламенения | 1100 °C |
| Критическая точка | температура: −45,65 °C |
плотность: 0,625 г/см³
Тетрафторметан — бинарное химическое соединение. Химическая формула — CF4. Синонимы: четырёхфтористый углерод, тетрафторид углерода, фреон 14, хладон 14.
Содержание
Свойства
Физические
При комнатной температуре представляет собой химически инертный, бесцветный газ без запаха.
Свойства соединения
Тетрафторметан является одним из самых стабильных соединений в органической химии. Из фторпроизводных метана, представленных фторметаном, дифторметаном, трифторметаном и тетрафторметаном, связь фтора и углерода в тетрафторметане является самой прочной.
Получение
Она также может быть получен фторированием двуокиси углерода, окиси углерода или фосгена с помощью тетрафторида серы. Коммерчески он производится реакцией фтора с дихлордифторметаном или хлортрифторметаном; также — в ходе электролиза фторидов металла MF, MF2 с помощью угольного электрода.
Тетрафторметан, как и другие фторуглероды, весьма устойчив благодаря связи фтор—углерод. Энергия связи в этом соединении равна 515 кДж/моль. В результате этого он инертен по отношению к кислотам и гидроксидам. Тем не менее, он реагирует со взрывом с щелочными металлами. При контакте тетрафторметана с пламенем получаются токсичные газы (например карбонилфторид или окись углерода); в присутствии воды получается фтороводород.
Синтез
Также можно получить данное вещество из углекислого газа, угарного газа или фосгена фторированием тетрафторидом серы:
При температуре в 350—375 °C углерод в форме графита реагирует с трифторидом азота:
Самым простым способом получения является реакция при температуре выше 900 °C углерода с фтором:

Использование
Воздействие на окружающую среду
Тетрафторметан является сильным парниковым газом, который способствует парниковому эффекту. Это очень стабильное соединение, время его распада составляет примерно 50 000 лет, в то время как самая высокая отметка ПГП составляет 6500 лет (главным парниковым газом является CO2).
Тетрафторметан схож по строению с хлорфторуглеродом (ХФУ), но в отличие от него тетрафторметан не разрушает озоновый слой. Это происходит потому, что с озоном взаимодействуют атомы хлора в ХФУ, которые образуются под действием ультрафиолетового излучения.
Опасность использования
При контакте кожи с жидкостью возможно обморожение. Вдыхание тетрафторметана может привести, в зависимости от концентрации, к головной боли, помутнению сознания, тошноте, головокружению и повредить сердечно-сосудистую систему. Длительное воздействие может вызвать серьёзные повреждения сердца.
Благодаря своей плотности тетрафторметан может вытеснить воздух, что может привести к удушению в недостаточно проветриваемых помещениях.
См. также
Примечания
Полезное
Смотреть что такое «Тетрафторид углерода» в других словарях:
Тетрафторид кремния — Тетрафторид кремния … Википедия
Тетрафторид теллура — Общие Систематическое наименование Тетрафторид теллура Традиционные названия Фтористый теллур Химическая формула TeF4 Физические свойства Состоян … Википедия
УГЛЕРОДА СЕМЕЙСТВО — ПОДГРУППА IVA. СЕМЕЙСТВО УГЛЕРОДА КРЕМНИЯ УГЛЕРОД, КРЕМНИЙ, ГЕРМАНИЙ, ОЛОВО, СВИНЕЦ Характерная для подгруппы IIIA особенность постепенного перехода от легкого неметаллического элемента к тяжелому типичному металлу наблюдается и в этой подгруппе … Энциклопедия Кольера
Список неорганических соединений по элементам — Основная статья: Неорганические соединения Список неорганических соединений по элементам информационный список неорганических соединений, представленный в алфавитном порядке (по формуле) для каждого вещества, водородные кислоты элементов (при их… … Википедия
Фтор — У этого термина существуют и другие значения, см. Фтор (значения). 9 Кислород ← Фтор → Неон … Википедия
Фторид диртути(2+) — Систематическое название Фторид диртути(2+) Другие названия Дифторид д … Википедия
Фреоны — (хладоны) техническое название группы насыщенных алифатических фторсодержащих углеводородов, применяемых в качестве хладагентов, пропеллентов, вспенивателей, растворителей. Кроме атомов фтора фреоны могут содержать атомы хлора или брома[1].… … Википедия
Тетрафторэтилен — Тетрафторэтилен … Википедия
Хлорфторуглероды — Хлорфторуглероды органические соединения, состоящие иcключительно из атомов хлора (Cl), фтора (F) и углерода (С). Различают низшие хлорфторуглероды (CFC) низкокипящие органические соединения на основе метанового, этанового и… … Википедия
Фторорганические соединения — – это галогенсодержащие соединения, содержащие хотя бы один атом фтора. В 30 х годах прошлого века для разделения изотопов UF6 возникла необходимость в устойчивых к нему смазочных материалах. Проблема была решена предоставленным Джоном Саймонсом… … Википедия
Газ cf4 что это
температура: −45,65 °C
плотность: 0,625 г/см³
Тетрафтормета́н — бинарное химическое соединение. Химическая формула — CF4. Другие названия — четырёхфтористый углерод, тетрафторид углерода. Коммерческие названия соединения при использовании в качестве хладагента: фреон-14, хладон-14.
Тетрафторметан является самым простым из перфторуглеродов. По сравнению с другими тетрагалогенидами углерода обладает более высокой химической стойкостью. Из-за большого количества связей углерод-фтор и высокой электроотрицательности фтора атом углерода в этом соединении имеет значительный положительный заряд, что укрепляет и укорачивает связь углерод-фтор.
Содержание
Физические свойства [ | ]
При комнатной температуре представляет собой химически инертный, бесцветный газ без запаха и вкуса, примерно в 3 раза тяжелее воздуха. Его температура плавления −184 °С и температура кипения −128 °С.
Очень плохо растворим в воде (20 мг/кг при 20 °С [2] ), в этаноле (около 80 мг/кг при 25 °С [3] ) и бензоле (около 64 мг/кг при 25 °C [4] ).
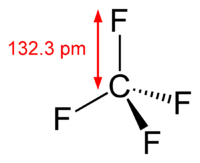
Из 4 фторпроизводных метана, — фторметана, дифторметана, трифторметана и тетрафторметана, связь между атомами фтора и углерода в тетрафторметане является самой прочной. Это обусловлено высокой электроотрицательностью атомов фтора, оттягивающих электронное облако от атома углерода на себя, в результате чего атом углерода оказывается заряжен положительно: +0,76 элементарного заряда и это усиливает кулоновские силы между положительно заряженным атомом углерода и отрицательно заряженными атомами фтора.
Химические свойства [ | ]
Тетрафторметан, как и другие перфторуглероды весьма устойчив благодаря прочности связи фтор—углерод и является одним из самых стабильных соединений среди всех органических веществ. Энергия связи в этом соединении равна 515 кДж/моль. Поэтому он инертен по отношению к кислотам и основаниям.
При высоких температурах в присутствии кислорода или на воздухе он разлагается с образованием карбонилфторида и оксида углерода (II).
Реагирует с некоторыми активными металлами, и с щелочными металлами:
При контакте тетрафторметана с пламенем в избытке кислорода получаются токсичные газы (карбонилфторид и окись углерода); в присутствии воды образуется фтороводород.
Получение [ | ]
Тетрафторметан может быть получен в лабораторных условиях при реакции карбида кремния с фтором:
При температуре в 350—375 °C углерод в форме графита реагирует с трифторидом азота:
Одним из способов получения является реакция при температуре выше 900 °C углерода с фтором:
В промышленности, из-за трудности получения элементарного фтора и его дороговизны тетрафторметан получают из дифтордихлорметана или хлортрифторметана воздействием фтороводорода:
В качестве побочного продукта тетрафторметан в промышленности образуется при фторировании любых органических соединений и при получении алюминия электролитическим способом, в ходе электролиза фторидов металлов, входящих в состав криолита с помощью угольного электрода.
Использование [ | ]
Воздействие на окружающую среду [ | ]
Тетрафторметан является газом, вызывающим сильный парниковый эффект. Потенциал глобального потепления (ПГП) тетрафторметана на временном интервале 100 лет составляет 7390 единиц, для сравнения, ПГП основного парникового газа — углекислого газа (CO2) принимается равным 1. Но этот газ не вносит пока существенный вклад в парниковый эффект, так как его концентрация в атмосфере очень низка. Тетрафторметан очень стабильное соединение, время его полураспада в атмосфере составляет примерно 50 000 лет и поэтому происходит его постепенное техногенное накопление в атмосфере.
Тетрафторметан схож по строению с хлорфторметанами, но в отличие от них тетрафторметан не разрушает озоновый слой. Это происходит потому, что озон разрушают атомы хлора, образующиеся при фотодиссоциации хлорфторуглеродов под воздействием ультрафиолетового излучения Солнца.
Опасность использования [ | ]
При вдыхании воздуха с бо́льшими концентрациями возможно кислородное голодание и развитие симптомов, сходных с высотной болезнью — сопровождающиеся головной болью, помутнением сознания, тошнотой, головокружением.
При контакте с кожей сжиженного тетрафторметана возможно обморожение.
Газ cf4 что это
температура: −45,65 °C
плотность: 0,625 г/см³
Тетрафтормета́н — бинарное химическое соединение. Химическая формула — CF4. Другие названия — четырёхфтористый углерод, тетрафторид углерода. Коммерческие названия соединения при использовании в качестве хладагента: фреон-14, хладон-14.
Тетрафторметан является самым простым из перфторуглеродов. По сравнению с другими тетрагалогенидами углерода обладает более высокой химической стойкостью. Из-за большого количества связей углерод-фтор и высокой электроотрицательности фтора атом углерода в этом соединении имеет значительный положительный заряд, что укрепляет и укорачивает связь углерод-фтор.
Содержание
Физические свойства
При комнатной температуре представляет собой химически инертный, бесцветный газ без запаха и вкуса, примерно в 3 раза тяжелее воздуха. Его температура плавления −184 °С и температура кипения −128 °С.
Очень плохо растворим в воде (20 мг/кг при 20 °С [2] ), в этаноле (около 80 мг/кг при 25 °С [3] ) и бензоле (около 64 мг/кг при 25 °C [4] ).
Из 4 фторпроизводных метана, — фторметана, дифторметана, трифторметана и тетрафторметана, связь между атомами фтора и углерода в тетрафторметане является самой прочной. Это обусловлено высокой электроотрицательностью атомов фтора, оттягивающих электронное облако от атома углерода на себя, в результате чего атом углерода оказывается заряжен положительно: +0,76 элементарного заряда и это усиливает кулоновские силы между положительно заряженным атомом углерода и отрицательно заряженными атомами фтора.
Химические свойства
Тетрафторметан, как и другие перфторуглероды весьма устойчив благодаря прочности связи фтор—углерод и является одним из самых стабильных соединений среди всех органических веществ. Энергия связи в этом соединении равна 515 кДж/моль. Поэтому он инертен по отношению к кислотам и основаниям.
При высоких температурах в присутствии кислорода или на воздухе он разлагается с образованием карбонилфторида и оксида углерода (II).
Реагирует с некоторыми активными металлами, и с щелочными металлами:
При контакте тетрафторметана с пламенем в избытке кислорода получаются токсичные газы (карбонилфторид и окись углерода); в присутствии воды образуется фтороводород.
Получение
Тетрафторметан может быть получен в лабораторных условиях при реакции карбида кремния с фтором:
При температуре в 350—375 °C углерод в форме графита реагирует с трифторидом азота:
Одним из способов получения является реакция при температуре выше 900 °C углерода с фтором:
В промышленности, из-за трудности получения элементарного фтора и его дороговизны тетрафторметан получают из дифтордихлорметана или хлортрифторметана воздействием фтороводорода:
В качестве побочного продукта тетрафторметан в промышленности образуется при фторировании любых органических соединений и при получении алюминия электролитическим способом, в ходе электролиза фторидов металлов, входящих в состав криолита с помощью угольного электрода.
Использование
Воздействие на окружающую среду
Тетрафторметан является газом, вызывающим сильный парниковый эффект. Потенциал глобального потепления (ПГП) тетрафторметана на временном интервале 100 лет составляет 7390 единиц, для сравнения, ПГП основного парникового газа — углекислого газа (CO2) принимается равным 1. Но этот газ не вносит пока существенный вклад в парниковый эффект, так как его концентрация в атмосфере очень низка. Тетрафторметан очень стабильное соединение, время его полураспада в атмосфере составляет примерно 50 000 лет и поэтому происходит его постепенное техногенное накопление в атмосфере.
Тетрафторметан схож по строению с хлорфторметанами, но в отличие от них тетрафторметан не разрушает озоновый слой. Это происходит потому, что озон разрушают атомы хлора, образующиеся при фотодиссоциации хлорфторуглеродов под воздействием ультрафиолетового излучения Солнца.
Опасность использования
При вдыхании воздуха с бо́льшими концентрациями возможно кислородное голодание и развитие симптомов, сходных с высотной болезнью — сопровождающиеся головной болью, помутнением сознания, тошнотой, головокружением.
При контакте с кожей сжиженного тетрафторметана возможно обморожение.
КриоМаркет
Холодильное оборудование и запчасти
Каталог

г. Ярославль,
ул. Вспольинское Поле, 14,
строение 2

Пн-ЧТ: 09:00 до 18:00,
Пт: 09:00 до 17:00,
Сб, Вс: выходной

info@kriomarket.com
Фреоны
Физические свойства
Фреоны — бесцветные газы или жидкости без запаха. Хорошо растворимы в неполярных органических растворителях, очень плохо — в воде и полярных растворителях.
Основные физические свойства фреонов метанового ряда:
| Химическая формула | Наименование | Техническое обозначение | Температура плавления, °C | Температура кипения, °C | Относительная молекулярная масса |
|---|---|---|---|---|---|
| CFH3 | фторметан | R-41 | -141,8 | -79,64 | 34,033 |
| CF2H2 | дифторметан | R-32 | -136 | -51,7 | 52,024 |
| CF3H | трифторметан | R-23 | -155,15 | -82,2 | 70,014 |
| CF4 | тетрафторметан | R-14 | -183,6 | -128,0 | 88,005 |
| CFClH2 | фторхлорметан | R-31 | — | -9 | 68,478 |
| CF2ClH | хлордифторметан | R-22 | -157,4 | -40,85 | 86,468 |
| CF3Cl | трифторхлорметан | R-13 | -181 | -81,5 | 104,459 |
| CFCl2H | фтордихлорметан | R-21 | -127 | 8,7 | 102,923 |
| CF2Cl2 | дифтордихлорметан | R-12 | -155,95 | -29,74 | 120,913 |
| CFCl3 | фтортрихлорметан | R-11 | -110,45 | 23,65 | 137,368 |
| CF3Br | трифторбромметан | R-13B1 | -174,7 | -57,77 | 148,910 |
| CF2Br2 | дифтордибромметан | R-12B2 | -141 | 24,2 | 209,816 |
| CF2ClBr | дифторхлорбромметан | R-12B1 | -159,5 | -3,83 | 165,364 |
| CF2BrH | дифторбромметан | R-22B1 | — | -15,7 | 130,920 |
| CFCl2Br | фтордихлорбромметан | R-11B1 | — | 51,9 | 181,819 |
| CF3I | трифториодметан | R-13I1 | — | -22,5 | 195,911 |
Химические свойства
Фреоны очень инертны в химическом отношении, поэтому они не горят на воздухе, невзрывоопасны даже при контакте с открытым пламенем. Однако при нагревании фреонов свыше 250 °C образуются весьма ядовитые продукты, например фосген COCl2, который в годы первой мировой войны использовался как боевое отравляющее вещество.
Устойчивы к действию кислот и щелочей.
Виды фреонов (хладонов)
| Группа | Класс соединений | Фреоны (хладоны) | Воздействие на озоновый слой |
|---|---|---|---|
| A | Хлорфторуглероды (CFC) | R-11, R-12, R-13, R-111, |
R-112, R-113, R-113а, R-114, R-115
R-13B1, R-21B1, R-22B1, R-114B2
R-131, R-132, R-133, R-141, R-142в, R-151, R-221,
R-222, R-223, R-224, R-225, R-231, R-232, R-233
R-152, R-161,R-227, R-236, R-245, R-254
Наиболее распространены следующие соединения:
История названия
В 1928 году американскому химику корпорации «Дженерал Моторс» («General Motors Research») Томасу Миджли (1889—1944) удалось выделить и синтезировать в своей лаборатории химическое соединение, получившее впоследствии название «Фреон». Через некоторое время «Химическая кинетическая компания» («Kinetic Chemical Company»), которая занималась промышленным производством нового газа — Фреон-12, ввела обозначение хладагента буквой R ( R efrigerant — охладитель, хладагент). Такое наименование получило широкое распространение и со временем полное название хладагентов стало записываться в составном варианте — торговая марка производителя и общепринятое обозначение хладагента. Например: торговая марка GENETRON®AZ-20 соответствует хладагенту R-410A, который состоит из хладагентов R-32 (50 %) и R-125 (50 %). Существует также торговая марка с таким же названием, как и у химического соединения — FREON® (Фреон), основным правообладателем которой ранее являлась американская компания «Дюпон» («DuPont»), а теперь компания The Chemours Company (Chemours), созданная на базе одного из подразделений Дюпон. Это совпадение в названии до сих пор вызывает путаницу и споры — можно ли словом фреон называть произвольные хладагенты.
Правила цифрового обозначения фреонов (хладонов)
По международному стандарту ISO № 817-74 техническое обозначение фреона (хладона) состоит из буквенного обозначения R (от слова refrigerant) и цифрового обозначения:
Воздействие на окружающую среду
Влияние на озоновый слой
Считалось, что одной из причин уменьшения озона в стратосфере и образование озоновых дыр является производство и применение хлор- и бромсодержащих фреонов. Попадая после использования в атмосферу, они разлагаются под воздействием ультрафиолетового излучения Солнца. Высвободившиеся компоненты активно взаимодействуют с озоном в галогеновом цикле распада атмосферного озона.
Подписание и ратификация странами ООН Монреальского протокола привело к уменьшению производства озоноразрушающих фреонов.
В связи с пагубным влиянием озоноразрушающего фреона R-22, его использования год от года сокращается в США и Европе, где с 2010 года официально запрещено применять этот фреон. В России c 2011 года прекращен импорт холодильного оборудования, в том числе кондиционеров промышленного и полу-промышленного класса, однако сам фреон пока производится в стране. На замену фреону R-22 должен прийти фреон R-410A, а также ретрофиты R-407C, R-422D.
В автомобильных кондиционерах до 1992 года применялся тип фреона R-12, но считалось, что он вреден для озонового слоя, поэтому был разработан и стали применять R-134, который считается безопасным для озонового слоя земли.
Парниковый эффект
Парниковая активность (англ. GWP — ПГП) фреонов в зависимости от марки варьирует в пределах от 1300 до 8500 раз выше чем у углекислого газа при одинаковых объёмах. Основным источником фреонов являются холодильные установки и аэрозоли.










