гармонический скальпель что это
Современные технологии в лечении хронического геммороя
Геморрой является одним из широко распространенных заболеваний взрослого населения индустриально развитых стран. Установлено, что у людей старше 40 лет симптомы геморроя обнаруживаются в 60-70 % случаев. На долю геморроя, в структуре колопроктологических заболеваний, приходится около 40%.
В последние годы в повседневную практику колопроктологов уже прочно внедрились малоинвазивные способы лечения геморроя. Преимущества этих методов перед хирургическими вмешательствами, заключаются в возможности их применения в амбулаторных условиях, без потери трудоспособности; высокой эффективности, при начальных стадиях заболевания; небольшом числе осложнений.
Наиболее часто используемыми малоинвазивными методами являются:
При выборе способа лечения больных геморроем, целесообразно пользоваться классификацией, которая подразделяет хронический геморрой на IV стадии.
К противопоказаниям относятся: сочетание геморроя с анальной трещиной, свищем прямой кишки, воспалительные заболевания анального канала и промежности, острый геморрой.
Лигирование геморроидальных узлов латексными кольцами является наиболее часто применяемой методикой (32-82%), а склеротерапия, в связи частым развитием осложнений (11-47%), используется все реже. Остальные методы малоинвазивного лечения применяются менее чем в 5% случаев.
Лигирование геморроидальных узлов латексными кольцами
Впервые разработал и использовал инструмент для наложения циркулярной латексной лигатуры на ножку геморроидального узла Blaisdell в 1954г. В последующем, были разработаны другие, более совершенные модели лигаторов.
Применение данного метода показано при внутреннем геморрое II, иногда III ст. Противопоказаниями для выполнения лигирования геморроидальных узлов являются: сочетание внутреннего геморроя с анальной трещиной и свищем прямой кишки; острый геморрой; воспалительные заболевания анального канала; лечение антикоагулянтами.
Существует две основные методики лигирования геморроидальных узлов. Первая основана на втягивании кавернозной ткани во втулку механического лигатора при помощи специального мягкого зажима, после чего на ножку геморроидального узла сбрасывается с инструмента одна или две лигатуры. Кольцо должно пережимать только ножку узла, не захватывая тканей, расположенных ниже аноректальной линии.
Во время первого сеанса проводится лигирование одного-, двух геморроидальных узлов. Следующий этап лечения назначается не раньше, чем через 15 дней.
Осложнениями лигирования геморроидальных узлов являются: болевой синдром (отмечается при условии неправильного выполнения манипуляции), тромбоз наружных геморроидальных узлов (возникает у 2-3% пациентов), кровотечение (наблюдается у 1% больных). Эффективность методики составляет более 80%.
Склеротерапия
Впервые склеротерапию, как метод лечения геморроя, применил И.И. Карпинский (Россия) в 1870 г., используя для этих целей персульфат железа и фенол. Однако часто развивающиеся осложнения, после такой склерозирующей терапии, привели к ограничению использования этого метода. С появлением новых склерозирующих препаратов, аноскопов, специальных игл, вновь возрос интерес к этой методике.
В Российской Федерации разрешены к применению препараты группы детергентов. К ним относятся: полидоканол-этоксисклерол, тромбовар, фибровейн, морруат натрия, тетрадецилсульфат натрия. Детергенты являются наиболее эффективными и безопасными флебосклерозирующими химическими веществами. В основе механизма действия данной группы препаратов лежит способность вызывать коагуляцию белков эндотелия и десквамацию эпителия. Детергенты оказывают местное воздействие на сосудистую ткань и не приводят к системному тромбообразованию.
Показанием для проведения склеротерапии является внутренний геморрой I-II стадии; продолжающееся кровотечение из геморроидальных узлов.
К противопоказаниям данного метода относятся: наружный геморрой, парапроктит, тромбоз геморроидальных узлов, изъязвление слизистой, анальная трещина.
Суть методики склерозирования заключается во введении препарата в толщу геморроидального узла, с помощью специально изогнутой иглы с ограничителем. В зависимости от величины геморроидального узла, вводят от 0,5 до 2.0 мл детергента.
В первый день после процедуры возникает реакция тканей на химическую коагуляцию и может развиться болевой синдром. Выраженная болевая реакция может быть связана с введением препарата не в толщу геморроидального узла, а в мышечный слой кишки, а так же с введением концентрированного склерозирующего препарата, в большем объеме. При этом может возникнуть тромбоз и некроз слизистой геморроидального узла.
С целью предотвращения развития болевого синдрома и воспалительного процесса целесообразно за один сеанс проводить склерозирование не более двух геморроидальных узлов. Повторный этап лечения назначают не раньше, чем через 2 недели. При контрольном осмотре на 12-14 день после процедуры, в анальном канале определяется плоский, округлый безболезненный склерозированный участок кавернозной ткани с неизмененной слизистой.
Склеротерапия геморроидальных узлов наиболее эффективна при I стадии геморроя. При увеличении стадийности заболевания, уменьшается количество хороших результатов и возрастает число рецидивов. Склерозирующая терапия не позволяет достичь радикального излечения больных от проявлений геморроидальной болезни, а хорошие отдаленные результаты лечения наблюдаются лишь у 20 % больных.
Инфракрасная фотокоагуляция
С началом применения в медицине ультрафиолетового и инфракрасного излучений, А. Neiger в 1978 г. предложил методику инфракрасной фотокоагуляции геморроидальных узлов. Метод отличается своей простотой и коротким временем воздействия. Применяется при начальных стадиях внутреннего геморроя, а так же для остановки геморроидального кровотечения. Противопоказаниями являются наружный геморрой, тромбоз внутренних геморроидальных узлов, сочетание с парапроктитом и с анальной трещиной.
Принцип действия фотокоагулятора заключается в том, что инфракрасный световой поток фокусируется и по световоду направляется в кавернозную ткань. Наконечник световода пропускает инфракрасный свет, который, проникая в геморроидальный узел, преобразуется в тепловую энергию. Вследствие этого происходит коагуляция подслизистых структур с развитием некробиотических процессов в эндотелии сосудов, что приводит к уменьшению кровенаполнения кавернозной ткани. Глубина некроза зависит от длительности воздействия.
За один этап целесообразно проводить коагуляцию не более двух геморроидальных узлов. Повторная процедура проводится через 2 недели. Возможны повторные курсы фотокоагуляции.
Наблюдение за пациентами и анализ результатов лечения показал, что данный метод наиболее целесообразно применять при I стадии хронического геморроя, а так же для остановки геморроидального кровотечения.
Криохирургическое лечение
Одним из малоинвазивных методов лечения геморроя является холодовая деструкция. Криотерапия основана на быстром замораживании геморроидальных узлов жидким азотом. Недостатками данного метода являются: выраженный, неконтролируемый отек перианальных тканей, чувство дискомфорта в анальном канале, болевой синдром, мокнущая рана, а так же длительные сроки выздоровления. Эти проявления отмечаются более чем у 50% пациентов.Ограниченное применение этого метода обусловлено так же сложностью контроля границы распространения криовоздействия, опасностью глубокого некроза тканей, возможностью развития кровотечения. В связи с этим,криотерапия, как метод лечения геморроя, в последние годы практически не используется.
Шовное лигирование геморроидальных артерий под контролемультразвуковой допплерометрии
Сравнительно новой малоинвазивной методикой, пока не получившей широкого распространения на нашем рынке услуг, являетсяшовное лигирование геморроидальных артерий под контролем ультразвуковой допплерометрии. Этот способ привлекает простотой выполнения и целенаправленным воздействием на этиологический фактор развития геморроя.
Метод основан на идентификации геморроидальных артерий, при помощи ультразвуковой (УЗ) допплерометрии, с последующим прошиванием и лигированием их обычной нитью. Данный метод был разработан и предложен японским хирургом Morigana R. (1996 г.)
Для диагностической допплерометрии используется ультразвуковой хирургический аппарат с преобразователем звука и аноскоп с вмонтированным в него ультразвуковым датчиком. После установления этого датчика над геморроидальной артерией на аппарате раздается световой и звуковой сигнал. Через инцизуру в аноскопе, над внутренним геморроидальным узлом производится прошивание и лигирование дистальной ветви геморроидальной артерии восьмиобразным швом. Критерием правильной перевязки артерии, является исчезновение звукового и светового сигналов. Таким же образом лигируются геморроидальные артерии по всей окружности прямой кишки. Это приводит к прерыванию избыточного кровоснабжения внутренних геморроидальных узлов и фиксации их в анальном канале. Эта методика наиболее эффективна при I-III стадиях геморроя.
Противопоказаниями являются наружный геморрой, тромбоз геморроидальных узлов, воспалительные заболевания анального канала, сочетание с парапроктитом и анальной трещиной.
К незначительному числу осложнений можно отнести кратковременную задержку мочеиспускания, чувство дискомфорта в области анального канала в течение 2-3 дней после процедуры. Однако следует помнить, что при чрезмерном затягивании лигатуры возможно прорезывание геморроидальной артерии с развитием массивного артериального кровотечения. Для профилактики отсроченного артериального кровотечения, целесообразно за один сеанс проводить прошивание не более 2 геморроидальных артерий. Последующие сеансы проводятся через 2 недели после первой процедуры. Шовное лигирование геморроидальных артерий под контролем УЗ допплерометрии возможно является перспективным малоинвазивным методом лечения геморроя. Однако, для оценки эффективности этого метода, как и других методик, необходимо изучение отдаленных результатов лечения.
Электрокоагуляция геморроидальных узлов
Одной из современных малоинвазивных методик является электрокоагуляция геморроидальных узлов. Впервые этот способ лечения больных геморроем предложил A.Gain в 1939 году. В литературе сообщается о коагуляции геморроидальных узлов различными аппаратами типа AKM, Bicap, Ultroid, WD-II. Все эти приборы основаны на принципе диатермического воздействия электрического тока, путем проведения его через проводник к слизисто-подслизистым структурам. Путем теплового и химического воздействия на кавернозную ткань происходит некроз её, с последующим фиброзом и образованием рубцовой соединительной ткани.
Методика манипуляции достаточно простая. В зависимости от типа используемого аппарата, производится аппликационная электрокоагуляция слизистой оболочки около ножки геморроидального узла (аппарат Bicap), по типу метода фотокоагуляции. При использовании аппарата WD-II, входящим в комплект двухточечным электродом прокалывается слизистая оболочка ножки геморроидального узла на глубину 0,5 см и при активизации прибора постепенно происходит электрокоагуляция кавернозной ткани. Сила тока регулируется индивидуально. Недостатком метода при использовании этого аппарата, является долгое время экспозиции электрода в одном геморроидальном узле (10-15 мин). За этот период лечения устает как пациент, находящийся в соответствующей позиции, так и врач, проводящий процедуру. Поэтому за один сеанс, возможно, коагулировать лишь один геморроидальный узел.
В заключение этого раздела, следует сказать, что накопленный личный опыт использования различных малоинвазивных методик, наблюдение за пациентами и анализ отдаленных результатов лечения таких больных показал, что эти методики наиболее эффективны при начальных стадиях геморроя. При IV и III стадиях заболевания целесообразно использовать оперативный метод лечения. Малоинвазивные методики при поздних стадиях геморроя могут быть применены для остановки геморроидального кровотечения, что может быть первым этапом дальнейшего радикального лечения таких больных, а так же у пожилых, соматически отягощенных пациентов с паллиативной целью. По нашему мнению не более 10-15 % пациентов с диагнозом хронический геморрой могут быть радикально вылечены, используя малоинвазивные методы. Однако сочетание различных способов позволяет расширить показания к их применению. Безусловно, положительной стороной малоинвазивных методик является простота применения, небольшое число осложнений, малая травматичность, хорошая переносимость процедуры, возможность их использования в амбулаторных условиях, что экономически выгодно в современных условиях страховой медицины.
Хирургическое лечение
В настоящее время в России все-таки самым распространенным методом лечения геморроя является геморроидэктомия. Большинство колопроктологов и хирургов в нашей стране применяют методику, направленную на иссечение основных коллекторов кавернозной ткани, предложенную Milligan E., и Morgan G. в 1937 г. Эта операция применяется в двух модификациях. Часть врачей применяют закрытую геморроидэктомию, когда после иссечения геморроидального узла, прошивания и перевязки сосудистой ножки, слизистая оболочка ушивается наглухо. Другие колопроктологии используют открытую методику, не восстанавливая целостность слизистой оболочки прямой кишки, с оставлением цельной кожно-слизистой полоски тканей между иссеченными геморроидальными узлами. Каждая модификация имеет свои преимущества и недостатки. В связи с развитием новых технологий и разработкой современных аппаратов, их стали использовать при выполнении геморроидэктомии, с целью уменьшения числа послеоперационных осложнений и сокращения сроков реабилитации пациентов после выполнения операции. Наиболее часто применяют ультразвуковой гармонический скальпель, электротермическую систему LigaSure, радиоволновой скальпель. В последние годы распространение получил метод циркулярной резекции участка слизисто-подслизистого слоя дистального отдела прямой кишки с помощью циркулярного сшивающего аппарата (метод Лонго).
Ультразвуковой гармонический скальпель
Данный метод в нашей стране начал применяться в практике хирургического лечения геморроя сравнительно недавно, но сразу привлек внимание. Принцип действия гармонического скальпеля отличается от других электрохирургических аппаратов тем, что основан на высокой частоте колебания рабочего лезвия в продольном направлении. Это позволяет одновременно коагулировать и рассекать ткани за счет механического разрезания, кавитации и температурного воздействия. Установка позволяет надежно коагулировать сосуды до 5 мм в диаметре. Важно отметить, что при этом происходит строго направленное воздействие на ткани, а глубина термического повреждения прилежащих структур не превышает 1,5мм, что выгодно отличает этот прибор от электрокоагуляторов.
При выполнении геморроидэктомии с использованием ультразвукового скальпеля, первым этапом производится рассечение перианальной кожи с помощью электрокоагулятора и отделение наружного геморроидального узла от волокон подкожной порции наружного сфинктера. Затем, используя режим коагуляции и резания, единым блоком иссекаются наружный и внутренний геморроидальные узлы. Обработка сосудистой ножки производится только в режиме коагуляции. Аналогичным способом удаляются оставшиеся геморроидальные узлы. Раны не ушивают, а оставляют открытыми.
Надежная коагуляция и практически бескровная эксцизия геморроидальных узлов, позволяет сократить время оперативного вмешательства. Неглубокое термическое повреждение тканей приводит к уменьшению болевой реакции в послеоперационном периоде. Все это положительно сказывается на частоте дизурических расстройств и сокращает сроки послеоперационной реабилитации пациентов.
Аппаратно контролируемая биполярная электрокоагуляция
Разработанная для биполярной электрокоагуляции и пересечения сосудов, электротермическая система LigaSure, осуществляет контролируемую подачу энергии на бранши зажима. В результате этого в тканях происходит денатурация коллагена и эластина с образованием зоны коагуляционного некроза. Кроме этого зажимом механически сдавливают ткани, к которым дозировано подается электрический ток. Прочность зоны воздействия, состоящей из частично денатурированного протеина, сравнима с прочностью прошитой ткани. В связи с этим, нет необходимости в выделении и дополнительном лигировании сосудистой ножки геморроидального узла. Весь процесс занимает около 5 секунд. Аппарат позволяет коагулировать сосуды до 7мм в диаметре. Глубина термического воздействия на ткани, согласно характеристикам составляет 2мм.
Электротермическая система LigaSure позволяет проводить геморроидэктомию практически бескровно, не используя шовный материал. При этом значительно сокращается время операции. Однако у некоторых пациентов, в ближайшем послеоперационном периоде развивается достаточно интенсивная болевая реакция, что может быть связано с глубоким термическим воздействием на ткани анального канала. В связи с этим, этот аппарат, по нашему мнению, наиболее целесообразно применять при геморроидэктомии крупных геморроидальных узлов.
Радиоволновой скальпель
Некоторые исследователи предлагают использовать для геморроидэктомии радиоволновой скальпель, который хорошо зарекомендовал себя в косметической хирургии.
Прибор излучает радиоволну, которая вызывает в тканях образование тепла, под воздействием которого происходит распад клеточных структур и происходит разделения тканей. В связи с этим аппарат обладает хорошими диссекционными свойствами. Тепловое повреждение тканей минимальное, что создает оптимальные условия для заживления ран. Однако гемостатические свойства радиоволнового скальпеля низкие, особенно в присутствии биологических жидкостей, что не позволяет использовать только этот аппарат (без электрокоагулятора) для выполнения геморроидэктомии.
Операция Лонго
Эта операция отличается от других методов оперативного лечения больных геморроем тем, что геморроидальные узлы не удаляются. За счет циркулярного иссечения участка слизистой оболочки дистального отдела прямой кишки, при помощи циркулярного сшивающего аппарата, происходит проксимальное подтягивание геморроидальных узлов и фиксация их в анальном канале. При этом происходит пересечение терминальных ветвей геморроидальных артерий, что приводит к значительному снижению кровенаполнения кавернозных сплетений. Все это обуславливает купирование клинических проявлений геморроя, после этой операции. Метод предложил в 1998г. итальянский хирург A. Longo.
Преимуществом аппаратной геморроидопексии является малая травматичность и небольшая продолжительность операции, невыраженный послеоперационный болевой синдром, короткие сроки реабилитации пациентов. Однако следует упомянуть, что у некоторых больных, в послеоперационном периоде была отмечена интенсивная геморрагия, потребовавшая повторной операции.
Несмотря на широкую распространенность данной методики за рубежом, в России эта операция выполняется сравнительно редко. Сдерживающими факторами является высокая стоимость аппарата и отсутствие данных об отдаленных результатах лечения. Безусловно, необходимо иметь сведения о том, что происходит с оставшимися геморроидальными узлами в отдаленные сроки наблюдения. Остается не ясным, происходит ли реваскуляризация оставшейся кавернозной ткани через несколько лет, надежная ли фиксация геморроидальных узлов в анальном канале, не произойдет ли возврат клинических проявлений болезни в отдаленные сроки наблюдения.
Итак, современные возможности хирургического лечения больных хроническим геморроем значительны. Арсенал методов воздействия на это распространенное заболевание велик. Нельзя приспосабливать имеющийся в клинике какой-либо один способ лечения, ко всем стадиям геморроя. Нужно умело определять показания к лечению и, в зависимости от стадии заболевания, выбирать наиболее подходящий способ. Следует помнить, что малоинвазивные методы лечения, на которые охотно соглашаются пациенты, тем более применяемые в амбулаторных условиях, наиболее эффективны при начальных стадиях геморроя. При увеличении стадийности заболевания, а так же при сочетании геморроя с другими заболеваниями анального канала и параректальной клетчатки, показано хирургическое лечение.
Ультразвуковой скальпель
Механизм резки основан на собственном колебательном движении лезвия. При этом происходит повышение температуры в результате трения и поглощения акустических колебаний. Тепловое повреждение тканей незначительно. Кроме того, ультразвуковой скальпель не предполагает прохождения электрического тока через тело пациента,что особенно важно при наличии имплантированного водителя ритма.
Преимущества
Использование ультразвукового скальпеля имеет ряд преимуществ:
Недостатки
Показания к применению
Ультразвуковые скальпели используются практически во всех областях медицины, но особенно ценным является использование ультразвуковых хирургических методов в абдоминальной хирургии.
Ультразвуковой скальпель зарекомендовал себя в применение различных лапароскопических вмешательствах, таких как:
Стоит отметить уникальность ультразвукового прибора в хирургическом лечении онкологических больных: даже на поздних стадиях, когда требуется удаление метастазов (распространение злокачественного новообразования за пределы первоначального очага), данный метод позволяет очень точно иссечь участок ткани без повреждения близлежащих структур (сосуды, нервы).
Противопоказания
В нашем центре при помощи данной технологии ежедневно успешно выполняется большой перечень оперативных вмешательств.
Высокая квалификация наших специалистов и использование новейших технологий позволит максимально сократить ваше время пребывания в клинике в послеоперационном периоде, а также ускорит восстановление после операции.
Врачи Университетской клиники МГУ им. М.В. Ломоносова во время хирургической операции
СПОСОБ ПОЛУЛОСКУТНОГО ВЫДЕЛЕНИЯ ВНУТРЕННЕЙ ГРУДНОЙ АРТЕРИИ С ИСПОЛЬЗОВАНИЕМ УЛЬТРАЗВУКОВОГО ГАРМОНИЧЕСКОГО СКАЛЬПЕЛЯ Российский патент 2020 года по МПК A61B18/04 A61B17/00
Описание патента на изобретение RU2731003C1
Изобретение относится к медицине, а именно к сердечно-сосудистой хирургии, и может быть использовано для реваскуляризации пораженного коронарного русла у больных с ишемической болезнью сердца (ИБС).
В современных рекомендациях по реваскуляризации миокарда в мировой практике отдается предпочтение использованию артериальных графтов ввиду их лучшей проходимости с течением времени и достоверному улучшению отдаленных результатов после операции коронарного шунтирования (КШ), а внутренняя грудная артерия (ВГА) и сложные составные кондуиты с ее использованием имеют максимальную проходимость среди всех известных сосудов, используемых для реваскуляризации миокарда. В настоящее время имеется тенденция к значительному увеличению возраста оперируемых пациентов с ИБС, при этом все чаще встречаются пациенты с мультифокальным атеросклеротическим поражением, в том числе и аорты. Поэтому встает вопрос об использовании двух внутренних грудных артерий в качестве сложных составных графтов или in situ без пережатия аорты.
Золотым стандартом использования левой ВГА является ее анастомозирование с передней межжелудочковой ветвью (ПМЖВ) левой коронарной артерии. Использование правой ВГА in situ для шунтирования сосудов бассейна огибающей (OA) и правой коронарной артерии (ПКА) часто ограничено из-за недостаточной ее длины. При этом гипертрофия левого желудочка, поражение дистальных отделов коронарных артерий, особенности конституции пациента могут сделать невозможным выполнение полной реваскуляризации миокарда. Поэтому поиск способа безопасного увеличения длины ВГА является актуальной задачей современной кардиохирургии. В современной кардиохирургии известно несколько способов.
Наиболее близким аналогом выбран способ выделения ВГА полулоскутным способом (Horii Т., Suma Н. Semiskeletonization of Internal Thoracic Artery: Alternative Harvest Technique. Ann Thorac Surg 1997; 63:867- 8). При этом способе ВГА артерия выделяется без внутренней грудной фасции, без вскрытия плевральной полости от первого ребра и до бифуркации ВГА. Выполняется клипирование проксимального участка каждой боковой ветви ВГА, а дистальный участок коагулируется. Выделение кондуита не занимает много времени. Однако этот способ обладает рядом недостатков: длина кондуита уступает скелетированному варианту, так как проксимально выделяется до 1-го ребра. Использование клипс ведет к потенциальной опасности повреждения ВГА. Имеются лишь два сообщения об использовании этого способа в практической медицине (Satdhabudha О., Noppawinyoowong N., A randomized comparison of flow characteristics of semiskeletonized and pedicled internal thoracic artery preparations in coronary artery bypassJournal of Cardiothoracic Surgery. 2017 12:28).
В основу нашего изобретения положено решение задачи, заключающейся в разработке оптимального, отвечающего современным тенденциям кардиохирургии способа выделения внутренней грудной артерии.
Решение данной задачи состоит в том, что использован полулоскутный забор ВГА в сочетании с мобилизацией проксимального ее участка до устья подключичной артерии с лигированием медиальной внутренней грудной вены, где лигирование боковых ветвей проводилось с использованием ультразвукового гармонического скальпеля.
Заявляемый способ позволяет получить ВГА для шунтирования коронарных артерий максимально возможной длины с минимальным риском травматизации ее стенки.
В практике медицины известно использование полулоскутного забора ВГА, однако в предлагаемом способе впервые применен ультразвуковой гармонический скальпель для такой техники выделения шунта и впервые выполнена высокая мобилизация проксимального участка ВГА с лигированием медиальной внутренней грудной вены для максимального удлинения кондуита.
Применение в сердечно-сосудистой хирургии способа полулоскутного забора внутренней грудной артерии с использованием ультразвукового гармонического скальпеля позволяет сохранить целостность плевральной полости, что нивелирует риски развития послеоперационного гидроторакса и снижает болевые ощущения пациентов в раннем послеоперационном периоде, а также позволяет увеличить процент успешного выполнения тотальной артериальной реваскуляризации миокарда, что оказывает положительное воздействие на отдаленные результаты операции.
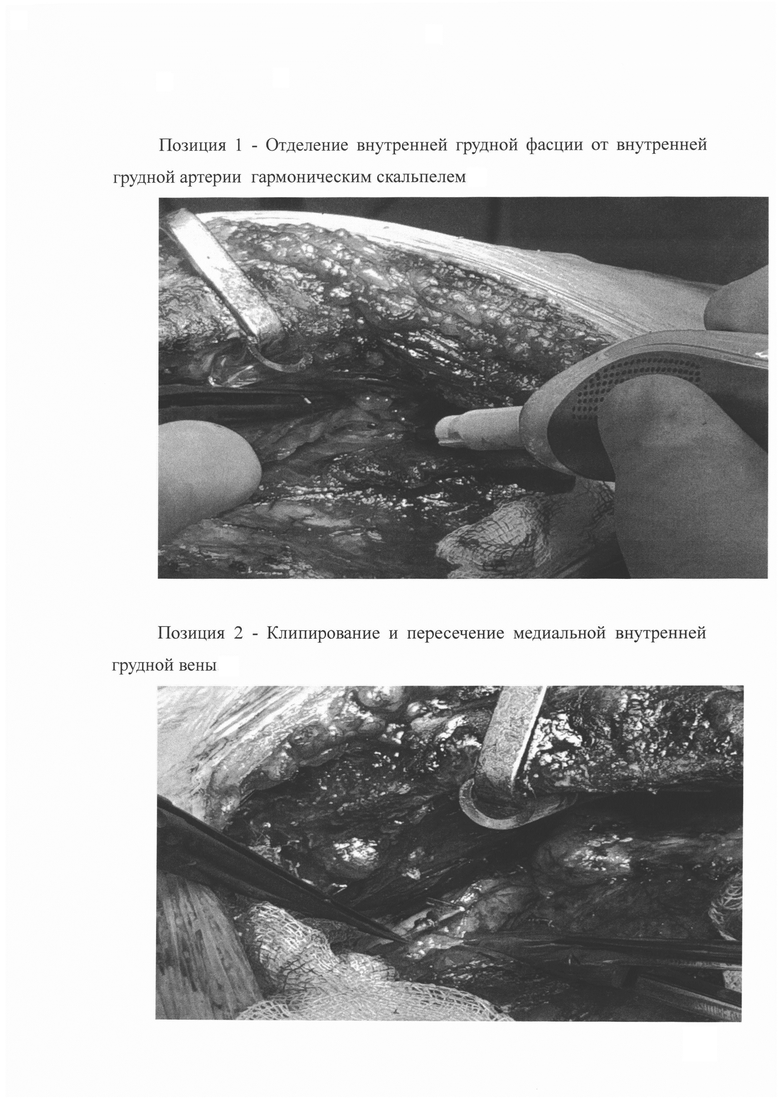
Способ полулоскутного забора ВГА с использованием ультразвукового гармонического скальпеля осуществляется следующим образом. Доступ к области выделения ВГА становится возможным после выполнения срединной стернотомии и отведении в латеральную сторону при помощи специального ретрактора фрагмента грудины (Позиция 1). После этого при выделении ВГА внутренняя грудная фасция вскрывается электрокоагулятором Soring единым разрезом медиальнее проекции ВГА и сопровождающих ее внутренних грудных вен от первого межреберья и до уровня прикрепления к телу грудины мечевидного отростка. При помощи электрокоагуляции отсепаровывается лоскут вместе с внутренней грудной фасцией, ВГА, сопровождающими ее внутренними грудными венами. Затем при помощи ультразвукового гармонического скальпеля выполняется лигирование боковых ветвей ВГА, идущих вверх от уровня 1-го межреберья и до бифуркации ВГА, при этом ветви, идущие в латеральном направлении, на этом этапе не пересекаются. Затем «холодным способом» при помощи наконечника электрокоагулятора Soring выполняется отсепаровывание ВГА от внутренней грудной фасции на всем протяжении, при этом плевральная полость не вскрывается. На следующем этапе выполняется коагуляция латеральных ветвей ВГА с подходом к ним как над ВГА, так и под ВГА, что значительно облегчает данную манипуляцию по сравнению с прототипом. В проксимальном отделе ВГА выделяется до места впадения ВГА в подключичную артерию. Мобилизуется латеральная поверхность артерии с сопровождающей ее латеральной внутренней грудной веной, а затем мобилизуется медиальная ее поверхность, при этом осуществляется лигирование сопровождающей медиальной внутренней грудной вены, что дополнительно создает мобильность и увеличивает длину ВГА (Позиция 2). Особое внимание уделяется лигированию боковых ветвей, питающих щитовидную железу, имеющих размеры до 0,3-0,5 мм. в диаметре. При выделении проксимального участка целесообразно на 1-1,5 минуты отключать аппарат ИВЛ для достижения наиболее оптимальной визуализации. Затем дистальный отдел ВГА клипируется и отсекается до бифуркации ВГА для сохранения коллатерального кровоснабжения между диафрагмальной и верхней надчревной артериями (Позиция 3).
С февраля по май 2019 года в Федеральном государственном бюджетном учреждении «Федеральный центр сердечно-сосудистой хирургии» Министерства здравоохранения Российской Федерации (г. Челябинск), являющийся базой кафедры госпитальной хирургии ФГБОУВО «Южно-Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации, заявленный способ был нами использован у 4-х пациентов.
Пациент Ш., 58 лет. Диагноз: ИБС. Стенокардия напряжения III функционального класса (ФК). Гипертоническая болезнь III стадия, риск 4. Хроническая сердечная недостаточность (ХСН) 1, ФК 2. Сопутствующие заболевания: хроническая болезнь почек (ХБП) С3а стадия. Ожирение 1 степени. Хронический обструктивный бронхит, ремиссия. Дыхательная недостаточность (ДН) 0.
По данным ЭКГ: Синусовый ритм с частотой сердечных сокращений (ЧСС) 85 уд/мин. Электрическая ось сердца не отклонена. Поворот сердца правым желудочком вперед относительно продольной оси. Повышена нагрузка на левое предсердие. Гипертрофия левого желудочка. Изменения миокарда в нижней стенке.
По данным коронарографии: Правый тип кровоснабжения миокарда. Стеноз устья ПМЖВ до 75%. Окклюзия огибающей артерии (OA) в проксимальной трети. Протяженный стеноз правой коронарной артерии (ПКА) в средней трети 70%, стеноз дистальной трети 90%.
С учетом критических стенозов OA и ПКА, относительно молодого возраста пациента решено было выполнить аутоартериальное шунтирование. Выполнена операция: коронарная реваскуляризация миокарда Т-графт (левая внутренняя грудная артерия (ЛВГА) и правая ВГА (ПВГА)) с ПМЖВ и OA. Аортокоронарное шунтирования (АКШ) левая лучевая артерия (ЛЛА) с задней межжелудочковой ветвью правой коронарной артерии (ЗМЖВ ПКА).
Операцию проводили в условиях нормотермического искусственного кровообращения и кровяной кардиоплегии. Использовалась методика забора ПВГА и ЛВГА по заявленному способу. После вскрытия перикарда и ревизии обнаружено значимое увеличение левых камер сердца. После пережатия аорты и асистолии выполнено формирование дистальных анастомозов с ПВГА с OA, ЛЛА с ЗМЖВ ПКА и ЛВГА с ПМЖВ, после повтора кардиоплегии выполнено формирование Т-графта между ЛВГА и ПВГА. При этом отмечено, что длина ПВГА достаточна для формирования анастомоза без малейших признаков натяжения. После снятия зажима с аорты сердечная деятельность возобновилась самостоятельно. Шунтирование закончено формированием проксимального анастомоза с ЛЛА. По данным интраоперационной флоуметрии, получены удовлетворительные показатели скорости потока и сопротивления ЛЛА 60 мл\мин. Пульсовой индекс (Pi) 1,8, ЛВГА до анастомоза 59 мл\мин. Pi 1,9, ЛВГА 27 мл\мин, Pi 2,1 ПВГА 29 мл\мин. 1,8 Операция закончена без особенностей. Послеоперационный период протекал без осложнений. На 10-е сутки пациент переведен на санаторно-курортный этап лечения. Через 3 месяца после операции пациент чувствует себя удовлетворительно. Ишемии миокарда на суточном мониторировании ЭКГ не регистрируются.
В трех других подобных случаях отмечалась достаточная длина шунта ЛВГА и ПВГА для шунтирования бассейнов ЛКА и ПКА. Во всех случаях отмечались удовлетворительные характеристики интраоперационных флоуметрических потоков. Наблюдался неосложненный послеоперационный период. Пациенты выписаны на 9-10 сутки. В отдаленном периоде через 1, 1,5 и 2 месяца после вмешательства у больных отсутствовала клиника стенокардии по данным суточного мониторирования.
Таким образом, применение заявленного способа дает возможность сохранить целостность плевральной полости, что снижает болевые ощущения пациентов в раннем послеоперационном периоде, а также позволяет успешно выполнять полную артериальную реваскуляризацию миокарда для улучшения отдаленных результатов операции.
Похожие патенты RU2731003C1
Иллюстрации к изобретению RU 2 731 003 C1
Реферат патента 2020 года СПОСОБ ПОЛУЛОСКУТНОГО ВЫДЕЛЕНИЯ ВНУТРЕННЕЙ ГРУДНОЙ АРТЕРИИ С ИСПОЛЬЗОВАНИЕМ УЛЬТРАЗВУКОВОГО ГАРМОНИЧЕСКОГО СКАЛЬПЕЛЯ
Изобретение относится к медицине, а именно к сердечнососудистой хирургии. Вскрывают внутригрудную фасцию разрезом медиальнее проекции ВГА и сопровождающих ее внутренних грудных вен от первого межреберья и до уровня прикрепления к телу грудины мечевидного отростка. Отсепаровывают лоскут внутренней грудной фасции с ВГА и сопровождающими ее внутренними грудными венами. При помощи ультразвукового гармонического скальпеля выполняется лигирование боковых ветвей ВГА, идущих вверх от уровня 1-го межреберья и до бифуркации ВГА. Выполняют отсепаровывание ВГА от внутренней грудной фасции на всем протяжении, при этом плевральную полость не вскрывают. На следующем этапе выполняют коагуляцию латеральных ветвей ВГА с подходом к ним как над ВГА, так и под ВГА. В проксимальном отделе ВГА выделяют до места впадения ВГА в подключичную артерию. Затем мобилизуют латеральную поверхность ВГА с сопровождающей ее латеральной внутренней грудной веной. После чего мобилизуют медиальную поверхность ВГА, при этом осуществляют лигирование сопровождающей медиальной внутренней грудной вены. Дистальный отдел ВГА клипируют и отсекают до бифуркации ВГА. Способ позволяет сохранить целостность плевральной полости, что нивелирует риски развития послеоперационного гидроторакса и снижает болевые ощущения пациентов в раннем послеоперационном периоде, а также увеличить процент успешного выполнения тотальной артериальной реваскуляризации миокарда, что оказывает положительное воздействие на отдаленные результаты операции. 1 пр., 3 ил.
Формула изобретения RU 2 731 003 C1
Способ полулоскутного забора ВГА с использованием ультразвукового гармонического скальпеля, включающий вскрытие внутригрудной фасции, отличающийся тем, что разрезом внутригрудной фасции медиальнее проекции ВГА и сопровождающих ее внутренних грудных вен от первого межреберья и до уровня прикрепления к телу грудины мечевидного отростка, отсепаровывают лоскут внутренней грудной фасции с ВГА и сопровождающими ее внутренними грудными венами, затем при помощи ультразвукового гармонического скальпеля выполняется лигирование боковых ветвей ВГА, идущих вверх от уровня 1-го межреберья и до бифуркации ВГА, затем выполняется отсепаровывание ВГА от внутренней грудной фасции на всем протяжении, при этом плевральная полость не вскрывается, на следующем этапе выполняют коагуляцию латеральных ветвей ВГА с подходом к ним как над ВГА, так и под ВГА, в проксимальном отделе ВГА выделяется до места впадения ВГА в подключичную артерию, затем мобилизуют латеральную поверхность артерии с сопровождающей ее латеральной внутренней грудной веной, а затем мобилизуют медиальную ее поверхность, при этом осуществляют лигирование сопровождающей медиальной внутренней грудной вены, затем дистальный отдел ВГА клипируют и отсекают до бифуркации ВГА.