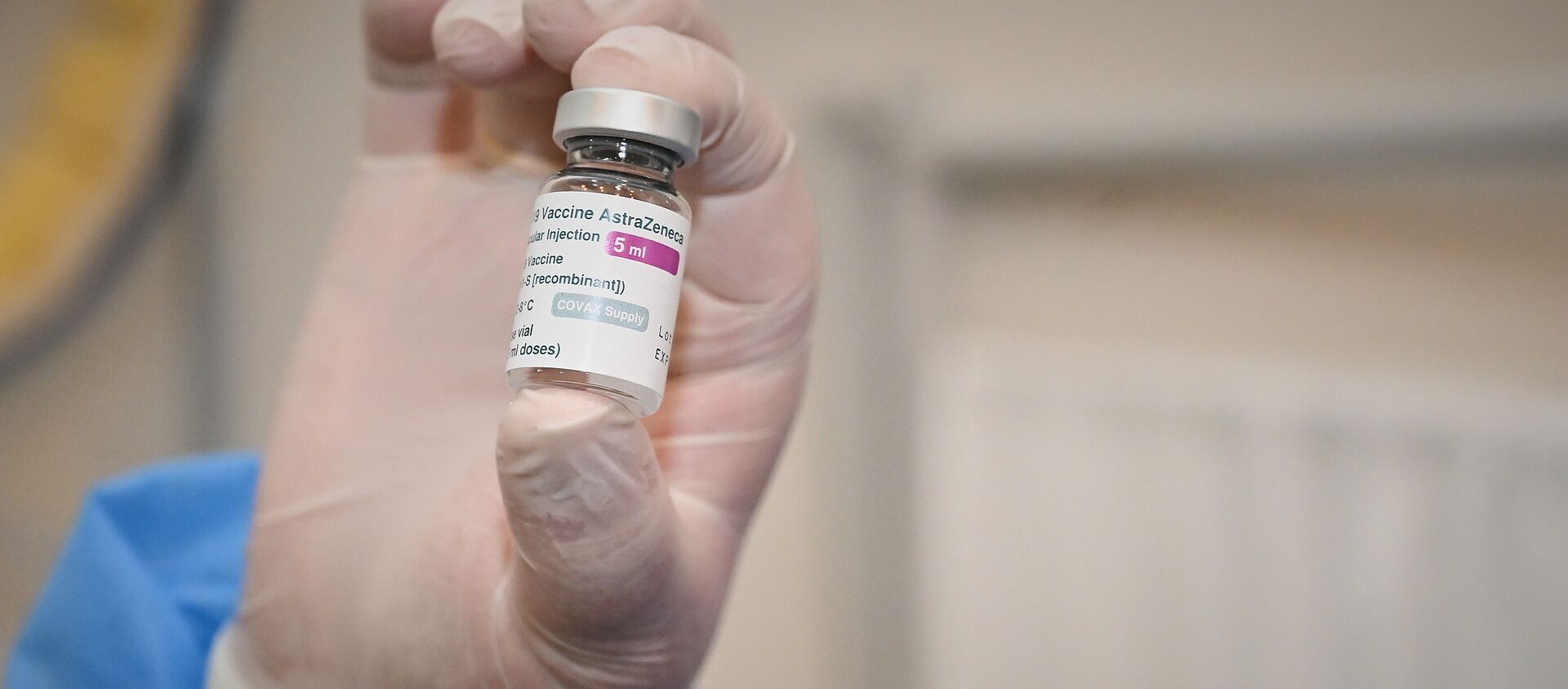
гам ковид вак и спутник v отличия в чем отличие
«Спутник-V», «ЭпиВакКорона» и «КовиВак»: чем отличаются вакцины против коронавируса
О важности вакцинации от гриппа и COVID-19 рассказывает заведующий отделом мониторинга эпидемиологии и иммунопрофилактики, врач-эпидемиолог ГБУЗС «Медицинский информационно-аналитический центр» Сергей Грыга.
Единственная специфическая профилактика данных заболеваний – вакцинация.
Вакцинацию нужно проводить каждый год по причине того, что меняются штаммы гриппа.
Всемирная организация здравоохранения и специалисты здравоохранения РФ прогнозируют штаммы, которые предположительно будут циркулировать у нас в следующем эпидемиологическом сезоне, в марте-апреле.
Под эти штаммы разрабатывается вакцина, которая выпускается в оборот обычно в августе. Срок ее годности не больше года, то есть на будущий год ее использовать нельзя.
Если говорить о неспецифической профилактике ОРВИ и гриппа в частности – применяется абсолютно индивидуальный подход, который определяет врач.
Каждый человек имеет право обратиться перед сезоном к медицинскому специалисту, чтобы поднять свой иммунитет или просто для поддержания противовирусной защиты любыми другими средствами.
Неспецифическую профилактику на сегодняшний день мы очень хорошо отработали на COVID-19.
В эпидемический сезон всегда рекомендовалось носить маски и обрабатывать руки любыми средствами дезинфекции. Такие меры актуальны для профилактики любой ОРВИ.
Борьба с коронавирусом
Коронавирусная инфекция известна в мире давно, она всегда циркулировала среди нас в осеннее-зимний период.
Обычный коронавирус не представлял ни для кого угрозы – он легко переносился, поэтом против него никогда вакцину не создавали. К сожалению, в прошлом году активно циркулировал мутированный вирус, который принял достаточно агрессивную форму.
COVID-19 распространился по всему миру. Ни в одной стране мира система здравоохранения не была готова к такому – не было ни лекарств, ни методов диагностики.
Естественно, инфекция приняла вид пандемии. На сегодняшний день вирус уже хорошо изучен, выявлены его мутации, но пока что они не существенны.
Уже подобраны схемы лечения, разработаны новые лекарственные препараты, тест-системы, которые позволяют достаточно быстро и эффективно определить коронавирус. Были введены строгие ограничительные мероприятия. Поэтому сегодня мы видим снижение заболеваемости.
Серьезную роль в борьбе с COVID-19 играет вакцинация.
В настоящее время в РФ созданы уже три вакцины – «Спутник V», «ЭпиВакКорона» и вакцина от Центра имени Чумакова «КовиВак».
В Севастополь поступает вакцина «Спутник V». Для этой вакцины были взяты аденовирусные векторы – вирусы, которые прекрасно живут вместе с нами и не вызывают никаких патологических явлений.
К этому вектору путем синтеза прикрепили кусочки белка, которые отвечают у коронавируса за прикрепление и внедрение в клетку. Я настоятельно рекомендую не бояться вакцинации живым вирусом. От коронавируса там только маленький кусочек, который прикреплен на абсолютно безопасный аденовирус.
Когда он попадает к нам в организм, то вызывает определенную реакцию в организме, благодаря которой вырабатывается иммунитет.
Почему вакцина двухкомпонентная?
Двухкомпонентная вакцина нужна для усиления иммунного ответа.
При первой прививке мы поднимаем его на уровень порядка 60%, после второго компонента – на 90-92%. По оценке ученых, благодаря этому срок действия вакцины может достигать двух и более лет.
В чем отличие других вакцин от «Спутник V»?
В «ЭпиВакКороне» взят обычный транспортировочный белок, который характерен для человека и применяется в большинстве вакцин.
К нему прикреплены три участка белка от коронавируса, которые отвечают за внедрение и усиленный адъювантами (комплекс веществ, используемое для усиления иммунного ответа). Эта вакцина мягче, но эффективность у нее такая же. Пока эту вакцину производят в небольших объемах. В Севастополе она не представлена.
Вакцина от Центра имени Чумакова самая сложная. Во время прививки к нам в организм будет поступать живой коронавирус, но обездвиженный, который не способен внедряться в клетку, не способен вырабатывать токсины, проще говоря, заболевание.
На сегодняшний день эту вакцину только зарегистрировали, и как она себя поведет очень сложно сказать. Считаю, что все три вакцины будут хороши, поскольку наша система иммунопрофилактики одна из лучших в мире.
Вакцинации всеми вакцинами будут проходить двукратно. «Спутник V» и «ЭпиВакКороне» – с разрывом в 21 день. Вакцина от Центра имени Чумакова – 14 дней.
На сегодняшний день в Севастополе можно привиться в любой взрослой поликлинике, записавшись через портал Госуслуги. Лица старше 65 лет могут записаться через регистратуру.
На сегодняшний день в Севастополе уже привито более 10 тысяч человек.
Как записаться на вакцинацию от коронавируса COVID-19 в Севастополе можно узнать в статье.
Лекция о важности вакцинации для профилактики опасных заболеваний была прочитана для родителей детей-инвалидов и сотрудников ГКУ СЗ «Севастопольский реабилитационный центр для детей и подростков с ограниченными возможностями». Мероприятие было организовано Центром общественного здоровья и медицинской профилактики ГБУЗС «МИАЦ».
ЭпиВакКорона, «Спутник V» или «КовиВак»: в чем разница вакцин
Изготовлены все три российские вакцины на разных технологических платформах, что, по мнению специалистов, позволит врачам подобрать наиболее подходящую для прививки своих пациентов.
Sputnik Грузия попытался разобраться, в чем разница между зарегистрированными российскими вакцинами от COVID-19.
В чем разница вакцин?
Принципы создания российских вакцин от коронавируса «ЭпиВакКорона», «Спутник V» и «КовиВак» разные.
«Спутник V» и «ЭпиВакКорона» созданы с помощью современных методов генной инженерии и не имеют опыта длительного применения.
«КовиВак», в отличие от двух первых, относится к классическому типу вакцин, которые уже с прошлого века масштабно производились и использовались.
«Спутник V»
Эффективность «Спутник V» или «Гам-Ковид-Вак», который вводят дважды с интервалом в три недели, составляет 91,4%, а при тяжелом течении заболевания — 100%. Иммунитет формируется, как уже доказано, на девять месяцев, но ожидается, что и на два года.
Вакцина противопоказана беременным и кормящим. Применять «Спутник V» нельзя при гиперчувствительности к какому-либо компоненту вакцины; тяжелых аллергических реакциях; острых инфекционных и обострении хронических заболеваниях. Прививку можно сделать через две-четыре недели после выздоровления или ремиссии, а при нетяжелых ОРВИ — после нормализации температуры.
Введение второго компонента вакцины «Спутник V» запрещается при тяжелых осложнениях после первой дозы (анафилактический шок, судорожный синдром, температура выше 40 градусов).
Вакцина «Спутник V» зарегистрирована в России и более чем в 30 странах мира. Заявки поданы на регистрацию в ЕС и на одобрение ВОЗ.
«ЭпиВакКорона»
Применять вакцину «ЭпиВакКорона» специалисты рекомендуют в возрасте 18—60 лет. Испытания вакцины проводились и на добровольцах 60+. Запланированы исследования на детях до 18 лет. Противопоказана вакцина «ЭпиВакКорона» беременным и кормящим.
Гам ковид вак и спутник v отличия в чем отличие
Гам-Ковид-Вак (торговая марка «Спутник V»)
Зарегистрирована в России и более чем в 30 странах мира, подана заявка на регистрацию в ЕС, подана заявка на одобрение ВОЗ.
Тип вакцины и способ введения
Генноинженерная векторная с использованием двух штаммов живых аденовирусов человека, лишенных способности размножаться.
Вводится двукратно с интервалом 3 недели.
Кем разработана, кто производит
Разработчик: НИЦ эпидемиологии и микробиологии имени Гамалеи Минздрава России.
Производят: НИЦ имени Гамалеи; BIOCAD (Санкт-Петербург); «Генериум» (Владимирская область); «Биннофарм Групп» (Зеленоград)
Эффективность и побочные проявления
Кому рекомендована, противопоказания, особенности
Применяют у взрослых 18-60 лет, также разрешено применение в возрасте 60+.
Противопоказана беременным и кормящим, планируются исследования на детях до 18 лет.
Кроме того, нельзя применять при гиперчувствительности к какому-либо компоненту вакцины; тяжелых аллергических реакциях в анамнезе; острых инфекционных и неинфекционных заболеваниях, обострении хронических заболеваний.
Прививку можно выполнить через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ- после нормализации температуры.
При тяжелых осложнениях после введения первой дозы (анафилактический шок, генерализованные аллергические реакции, судорожный синдром, температура выше 40°С и т.д.) введение второго компонента также запрещается.
С осторожностью можно применять при хронических заболеваниях печени и почек, сахарном диабете, тяжелых заболеваниях системы кроветворения, эпилепсии, инсультах и других заболеваниях ЦНС, инфарктах миокарда в анамнезе, ИШМ и других заболеваниях сердца, первичных и вторичных иммунодефицитах, аутоиммунных заболеваниях, заболеваниях легких, астме и ХОБЛ и др.
«ЭпиВакКорона»
Зарегистрирована в России и Туркменистане.
Тип вакцины и способ введения
Вводится двукратно внутримышечно с интервалом в 2-3 недели.
Кем разработана, кто производит
Разработана и производится ГНЦ вирусологии и биотехнологии «Вектор» Роспотребнадзора.
Эффективность и побочные проявления
Иммунологическая эффективность 100%.
Иммунная защита будет действовать один год.
Сильных нежелательных явлений, связанных с действием вакцины не выявлено, отмечается боль в месте укола и повышение температуры до 38,5 градусов.
Кому рекомендована, противопоказания, особенности
Применяют у взрослых 18-60 лет, также проводились испытания вакцины на добровольцах 60+.
Противопоказана беременным и кормящим, планируются исследования на детях до 18 лет.
Также запрещено делать прививку при гиперчувствительности к компонентам препарата (гидроокиси алюминия и др.); при тяжелых формах аллергических заболеваний; первичном иммунодефиците, злокачественных заболеваниях крови и новообразованиях, поствакцинальных осложнениях при предыдущем введении вакцины; острых инфекционных и неинфекционных заболеваниях, хронических заболеваниях в стадии обострения.
Прививку можно делать не ранее чем через месяц после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ вакцинацию проводят после нормализации температуры.
«КовиВак»
Зарегистрирована Минздравом России 20 февраля 2021 года, планируется проведение процедуры перерегистрации ВОЗ, а также регистрация в зарубежных странах.
Тип вакцины и способ введения
Вводится двукратно внутримышечно с интервалом две недели.
Кем разработана, кто производит
Разработана и производится ФНЦ исследований и разработки иммунобиологических препаратов имени Чумакова РАН.
Эффективность и побочные проявления
Иммунологическая эффективность составляет 85% (образование антител в определенные протоколом сроки, однако разработчики не исключают, что иммунный ответ может сформироваться несколько позже).
Сроки действия иммунитета будут объявлены после окончания клинических исследований.
Кому рекомендована, противопоказания, особенности
Применяют у взрослых 18-60 лет.
Вакцины такого типа применяют у людей с иммуносупрессивными и иммунодефицитными состояниями.
Противопоказана беременным, кормящим и детям, так как исследования на этих группах не проводились. Также не применяют у людей, у которых наблюдались тяжелые поствакцинальные осложнения на любые предыдущие вакцинации, а также людям с тяжелыми аллергиями.
Временно противопоказана: при острых лихорадочных состояниях, острых инфекционных и обострении хронических заболеваний. Прививку делают через 2-4 недели после выздоровления.
Допускается возможность вакцинации при хронических заболеваниях почек, печени, нейроэндокринной системы, тяжелых заболеваниях кроветворения, аутоиммунных, аллергических заболеваниях, бронхиальной астме и др. Состояние пациента и возможность прививки с учетом фактора польза-риск оценивает лечащий врач.
Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
| ▼ Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном порядке. |
Регистрационный номер:
Торговое наименование:
Гам-КОВИД-Вак-М Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Международное непатентованное или группировочное наименование:
Вакцина для профилактики COVID-19
Лекарственная форма:
раствор для внутримышечного введения
Состав на 1 дозу
Компонент I содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (2,0±1,5)×10 10 частиц.
Вспомогательные вещества: трис(гидроксиметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, полисорбат 80 – 250 мкг, магния хлорида гексагидрат – 102,0 мкг, ЭДТА динатриевая соль дигидрат – 19,0 мкг, этанол (спирт этиловый) 95% – 2,5 мкл, вода для инъекций – до 0,5 мл.
Компонент II содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 5 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (2,0±1,5)×10 10 частиц.
Вспомогательные вещества: трис(гидроксиметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, полисорбат 80 – 250 мкг, магния хлорида гексагидрат – 102,0 мкг, ЭДТА динатриевая соль дигидрат – 19,0 мкг, этанол (спирт этиловый) 95% – 2,5 мкл, вода для инъекций – до 0,5 мл.
Описание
Компонент I. Раствор замороженный – плотная затвердевшая беловатого цвета масса. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Компонент II. Раствор замороженный – плотная затвердевшая беловатого цвета масса. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент I и компонент II.
В состав компонента I входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2, в состав компонента II входит вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа:
Код АТХ:
Фармакологические свойства
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологические свойства и безопасность вакцины изучали в клиническом исследовании у добровольцев обоего пола в возрасте от 12 до 17 лет включительно.
Промежуточный анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев. При исследовании гуморального иммунного ответа сыворотки добровольцев были проанализированы на наличие антител, специфичных к рецептор-связывающему домену гликопротеина S вируса SARS-CoV-2 на 42 день от начала вакцинации: уровень сероконверсии составил 100%.
Иммунизация препаратом Гам-КОВИД-Вак-М формирует антиген-специфический клеточный противоинфекционный иммунитет у 93,2% обследованных добровольцев (формирование антиген-специфичных клеток обоих популяций Т-лимфоцитов: Т-хелперных (CD4+) и Т-цитотоксических (CD8+) и достоверное повышение секреции ИФНγ).
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания к применению
Профилактика COVID-19 у подростков в возрасте от 12 до 17 лет (включительно).
Противопоказания
Противопоказания для введения компонента II:
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Отсутствует опыт клинического применения Гам-КОВИД-Вак-М при беременности. Согласно результатам изучения репродуктивной токсичности на животных не установлено отрицательного влияния на течение беременности, эмбриофетальное развитие (на самках) и пренатальное развитие потомства. В связи с этим применять препарат Гам-КОВИД-Вак-М при беременности следует только в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22-х недель беременности.
Клинические данные по применению препарата Гам-КОВИД-Вак-М у женщин, кормящих грудью, и младенцев отсутствуют. В настоящий момент нет данных выделяется ли вакцина с молоком. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу – препарат вводят в латеральную широкую мышцу бедра.
Вакцинацию проводят в два этапа: вначале компонентом I в дозе 0,5 мл, затем, через 3 недели – компонентом II в дозе 0,5 мл.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Перед иммунизацией флакон с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Не допускается хранение размороженного препарата!
Повторное замораживание не допускается!
| ▼ Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата, путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ. |
Побочное действие
Нежелательные явления (НЯ), характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Чаще других могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией; общим недомоганием; утомляемость, головная боль) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Реже отмечаются: тошнота, диспепсия, иногда – заложенность носа увеличение регионарных лимфоузлов, паническая атака. У некоторых пациентов возможно развитие аллергических реакций, кратковременное изменение лабораторных показателей крови повышение уровня билирубина, снижение уровня нейтрофилов) в сыворотке крови.
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата Гам-КОВИД-Вак-М после вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: гипертермия, боль, отек, зуд в месте вакцинации, астения. Частота развития – очень часто и часто.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: заложенность носа. Частота развития – редко.
«Нарушения со стороны нервной системы»: головная боль; головокружения – редко. «Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия – редко.
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей. Все НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/НПВС и десенсибилизирующие средства, кортикостероиды – парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось. Ввиду отсутствия данных исследований совместимости, вакцину Гам-КОВИД-Вак-М (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2) нельзя смешивать с другими вакцинами или иными лекарственными средствами в одном шприце.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности.
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, компонент I – 0,5 мл/доза + компонент II – 0,5 мл/доза.
По 0,5 мл (1 доза) каждого компонента препарата во флаконы нейтрального стекла, герметично укупоренные пробками из резины, обжатые алюмопластиковыми колпачками.
1 флакон компонента I с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного; 1 флакон компонента II с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного.
Условия хранения
Хранить в защищенном от света месте, при температуре не выше минус 18 °С. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Условия транспортирования
При температуре не выше минус 18 °С.
Срок годности
Компонент I – 6 месяцев. Компонент II – 6 месяцев.
Не применять по истечении срока годности.
Условия отпуска:
для лечебно-профилактических учреждений.
Производитель
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18 (все стадии производства).
Выпускающий контроль качества
Филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России, Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения / организация, принимающая претензии потребителя:
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи» Министерства здравоохранения Российской Федерации (ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России).
Россия, 123098, г. Москва, улица Гамалеи, д. 18.