что нужно принимать при пролапсе митрального клапана
Что такое пролапс митрального клапана? Причины возникновения, диагностику и методы лечения разберем в статье доктора Карченова Е. В., кардиолога со стажем в 37 лет.
Определение болезни. Причины заболевания
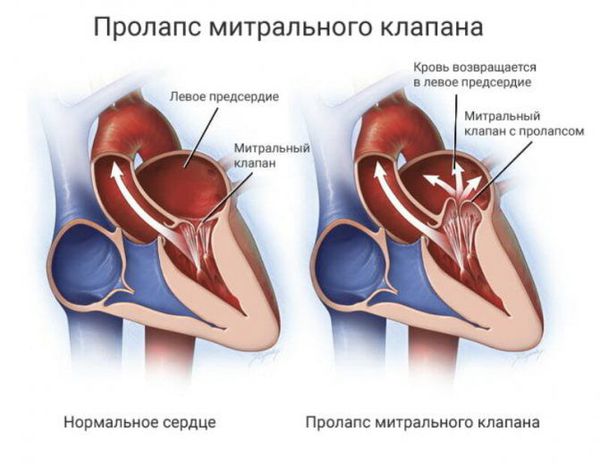
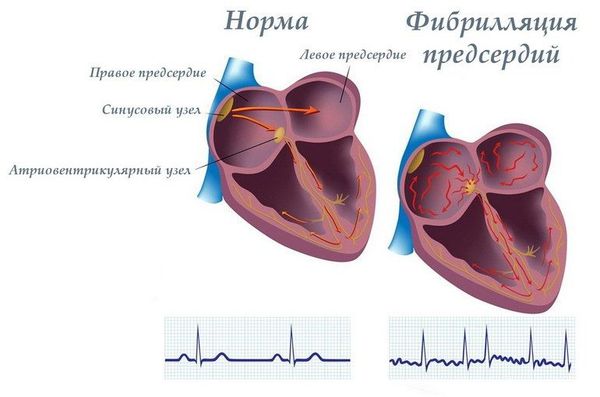
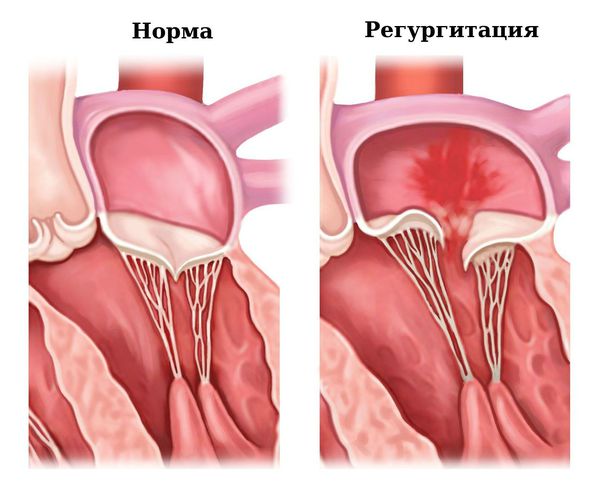
Из предсердий кровь должна поступать в желудочки сердца. Однако при определённой величине прогиба створки возможна митральная регургитация — обратный ток крови из желудочка в предсердие. Это может вызвать увеличение полости предсердия, повышенное гидростатическое давление и нагрузку на него.
Распространённость пролапса митрального клапана
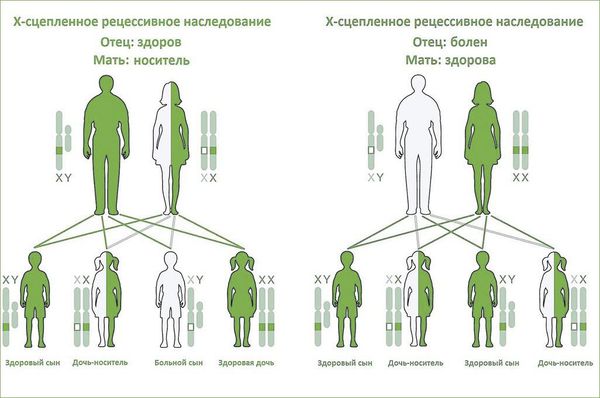
Выделяют первичный (врождённый) пролапс митрального клапана и вторичный (приобретённый). Первичный ПМК бывает семейным (наследственным) или несемейным (случайным).
Причины пролапса митрального клапана
Отмечается увеличение частоты случаев пролапса митрального клапана, ассоциированных со вторичным дефектом межпредсердной перегородки и/или левосторонними атриовентрикулярными дополнительными проводящими путями, а также с наджелудочковыми аритмиями.
Вторичным считают прогиб створки митрального клапана, который возникает в результате воспаления или повреждения окружающих тканей и самого клапана. ПМК вторичной природы может быть следствием различных состояний:
Симптомы пролапса митрального клапана
Болевой синдром в груди чаще сосредоточен в области сердца, бывает длительным, в отличие от стенокардии, он не связан с физической нагрузкой. Пациенты обычно описывают острые, «колющие» боли, однако обычно они не являются предвестниками тяжёлого состояния.
Симптомы врождённого и приобретённого ПМК
При врождённом пролапсе митрального жалоб у пациентов может не быть вовсе или они незначительны и не сильно беспокоят.
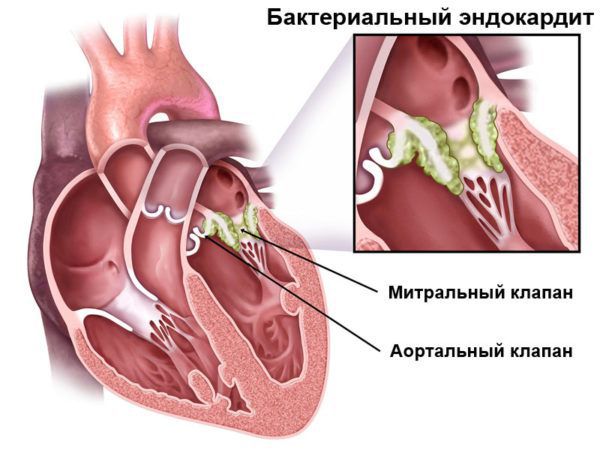
Приобретённый пролапс митрального клапана возникает после тяжёлых заболеваний: ишемической болезни сердца, инфаркта миокарда, ревматических заболеваний сердца, инфекционного септического эндокардита и в редких случаях при травме грудной клетки. Отдельных жалоб из-за пролапса митрального клапана может не быть, но пациента беспокоят симптомы основных болезней, например одышка при небольшой физической нагрузке и отёки.
Симптомы пролапса митрального клапана у детей
Симптомы ПМК у детей те же, что и у взрослых: повышенная утомляемость, психоэмоциональная неустойчивость и ощущение перебоев в работе сердца.
Патогенез пролапса митрального клапана
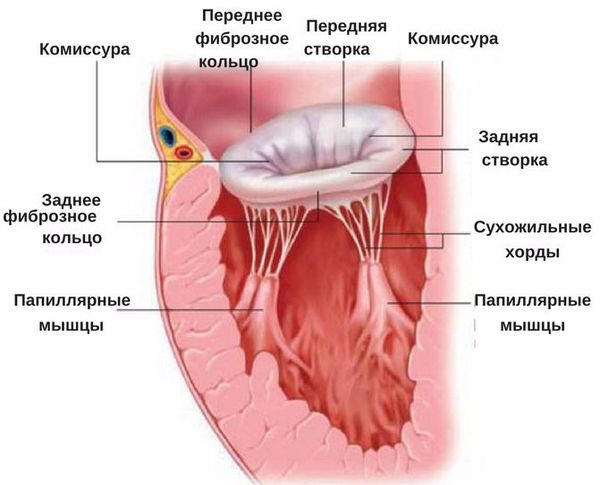
Строение митрального клапана [3] [4]
Многочисленными исследованиями показано, что митральный клапан в норме состоит из трёх зон, расположенных от кольца клапанного отверстия до свободного края клапана:
Механизм развития ПМК различен при первичных и вторичных пролапсах. При первичной патологии прогиб створок митрального клапана происходит из-за избыточности ткани створки и включает в себя как неизменённые, так и деформированные участки створок. Основные особенности внутреннего строения при первичном пролапсе митрального клапана:
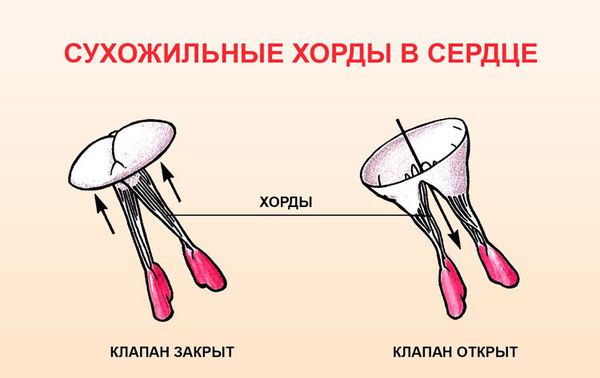
Всё это приводит к тому, что в период систолы под влиянием внутрижелудочкового давления створки прогибаются в сторону левого предсердия. По мере взросления человека увеличивается нагрузка на все органы, в том числе и на клапаны сердца. Так как ткани митрального клапана имеют более «хрупкое» строение, у людей с генетически обусловленными особенностями клапан начинает провисать, хорды, которые его удерживают, утолщаются или удлиняются. В результате кровь движется в обратном направлении (регургитация) из желудочка в предсердие.
В связи с вегетативной дисфункцией ( нарушением регулирования сосудистого тонуса) у пациентов появляются боли в области сердца, нарушения ритма, нестабильное артериальное давление, липотимии (предвестники обмороков — слабость, бледность, нарушение потоотделения), гипервентиляционный (одышка) и астенический синдромы.
При вторичном пролапсе имеется поверхностный фиброз (уплотнение, рубцевание) створок клапана, истончение и/или удлинение хорд и нарушение желудочковой жёсткости. При этом сами «листочки» клапана теряют эластичность из-за недостатка фиброэластина. Уплотняется мышечное кольцо клапана, в результате чего размер отверстия и площадь створок клапана перестают совпадать. Это приводит к обратному «забросу» крови, недостаточности митрального клапана, от степени которой зависит состояние и самочувствие человека.
Классификация и стадии развития пролапса митрального клапана
Пролапс классифицируют по степени прогиба (пролапса) створок клапана:
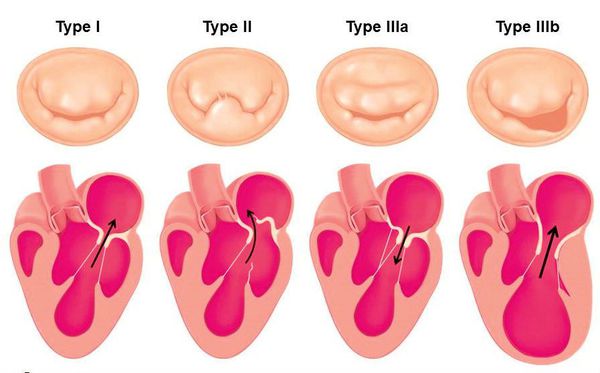
На прогноз клинического течения пролапса митрального клапана влияет наличие и степень митральной регургитации. Согласно Клиническим рекомендациям, утверждённым Министерством здравоохранения Российской Федерации в 2016 году, для оценки типа и степени митральной регургитации применяется анатомо-функциональная классификация по Карпантье [12] :
Тип I. Нормальная подвижность створок:
Тип II. Прогибание створок:
Тип III. Ограничение подвижности створок.
Тип IIIА. Нормальные сосочковые мышцы:
Тип IIIБ. Аномалия сосочковых мышц:
При пролапсе митрального клапана может развиваться митральная недостаточность. Она бывает первичной и вторичной:
В зависимости от степени регургитации выделяют 4 степени митральной недостаточности:
Диагностируют и оценивают степень тяжести регургитации при проведении эхокардиографии с помощью специальных программ.
Осложнения пролапса митрального клапана
Наиболее тяжёлыми осложнениями пролапса митрального клапана являются:
Несмотря на то, что у мужчин пролапс митрального клапана встречается реже, тяжесть осложнений этого заболеваний у них более выражена. Этот факт требует дальнейшего изучения, так как его причина неизвестна.
Диагностика пролапса митрального клапана
Критерии постановки диагноза
Пролапс митрального клапана чаще всего диагностируется неинвазивными методами обследования — врач учитывает жалобы пациента и наследственность. Но окончательный диагноз устанавливается с помощью трансторакальной эхокардиографии.
Инструментальные методы диагностики
При аускультативном обследовании (выслушивании сердца) с помощью стетоскопа врач может услышать характерный систолический щелчок и/или поздний систолический шум над верхушкой сердца. В положении пациента стоя систолические щелчок и шум появляются в начале систолы (сокращения). В положении пациента лежа или сидя на корточках эти звуковые феномены уменьшаются.
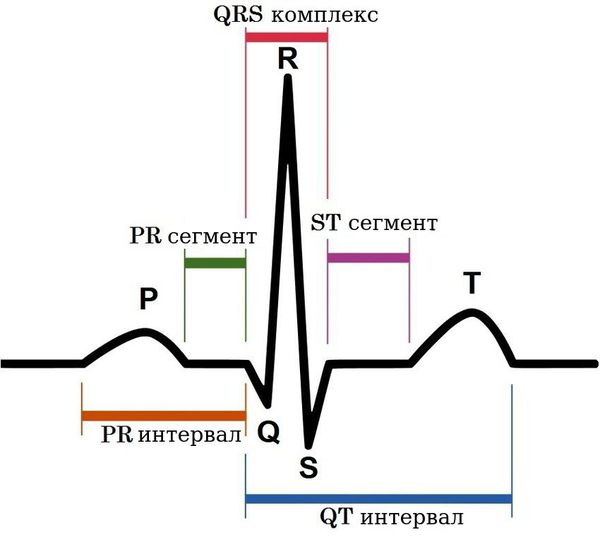
На электрокардиограмме можно обнаружить неспецифические изменения сегмента ST и зубца Т в отведениях III и aVF. При наличии пролапса митрального клапана на ЭКГ можно диагностировать феномен предвозбуждения («синдром укороченного PQ»), наджелудочковые (предсердные) тахикардии, желудочковую экстрасистолию.
Рентгенограмма грудной клетки может быть вариантом нормы или обнаружить признаки сглаженного лордоза («прямая спина»). Расширение сердца может быть диагностировано у некоторых больных с очень маленьким переднезадним размером грудной клетки.
Трансторакальная эхокардиография ( Эхо-КГ). Проводится с помощью ультразвукового датчика, поставленного врачом на определённые точки грудной клетки. Является самым важным рутинным методом обследования в диагностике пролапса митрального клапана. К отличительным и важным эхокардиографическим признакам данной патологии относят прогиб задней или обеих створок митрального клапана в полость левого предсердия в середине систолы, в позднюю систолу или во всю систолу. Чаще встречается прогиб (провисание) митрального клапана в середине систолы, что соответствует данным, получаемым при аускультации и при ангиографии.
Существуют и другие эхокардиографические признаки, они неспецифические, но высокочувствительные:
Трансторакальную эхокардиографию рекомендуется проводить каждые 6-12 месяцев всем бессимптомным пациентам с умеренной или тяжёлой митральной регургитацией. Это необходимо, чтобы оценить фракцию выброса (насосную функцию сердца, в норме она должна быть не менее 55 %) и конечный систолический размер.
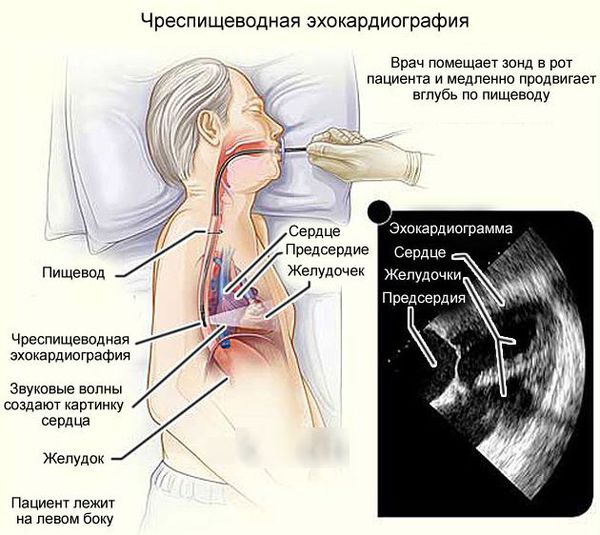
Чреспищеводная эхокардиография. Это ультразвуковое исследование, при котором датчик вводится в пищевод. Показано только при отсутствии противопоказаний в следующих случаях:
Разновидностью пролапса является так называемый болтающийся клапан (floppy mitral valve). Обычно он обнаруживается при разрыве хорд или отрыве папиллярной мышцы (чаще встречается при остром инфаркте миокарда). При эхокардиографии в В-режиме отчётливо видно свободно перемещающуюся сосочковую мышцу и «болтающуюся» створку митрального клапана. Створка совершает неправильные, произвольные движения в диастолу (период расслабления сердечной мышцы) и «проваливается» в полость левого предсердия в систолу желудочков. В М-режиме характерными эхокардиографическими признаками такого клапана является наличие:
Радионуклидная равновесная вентрикулография проводится для оценки фракции выброса и оценки степени тяжести сердечной недостаточности. Метод основан на внутривенном введении радионуклида с фиксацией его на эритроцитах крови и последующей количественной оценкой сократительной способности сердца.
Дифференциальная диагностика
Стратегия и тактика ведения пациента зависит от происхождения пролапса — врождённый он или приобретённый, поэтому дифференциальная диагностика проводится только между этими типами пролапса митрального клапана.
Лечение пролапса митрального клапана
При неосложнённом пролапсе митрального клапана лечение в большинстве случаев не требуется. В том числе лечение не назначают при колющих болях в области сердца и простых аритмиях. Пациенту рекомендуется обычный образ жизни, регулярные физические нагрузки, клинический контроль каждые 3-5 лет. Полезными аэробными нагрузками являются плавание, ходьба в быстром темпе, особенно «скандинавская», лыжи и велосипед.
В каких случаях требуется лечение ПМК
Медикаментозное лечение пролапса митрального клапана назначается при определённых клинических проявлениях. Больному с приступами сердцебиения, влияющими на функцию сердца, можно назначить препарат из группы β-адреноблокаторов. Если при перемене положения тела случаются потери сознания (ортостатические коллапсы), советуют увеличить количество жидкостей и соли.
Больному с перенесённой транзиторной ишемической атакой и ишемической болезнью сердца рекомендуется профилактическая доза ацетилсалициловой кислоты (выбирается лечащим врачом).
Больным с тяжёлой митральной недостаточностью и фибрилляцией предсердий (мерцательной аритмией) рекомендуется назначение противосвёртывающей (антикоагулянтной) терапии, рассматривается способ хирургического лечения ПМК.
При тяжёлой митральной недостаточности, которая чаще всего возникает при растяжении или отрыве хорд митрального клапана, проводится реконструктивное хирургическое лечение. Операция, как правило, восстанавливает рабочие функции сердца. Хирургическое вмешательство на митральном клапане зависит от особенностей работы сердца у конкретного пациента и состояния его клапана. Возможно проведение реконструкции митрального клапана, протезирования клапана с сохранением части или всего митрального аппарата и протезирование с удалением митрального аппарата.
Людям с высоким операционным риском проводится полностью эндоскопическая клапаносохраняющая операция (т. е. без разреза на грудной клетке, через сосуды) с помощью инновационной технологии 3D-визуализации (в России — с 2018 года, НМИЦ им. акад. Е. Н. Мешалкина).
Как лечить ПМК при дисплазии соединительной ткани
Пациентам следует принимать курсами препараты, которые стимулируют образование коллагена: аскорбиновую кислоту, витамины группы В, магний оротат (но его не назначают пациентам младше 16 лет), хондропротекторы, некоторые БАДы и препараты с фосфорными соединениями.
Прогноз. Профилактика
Прогноз заболевания в целом благоприятный, однако важным является клиническое наблюдение за пациентами. Целью динамического клинического наблюдения является оценка степени недостаточности митрального клапана.
При отсутствии митральной недостаточности и бессимптомном течении достаточно повторять допплерэхокардиографию каждые 3-5 лет.
Пациентам, у которых есть выраженная митральная регургитация, миксоматозная дегенерация, увеличение створок, удлинение хорд, фракция выброса левого желудочка менее 50 %, необходимо каждые 6 месяцев проводить ЭКГ и эхокардиографию, а также мониторирование ЭКГ по Холтеру. При необходимости выполняется чреспищеводная эхокардиография.
Наличие пролапса митрального клапана часто не нарушает физическую выносливость, поэтому среди людей с пролапсом митрального клапана и гипермобильными суставами можно встретить известных спортсменов, цирковых акробатов, артистов балета.
Однако не всем людям с ПМК разрешены занятия спортом. Спортивные нагрузки не рекомендуются больным с пролапсом митрального клапана, у которых выявлено более одного из следующих признаков:
Таким лицам можно рекомендовать аэробные нагрузки, бильярд, гольф, боулинг и стрельбу.
Может ли измениться прогноз при ПМК
Прогноз может ухудшиться при чрезмерных физических нагрузках и частых нелеченых инфекциях. В результате степень пролапса может усилиться и появляются признаки сердечной недостаточности.
Беременность при ПМК
Терапия препаратами магния при первичном пролапсе митрального клапана
Нормальный уровень магния в организме человека признан основополагающей константой, контролирующей здоровье человека [2, 7, 8]. В настоящее время среди возможных патогенетических механизмов дисплазии соединительной ткани (ДСТ) многие исследователи указыв
Нормальный уровень магния в организме человека признан основополагающей константой, контролирующей здоровье человека [2, 7, 8]. В настоящее время среди возможных патогенетических механизмов дисплазии соединительной ткани (ДСТ) многие исследователи указывают на хронический дефицит ионов магния, что ведет к нарушению формирования соединительнотканных структур, обусловливает хаотичность расположения волокон коллагена — основной морфологический признак ДСТ [5, 7, 9, 10].
Сведения о распространенности дефицита магния (норма магния в сыворотке крови: 1,0–1,15 ммоль/л) варьируются в широких пределах в зависимости от исследованной популяции, критериев диагностики и использованных методов исследования. По данным исследований, проведенных в России с участием пациентов с идиопатическим пролапсом митрального клапана (ПМК), уменьшение содержания магния в волосах выявлено в 72,0% случаев [5]. В схемы комплексного ведения пациентов с первичным ПМК прочно вошли препараты магния [5].
С целью сравнения эффективности применения у пациентов с идиопатическим ПМК препаратов Магнерот и Магне В6 мы провели простое сравнительное открытое проспективное исследование.
Критериями включения служили:
Критериями исключения были:
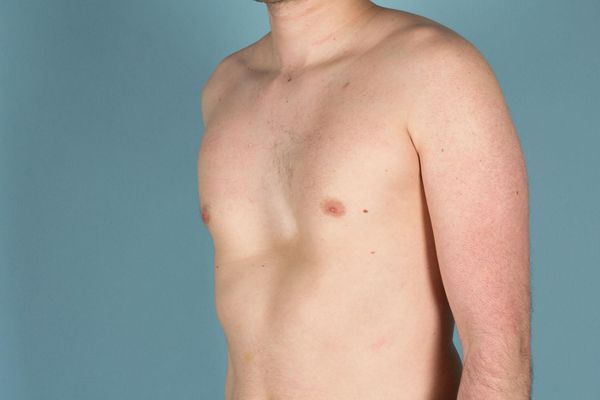
В соответствии с критериями включения и исключения (табл. 1), в исследование были включены 90 пациентов с идиопатическим ПМК (45 мужчин и 45 женщин) в возрасте 23,3 ± 5,2 года. У 52 пациентов функция митрального клапана была нарушена в виде наличия митральной регургитации различной степени выраженности (39% — регургитация 1-й степени, 39% — 2-й степени, 22% — 3-й степени); у 32 больных функция митрального клапана была сохранена; в 64% случаев выявлялась миксоматозная дегенерация митрального клапана. Кроме того, отмечены: в 14% случаев — расширение аорты, в 20% — пролапс трикуспидального клапана, в 87% — аномально расположенные хорды, в 56% — удлинение хорд митрального клапана. Все пациенты имели те или иные фенотипические признаки ДСТ: у всех выявлен астенический тип конституции, у 78% наблюдались деформации грудной клетки или позвоночника, у 26% — другие локомоторные проявления ДСТ (синдром гипермобильности суставов, плоскостопие, искривление нижних конечностей), у 34% — птозы внутренних органов, у 72% — дефицит массы тела. В качестве группы контроля были обследованы 30 практически здоровых добровольцев (15 мужчин и 15 женщин, средний возраст — 22,3 ± 3,5 года), соответствующих по полу и возрасту.
Всем пациентам было проведено общеклиническое обследование, эхокардиография, суточное мониторирование ЭКГ по Холтеру (Холтер-ЭКГ), велоэргометрия (ВЭМ), а также определение уровня магния в слюне и сыворотке. Исходный вегетативный тонус оценивали на основании клинических тестов (А. М. Вейн, 1998). Для выявления и оценки невротических нарушений использовался опросник, разработанный Д. М. Менделевичем и К. К. Яхиным [3]. Статистическая обработка результатов проводилась с использованием пакета программ SPSS for Windows.
Результаты. Оценка субъективного статуса пациентов, проведенная до начала медикаментозной терапии, продемонстрировала преобладание жалоб со стороны сердечно-сосудистой системы — 89%. Далее по частоте отмечены жалобы астенического характера (слабость, вялость, легкая утомляемость, снижение работоспособности, апатия): они регистрировались у 80% пациентов.
При проведении ЭКГ и Холтер-ЭКГ были выявлены случаи манифестных и латентных нарушений ритма и проводимости сердца. Проведение Холтер-ЭКГ в большинстве случаев было более информативно в диагностике нарушений ритма пациентов с ПМК, что диктует необходимость включения этого метода диагностики в программу обследования пациентов с ДСТ. По данным Холтер-ЭКГ, у пациентов с ПМК фиксировались суточные колебания сердечного ритма от 39-59 до 109-182 уд/мин. У 42% (38 пациентов) выявлен синдром ранней реполяризации желудочков, у 68 человек — нарушения процессов реполяризации различной степени выраженности, у 24 больных — удлинение интервала QT в сравнении с должной величиной.
По данным анкетирования, у 76 (84%) пациентов была выявлена вегетососудистая дистония, при этом у 54 больных (71%) обнаружена симпатикотония, у 22 (24%) — ваготония, у 14 человек — эутония. Анализ вариабельности сердечного ритма у пациентов с ПМК продемонстрировал достоверно более высокие значения среднесуточных показателей — SDNN, SDNNi, RMSSD с преобладанием активности симпатического отдела (SDANN — 149,4 мс, р = 0,004).
Уровни магниемии у пациентов с ПМК достоверно не отличались от контрольной группы и от нормального содержания магния в сыворотке крови, тогда как исследование концентрации магния в ротовой жидкости документировало дефицит данного макроэлемента у пациентов с ПМК, подтверждая имеющиеся литературные данные (табл. 2)
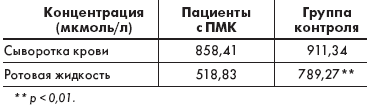 |
| Таблица 2. Содержание магния в сыворотке крови и ротовой жидкости пациентов с ПМК |
Анализ показателей клинического опросника для выявления и оценки невротических состояний выявил присутствие в психологическом профиле пациентов такого феномена, как невротическая тревога (табл. 3). Кроме того, значения по шкалам астении и вегетативных нарушений превысили уровень показателей нормального диапазона, что отражало формирование психического истощения, обусловленного вегетативной напряженностью, являющейся одним из облигатных признаков ДСТ [4].
После проведенного обследования пациенты с ПМК были распределены методом последовательного включения на две группы, сопоставимые по полу и возрасту. Пациентам группы I (45 человек) назначался Магнерот по схеме: 2 таблетки 3 раза в день первые 7 дней, затем по 1 таблетке 3 раза в день в течение 8 нед. В группе II (45 человек) назначался Магне В6: 2 таблетки 3 раза в день в течение 8 нед.
 |
| Таблица 3. Величины диагностических коэффициентов по шкалам невротических расстройств |
Повторное обследование пациентов проводилось после завершения курса лечения. Уровень магния в ротовой жидкости достоверно повысился в обеих группах (0,903 ммоль/л, р 2 соответственно до и после лечения (p > 0,05)). Изменения массы тела были отмечены у 42% пациентов этой группы (р = 0,091). Наибольшая прибавка составила 3 кг к завершению курса лечения; вместе с тем у большинства пациентов данной группы показатели индекса массы тела оставались ниже возрастной нормы. При этом следует отметить, что все 19 пациентов, отмечавших положительную динамику массы тела, активно интересовались возможностью продлить курс лечения Магнеротом. Вопрос, связан ли описанный эффект с особенностью препарата — наличием в составе оротовой кислоты — требует уточнения.
В обеих группах все пациенты завершили полный курс лечения препаратом. Курсовая доза магния, полученная в первой группе Магнерот, составила 6 888 мг, во второй группе (Магне В6) — 16 128 мг. Препараты магния хорошо переносились больными, лишь у двух человек группы I (4%) были жалобы на головокружение и нарушение стула при приеме 6 таблеток Магнерота в день, которые исчезли через 2 дня после снижении дозы препарата наполовину. Других отступлений от протокола лечения не наблюдалось.
Выводы
Литература
Г. И. Нечаева, доктор медицинских наук, профессор
И. В. Друк, кандидат медицинских наук
О. В. Тихонова, кандидат медицинских наук
С. Л. Морозов
Омская ГМА, Омск
Ведение пациентов с пролапсом митрального клапана в поликлинике
Каковы методы диагностики пролапса митрального клапана? Каковы принципы ведения пациентов с пролапсом митрального клапана в амбулаторных условиях? В последние годы пролапс митрального клапана (ПМК) привлекает к себе пристальное внимание врачей
Каковы методы диагностики пролапса митрального клапана?
Каковы принципы ведения пациентов с пролапсом митрального клапана в амбулаторных условиях?
В последние годы пролапс митрального клапана (ПМК) привлекает к себе пристальное внимание врачей как наиболее часто встречающийся компонент синдрома дисплазии соединительной ткани сердца [2, 3, 6]. Частота ПМК в популяции — 5-10%. В структуре заболеваемости женщины составляют 2/3–3/4 больных [3, 4].
Так что же такое ПМК — синдром или нозологическая форма? С. А. Аббакумов и соавт. [1] считают его синдромом на грани нормы и патологии. Более распространено мнение о ПМК как о самостоятельной нозологической форме (МКБ 10 — рубрика I. 134. 1).
«Клапанная» теория происхождения ПМК предполагает наличие генетически детерминированного дефекта коллагена, приводящего к «слабости» соединительной ткани (СТ) створок и их пролабированию. Обнаружен аутосомно-доминантный тип наследования особенностей структуры СТ клапанов, характера вегетативного реагирования, изменяющегося в определенных условиях внешней среды [2, 3].
Диагностика ПМК по клинической картине затруднена ввиду ее полиморфизма, «мозаичности». «Неспецифические» симптомы нейроциркуляторной дистонии (НЦД) выявляются в 82-100% случаев [1, 5], у 20-60% пациентов отсутствуют какие-либо субъективные симптомы [4]. Основные клинические проявления ПМК [3, 6]:
Частота кардиалгий составляет от 32 до 98%. Наиболее приемлемой нам представляется точка зрения, отстаивающая предположение ведущей роли дисфункции вегетативной нервной системы в происхождении кардиалгий у лиц с ПМК [2, 3]. Болевые ощущения в прекардиальной области лабильны: слабая и умеренная интенсивность болей, чувство дискомфорта в грудной клетке. Кардиалгии возникают спонтанно или в связи с переутомлением, психоэмоциональными стрессами; прекращаются самостоятельно либо при приеме «сердечных» препаратов (валокордин, корвалол, валидол).
Нарушения ритма и проводимости встречаются в 16-79% случаев [3, 6]. Субъективные ощущения при аритмиях — учащенное сердцебиение, «перебои», толчки, «замирание». Тахикардия и экстрасистолия лабильны, ситуационно обусловлены (волнение, физическая нагрузка, употребление чая, кофе).
Клинические симптомы вегетативной дисфункции достоверно чаще встречаются у женщин: тошнота и «ком в горле», вегетативные кризы, повышенная потливость, астеновегетативный синдром, периоды субфебрилитета, синкопальные состояния [2]. Вегетативные кризы при ПМК обнаруживаются в 8-55% случаев. Они возникают спонтанно или ситуационно, повторяются не менее трех раз в течение трех недель, не связаны со значительным физическим напряжением или угрожающей жизни ситуацией. Кризы, как правило, не сопровождаются яркой эмоциональной и вегетативной аранжировкой.
Цефалгии при ПМК регистрируются в 51-76% случаев, проявляются в виде периодически повторяющихся приступов и чаще имеют характер болей напряжения. Цефалгии провоцируются психогенными факторами, изменением погоды, захватывают обе половины головы. Реже (11-51%) отмечаются мигренозные головные боли [2, 3, 4].
В физикальном статусе больных с ПМК достоверно чаще, чем в популяции, встречаются маркеры соединительнотканной дисплазии (СТД). У подростков, лиц молодого и среднего возраста с СТД сердца в подавляющем большинстве случаев удается выявить три и более фенотипических стигм. С увеличением числа внешних маркеров нарастает частота выявления СТД сердца [3].
Ведущим аускультативным признаком ПМК является систолический щелчок в зоне верхушки сердца и вдоль левого края грудины, в середине или в конце систолы, обусловленный избыточной подвижностью измененного клапана, натяжением сухожильных хорд. Второй аускультативный феномен — систолический шум после «щелчка», появляющийся с момента регургитации в левое предсердие и определяющийся ее выраженностью [4]. Классическая звуковая симптоматика выявляется в 25-70% случаев, шум изменяется при перемене положения тела, физических нагрузках и под воздействием фармакологических средств. Частота «немого» варианта ПМК — от 33 до 80% случаев.
На электрокардиограмме (ЭКГ) покоя наиболее часто (82,7%) отмечаются неспецифические изменения конечной части желудочкового комплекса: депрессия сегмента ST и/или инверсия зубца Т во II, III, aVF, V5-6 [4, 6]. У некоторых пациентов выявляются нарушения ритма и проводимости (предсердная и желудочковая экстрасистолия, синдромы WPW, CLC, ранней реполяризации желудочков; атриовентрикулярная блокада, блокада ножек пучка Гиса).
Основной метод диагностики ПМК — двухмерная эхокардиография (ЭхоКГ; чувствительность — 69-96%, специфичность — 87-100%). ЭхоКГ позволяет обнаружить ПМК у 10% тех пациентов, у которых не выявлено ни жалоб, ни аускультативных признаков пролабирования. Необходима комплексная оценка пролабирования створок с использованием М- и В-режимов, всех трансторакальных доступов [6].
Поскольку ПМК — заболевание, характеризующееся наличием чрезмерного количества аномальной в структуре клапанной ткани, при ЭхоКГ отмечается широкий спектр изменений толщины створок митрального клапана: от «булавочного» утолщения на концах до выраженного утолщения и удлинения. Чем грубее деформация клапана, тем больше выражены клинические проявления, чаще возникают осложнения. Частота митральной регургитации (МР) — 42-100%. Среди больных с регургитацией II-III стадии преобладают мужчины (74%) и лица старше 50 лет.
Амбулаторно первичный ПМК диагностирован у 208 человек (76 мужчин и 132 женщины), средний возраст 28,88±5,37 года.
По клинико-инструментальным данным пациентов разделили на четыре подгруппы. В 1-ю подгруппу (57 человек) вошли лица, у которых ПМК выявлен случайно при ЭхоКГ, жалоб пациенты не предъявляли, к врачу не обращались. Учитывая малосимптомность и благоприятный характер течения заболевания у лиц данной подгруппы, а также с целью исключения ятрогении медикаментозное лечение признано нецелесообразным. Данным пациентам были предложены программы семейной профилактики — «школа больного». Пациенту и его семье давались советы по выбору образа жизни, адекватного возможностям больного; режиму труда и отдыха; исключению переутомления, чрезмерных психоэмоциональных и физических нагрузок, интоксикаций в быту и на производстве. Рекомендованы умеренные систематические физические нагрузки, полноценный отдых (ежедневный, еженедельный, ежегодный); посещение климатических и бальнеологических курортов с мягким климатом. Всем больным проводили санацию очагов хронической инфекции. При профессиональном ориентировании предлагали отказаться от выбора специальностей, заведомо связанных с физическими и психоэмоциональными перегрузками, воздействием неблагоприятных физических и химических факторов.
В подгруппу 2а (41 человек) выделены больные, у которых признаки ПМК сочетались с перманентными вегетативными расстройствами (НЦД) — кардиалгиями, цефалгиями, гипервентиляционным синдромом, метеотропностью. В подгруппу 2б (27 человек) вошли пациенты с симптомами НЦД и парциальными вегетативными кризами («паническими атаками»). Программа вмешательства включала:
В 3-ю подгруппу (66 человек) выделены лица, у которых признаки ПМК и НЦД сопровождались изменениями конечной части ЭКГ (депрессия сегмента ST, отрицательный двухфазный зубец Т). Основу базисной терапии составили кардиоселективные β-адреноблокаторы в малых и средних дозах; «курсами» по 2-3 недели назначались препараты с кардиопротективным действием (рибоксин, панангин, оротат калия, витамины В1, В6). При выраженной симптоматике НЦД применяли малые транквилизаторы, седативные фитопрепараты. Рекомендации по диететике: «средиземноморская диета» (овощи, фрукты, морская рыба).
В 4-ю подгруппу (17 человек) включены пациенты с гемодинамически значимой МР, нарушениями внутрисердечной гемодинамики, начальными признаками хронической сердечной недостаточности (ХСН). В данной подгруппе базисными препаратами явились ингибиторы ангиотензинпревращающего фермента в индивидуально подобранных дозах. Курсами по 3-7 недель назначались кардиопротективные метаболические препараты. Отдельных пациентов с выраженной МР консультировал кардиохирург. Оперативное лечение было признано нецелесообразным (начальная стадия ХСН, отсутствие жизнеопасных аритмий, инфекционного эндокардита).
Оценку эффективности программ проводили через 6-12 месяцев после вмешательства, направленного на изменение качества жизни (КЖ) больного. В результате реализации предложенных программ удалось добиться достоверного (р±0,05) повышения показателя КЖ в подгруппах 1, 2а, 3.
В 4-й подгруппе значение КЖ хотя и несколько повысилось (р±0,05), однако как до, так и после вмешательства было гораздо ниже, чем в других подгруппах.
Проведенное исследование показало, что разработанные и апробированные программы вмешательства у пациентов с первичным ПМК высокоэффективны и могут успешно использоваться в работе врача первого контакта.
Литература
1. Аббакумов С. А., Веденяпина О. На грани нормы и патологии //Врач. 1998. № 3. С. 29-32.
2. Вейн А. М., Соловьева А. Д., Недоступ А. В., Федорова В. И., Морозова Н. С. Вегетативные нарушения при пролапсе митрального клапана //Кардиология. 1995. Т. 35. № 2. С. 55-58.
3. Земцовский Э. В. Соединительнотканные дисплазии сердца, Спб: ТОО «Политекс-Норд-Вест» 1998. 96 с.
4. Кузнецов Г. П., Лебедев П. А. Пролапс митрального клапана. Методическое пособие для врачей и студентов. Самара: МЗ РФ, СамГМУ, 1997. 24 с.
5. Маколкин В. И. Возможно ли использование термина «функциональные болезни сердца»? //Тер. архив. 1998. № 8. С. 5-7.
6. Мартынов А. И., Степура О. Б., Остроумова О. Д., Пак Л. С. Мдинарадзе Ю.С. Пролапс митрального клапана. Часть 1. Фенотипические особенности и клинические проявления //Кардиология. 1998. Т.38. № 1. С. 72-80.