что больше молекула или атом и почему
Атом и молекула – что это и отличия
Мельчайшие частицы – атом и молекула, об этом знают многие люди, но не все могут рассказать подробно, что же это такое. Также сложно, не имея специальных знаний, объяснить, в чем состоят отличия между этими структурами. Из различных исторических источников известно, что про эти структурные единицы знали еще древнегреческие ученые. Так философ Демокрит одним из первых высказал предположение о том, что все известная людям материя состоит из крошечных по своим размерам, неделимых человеческому глазу частиц. Их он назвал атомами. Современные ученые подтвердили эту теорию и установили опытным путем, что вещества состоят из атомов и молекул. Для того чтобы установить разницу межу этими структурными единицами, необходимо сначала дать им определение, а затем сравнить, чтобы определить, в чем состоят различия.
Определение понятий
На первых этапах изучения считалось, что атом и молекула – элементы неделимые. Более глубокие исследования и всесторонние изучения позволили опровергнуть это мнение. Сегодня этими терминами обозначают самостоятельные элементы, которые образуют все, что окружает человека.
Атомом называют мельчайшую структурную единицу, составляющую любое вещество.
Молекулой принято считать элементарную частицу, из которых состоят все окружающие людей вещества, материи и компоненты.
Сравнение
После приведенных определений можно приступить к сравнению элементарных структурных единиц вещества. Атом является наименьшей ее составляющей. Он имеет собственную массу и размер. Основная задача – определение, какими свойствами будет обладать то или иное химическое вещество.
Нужно учитывать, что атом не является конечным элементом. Он в свою очередь делится на ядро и электроны, которые совершают движение по орбите, расположенной вокруг ядра. Подобное строение и определяет, какими свойствами будет обладать то или иное вещество. Особенностью атома является то, что его невозможно увидеть вне компонента, в свободном состоянии. Все атомы имеют тесные связи между собой, которые и образуют молекулу. Происходит это благодаря электрическим зарядам частиц, из которых состоят атомы.
Молекула — это единица, составляющая вещество. В состав молекул входят атомы. Разное их количество определяет свойства. Атомы внутри молекулы имеют межатомные связи. Каждая молекула состоит из атомных ядер и внутренних электронов. Они совершают движение по своим орбитам. В состав входят также внешние валентные электроны. В разных молекулах находится разное количество атомов. Это свойство и определяет разнообразие химических веществ и компонентов. Молекула имеет сложную архитектурную постройку. Так у каждого атома свое место внутри молекулы. Количеством атомов в ней определяются свойства – химические реакции и превращения. Имеющиеся свойства влияет порядок и конфигурация соединения всех атомов. Атомная постройка, которая образует молекулу, может быть жесткой. Также бывают и исключения. Особенность мельчайшей единицы – постоянное движение. Атомы никогда не останавливаются, они продолжают колебание на положенном ему месте в молекуле, чтобы удержать равновесие.
Выводы
Атомы и молекулы – структурные единицы, образующие любое вещество. Атомы образуют молекулу. В составе атома присутствуют еще более мелкие элементы — ядро и электроны, которые движутся по своим орбитам вокруг ядра. Молекулы состоят из атомов (одного или нескольких).
Атом имеет электрический заряд (положительный или отрицательный) а молекула по этому показателю полностью нейтральная. Только молекула в веществе обладает способностью к самостоятельному существованию.
Что меньше: атом или молекула?
Частицы в физике делятся на элементарные и составные. Элементарные частицы не обладают внутренней структурой, то есть не содержат в себе других частиц. Составные же, напротив, имеют сложную внутреннюю структуру и состоят из частиц меньшего размера. К составным частицам относятся атомы и молекулы.
«Бери и Делай» рассказывает, что такое атом и молекула, и какая из этих двух частиц имеет меньший размер.
Слово «атом» произошло от древнегреческого ἄτομος — «неделимый». Это наименьшая частица вещества, из которой образуется химический элемент. Каждый атом состоит из ядра и элементарных частиц — одного или нескольких электронов, окружающих его. Ядро, в свою очередь, состоит из одного или нескольких протонов и нескольких нейтронов. Больше 99 % массы атома находится именно в ядре. Атомы могут присоединяться друг к другу с помощью химических связей и образовывать молекулы.
Что такое молекула
Слово «молекула» произошло от новолатинского molecula, которое, в свою очередь, является производным от другого латинского слова moles — «масса». В научном смысле название отражает понимание молекулы как мельчайшей части, на которую можно разделить вещество, не нарушая его химические свойства. Структурно молекула представляет собой группу из двух или более атомов, удерживаемых вместе химическими связями. Большая часть органических и неорганических веществ на планете является молекулами. Например, вода, сахар, витамины или аминокислоты, из которых состоит ДНК.
Что меньше: атом или молекула?
Атом. Поскольку он является составной частью молекулы и вместе с другими атомами образует ее структуру. Несмотря на меньший размер, атом, как и молекула, относится к составным частицам. Его структуру, в свою очередь, образуют элементарные частицы меньшего размера — протоны, электроны и нейтроны.
Есть ли разница между атомом и молекулой?
Атомы и молекулы — это два самых основных термина, которые используются, когда мы говорим о составе элемента или соединения. Существенная разница между атомом и молекулой состоит в том, что атом рассматривается как мельчайшая частица, составляющая материю. Напротив, молекула — это комбинация двух или более мельчайших единиц, то есть атомов, которые химически связаны вместе.
Всякий раз, когда используются названия атомов и молекул, возникает путаница относительно того, чем они отличаются и какие сходства существуют между ними.
По сути, то, что требует определенного пространства и имеет определенную массу, определяется как материя, которая состоит из атомов и молекул. Все в этой вселенной состоит из атомов. От маленького куска мела до большой доски, от единственной стены до целого дома, от маленького муравья до гигантского человека, от гигантского человека до всей Земли — все состоит из атомов. Но атомы настолько малы, что их невозможно визуализировать человеческим зрением или каким-либо микроскопическим устройством.
| Сравниваемые параметры | Атом | Молекула |
| Основные | Наименьшая неделимая единица материи — атом | Комбинация нескольких атомов, которые можно разделить, представляет собой молекулу |
| Существование | Не независимый | Независимый |
| Составные части | Нуклоны (имеющие протоны, нейтроны) и электроны | Два или более атомов, связанных вместе |
| Природа | Неустойчивый | Устойчивый |
| Видимость | Нет | Да, но только через микроскоп |
| Масса | Примерно равно сумме масс протонов, нейтронов и электронов, составляющих этот атом | Сумма масс каждого отдельного атома, образующего молекулу |
| Форма | Не имеет фиксированной формы, но обычно считается сферическим | Существует в линейных, тригональных, пирамидальных формах и других |
| Реактивность | Высокая | Низкая |
| Размер | Небольшой | Сравнительно большой |
| Связь | Кулоновская сила притяжения связывает субатомные частицы | Ковалентная связь существует между двумя или более атомами |
| Образец | Сера, азот, натрий, углерод и другие | Вода, сахар, углекислый газ, перекись водорода и другие |
Определение атома
Самая маленькая неделимая по природе частица, составляющая материю, известна как атом. Каждый атом состоит из трех основных субатомных компонентов, а именно: электрон, протон и нейтрон. И каждый атом отличается друг от друга, потому что у них разное количество протонов.
Атомы считаются основным строительным материалом любой материи и проявляют свое существование повсюду вокруг нас.
По сути, теория, лежащая в основе этого, согласно Махариши Канаду, заключается в том, что при разделении любой материи будут получены более мелкие и мелкие частицы. Но по прошествии определенного времени частицы станут настолько маленькими, что их дальнейшее деление станет невозможным. Эта окончательная неделимая частица называется атомом.
Слово «атом» образовано от комбинации слов «А» и «томас» (tomas), где «А» означает «не», а «томас» соответствует «вырезать».
Каждый атом проявляет свойства химического элемента, в котором он присутствует. Атомный номер — важнейшее свойство атома, которое соответствует количеству положительных зарядов, существующих в ядре.
Определение молекулы
Химическая комбинация нескольких неделимых мельчайших единиц вещества, то есть атомов, порождает молекулу. Когда два или более атома прочно связаны друг с другом некоторой силой притяжения, их индивидуальная комбинация дает молекулу. Молекула — это мельчайший объект материи, который проявляет независимое существование, может делиться дальше и проявляет характеристики материи.
Комбинация атомов, образующих молекулу, может состоять из одинаковых или разных элементов.
В целом молекулы классифицируются как:
Молекулы элементов: это молекулы, образованные комбинацией атомов одного типа. Например, кислород (O2) — это молекула, состоящая из 2 отдельных атомов кислорода, то есть двухатомная молекула.
Молекулы соединений: это молекулы, состоящие из атомов различных типов элементов.
Например, Оксид кальция (CaO) представляет собой молекулу, которая представляет собой комбинацию атома углерода и кислорода.
Различные атомы в молекуле связаны вместе, разделяя электроны, присутствующие в их внешних оболочках, посредством ковалентной связи.
Ключевые различия между атомом и молекулой
Вывод
Итак, из этого обсуждения мы можем сделать вывод, что атомы и молекулы похожи в том, что оба составляют материю. Однако атомы не могут быть далее разделены, примерами атомов являются азот, сера, углерод и другие. А вот молекулы можно дополнительно разделить, деление которых предоставит нам атомы, показывающие характеристики вещества, некоторыми примерами молекул являются вода, диоксид углерода, и другие.
Из чего состоит все вокруг или что такое молекула?
Каждый раз, когда два атома соединяются вместе, они образуют молекулу. На самом деле все, что нас окружает – да и мы сами – состоит из триллионов различных типов молекул. Понятие молекулы было принято в 1860 году на международном съезде химиков в Карлсруэ. Согласно принятому определению молекула – это наименьшая частица химического вещества, которая обладает всеми его химическими свойствами (растворимость, вкус, способность вступать в соединения и пр). Введение понятия молекулы подтолкнуло развитие физики, химии и других естественных наук. В более общем понимании молекулой называют частицу, образованную из двух или более атомов, соединенных между собой ковалентными связями.
Молекула воды содержит 1 атом кислорода и 2 атома водорода
Атом – мельчайшая частица вещества, которая обладает всеми его физическими свойствами (цвет, твердость, плотность и пр.)
Когда атомы различных типов элементов соединяются вместе, они образуют молекулы, называемые соединениями. Так, вода состоит из сложных молекул, состоящих из 2 атомов водорода и 1 атома кислорода. Вот почему она называется H2O: у молекулы воды всегда будет в 2 раза больше атомов водорода, чем атомов кислорода. Существует чуть более 100 типов атомов, но типов различных веществ миллионы. Причина такого неравенства кроется в том, что они состоят из различных типов молекул.
Важно понимать, что молекулы состоят не только из различных типов атомов, но и из различных соотношений. Как и в приведенном выше примере с водой, молекула воды состоит из двух атома водорода и одного атома кислорода, что записывается как H2O. Другими примерами являются углекислый газ (C02), аммиак (NH3) и сахар или глюкоза (C6H12O6). Некоторые молекулярные формулы могут получиться довольно длинными и сложными. Давайте посмотрим на молекулу сахара:
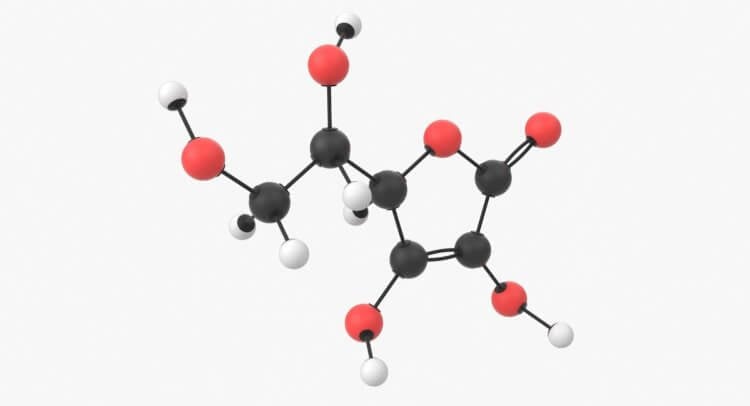
Чтобы она получилась, нужны определенные атомы в определенном количестве. Но молекулы могут быть гораздо больше. Одна молекула витамина С состоит из 20 атомов (6 атомов углерода, 8 атомов водорода и 6 атомов кислорода – C6H8O6). Если взять эти 20 атомов витамина С и смешать, соединяя их вместе в другом порядке, то получится совершенно другая молекула, которая не только выглядит по-другому, но и действует иначе.
Молекула витамина С выглядит так
Некоторые молекулы, особенно некоторые белки, содержат сотни или даже тысячи атомов, которые соединяются вместе в цепи, которые могут достигать значительной длины. Жидкости, содержащие такие молекулы, иногда ведут себя странно. Например, жидкость может продолжать вытекать из колбы, из которой была вылита некоторая ее часть, даже после того, как колба будет возвращена в вертикальное положение.
Факты о молекулах
Чтобы всегда быть в курсе последних научных открытий, подписывайтесь на наш новостной канал в Telegram
Химические связи
Молекулы и соединения удерживаются вместе силами, называемыми химическими связями. Существует четыре типа химических связей, которые удерживают большинство соединений вместе: ковалентные связи, ионные связи, водородные и металлические, однако в качестве основных выделяют ковалентные и ионные, так как они связаны с электронами. Как известно, электроны вращаются вокруг атомов в оболочках. Эти оболочки хотят быть «полными» электронов. Когда они не заполнены, то будут пытаться соединиться с другими атомами, чтобы получить нужное количество электронов и заполнить их оболочки.
Ковалентные связи делят электроны между атомами. Это происходит, когда получается, что атомы делятся своими электронами, чтобы заполнить свои внешние оболочки. В свою очередь ионные связи образуются, когда один электрон передается другому. Это происходит, когда один атом отдает электрон другому, чтобы сформировать баланс и, следовательно, молекулу или соединение.
Еще больше увлекательных статей о том, как ученые дробят реальность на атомы, читайте на нашем канале в Яндекс.Дзен. Там выходят статьи, которых нет на сайте!
Знания о свойствах и строении молекул легли в основу современной науки и нашего понимания Вселенной
Немаловажным также является тот факт, что молекулы всегда находятся в движении. В твердых телах и жидкостях они находятся очень близко друг к другу, а их движение можно сравнить с быстрой вибрацией. В жидкостях молекулы могут свободно перемещаться между собой, как бы скользя. В газе плотность молекул обычно меньше, чем в жидкости или твердом теле того же химического соединения, а потому молекулы движутся даже более свободно, чем в жидкости. Для конкретного соединения в данном состоянии (твердом, жидком или газообразном) скорость молекулярного движения возрастает с увеличением абсолютной температуры.
15 самых интригующих фактов об атомах
Все во Вселенной — от ядра Земли до самых дальних галактик — состоит из атомов. Это фундаментальная единица элемента.
К настоящему времени было идентифицировано 118 элементов (все они перечислены в периодической таблице).
Слово «атом», означающее «неделимый», происходит от древнегреческого слова «ἄτομος». Древнегреческие философы считали, что атом невозможно разделить на что-то меньшее. Однако ученые доказали этот факт неправильно в начале 20 века, когда они открыли субатомные частицы (электроны, протоны, нейтроны).
Ниже мы перечислили некоторые из наиболее интригующих фактов об атомах, которые только сделают вас умнее. Так что давайте начнем с самого короткого и простого.
1. Состав атомов
Каждый атом содержит одно ядро [в центре] и один или несколько электронов. Ядро обычно состоит из равного числа протонов и нейтронов, вместе называемых нуклонами.
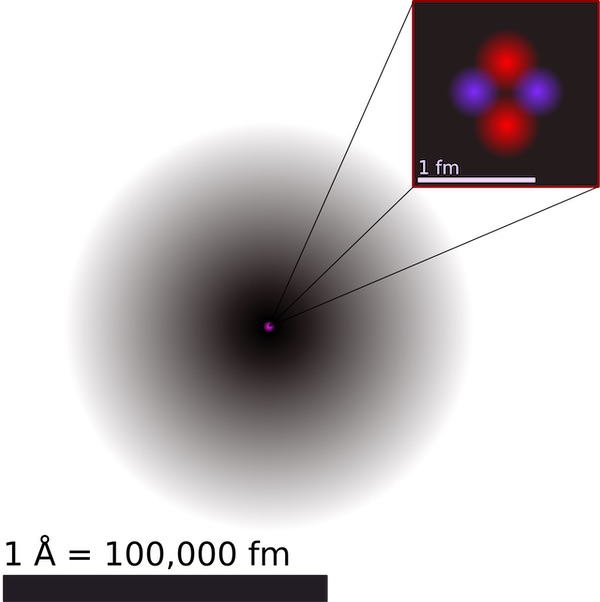
2. Ядро содержит почти всю массу
Ядро, расположенное в центре атома, составляет более 99,9 % его массы, но занимает лишь одну триллионную его общего объема. Таким образом, большая часть пространства внутри атома пуста.
3. Электроны чрезвычайно малы
Электрон является наиболее активным компонентом атома, но он почти ничего не вносит в массу атома. Например, в атоме водорода масса электрона составляет всего 0,0005 массы ядра.
4. Атом может иметь электрический заряд
Электроны несут отрицательный заряд, протоны несут положительный заряд, а нейтроны не имеют электрического заряда. Атом электрически нейтрален, если он имеет одинаковое количество электронов и протонов.
Однако, если атом имеет меньше или больше протонов, чем электронов, он имеет общий положительный или отрицательный заряд (известный как Ион).
5. Что удерживает протоны и нейтроны вместе?
Ядерная сила удерживает протоны и нейтроны вместе в ядре атома. Электроны притягиваются к протонам другой силой, называемой электромагнитной силой, которая слабее ядерной силы.
6. 94 Атома естественного происхождения на Земле
Из 118 известных атомов 94 встречаются в природе, хотя некоторые встречаются в незначительных количествах. Остальные 24 были синтезированы только в лабораториях или ядерных реакторах.
7. Каждый атом уникален
Каждый атом содержит определенное количество протонов в ядре. Например, все атомы натрия содержат 11 протонов, а все атомы серебра содержат 47 протонов.
Изотоп элемента определяется числом нейтронов, а магнитные характеристики зависят от количества электронов в атоме.
8. Самый большой и самый маленький атом
Самым большим элементом (по размеру) является Франций, но поскольку он крайне нестабилен, предпочтение отдается Цезию. У него большая валентная оболочка и относительно менее эффективный заряд ядра.
Иллюстрация атома гелия | Предоставлено: Викимедиа.
9. Самый тяжелый и легкий атом
Оганессон, однако, является самым тяжелым синтетическим химическим элементом. Самым тяжелым природным элементом является Уран с атомным весом 238,029.
Элемент, который имеет самый легкий атом-это водород. У него есть только один протон, обращающийся вокруг одного электрона. Его самый распространенный изотоп, известный как Протий, состоит из одного протона и нулевых нейтронов.
10. Возможно ли преобразовать один элемент в другой?
В некоторых экстремальных условиях электромагнитная сила (которая отталкивает электроны и протоны) преодолевает сильную ядерную силу, выбрасывая нуклоны из атомного ядра и оставляя после себя совершенно другой элемент. Это именно то, что происходит при делении ядер.
Однако этот процесс [распада] является дорогостоящим и опасным. Ученые пока не смогли безопасно генерировать энергию с помощью ядерного деления.
11. Атомы в человеческом теле
Тело человека весом 70 кг состоит из 7 × 10 27 атомов. Три атома (водород, кислород и углерод) составляют до 99 процентов от общего количества.
12. Сколько атомов существует во Вселенной?
Наблюдаемая вселенная огромна: она охватывает приблизительно 93 миллиарда световых лет. Согласно теоретической оценке, в нашей вселенной насчитывается от 10 78 до 10 82 атомов.
Это не какой-то выдуманный номер. Расчеты основаны на достоверных данных (что мы знаем о вселенной). Однако между этими оценками существует огромная разница, что говорит о значительной степени ошибки. Более точные цифры будут доступны, когда мы узнаем больше о космосе.
13. Радиоактивные атомы
В нестабильном атоме силы неуравновешенны. В этом случае атомное ядро содержит избыток либо протонов, либо нейтронов. Атом пытается достичь стабильного состояния, выбрасывая свои дополнительные частицы или высвобождая энергию в других формах. Элементы, содержащие такие нестабильные ядра, называются радиоактивными.
Фермий, например, является радиоактивным элементом: его самый стабильный изотоп (Fm-257) имеет период полураспада 100,5 суток.
14. Видя атомы
Поскольку атомы невероятно малы по сравнению с длиной волны видимого света, их нельзя наблюдать даже с самым мощным в мире оптическим микроскопом.
Сканирующий туннельный микроскоп захватывает атомы кремния на поверхности кристаллического карбида кремния
Вот почему ученые используют микроскоп другого типа, известный как сканирующий туннельный микроскоп. Он может обеспечить боковое разрешение 0,1 нм и разрешение по глубине 0,01 нм, что достаточно для изображения отдельных атомов в материалах.
15. Квантовая природа атомных свойств
Поскольку атомы чрезвычайно малы по размеру, они проявляют квантовые свойства, поэтому предсказание их поведения с применением классической физики всегда приведет к неверным результатам.
Когда электрон прыгает с одного энергетического уровня (орбиты) на другой, он не перемещается в пространстве между ними. Вместо этого он исчезает с одной орбиты, а затем сразу же появляется на другой орбите.
Чтобы лучше описать и оценить их поведение, несколько атомных моделей включили в себя законы квантовой физики.