чпс что это в медицине
Чреспищеводное электрофизиологическое исследование сердца (ЧПЭФИ)
2-е кардиологическое отделение
Электрофизиологическое исследование (ЭФИ) сердца — это метод диагностики нарушений ритма и проводимости сердца. Во время исследования производится стимуляция различных отделов сердца для выявления возможных нарушений ритма. Главным преимуществом ЭФИ перед электрокардиографией или суточным мониторированием ЭКГ является возможность выявления нарушений ритма и проводимости, которые невозможно было обнаружить первыми двумя способами.
При ЭФИ нагрузка на сердце тоже возрастает, но не вследствие физической активности, а в результате электрической стимуляции миокарда. Такая стимуляция проводится с помощью электродов, которые начинают подавать к сердечной мышце электротоки физиологической мощности, но с высокой частотой. В итоге миокард сокращается быстрее, возникает спровоцированное учащение сердцебиения. А при высокой частоте сердечных сокращений возникают либо аритмия, либо ишемия, если у человека уже имеются патологические процессы в миокарде, являющиеся предпосылками к развитию этих заболеваний. Другими словами, ЭФИ позволяет спровоцировать искомые заболевания и зарегистрировать их на ЭКГ с целью дальнейшего лечения пациента
Существует два вида электрофизиологического исследования сердца: инвазивное (эндокардиальное, эпикардиальное, комбинированное) и неинвазивное (ЧПЭФИ).
Чреспищеводное ЭФИ (ЧПЭФИ). Электроды подводятся с помощью зонда, вводимого в просвет пищевода. Является неинвазивной методикой, а по технике напоминает обычную фиброгастроскопию.
ЧПЭФИ проводится чаще, так как имеет наименьшее число осложнений и побочных эффектов, если сравнивать с инвазивными методами.
Чреспищеводное электрофизиологическое исследование сердца осуществляется по следующим показаниям:
Чреспищеводная эхокардиография
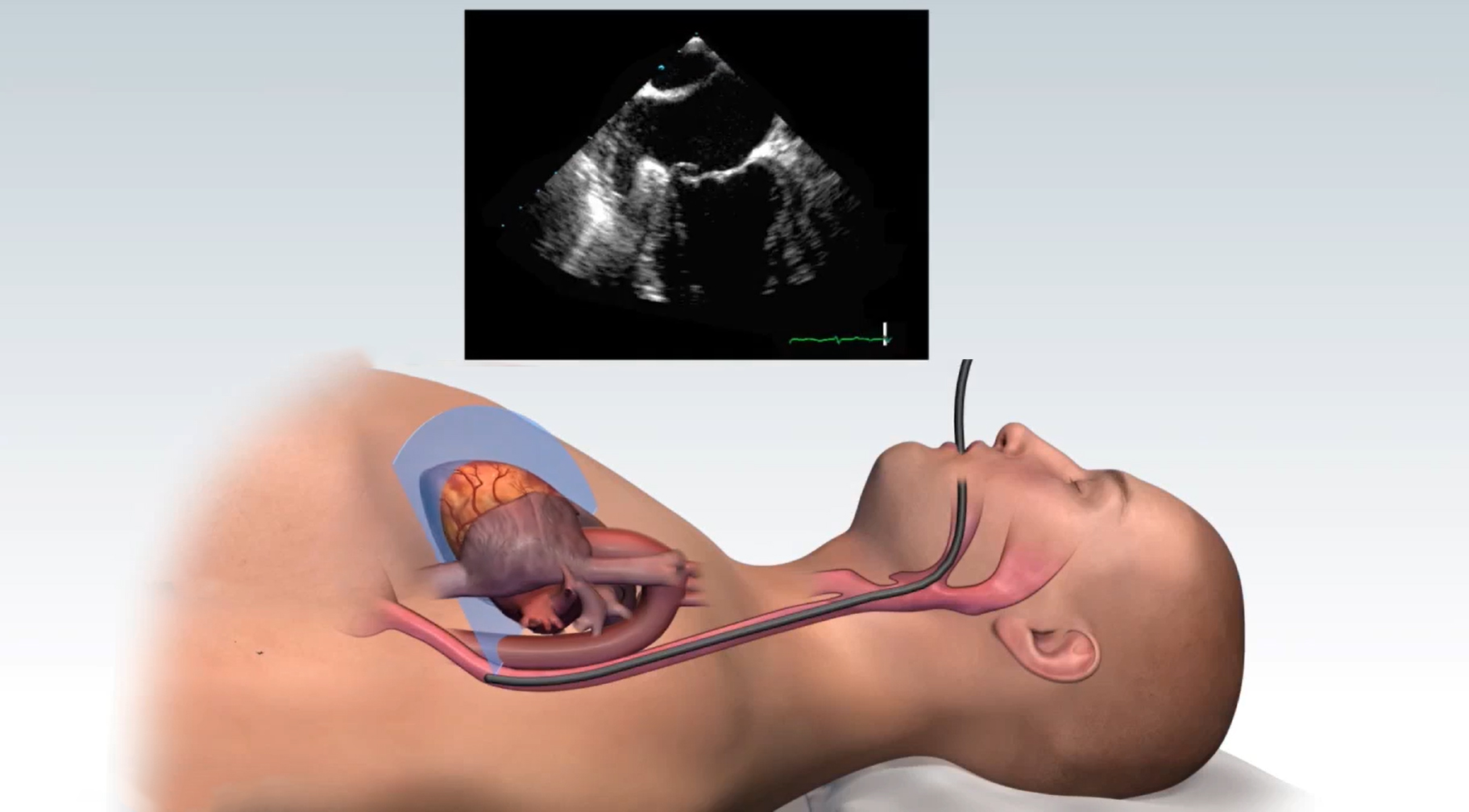
Чреспищеводная эхокардиография (ЧЭ или ЧпЭхоКГ) позволяет с помощью высокочастотных звуковых волн (ультразвука) получить подробные изображения вашего сердца. Эхопреобразователь, излучающий звуковые волны, прикреплен к тонкой трубке (толщина варьируется от 9 до 11 мм), которая проходит через рот, спускается по горлу и в пищевод. Поскольку пищевод находится близко к верхним камерам сердца, можно получить очень четкие изображения этих структур и клапанов сердца.
Почему проводят чреспищеводную эхокардиографию?
Врачи используют ЧЭ, чтобы найти проблемы в структуре и функциях сердца. ЧЭ может дать более четкие изображения верхних камер сердца и клапанов между верхней и нижней камерами сердца, чем стандартные эхокардиограммы.
Подробные изображения, предоставленные ЧЭ, могут помочь врачам увидеть:
Чреспищеводную эхокардиографию часто используют для получения информации во время хирургических операций по восстановлению сердечных клапанов, разрывов аорты или врожденных пороков сердца. Также используется во время хирургического лечения эндокардита, бактериальной инфекции внутренней оболочки сердца и клапанов.
Осмотр (консультация) врача функциональной диагностики
Эхокардиография чреспищеводная
Каковы риски ЧЭ?
Какие есть противопоказания?
Как подготовиться к ЧЭ?
Проконсультируйтесь со своим врачом. Вас могут попросить не употреблять алкогольные напитки в течение нескольких дней, а также ничего не есть и не пить как минимум за 4-6 часов до исследования. Потребление воды допускается не позднее, чем за 2 часа до сеанса.
Что происходит во время ЧЭ?
Чреспищеводную эхокардиографию выполняют специально обученные врачи. Процедура обычно проводится в больнице или клинике и длится от 30 до 60 минут.
Врача необходимо предупредить о любых проблемах, связанных с ротовой полостью, а также сообщить ему о наличии патологий пищеварительной системы, рассказать об аллергии на лекарственные средства.
Что происходит после ЧЭ?
Ваше горло может онеметь на короткое время. Не ешьте и не пейте ничего, пока не пройдет чувство онемения – вы можете подавиться.
На что мне обратить внимание?
Если боль в горле усиливается или не проходит через несколько дней, обратитесь к врачу.
Как я могу узнать больше о ЧЭ?
Поговорите со своим врачом. Вот несколько хороших вопросов:
Чреспищеводная электрокардиостимуляция
Чреспищеводная электрокардиостимуляция – неинвазивная процедура, направленная на получение записи биологических потенциалов с внешней поверхности сердца, используя при этом специальный пищеводный электроды и регистрационную аппаратуру.
Проведение специальных видов стимуляции для изучения электрофизиологических свойств проводящей системы, миокарда предсердий и желудочков. Выявление субстратов аритмии, их локализации и электрофизиологических характеристик. Контроль лекарственной и/или нефармакологической терапии.
Ненвазивное электрофизиологическое исследование сердца (ЧПЭФИ)
Опыт применения ЧПЭС в кардиологии насчитывает более 30 лет.
В нашей стране первое сообщение о применении ЧПЭС у больных с ишемической болезнью сердца появилось в научной медицинской литературе более 10 лет назад.
За этот период времени отношение к любому методу исследования уже носит устойчивый характер, а возможности самого метода хорошо изучены.
Следует сказать, что отношение кардиологов к методу ЧПЭС в течение этого времени менялось в зависимости от развития самой кардиологии и технических возможностей применяемых стимуляторов.
Повышенный интерес к этому методу в настоящее время обусловлен с одной стороны, бурным развитием самой кардиологии, как науки, в частности ее аритмологии, а также появлением современных стимуляторов с хорошими техническими характеристиками, позволяющими производить исследование с минимальными неприятными ощущениями для больного.
Применение ЧПЭФИ помогает решить три основные задачи: диагностика, лечение (терапевтическое, подбор антиаритмических препаратов) и прогнозирование во многих клинических ситуациях.
Скачать руководство по ЧПЭС. «Основы клинической чреспищеводной электростимуляции сердца» А.Н.Толстов
Скачать руководство по ЧПЭС. » Неинвазивное электрофизиологическое исследование при аномалиях проводящей системы сердца» Ю.В.Шубик
Область применения ЧПЭС в кардиологии
У больных ишемической болезнью сердца:
1) диагностика коронарной недостаточности;
2) определение степени (функционального класса) коронарной недостаточности,
3) диагностика безболевой ишемии миокарда;
4) выделение группы больных с ишемической болезнью сердца (ИБС), имеющих высокий риск внезапной сердечной смерти;
5) подбор оптимальной эффективной дозы антиангинального препарата и наиболее рационального приема его в течение суток;
6) выделение группы больных, которым наиболее целесообразно проведение коронароангиографии и последующего оперативного лечения ИБС;
7) верификация крупноочаговых рубцовых изменений миокарда у больных с синдромом WPW;
8) одновременная регистрация эхокардиограммы по программе стресс ЭхоКГ при проведении дозированной частотной нагрузки при ЧПЭС позволяет диагности¬ровать скрытые формы коронарной и миокардиальной недостаточности.
У больных с нарушениями ритма сердца:
1) оценка функции синусового узла:
— диагностика синдрома слабости синусового узла (СССУ);
— диагностика функциональной дисфункции синусового узла (чаще всего связанной с повышенной активностью п.Vagus)
— оценка функционального состояния миокарда перед установкой постоянного эндокардиального кардиостимулятора;
2) оценка функции атриовентрикулярного (AB) узла;
3) дифференциальная диагностика пароксизмальных суправентрикулярных тахиаритмий с помощью метода провокации тахиаритмий и последующей регистрацией пищеводной электрограммы (ПЭ);
4) диагностика и изучение электрофизиологических свойств дополнительных, аномальных путей проведения (пучок Кента и пучок Джеймса);
— диагностика синдрома преждевременного возбуждения желудочков в случае функционирования п. Кента или п. Джеймса;
— диагностика пароксизмальных тахиаритмий при синдроме Вольфа-Паркинсона-Уайта (ВПУ) или Клерка-Леви-Кристеску (CLC), Лауна-Ганонга-Левина (LGL);
— выделение группы больных синдромом ВПУ и мерцательной аритмии угрожаемых по развитию фибрилляции желудочков;
5) подбор оптимальной эффективной дозы противоаритмического препарата:
— для купирования пароксизма тахиаритмии;
— для профилактики возникновения пароксизма тахиаритмии;
— выявление аритмогенного эффекта препарата;
6) купирование пароксизмальных суправентрикулярных тахиаритмий (кроме мерцательной аритмии);
7) поддержание необходимой частоты сердечного ритма (ЧСС) во время проведения операции в случае исходной брадикардии;
8] изучение электрофизиологических свойств суправентрикулярной зоны: предсердий, АВ-узла, дополнительных путей проведения (рефрактерные периоды структур);
9) регистрация тахизависимой экстрасистолии и внутрижелудочковых блокад;
ЧПЭС имеет широкий спектр применения от амбулаторно-поликлинических, до стационарных подразделений. Метод для клиницистов в их клинической деятельности наиболее доступен и менее обременителен для больного.
Диагностические возможности ЧпЭФИ ограничиваются стимуляцией левого предсердия. В ряде случаев, может быть достигнута стимуляция левого желудочка, но для этого необходимо подавать напряжение с амплитудой 30-60 В (мА), что практически невозможно без применения наркоза.
Применение ЧПЭС при нарушениях ритма сердца
Применение ЧПЭС при нарушениях ритма сердца было обосновано в результате быстрого развития аритмологии и исходя из ее проблем.
Применение ЧПЭС у этой категории больных решило многие проблемы суправентрикулярных аритмий и полноценно заменило собой такой метод исследования как внутрисердечное электрофизиологическое исследование (ЭФИ).
Поэтому, показания для ЭФИ в настоящее время сужены и могут быть определены следующими состояниями:
1 Уточнение диагноза и подбор терапии у бальных с желудочковыми тахикардиями.
2. Синкопальные состояния, неясной этиологии.
3. Перед проведением хирургического лечения аритмий.
4. Перед имплантацией кардиостимулятора или кардиовертера-дефибриллятора больным с тахиаритмиями.
5. Для проведения криодеструкции аномальных путей проведения в случае их правостороннего прохождения.
6. Больные с синдромом WPW и пароксизмальной мерцательной аритмией, протекающей с потерей сознания и угрозой трансформации в фибрилляцию желудочков.
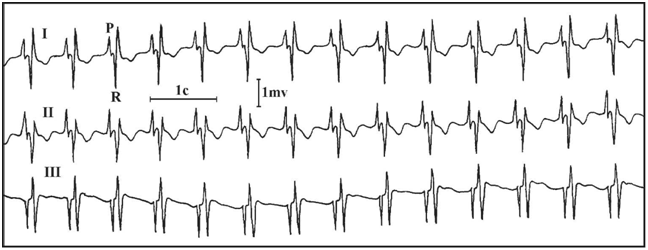
Рис. Чреспищеводная электрограмма, биполярная запись
Начиная исследование по программе нарушения ритма с помощью метода ЧПЭС, врач, проводящий его, должен быть уверен что все подготовлено на случай проведения реанимационных мероприятий: дефибриллятор подготовлен и включен, есть необходимый набор реанимационных лекарств и средств.
Кроме того, врач проводящий исследование, должен быть хорошо подготовлен по таким дисциплинам как клиническая кардиология с аритмологией, клиническая электрокардиография, знать электрофизиологию миокарда, вопросы неотложной кардиологии и реанимации.
ЧПЭС может проводится с диагностической и лечебной целью. В случае диагностического исследования должны отменяться все противоаритмические препараты.
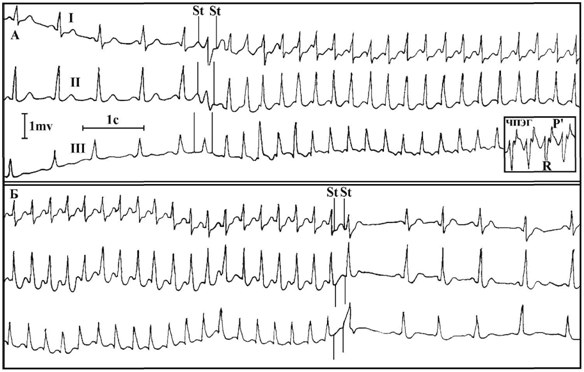
Рис.
А. Парной стимуляцией предсердий вызван пароксизм АВ реципрокной ортодромной тахикардии. RP’-интервал на ЧПЭГ меньше 1/2 RR-интервала и = 120 мс.
Б. Купирование пароксизма парной стимуляцией.
Оценка коронарного кровообращения методом ЧПЭС
Данная программа стимуляции является той основой с чего вообще начался метод ЧПЭС, как один из нагрузочных тестов (нагрузка ритмом) в кардиологии.
Применение программы стимуляции позволяет постепенно и дозированно увеличивать частоту сокращений желудочков с постоянной оценкой изменений конечной части желудочкового комплекса по монитору и при записи ЭКГ.
Применение ЧПЭС с целью оценки коронарного кровообращения позволяет кардиологу решать ряд важных задач:
1. устанавливать сам факт наличия у больного ишемической болезни сердца (ИБС) и ее форм, в частности, определять безболевую ишемию миокарда;
2. определять степень коронарной недостаточности;
3. определять оптимально эффективную дозу антиангинального препарата и кратность его приема;
4. выделять группу больных ИБС с тяжелой коронарной недостаточностью, которым настоятельно рекомендуется проведение коронароангиографии и возможным оперативным лечением ИБС;
5. определять прогноз и тактику ведения больных ИБС, после перенесенного инфаркта миокарда;
6. выделять группу больных ИБС, имеющих высокий риск внезапной сердечной смерти с целью проведения профилактического лечения;
7. проводить дифференциальную диагностику постинфарктного кардиосклероза у больных с синдромом Вольфа-Паркинсона-Уайта;
8. выявление скрытых форм нарушений ритма и проводимости;
9. при динамическом проведении ЧПЭС у одного и того же больного ИБС косвенно судить о скорости прогрессирования коронарного атеросклероза и эффективности проводимого лечения.
Кроме противопоказаний общего характера, проведение ЧПЭС по программе оценки коронарного кровообращения нецелесообразно в следующих случаях:
1. при наличии стойкой полной блокады левой ножки пучка Гиса;
2. при регистрации на ЭКГ-покоя явного (манифестирующего) синдрома преждевременного возбуждения желудочков, обусловленного функционированием пучка Кента;
3. у больного ИБС с 3 4 функциональным классом;
4. у больного с впервые возникшей стенокардией в течение первых 4-х недель и у больного с нестабильной стенокардией;
5. в течение первых 3-х недель неосложненного инфаркта миокарда;
6. при выраженной гипертрофии миокарда левого желудочка с вторичными изменениями конечной части желудочкового комплекса на ЭКГ.
ЧПЭС проводится по назначению лечащего врача через 2 часа после еды на фоне отмены коронароактивных препаратов в случае диагностического исследования. При этом необходимо согласие больного на проведение ЧПЭС, регистрация ЭКГ-покоя и эхокардиограммы (ЭхоКГ).
Программа стимуляции с целью оценки коронарного кровообращения довольно проста. После получения устойчивого ритма кардиостимулятора, превышающего собственную частоту ритма сердца на 20 имп./мин., проводят непрерывную ступенчатую стимуляцию. Длительность каждой ступени 1 минута.
При отсутствии изменений р конце ступени частоту стимуляции повышают на 10-20 имп./мин. до достижения максимальной частоты 160 имп/мин. По истечении каждой ступени стимуляции проводят оценку коронарного кровообращения по изменениям сегмента ST на ЭКГ.
Если после достижения максимальной частоты (160 имп./мин.) ишемических изменений на ЭКГ не наблюдается, то время стимуляции продлевается до 2 минут, после чего проводится окончательная оценка проведенного исследования. Считается нецелесообразным проводить оценку коронарного кровообращения при частоте стимуляции более 160 имп./мин., т.к. при этом значительно возрастает количество ложноположительных результатов, что отчасти связано с так называемым постдеполяризационным синдромом.
Постдеполяризационный синдром выражается в возникновении на ЭКГ депрессии сегмента ST и инверсии зубца «Т» после прекращения высокой частоты желудочков. Хорошо известно развитие этого синдрома после купирования пароксизма желудочковой тахикардии.
При отсутствии у больного верифицированной ИБС данный синдром свидетельствует о нарушениях процессов реполяризации желудочков не связанное с ухудшением коронарного кровообращения.
Осложнения при проведении ЧПЭС
Следует сразу оговориться, что пароксизмальные нарушения ритма, которые прежде рассматривались как осложнение метода ЧПЭС в настоящее время таковыми не являются.
Связано это с быстрым развитием аритмологии и изменением представлений. Однако, при этом необходимо иметь в виду, что врач, проводящий исследо¬вание, может столкнуться с двумя проблемами:
1. при проведении ЧПЭС врач сознательно пытается спровоцировать пароксизм суправентрикулярной тахиаритмии, используя различные режимы стимуляции, т. е. индукция тахикардии является целью самого исследования. Вряд ли эту ситуацию следует рассматривать как осложнение метода;
2. при проведении ЧПЭС, индукция тахикардии является неожиданностью для врача, проводящего исследование и возникает впервые в жизни больного. Пароксизм тахикардии может возникнуть при использовании любого режима стимуляции. В данной ситуации вопрос решается не однозначно, а в зависимости от конкретной формы пароксизма.
Сам факт возможности провокации тахикардии говорит о том, что в сердце больного сформировались все необходимые предпосылки для реализации механизма повторного входа и нужен лишь пусковой механизм для возникновения тахикардии.
Следует учитывать и конкретную форму спровоцированного пароксизма, исходя из сложности лечения и возможных осложнений данного пароксизма. Так, пароксизм узловой АВ-тахикардии или пароксизм реципрокной АВ-тахикардии у больного с синдромом WPW (ортодромный или антидромный вариант) достаточно легко купируются С помощью метода ЧПЭС и как правило не требуют внутривенного введения лекарств (не надо забывать и о возможности купировать данные пароксизмы с помощью вагусных проб).
Индукция впервые в жизни больного пароксизма мерцательной аритмии требует в дальнейшем применения лекарственных препаратов для ее купирования, т. к. метод ЧПЭС не купирует мерцательную аритмию.
Провокация у больного впервые в жизни мерцательной аритмии зачастую свидетельствует либо о критической дилатации предсердий, либо о выраженных дистрофических изменениях в миокарде предсердий [после перенесенного миокардита или хронической алкогольной интоксикации) после чего сохранение синусового ритма становится сложновыполнимой задачей.
1. Введение пищеводного электрода в трахею, вместо пищевода.
Это осложнение обычно случается у врачей, которые только начинают самостоятельно проводить исследование ЧПЭС и связано как правило с их торопливостью при введении зонда в пищевод. Это осложнение крайне редко возникает при неторопливом введении зонда в момент проглатывания слюны, когда происходит подъем надгортанника и закрытие трахеи.
Для избежания подобных случаев необходимо обращать внимание на крайне низкую амплитуду зубца «Р» на пищеводной электрограмме в начале исследования, а также появление кашля при включении стимуляции.
2. Ощущение жжения в области пищевода, за грудиной.
Появление этих ощущений обязательно при включении стимуляции, а их отсутствие у больного должно быть связано с неисправностью аппаратуры. Степень ощущений больного обычно невысокая или легко переносимая. При выраженных ощущениях и отказе больного от исследования, исследование прекращают.
3. При проведении стимуляции больной ощущает боли в области спины, связанные С сокращением позвоночных мышц. При выраженных болях исследование прекращают.
4. При включении стимулятора происходит эффективная стимуляция диафрагмы, что сопровождается ритмичными ее сокращениями с той частотой, которую в данный момент времени дает стимулятор. Больной при этом ощущает частую икоту или одышку, а врач, проводящий исследование наблюдает частое сокращение диафрагмы, которое исчезает сразу же после выключения стимулятора.
Наиболее часто это осложнение встречается у больных гиперстенического телосложения или с ожирением, т. к, расположение сердца в грудной клетке у таких больных таково, что сердце практически лежит на высоко расположенной диафрагме и полюса пищеводного электрода при ЧПЭС расположены в непосредственной близости не только к предсердиям, но и к диафрагме. Как правило, исследование при появлении этого осложнения прекращается.
Противопоказания к проведению ЧПЭС
1) постоянная форма мерцательной аритмии;
2) АВ-блокада 2-3 степени;
3) пороки сердца с выраженным нарушением внутрисердечной (по данным ЭхоКГ) и центральной гемодинамики (клиническая картина сердечной недостаточности выше 2 стадии или выше 2-го функционального класса);
4) дилатация полостей сердца;
5) аневризма сердца;
6) острая стадия любого заболевания (кроме пароксизма суправентрикулярной тахикардии и трепетания предсердий);
7) заболевания пищевода: опухоль, дивертикулез, стриктуры, ахалазия, эзофагит в стадии обострения, варикозное расширение вен;
8) артериальная гипертензия выше 220/120 мм.рт.ст. вне криза и обострения;
9) опухоли сердца (миксомы);
10) перикардит.
Кроме того, проведение ЧПЭС по программе ИБС нецелесообразно в следующих случаях:
1) при наличии стойкой полной блокады левой ножки пучка Гиса;
2) при регистрации явного [манифестирующего] синдрома WPW;
3) при нестабильной стенокардии в течение 4-х недель с момента установления диагноза;
4) в течение первых 3-х недель неосложненного инфаркта миокарда;
5) при стенокардии напряжения 3-4 функционального класса;
6) при выраженной гипертрофии миокарда левого желудочка с вторичными изменениями конечной части комплекса QRS-T на ЭКГ
Сервер медицинского оборудования МедКом
Партнеры
На форуме
Меню раздела
Партнеры
Чрезпищеводная электростимуляция
Суть метода, техника проведения, используемое оборудование.
Значение методов электрокардиостимуляции в диагностике и лечении нарушений ритма сердца в настоящее время не вызывает сомнений. Наравне с такими
методами, как-велоэргометрия, стресс-эхокардиография, радиоизотопные методики, фармакологические пробы, метод электрокардиостимуляции имеет
большое значение в диагностике ИБС.
Значение методов электрокардиостимуляции в диагностике и лечении нарушений ритма сердца в настоящее время не вызывает сомнений. Наравне с такими
методами, как-велоэргометрия, стресс-эхокардиография, радиоизотопные методики, фармакологические пробы, метод электрокардиостимуляции имеет
большое значение в диагностике ИБС. Однако методы эндокардиальной электрокардиостимуляции, как наиболее информативные в диагностике и эффективные в лечении, являются инвазивными, чреваты осложнениями, требуют специально оборудованного кабинета или операционной, могут выполняться лишь в специализированных отделениях стационара при наличии дорогостоящей аппаратуры.
Показания для проведения чреспищеводной электростимуляции сердца
1. Подозрение на синдром слабости синусового узла (СССУ), с целью верификации диагноза и выбора тактики лечения.
2. Часто рецидивирующие пароксизмы суправентрикулярных тахикардий, с целью определения их вида и выбора адекватного профилактического лечения.
3. Подозрение на латентный или скрытый синдром Вольфа-Паркинсона-Уайта (ВПУ), с целью верификации диагноза, оценки участия дополнительных путей
проведения в развитии пароксизмов тахикардии и выбора тактики лечения.
4. Подозрение на скрытую коронарную недостаточность, с целью верификации диагноза, при невозможности выполнить другие методики диагностики ИБС.
5. Купирование пароксизмов суправентрикулярных тахикардий.
Противопоказания к проведению чреспищеводной электростимуляции сердца
1. Острый или подострый инфаркт миокарда.
2. Нестабильная стенокардия.
4. Заболевания пищевода и носоглотки.
5. Наличие в анамнезе острой недостаточности кровообращения во время приступов тахикардии.
6. Наличие в анамнезе фибрилляции желудочков.
7. Наличие в анамнезе тромбоэмболических осложнений.
При диагностической ЧПЭС выделяют следующие этапы :
1. Установка пищеводного электрода;
2. Определение порога стимуляции;
3. Подача на электрод стимулирующих импульсов по определенному протоколу;
4. Отбор, оценка и анализ информативных фрагментов ЭКГ;
5. Формирование архива пациентов, которым была выполнена ЧПЭС
.
В клиниках используются несколько моделей отечественных и зарубежных чреспищеводных кардиостимуляторов, модификации эндокардиальных
кардиостимуляторов и трансторакальные стимуляторы. В нашей клинике используется автоматизированный комплекс “ЭЛКАРТ-ЧПС” (“Электропульс”, Томск).
Для проведения чреспищеводной электростимуляции сердца необходимо иметь:
1. автоматизированный комплекс “ЭЛКАРТ-ЧПС”;
2. пищеводные электроды;
3. аппарат для измерения артериального давления;
5. аппарат для проведения искусственного дыхания;
6. стерильные шприцы, иглы, системы для внутривенного вливания;
7. комплект медикаментов:
1. обзидан, анаприлин, финоптин (изоптин), этмозин, этацизин, новокаинамид, кордарон, ритмилен, хинидин, кинилентин, лидокаин и другие доступные
антиаритмические препараты;
4. атропин в ампулах;
5. седуксен (реланиум) в ампулах;
6. адреналин, норадреналин, мезатон в ампулах;
7. стерильный изотонический раствор натрия хлорида.
Непосредственно перед исследованием, при выраженном рвотном рефлексе, желательно проведение анестезии корня языка и задней стенки глотки раствором 10% новокаина или 0,5% раствора дикаина (не более 3 мл). Регистрируется исходная ЭКГ во всех отведениях и артериальное давление (АД),
затем вводят электрод и приступают к проведению ЧПЭС.
Электрод должен быть простерилизован. Существует 2 способа введения электрода: через нос и через рот. Предпочтительнее первый, но для него необходим достаточно тонкий электрод (диаметром не более 3-4 мм) и свободная проходимость носовых ходов.
Предсердный потенциал (зубец Р, потенциал А) на пищеводной ЭГ, как правило, положительный и остроконечный, в то время как комплекс QRS обычно имеет форму QS, а зубец Т отрицателен.
Оптимальным считается положение электрода, когда с одного из его полюсов регистрируется потенциал предсердий максимальной величины. Поэтому, если
после введения электрода на расчетную глубину ни с одного из его полюсов не регистрируется потенциал предсердий величиной менее 1/5 величины желудочкового комплекса, электрод необходимо подтянуть наружу, непрерывно регистрируя при этом пищеводную ЭКГ. Продвижение или подтягивание
электрода продолжают до тех пор, пока не будет зарегистрирован потенциал предсердий, величина которого составляет примерно 1/3 величины потенциала
желудочков. При необходимости проведения чреспищеводной желудочковой стимуляции электрод от точки максимальной величины А продвигают вглубь еще на
4-6 см, при этом на пищеводной электрограмме величина комплекса QRS в норме должна превышать величину потенциала А в 5-6 раз. После этого проводят
пробную электрокардиостимуляцию и при ее устойчивости (когда каждый электростимул вызывает появление зубца Р или комплекса QRS) фиксируют электрод во избежание его смещения. Необходимо иметь в виду, что при регистрации пищеводной ЭКГ изолиния на кардиографе “плавает” из-за непроизвольного сокращения стенок пищевода. Поэтому необходимо перед регистрацией ЭКГ выждать какое-то время для того, чтобы пищевод “привык” к нахождению в нем инородного тела и проводить регистрацию ЭКГ на задержке дыхания.
Для диагностики СССУ достаточно регистрации наружной ЭКГ в любом отведении, где четко виден зубец Р. Для диагностики формы пароксизмальной тахикардии или синдрома ВПУ необходима регистрация ЭКГ в отведениях V 1-6 или I-III. Во время спонтанного или индуцированного пароксизма тахикардии обязательна регистрация по крайней мере двух отведений ЭКГ: пищеводного и наружного. Для диагностики коронарной недостаточности необходима регистрация ЭКГ во всех 12 стандартных и дополнительных отведениях.
Перед началом какой-либо из программ ЧПЭС необходимо провести пробную стимуляцию сердца. Для этого на шкале электрокардиостимулятора устанавливают частоту стимуляции, превышающую частоту спонтанного ритма на 10-15%, затем включают электрокардиостимулятор и плавно увеличивают амплитуду стимулов до тех пор, пока в ответ на каждый стимул на ЭКГ не будет регистрироваться зубец Р и комплекс QRS (для предсердной стимуляции) или только комплекс QRS (для желудочковой).
Требования к выполнению чреспищеводной электростимуляции сердца ЧПЭС должны выполнять врачи, прошедшие специализацию по вопросам электрокардиостимуляции, владеющие методикой интерпретации ЭКГ и реанимационных мероприятий. Необходимо тщательно ознакомиться с анамнезом и клиническим течением заболевания, составить четкий план и цель исследования,
предварительно наметить возможные способы купирования пароксизмов тахи- или брадикардий, приступов стенокардии, гипотонии или коллапса.
При выполнении чреспищеводной электростимуляции сердца врач должен:
1. проводить постоянную оценку ЭКГ
2. проводить постоянную клиническую оценку состояния больного
3. периодически или постоянно (при тяжелом состоянии больного) измерять артериальное давление.
В связи с тем, что нередко синусовая брадикардия или аритмия могут быть обусловлены вегетативными влияниями на синусовый узел, в настоящее время
принято верифицировать диагноз СССУ после медикаментозной “денервации” синусового узла, которую осуществляют:
1. Вначале медленным введением внутривенно 0,025 мг/кг 1% р-ра атропина. После его внутривенного введения должно отмечаться адекватное (в 1,5
раза) увеличение частоты сердечных сокращений.
2. Затем медленно вводят внутривенно 0,2 мг/кг обзидана (лучше в разведении на изотоническом растворе хлорида натрия).
Через 3-5 мин после окончания введения препаратов регистрируют ЭКГ, рассчитывают полученную частоту синусового ритма и сравнивают ее с расчетной
должной частотой сердечных сокращений (ЧСС).
Если после введения препаратов ЧСС меньше должной расчетной, есть основания думать о СССУ. Однако окончательно диагноз СССУ подтверждается после
проведения ЧПЭС на фоне “денервации” синусового узла; при этом ЧПЭС проводят с такими же частотами и такой же длительностью каждого этапа, что и
на безмедикаментозном фоне, вплоть до развития периодики Венкебаха.
В случаях, когда ВВФСУ м КВВФСУ после проведения внутривенного вливания атропина и обзидана на одном из этапов ЧПЭС превышают соответственно 1600
мс и 525 мс, диагноз СССУ считается подтвержденным.
Необходимо иметь в виду, что у некоторых больных ВВФСУ может превышать 5 и более секунд, поэтому во избежание приступов потери сознания необходимо следить за длительностью постстимуляционной паузы и быть постоянно готовым к проведению ЧПЭС. В редких случаях приходится проводить учащающую ЧПЭС относительно долгое время с постоянно уменьшающейся частотой до восстановления достаточно частого синусового ритма.
Учитывая, что СССУ может сочетаться с пароксизмами тахикардии (синдром бради-тахи), а также для решения вопроса о тактике лечения необходимо провести попытку провоцирования пароксизма тахикардии одним из способов ЭКС, описанных ниже. При подтвержденном диагнозе СССУ, для решения вопроса
о месте имплантации эндокардиального электрода проводят желудочковую ЧПЭС с регистрацией пищеводной ЭКГ с целью документации наличия или отсутствия ретроградного желудочково-предсердного проведения возбуждения по нижеописанной методике.
Если же значение ВВФСУ и КВВФСУ лишь немного превышает норму, это может являться формальным подтверждением дисфункции синусового узла, но не позволяет сделать более определенные выводы и тем более решить вопрос о необходимости имплантации искусственного водителя ритма.
Критерии диагностики атриовентрикулярной реципрокной пароксизмальной тахикардии у больных с манифестирующим синдромом WPW
1. Явно функционирующие дополнительные пути проявляются на ЭКГ признаками синдрома ВПУ и выявляются обычно во время диагностической предсердной
стимуляции.
2. С увеличением частоты предсердной стимуляции комплексы QRS расширяются и приобретают типичную для синдрома ВПУ форму с дельта-волной. При этом часто, но необязательно, встречается укорочение интервала P-Q.
3. Интервал VA при тахикардии равен 150мс.
Критерии наличия латентных дополнительных путей проведения в антеградном направлении
1. Латентно функционирующие дополнительные пути не проявляются на ЭКГ признаками синдрома ВПУ и выявляются обычно во время диагностической
предсердной стимуляции.
2. С увеличением частоты предсердной стимуляции комплексы QRS расширяются (>100 мс) и приобретают типичную для синдрома ВПУ форму с дельта-волной. При этом часто, но необязательно, встречается укорочение интервала P-Q.
3. Во время проведения программированной стимуляции предсердий с уменьшением задержки экстрастимула комплекс QRS после экстрастимула приобретает форму, типичную для синдрома ВПУ.
4. Расположения интервала VA при тахикардии: VA>AV.
5. Интервал RP превышает Ѕ интервала RR.
6. Если ЧПЭС провоцирует пароксизм тахикардии, форма комплекса QRS широкая и имеется выраженная дельта-волна, такая тахикардия носит название антидромной. По ЭКГ такая форма тахикардии напоминает желудочковую, но при регистрации пищеводной ЭКГ перед каждым комплексом QRS выявляется предсердный потенциал.
Для выявления возможной частоты предсердно-желудочковой проводимости существует 2 способа. Первый из них заключается в проведении предсердной
стимуляции с возрастающей частотой до тех пор, пока в ответ на стимул на ЭКГ не будут регистрироваться комплексы QRS без дельта-волны. Если же, при достижении частоты стимуляции в 250 имп/мин не наступила блокада проведения по ДПП, искусственно вызывается фибрилляция предсердий. Для этого проводят сверхчастую ЧПЭС с частотой 300-500 (иногда 800-1000) импульсов в мин. При этом определяется самый короткий интервал между двумя комплексами QRS, имеющими дельта-волну, который и принимается за частоту пропускания импульсов. Если в результате стимуляции развивается трепетание предсердий или мерцательная аритмия, необходимо провести попытку устранения трепетания предсердий (см.ниже) сверхчастой ЧПЭС, а мерцание предсердий внутривенным введением антиаритмических препаратов либо кардиоверсией.
Необходимо помнить, что при коротком рефрактерном периоде ДПП проведение залповой или сверхчастой ЧПЭС противопоказано, т.к. может развиться фибрилляция желудочков.
Критерии диагностики скрытых дополнительных путей проведения, функционирующих в ретроградном направлении. На обычной ЭКГ и по данным диагностической предсердной стимуляции признаков синдрома ВПУ не выявляется, поэтому диагностические критерии скрытых дополнительных путей следующие:
1. Постоянство интервала желудочково-предсердного проведения (далее интервал Q-P) при стимуляции желудочков с возрастающей частотой. Условием для оценки ретроградного желудочково-предсердного проведения является наличие пищеводного электрода, позволяющего проводить одновременно ЧПЭС желудочков и регистрировать потенциал предсердий пищеводной ЭКГ. При ЧПЭС принято измерять длительность интервала Q-P от артефакта электростимула до начала предсердного отклонения на пищеводной ЭКГ.
2. Постоянство интервала Q-P при проведении программированной стимуляции желудочков с уменьшающейся задержкой экстрастимула.
3. Интервал Q-P во время спонтанного или спровоцированного пароксизма тахикардии обычно равен 60 мс.
4. Нет парадоксального более чем на 50% удлинения интервала Q-P в ответ на предсердный экстрастимул, при программированной стимуляции предсердий с уменьшающейся задержкой.
5. Обычно интервал Q-P при проведении желудочковой стимуляции равен интервалу Q-P во время тахикардии.
6. Ширина комплексов QRS при тахикардии 100 мс 100 мс
Расположение интервала VA при тахикардия VA=0 VAAV VA=AV
Постоянство интервала VA при учащающей или программированной ЧПЭС желудочков Нет Да Да, VA может не быть, нет Нет, VA может не быть
Резкое удлинение интервала PQ перед началом тахикардии (при программированной предсердной ЧПЭС) Да Нет, может быть Отличительный признак от желудочковой тахикардии – наличие предсердного потенциала перед началом QRS на пищеводной ЭГ Нет
Методика индуцирования пароксизмов тахикардии и оценки эффективности антиаритмического лечения
Самым простым и быстрым способом провоцирования пароксизма тахикардии является нанесение на предсердие залпа (10-15 имп) электрических импульсов
с частотой 200-400 в мин или проведение ЧПЭС с частотой 400-600 (иногда до 1200) имп/мин в течение 1-10 секунд (сверхчастая ЧПЭС). Таким же способом можно купировать вызванный пароксизм, однако при данном способе остаются неуточненными многие моменты электрофизиологии сердца, не позволяющие провести дифференциальную диагностику формы тахикардии и оценить перспективы медикаментозного лечения, поэтому в настоящее время
применяется ниже описываемая методика.
Рекомендуется начинать предсердную стимуляцию с возрастающей частотой до развития периодики Венкебаха. На каждой частоте стимуляции, длительность
которой, за исключением случаев подозрения на СССУ, составляет 10-15 секунд, регистрируют ЭКГ на фоне ЧПЭС и после ее отключения. При этом обращают внимание на ВВФСУ, КВВФСУ, ширину и форму комплекса QRS, длительность интервала P-Q, частоту стимуляции, при которой возникает периодика
Венкебаха. При проведении учащающей ЧПЭС возможно развитие пароксизма тахикардии, во время которого необходимо одновременно регистрировать
пищеводную и наружную ЭКГ с целью дифференциальной диагностики формы тахикардии.
Приступ тахикардии, за исключением трепетания предсердий, обычно легко купируется одним из способов ЧПЭС. После завершения этапа учащающей
проводят программированную стимуляцию предсердий.
Аналогично проводится программированная стимуляция желудочков, при которой, наряду с определением их ЭРП и возможностью провоцирования тахикардии, определяется наличие или отсутствие ретроградного желудочково-предсердного проведения, т.е. проведения желудочкового возбуждения через АВ узел или ДПП.
ЭКГ необходимо записывать при каждой новой задержке экстрастимула таким образом, чтобы зарегистрировать 2-3 навязанных комплекса базового ритма,
комплексы Р и QRS в ответ на экстрастимул и 3-4 спонтанных сокращения сердца после прекращения ЧПЭС.
Как правило, во время программированной ЧПЭС неоднократно провоцируются пароксизмы тахикардии, при которых необходимо зарегистрировать наружное и
пищеводное отведения ЭКГ, а затем купировать их ЧПЭС.
У некоторых пациентов программированной ЧПЭС вызвать пароксизм тахикардии не удается. В таких случаях необходимо на фоне базовой навязанной частоты после 8-го стимула наносить не один, а 2-3 экстрастимула с постепенно уменьшающейся задержкой как между ними, так и между первым экстрастимулом и последним (8-м) стимулом базовой частоты.
Завершив программу диагностической ЧПЭС, приступают к оценке эффективности профилактической антиаритмической терапии.
Вначале выполняется на “чистом фоне”, то есть без приема антиаритмических препаратов, контрольное исследование. Спустя 48 ч после отмены всех антиаритмических препаратов (за исключением амиодарона и сердечных гликозидов, период отмены которых составляет 10-14 суток) оценивается
возможность провокации наджелудочковой пароксизмальной тахикардии с помощью ЧПЭС предсердий. Если эта попытка удается, то на основании изложенных
ранее критериев устанавливается конкретная электрофизиологическая форма тахикардии и больные могут быть включены в программу серийного тестирования антиаритмических препаратов в условиях ЧПЭС. Повторную попытку провокации пароксизмальной тахикардии с помощью установленного ранее режима ЧПЭС предсердий предпринимают не ранее чем на 3-5-й день от начала приема антиаритмического препарата в средних терапевтических дозах; для амиодарона этот срок равен 10-14 дням. Выбор последовательности назначения антиаритмических препаратов зависит от анамнестических данных об
эффективности проводившейся ранее антиаритмической терапии, а также от электрофизиологических механизмов пароксизмальной тахикардии. Целесообразно назначать препараты перорально, т.к. это более, чем внутривенное введение, соответствует достоверности оценки именно профилактического лечения.
Повторную ЧПЭС проводят по той же программе, что и до назначения препарата. При этом оценивается изменение рефрактерных периодов предсердий, АВ
узла, желудочков, анте- и ретроградное проведение по ДПП, пропускную способность АВ узла и ДПП, изменение длительности “зоны тахикардии”,
возможность провоцирования тахикардии и частоту сердечных сокращений во время пароксизма.
Если пароксизмы тахикардии не провоцируются или они возникают и спонтанно прекращаются в течение 2-х минут, эффект антиаритмического препарата
считается хорошим, и он может быть назначен с профилактической целью. В противном случае надо оценивать влияние других антиаритмиков или их комбинаций до достижения вышеописанного эффекта. Следует учитывать, что новый антиаритмический препарат может быть назначен не ранее, чем окончится действие предыдущего. Иногда эффективное лечение может подбираться несколько дней.
Чреспищеводная электростимуляция у больных с желудочковыми пароксизмальными тахикардиями
Основной причиной, ограничивающей использование традиционной методики ЧПЭС для проведения электрической стимуляции желудочков сердца у больных,
находящихся в сознании, является выраженный, часто непереносимый дискомфорт во время процедуры, возникающий из-за сильных болевых ощущений, а также в связи с сокращениями грудных мышц диафрагмы и грудной клетки. Он обусловлен в первую очередь тем, что для стимуляции желудочков сердца через пищевод необходимо использовать электрические импульсы с амплитудой 30-50 В, а иногда 90 В (известно, что больные хорошо переносят чреспищеводную стимуляцию в диапазоне амплитуд от 10 до 20 В).
Для снижения амплитуды импульсов, использующихся для проведения неинвазивной стимуляции желудочков сердца, разработана новая оригинальная методика, позволяющая существенно снизить дискомфорт процедуры.
После введения в пищевод электрод продвигается в полость желудка, где под рентгеноскопическим контролем из него формируется петля таким образом,
чтобы стимулирующие полюса электрода находились в своде желудка и максимально прилегали к нижнему краю рентгеноскопической тени сердца. С накоплением опыта надобность в рентгеноскопическом контроле резко уменьшается. При использовании традиционной методики с расположением электрода в пищеводе средний порог стимуляции желудочков сердца был высоким, составляя в среднем 37,5±3,5 В, а стимуляция плохо переносилась больными. В то же время методика электрической стимуляции сердца из желудка позволили снизить средний порог стимуляции до 21,6±3,9 В, что переносилось больными так же, как ЧПЭС предсердий.
Таким образом, методика неинвазивной электрической стимуляции желудочков сердца при локализации стимулирующего электрода в своде желудка позволяет существенно уменьшить дискомфорт процедуры, значительно снизить амплитуду импульсов и повысить ее переносимость. Она позволяет получить достоверную информацию о функциональном состоянии миокарда желудочков сердца, а у ряда больных с рецидивирующими пароксизмами устойчивой желудочковой тахикардии дает возможность индуцировать и купировать приступы желудочковой тахикардии. Это создает предпосылки для использования этого неинвазивного метода при подборе медикаментозной антиаритмической терапии больным с рецидивирующими реципрокными желудочковыми тахикардиями с помощью серийного тестирования антиаритмических препаратов.
Методика проведения чреспищеводной электростимуляции сердца для диагностики скрытой коронарной недостаточности
Предсердную стимуляцию начинают с частоты, превышающей частоту спонтанного синусового ритма на 15-20%, и увеличивают ее каждый раз на 10 имп/мин
до достижения субмаксимальной для данного возраста частоты стимуляции. Длительность ЧПЭС на каждой частоте составляет 3 мин, а перерыв между ЧПЭС
с разными частотами 3-5 мин. ЭКГ записывают ежеминутно и в момент отключения стимуляции; при этом надо зарегистрировать 4-5 навязанных комплексов и 7-10 комплексов QRS после прекращения ЧПЭС.
Иногда у больных с очень большими подозрениями на ИБС при отсутствии стенокардии и изменений на ЭКГ ишемического типа проводят ЧПЭС по вышеописанной программе с частотой 150-160 имп/мин в течение 8-10 мин. Также ежеминутно регистрируют ЭКГ и при выявлении признаков ИБС ЧПЭС прекращают.
Критерии ИБС при ЧПЭС такие же, как и при выполнении пробы с дозированной физической нагрузкой:
1. Появления типичных приступов стенокардии
2. Ишемические изменения сегмента ST
В то же время при ЧПЭС в самом ее начале чаще могут выявляться изменения сегмента ST, но они не должны рассматриваться как патологические, если при продолжающейся стимуляции проходят. Наоборот, усугубление ишемических изменений ЭКГ на 2-й и более минутах ЧПЭС расценивается как положительный результат.
Следует иметь в виду, что при наличии изменений сегмента ST на исходной ЭКГ динамика его изменения должна оцениваться от первоначального уровня.
Во время проведения ЧПЭС необходимо дифференцировать загрудинные боли, обусловленные стенокардией от болей, связанных с раздражением стенки пищевода электрическими импульсами. Прекращение ЧПЭС, как правило, сразу приводит к устранению болей, в то время как при стенокардии боли остаются
и после прекращения стимуляции. Кроме того, боль от электрических импульсов носит пульсирующий, жгучий характер, и больные, если их настроить на дифференциацию характера болей, могут это отличить.
Методика купирования пароксизма тахикардии
Основой купирования пароксизма тахикардии ЧПЭС является “попадание” электрического импульса в круг ри-ентри с изменением рефрактерного периода
какого-либо его участка, что дает возможность прерывания круга ри-ентри и делает невозможным дальнейшее продолжение тахикардии.
ЧПЭС можно применять для устранения пароксизмов, возникших как в ходе диагностической стимуляции, так и спонтанных при безуспешности медикаментозного лечения, в том числе в поликлиниках и в условиях “скорой помощи”. Как правило, для купирования пароксизмов тахикардии используется предсердная стимуляция, реже желудочковая.
Наиболее часто применяемыми и наиболее простыми в использовании для купирования пароксизмов являются залповая или сверхчастая предсердная
стимуляция. В первом случае на сердце наносится асинхронный залп электрических импульсов в количестве 3-10 (иногда до 20) с частотой следования импульсов 200-400 в минуту (иногда до 1200 в минуту), длительностью от 1 до 3 секунд. В начале используется залповая стимуляция, причем, если синусовый ритм не восстановился, залповую ЧПЭС повторяют несколько раз, увеличивая число импульсов. Если залпом импульсов прекратить тахикардию не удалось, приступают к сверхчастой ЧПЭС, которую при сохраняющейся тахикардии допустимо повторять, увеличивая ее длительность.
Противопоказано проведение залповой, частой и сверхчастой ЧПЭС при наличии антерограднных дополнительных путей проведения с коротким рефрактерным
периодом и высокой (более 200-300 имп/мин.) предсердно-желудочковой проводимостью.
Условием купирования тахикардии является обязательное навязывание сердцу либо всех (частая и программированная), либо части (конкурентная, залповая и сверхчастая ЧПЭС) наносимых на сердце импульсов. У части больных, особенно при применении асинхронных способов ЧПЭС, развивается фибрилляция предсердий, которая в 70-80% случаев в течение нескольких минут самостоятельно переходит в синусовый ритм. Если фибрилляция предсердий имеет нормосистолическую форму и длительно сохраняется, исследование прекращают и оставляют больного под наблюдением. При пароксизме фибрилляция предсердий с высокой частотой желудочкового ритма, особенно при резком ухудшении состояния больного, аритмию купируют медикаментозно или дефибрилляцией.
Возможные осложнения чреспищеводной электростимуляции сердца и тактика их лечения
1. Болевые ощущения во время ЧПЭС. Их устранения можно достигнуть изменением положения электрода в пищеводе, изменением расстояния между полюсами электрода и увеличением длительности импульса. В крайних случаях допустимо введение анальгетиков.
2. Сокращение диафрагмы и мышц грудной клетки (при монополярной стимуляции) требует изменения положения электрода и уменьшения амплитуды импульса.
3. Раздражение носоглотки и пищевода. Уменьшается местной анестезией слизистых оболочек.
4. Ущемление электрода в носовых ходах можно устранить осторожным вращением электрода вокруг оси, введением или, наоборот, удалением стилета.
5. Приступ стенокардии требует прекращения ЧПЭС, приема нитроглицерина или анальгетиков.
6. Развитие некупирующегося ЧПЭС пароксизма тахикардии требует внутривенного введения медикаментов или кардиоверсии.
7. Развитие острой сердечной или сосудистой недостаточности требует немедленного прекращения исследования, введения кардиотонических или
вазопрессорных препаратов.
8. При несоблюдении правил ЧПЭС, в очень редких случаях, возможно развитие фибрилляции желудочков или асистолии, требующей немедленных реанимационных мероприятий.