быстрый рост в детстве что это такое
Особенности диагностики и лечения высокорослости у детей
Особенности диагностики и лечения высокорослости у детей
По данным эпидемиологических исследований, высокие темпы роста часто встречаются у детей и редко являются причиной обращения к врачу. Обычно родители обращаются за консультацией к детскому эндокринологу по поводу высокорослости в связи с наличием сопутствующих ей симптомов: утомляемости, синкопальных состояний, различных нарушений осанки, задержки или ускоренного полового развития. Однако у подростков с высоким ростом часто наблюдается отставание в формировании сосудистой системы, что создает предпосылки для нарушения регуляции тонуса сосудов, повышения артериального давления, нарушения адаптации сердца к физической нагрузке. Кроме того, у части детей с высокорослостью отмечаются психологические и социальные проблемы.
Следует отметить, что высокий рост и, главным образом, быстрые темпы роста могут быть признаком различных эндокринных заболеваний – таких, как соматотропинома, преждевременное половое развитие и тиреотоксикоз.
Определение высокорослости
Объективная оценка роста ребенка проводится с использованием коэффициента стандартного отклонения (SDS, standard deviation score), показывающего, сколько сигмальных отклонений от популяционной нормы составляет разница.
Высокорослость у детей диагностируется при превышении длины тела более чем на 2 стандартных отклонения (SD), гигантизм – более чем на 3 SD для данного пола и хронологического возраста.
Кроме оценки роста, у детей с высокорослостью необходимо рассчитать скорость роста, оценить наличие диспропорционального телосложения и конечный прогнозируемый рост. Для вычисления скорости роста необходимо иметь данные о двух документально подтвержденных измерениях роста в интервале не более 6 месяцев в целях нивелирования возможной погрешности в расчетах. Следует отметить, что оценка темпов роста наиболее информативна у детей допубертатного возраста.
Для оценки пропорциональности телосложения проводится измерение роста сидя с оценкой соотношения верхнего сегмента тела к нижнему.
Конечный прогнозируемый рост ребенка может быть рассчитан исходя из роста его родителей и значений достигнутого костного возраста.
Дифференциальная диагностика высокорослости
В большинстве случаев у детей высокорослость не является патологической, однако основная задача детского эндокринолога состоит в проведении дифференциальной диагностики других заболеваний, симптомом которых являются высокие темпы роста.
При сборе анамнеза следует обратить внимание на показатели роста и веса при рождении. Так, при синдромах Марфана, Беквита – Видемана, Симпсона – Голаби – Бемеля, Банаяна – Райли – Рувалькаба и конституциональной высокорослости отмечаются высокие значения длины тела при рождении. Для большинства синдромальных форм высокорослости (синдромы Сотоса и Вивера, Кляйнфельтера, синдром «ломкой» Х-хромосомы, гомоцистинурия и др.) характерны задержка нервно-психического развития или поведенческие проблемы. Важно выяснить наличие у пациента сопутствующей патологии. Например, фактопатии характерны для синдрома Марфана и гомоцистинурии; патологии середечно-сосудистой системы чаще встречаются при синдроме Марфана, синдроме Луис – Дейц, гомоцистинурии. Неонатальная гипотония часто встречается при синдроме Сотоса, а дефекты передней брюшной стенки – при синдроме Беквита – Видемана. Уточнение роста родителей важно не только при расчете целевого роста, но и для проведения дифференциальной диагностики с синдромальными формами высокорослости. При анализе антропометрических показателей важно оценить пропорциональность телосложения. Формирование диспропорций тела характерно для синдромов Марфана, Кляйнфельтера, Луис – Дейц, гомоцистинурии, врожденной контрактурной арахнодактилии (синдром Билса), в то время как пациенты с синдромами «ломкой» Х-хромосомы, Сотоса, Вивера, Беквита – Видемана имеют нормальное соотношение верхнего и нижнего сегментов. Большие размеры окружности головы характерны для синдромов Сотоса, Вивера и Банаяна – Райли – Рувалькаба.
Оценка полового развития является важнейшим аспектом в уточнении причины высокорослости у детей. Ускорение роста в сочетании с телархе у девочек до 8 лет указывает на преждевременное половое развитие. Высокие темпы роста у мальчиков в сочетании с увеличением размеров тестикул также свидетельствуют о наличии преждевременного полового развития. Однако не стоит забывать, что макроорхидизм в сочетании с высокорослостью является клиническим проявлением синдрома «ломкой» Х-хромосомы. К другим эндокринным заболеваниям, сопровождающимся высокими темпами роста, относятся гипертиреоз и гипофизарный гигантизм. Диагностика этих и других заболеваний, ассоциированных с высокорослостью, представлена в таблице 1. Кроме того, ускорение темпов роста характерно для детей с конституционально-экзогенным ожирением.
Таблица 1. Дифференциальная диагностика высокорослости у детей
Заболевание
Диагностические тесты
Синдром Марфана
Осмотр офтальмолога, кардиолога, генетика с использованием Гентских критериев
Синдром Кляйнфельтера
Синдром «ломкой» Х-хромосомы
Генетическое исследование (ген FMR1)
Гомоцистинурия
Уровень гомоцистина сыворотки
Синдром Сотоса
Использование специальных критериев, костный возраст, консультация генетика, исследование гена NSD1
Другие синдромы
Консультация генетика, специфические генетическое тесты
Преждевременное половое развитие
ЛГ, ФСГ, эстрадиол (девочки), тестостерон (мальчики), костный возраст
Преждевременное адренархе
Надпочечниковые андрогены, тестостерон, эстрадиол, АФП, В-ХГЧ, костный возраст
Гипофизарный гигантизм
ГР, ИФР-1, ИФРСБ3, супрессивный тест с глюкозой (ОГТТ)
Гипертиреоз
Семейная глюкокортикоидная недостаточность
Дефицит эстрогенов
ЛГ, ФСГ, эстрадиол, костный возраст
Конституциональная высокорослость
Возможности лечения высокорослости у детей
Абсолютному большинству детей с высокорослостью специфическое (ростоостанавливающее) лечение не требуется; рекомендуется динамическое наблюдение с контролем темпов роста.
Вопрос о возможности лечения высокорослости является спорным, так как до настоящего времени нет убедительных данных о его эффективности и безопасности. Кроме того, точно не определены сроки и условия, при которых такое лечение может быть проведено. Согласно мнению большинства экспертов, специфическое лечение высокорослости возможно при превышении показателя прогнозируемого роста более 2,5 SD от популяционных значений. Основными методами лечения высокорослости у детей являются хирургический и медикаментозный.
Наиболее часто применяется гормональная терапия с использованием высоких доз половых стероидов, что способствует ускоренному закрытию зон роста. В исследовании Hendriks A.E. с соавт. было показано, что использование высоких доз эстрогенов (100 мкг этинилэстрадиола) эффективно в отношении лечения высокорослости у высокорослых девочек. Степень снижения конечного прогнозируемого роста оказалась крайне вариабельна и сильно зависела от показателя костного возраста, при котором было начато лечение. Чем позже было начато лечение, тем меньшим оказалось снижение конечного роста. Кроме того, терапия эстрогенами в высоких дозах сопровождалась такими побочными эффектами, как гинекомастия у мальчиков, тошнота, головные боли, внутричерепная гипертензия, склонность к тромбозам у пациентов обоих полов. Проспективные исследования последних лет указывают на отсроченные побочные эффекты терапии эстрогенами в виде снижения фертильности у женщин. Применение более высоких доз эстрогенов (200 мкг этинилэстрадиола) не дает преимуществ в снижении конечного роста и ассоциировано с первичной овариальной недостаточностью и повышением риска рака груди у женщин. Использование сверхвысоких доз эстрогенов (от 250 до 1000 мг) связано со значительным повышением риска развития меланомы у женщин.
У высокорослых мальчиков для снижения конечного прогнозируемого роста используется препараты тестостерона в высоких дозах (500 мг, в/м каждые 2 недели), однако их эффективность значительно ниже, чем при терапии препаратами эстрогенов. Эффективность лечения также зависит от степени костного созревания, при котором было начато лечение. К побочным эффектам терапии андрогенами относится акне, агрессивное поведение, появление спонтанных болезненных эрекций. Подобная терапия также успешно применяется у пациентов с синдромом Марфана без сердечно-сосудистой патологии. Убедительных данных о повышении частоты онкологических заболеваний (в том числе рака простаты) и снижении фертильности у мужчин после применения высоких доз андрогенов не получено.
Высокая частота побочных эффектов терапии половыми стероидами заставляет проводить исследования по применению других препаратов, ингибирующих центральную секрецию гормона роста (аналоги соматостатина или антихолинэргические препараты) или блокирующих периферическое действие гормона роста.
Наиболее распространенной хирургической манипуляцией, направленной на снижение конечного роста, является билатеральный чрескожный эпифизиодез дистальных эпифизов бедренной кости и проксимальных эпифизов большеберцовой и малоберцовой кости. Результат хирургического лечения также зависит от времени начала лечения. Для снижения конечного прогнозируемого роста на треть хирургическое лечение необходимо провести при костном возрасте до 12,5 лет у девочек с ростом до 170 см и 14 лет – у мальчиков с ростом до 185 см. При проведении оперативного лечения есть риск формирования диспропорций тела, так как результатом лечения является прекращение роста нижних конечностей, но не позвоночника. Послеоперационные осложнения (экзостозы, угловые деформации нижних конечностей) при проведении операции опытным хирургом практически отсутствуют. Есть положительный опыт применения эпифизиодеза у пациентов с синдромом Марфана.
Заключение
Высокорослость у детей чаще всего не является патологическим состоянием, требующим специфической терапии. Основная задача детского эндокринолога состоит в выявлении причины высокорослости, что и определяет дальнейшую тактику.
Основными методами лечения высокорослости являются гормональная терапия половыми стероидами и хирургические методы лечения. Терапия высокими дозами эстрогенов у девочек с высокорослостью обладает невысокой эффективностью и связана с серьезными побочными эффектами, что значительно ограничивает их использование в повседневной клинической практике. Хирургические методы более предпочтительны для лечения высокорослости, однако до настоящего время недостаточно изучены профиль безопасности и эффективность данного метода лечения.
При подготовке данного материала использовались:
Hannema S. E., Sävendahl L. The Evaluation and Management of Tall Stature. Horm Res Paediatr 2016;85:347-352.
Проблема РОСТА
Задержка роста (ЗР) сейчас стала встречаться реже, для детей всё больше характерна акселерация (опережение физического развития). Но проблема не исчезла совсем, она всегда становится существенной причиной беспокойства родителей мальчиков, родителей девочек несколько реже.
У процессов роста в норме есть свои природные закономерности:
Теперь немого о том, в какие «жизненные» периоды ребёнка какие гормоны и другие биохимические факторы влияют на рост. Знание этих факторов позволяет быстрее понять причины задержки роста.
Внутриутробно, при беременности, на скорость роста плода влияют: факторы роста матери, питание матери и состояние плаценты!
До 3-4 лет лет жизни – это гормоны щитовидной железы и гормон роста!
Я намеренно не отражаю в этой заметке генетические заболевания, приводящие к задержке роста, чтобы не перезагружать вас информацией, к тому же встречаются они редко.
Как же обследуется нарушение роста:
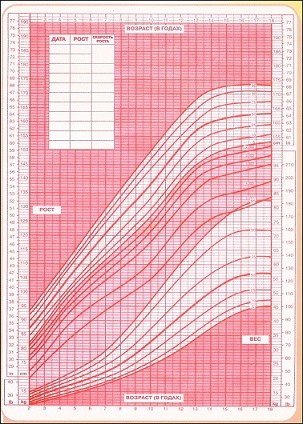
Какие есть критерии оценки костного возраста по рентгеновскому снимку:
Важно! Обращение администрации сайта о вопросах в блоге:
Уважаемые читатели! Создавая этот блог, мы ставили себе цель дать людям информацию по эндокринным проблемам, методам диагностики и лечения. А также по сопутствующим вопросам: питанию, физической активности, образу жизни. Его основная функция – просветительская.
В рамках блога в ответах на вопросы мы не можем оказывать полноценные врачебные консультации, это связано и недостатком информации о пациенте и с затратами времени врача, для того чтобы изучить каждый случай. В блоге возможны только ответы общего плана. Но мы понимаем, что не везде есть возможность проконсультироваться с эндокринологом по месту жительства, иногда важно получить еще одно врачебное мнение. Для таких ситуаций, когда нужно более глубокое погружение, изучение медицинских документов, у нас в центре есть формат платных заочных консультаций по медицинской документации.
Как это сделать? В прейскуранте нашего центра есть заочная консультация по медицинской документации, стоимостью 1200 руб. Если эта сумма вас устраивает, вы можете прислать на адрес patient@mc21.ru сканы медицинских документов, видеозапись, подробное описание, все то, что сочтете нужным по своей проблеме и вопросы, на которые хотите получить ответы. Врач посмотрит, можно ли по представленной информации дать полноценное заключение и рекомендации. Если да, вышлем реквизиты, вы оплатите, врач пришлет заключение. Если по предоставленным документам нельзя дать ответ, который можно было бы рассматривать как консультацию врача, мы пришлем письмо о том, что в данном случае заочные рекомендации или выводы невозможны, и оплату брать, естественно, не будем.
С уважением, администрация Медицинского центра «XXI век»
Быстрый рост в детстве что это такое
Жалобы на высокий рост менее распространены, чем на низкий, поскольку многие родители гордятся тем, что их дети высокого роста. Однако некоторые подростки (в основном девочки) проявляют обеспокоенность и считают себя слишком высокими во время пубертатного скачка роста. Причины высокорослости приведены ниже.
Причины преждевременного развития или высокого роста:
I. Ожирение:
— Пубертатный период наступает раньше, поэтому финальная центиль роста меньше, чем в детстве
II. Вторичные:
— Гипертиреоз
— Избыток половых гормонов — преждевременный пубертатный период по какой бы то ни было причине
— Избыток гормонов надпочечников и андрогенов — врождённая гиперплазия надпочечников
— Истинный гигантизм (избыточная секреция ГР)
III. Синдромы:
— Высокий рост и слишком длинные ноги:
• синдром Марфана
• гомоцистинурия
• синдром Клайнфельтера (47 XXY и XXY кариотип)
— Пропорциональный высокий рост при рождении:
• диабет у матери
• первичный гиперинсулинизм
• синдром Беквита
— Синдром Сотоса сопровождается увеличением головы, характерными особенностями лица и трудностью обучения
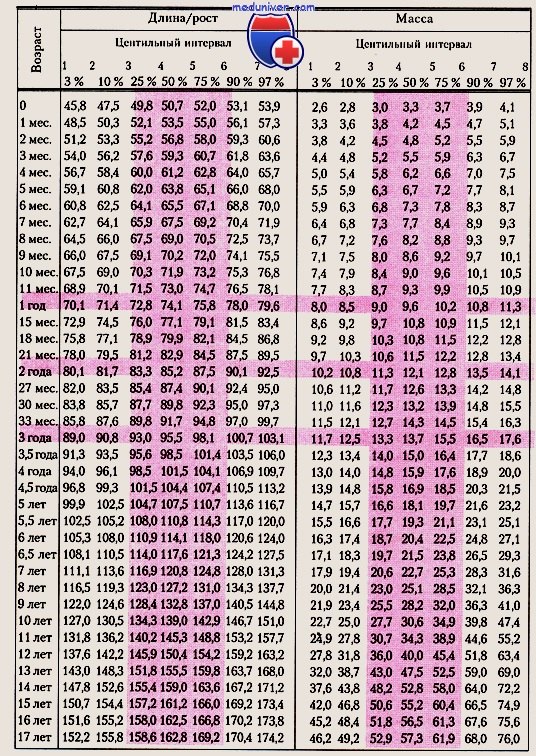
Центильные интервалы роста и веса детей
В большинстве случаев высокий рост наследуется от рослых родителей. Переедание в детском возрасте, вызывающее ожирение, стимулирует раннее развитие и приводит к высокому росту. Однако поскольку в этом случае пубертатный период обычно наступает несколько раньше среднего, окончательный рост может быть не слишком высоким.
Вторичные эндокринные заболевания встречаются редко. Как врождённая гиперплазия надпочечников, так и раннее половое созревание приводят к раннему слиянию эпифизов, так что после раннего бурного роста его скорость снижается и окончательный рост не сильно превышает норму.
Синдромы Марфана (заболевание рыхлой волокнистой соединительной ткани) и Клайнфелтера (XXY) вызывают высокий рост с непропорционально длинными ногами, а состояние XXY также сопровождается бесплодием и трудностями при обучении.
Высокие дети могут испытывать неудобства вследствие того, что с ними ведут себя как со взрослыми, поскольку они выглядят старше своего хронологического возраста. Избыточный рост в предпубертатном или в раннем пубертатном периоде у девочек-подростков можно регулировать с помощью терапии эстрогеном для индуцирования раннего заращения эпифизов.
Однако поскольку это лечение приводит к разнообразным результатам и имеет опасные побочные эффекты, его редко применяют. В случаях особо выраженной высокорослости может рассматриваться возможность хирургической деструкции эпифизов на ногах.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Университет
Длительно некомпенсированные нарушения углеводного обмена у беременной — наиболее частая причина рождения ребенка с макросомией. Длительная гипергликемия у беременной при недиагностированном (гестационном), суб- или декомпенсированном сахарном диабете приводит к гиперплазии β-клеток поджелудочной железы плода, вызывая повышение секреции фетального инсулина. Хроническая гиперинсулинемия стимулирует увеличение экспрессии ИФР-1, что проявляется повышениями концентрации ИФР-1 при рождении ребенка. С другой стороны, инсулин, обладая анаболическим действием, оказывает ростстимулирующий эффект на плод.
При наличии тяжелой плацентарной дисфункции, сосудистых нарушений у новорожденного от матери с сахарным диабетом может наблюдаться внутриутробная задержка роста, врожденные пороки развития (сердца, мочевыводящей системы, глаз, каудальная дисгенезия, микроцефалия). Частая проблема — транзиторная ранняя постнатальная гипогликемия. У матерей с некомпенсированным сахарным диабетом повышен риск рождения недоношенных, детей с болезнью гиалиновых мембран, гипокальциемией, пролонгированной гипербилирубинемией, тромбозом (почечных вен), транзиторной кардиомиопатией.
Это группа врожденных заболеваний, в основе которых лежит дефект развития или функционирования β-клеток поджелудочной железы, вызывающий неконтролируемую секрецию инсулина. Последняя приводит к повышенной утилизации глюкозы и развитию тяжелых гипогликемий. Частота встречаемости ПГГ составляет 1 случай на 50 000 новорожденных в европейской популяции.
Выделяют две формы ПГГ новорожденных: фокальную (изолированную) и диффузную гиперплазию -клеток поджелудочной железы. Большинство семейных и спорадических случаев заболевания имеет аутосомно-рецессивный тип наследования. При некоторых семейных формах ПГГ обнаруживаются мутации в KCNJ11 и ABCC8 генах (SUR1 и Kir6.2 субъединицах панкреатического КАТФ-канала).
Классическое клиническое проявление ПГГ — макросомия для данного гестационного возраста и стойкая симптоматическая гипогликемия в первые дни жизни.
Для коррекции требуется высокая скорость подачи глюкозы — более 10 мг/кг/минуту. К лабораторным критериям гиперинсулинемической гипогликемии относят низкий уровень кетоновых тел и свободных жирных кислот, высокие показатели инсулина и С-пептида.
Синдром Беквита — Видемана (СБВ)
Описана группа синдромов, которые сопровождаются макросомией новорожденного с увеличением внутренних органов. В их основе лежит избыточная секреция инсулиноподобного фактора роста — 2 (ИФР-2). Наиболее распространенным заболеванием является синдром Беквита — Видемана (синоним: синдром висцеромегалии, омфацеле и макроглоссии). Частота встречаемости СБВ составляет 1 случай на 13 700 новорожденных.
Причина СБВ — изменение количества рострегуляторных генов, расположенных на конце короткого плеча 11-й хромосомы (11р15.5). Молекулярные нарушения при данном заболевании имеют сложный характер и объясняют вариабельность фенотипа. 10% больных СБВ имеют хромосомные нарушения. В других 90% случаев определяются молекулярные дефекты известных генов, участвующих в патогенезе синдрома, и генов-кандидатов, выявляемых в спорадических случаях.
Минимальные диагностические признаки СБВ включают макроглоссию, грыжу пупочного канатика, макросомию, насечки на мочках ушных раковин, гипогликемию.
Частые аномалии — макроглоссия и омфацеле (реже расхождение прямых мышц живота). Макросомия отмечается с рождения (длина новорожденного более 52 см и масса свыше 4 кг) или развивается постнатально. Могут наблюдаться микроцефалия или гидроцефалия; выступающий затылок; аномалии прикуса, связанные с гипоплазией верхней челюсти и относительной гиперплазией нижней; экзофтальм; относительная гипоплазия орбит. Нередко имеют место гемигипертрофия и пигментные невусы.
Отмечаются висцеромегалия (гепатомегалия, спленомегалия, нефромегалия, панкреатомегалия, реже — кардиомегалия), гиперплазия матки, мочевого пузыря, клитора, тимуса.
У 30–50% больных наблюдают гиперинсулинемическую гипогликемию вследствие гиперплазии -клеток поджелудочной железы. В большинстве случаев она носит транзиторный характер и купируется введением глюкозы и диазоксида. У части больных для нормализации показателей гликемии требуется частичная панкреатоэктомия. Умеренная умственная отсталость обычно связана с гипогликемиями.
У пациентов с СБВ повышен риск развития эмбриональных опухолей (опухоль Вильмса, гепатобластома, адренокортикальная карцинома, гонадобластома).
Синдром Симпсона — Голаби — Бемеля (СГБ)
Заболевание относится к Х-связанным синдромам с пренатальной и постнатальной высокорослостью. Минимальные диагностические признаки — макросомия (масса при рождении 4 000–5 000 г), аномалии лицевой части черепа, полидактилия, гипоплазия ногтей.
Другие фенотипические проявления сходны с СБВ. Отмечаются макроглоссия, висцеромегалия, гиперинсулинемическая гипогликемия, склонность к эмбриональным опухолям. Рост мужчин достигает 192–210 см.
В основе синдрома СГБ лежат функциональные нарушения гена, играющего роль в контроле роста эмбриональной мезодермальной ткани, glypican 3 (GPC3). Обсуждается потенциальная взаимосвязь рецептора этого гена и ИФР-2, что может объяснить сходные клинические признаки синдромов СГБ и СБВ.
Синдром Перлмана
Это редкое генетическое заболевание характеризуется пренатальной макросомией, почечной гамартомой, предрасположенностью к фетальным опухолям (опухоль Вильмса), гипогликемией на фоне гиперплазии островковых клеток поджелудочной железы, лицевыми дисморфиями. Большинство пациентов погибает в неонатальном периоде. Причина заболевания в настоящее время неизвестна.
Фетальная макросомия с нормальным уровнем инсулина
Синдром Сотоса
Популяционная частота синдрома Сотоса (синдром церебрального гигантизма) неизвестна. Большинство случаев носят спорадический характер. Семейные формы синдрома имеют аутосомно-доминантный тип наследования. Минимальные диагностические признаки включают акромегалию, усиленный рост, умственную отсталость, нарушение координации. При рождении характерно увеличение показателей массы тела и роста более 90-й перцентили. Отмечается ускорение роста в первые годы жизни, рост больных превышает 97-ю перцентиль. Акселерация роста продолжается до 4–5 лет. Половое развитие наступает в нормальные сроки, может отмечаться ранний пубертат.
Результаты уровней (базальные и в ходе ОГТТ) СТГ, ИФР-1, ИФРСБ-3 имеют нормальные значения. Отсутствуют специфические лабораторные и инструментальные признаки синдрома.
Наблюдаются макроцефалия с выступающими лобными буграми, прогнатия, гипертелоризм, антимонголоидный разрез глаз, выступающая нижняя челюсть, макроглоссия, высокое нёбо, косоглазие. Описаны сколиоз, увеличенные стопы и кисти, синдактилия пальцев стоп. Повышен риск неоплазий, в частности печеночной карциномы, опухоли Вильмса, яичников, паращитовидных желез. Степень умственной отсталости умеренная. Отмечаются судороги, нарушение координации.
Синдром Маршалла — Смита
Это заболевание относится к редким генетическим синдромам и характеризуется пренатальной высокорослостью, прогрессированием костного возраста, задержкой умственного развития, лицевыми стигмами, большими размерами кистей и стоп, утолщением проксимальных и средних фаланг пальцев рук. Основная причина смерти пациентов в раннем детском возрасте — легочная недостаточность. Молекулярная причина развития синдрома в настоящее время неизвестна.
Фетальная макросомия с нормальным уровнем инсулина
Синдром Вивера — Смита
Популяционная частота неизвестна. Большинство описанных случаев носят спорадический характер, возможен аутосомно-рецессивный, Х-сцепленный и (или) аутосомно-доминантный типы наследования. К минимальным диагностическим признакам относятся лицевые стигмы (эпикант, большие уши, длинный фильтр, микрогения, высокий лоб), рентгенологические (расширение метафизов костей, нарушение (диссоциация) костного созревания), камптодактилия, легкая умственная отсталость.
Отмечается пре- и постнатальная высокорослость. Средние показатели массы тела и роста при рождении у мальчиков составляют 4,8 кг и 56 см, у девочек — 3,9 кг и 53 см. С первых месяцев жизни — высокая скорость роста и прогрессирование костной зрелости. Окончательный средний рост мужчин достигает 194,2 см, женщин — 176,3 см.
Наблюдаются лицевые дисморфии, камптодактилия, контрактура коленных суставов, клинодактилия. Неврологическая симптоматика встречается в 80% случаев и включает легкую умственную отсталость, гипертонус мышц.
Синдром Нево
Характерен высокий рост при рождении, контрактуры стоп, врожденный отек, гипотония, прогрессия костного возраста, долихоцефалия, длинные конечности, задержка умственного развития.
Синдром Элеялде
Редкое генетическое заболевание с фетальной макросомией, полидактилией, избыточным развитием соединительной ткани и разрастанием волокон периваскулярных нервов во многих тканях, утолщением кожи, краниоостозом и поликистозом почек. Часто поражения органов и тканей при рождении ребенка не совместимы с жизнью.
Причина синдрома в настоящее время неизвестна.
Постнатальное опережение физического развития, ведущее к высокорослости в детском возрасте
Семейная (конституциональная) высокорослость
Свойственна большая скорость роста с рождения, родители высокие. Прогнозируемый рост ребенка по костному возрасту (рентгенограмма кисти и запястья) с расчетом по индексным таблицам совпадает с генетическим (целевым) ростом. Отсутствуют типичные клинико-лабораторные и инструментальные нарушения, характерные для патологической гиперсекреции соматотропного гормона (СТГ) — нормальные уровни инсулиноподобного фактора роста — 1 (ИФР-1) и инсулиноподобного фактора роста, связывающего белок — 3 (ИФРСБ-3), супрессия показателей СТГ при проведении орального глюкозотолерантного теста (ОГТТ), нормальный кариотип.
Синдром Вивера — Смита (см. выше).
Синдромы Беквита — Видемана и Сотоса
Синдром Марфана
Популяционная частота — 0,04 на 1 000 человек. Тип наследования аутосомно-доминантный с высокой пенетрантностью и различной экспрессивностью. Минимальные диагностические признаки: высокий рост, арахнодактилия, гиперподвижность суставов, подвывих хрусталика, аневризма аорты.
Типичны высокий рост, длинные тонкие конечности, особенно дистальные отделы. Отмечаются сколиоз, кифоз, воронкообразная или килевидная грудная клетка, долихоцефалия, готическое нёбо, плоскостопие. Поражения глаз включают двусторонний подвывих хрусталика, сферофакию, микрофакию. Наблюдаются миопия высокой степени, отслойка сетчатки, гетерохромия радужки, мегалокорнеа, голубые склеры.
Свойственны нарушения со стороны сердечно-сосудистой системы: расширение восходящей части (реже грудного или брюшного отдела) аорты с развитием расслаивающейся аневризмы и недостаточность сердечных клапанов. Встречаются грыжи (бедренные, диафрагмальные, паховые), гипоплазия мышц и подкожной клетчатки, нефроптоз.
Синдром хромосомы фрагильной Х (синдром Мартина — Белла)
Популяционная частота 0,5 на 1 000 мальчиков. Тип наследования Х-сцепленный рецессивный. Минимальные диагностические признаки: умеренная или глубокая умственная отсталость; большие оттопыренные ушные раковины; выступающий лоб и массивный подбородок; макроорхидизм; ломкость Xq 28 участка.
Масса тела и длина при рождении нормальные или незначительно превышают популяционную норму, увеличена окружность головы. У старших детей лицо имеет прямоугольную форму с высоким лбом, тонким длинным носом, гиперплазией нижней челюсти, часто встречаются расщелины нёба. Кисти широкие. С началом полового созревания отмечается макроорхидизм. Могут наблюдаться аутизм, гиперреактивность, мышечная гипотония, судороги.
У некоторых пациентов отмечаются ожирение, гинекомастия, гипоспадия, пролапс митрального клапана.
Синдром Клайнфелтера
Популяционная частота синдрома Клайнфелтера (ХХY синдром) — 1 на 500–1 000 мальчиков. Чаще отмечается кариотип 47ХХY. Возможны следующие варианты: 46ХY/ХХY мозаицизм; 48ХХYY; 48ХХХY; 49ХХХYY; 49ХХХХY. Клинические проявления заболевания наблюдаются у фенотипических мальчиков с кариотипом 46 ХХ в результате транслокации Y (SRY) на Х хромосому. Кариотип 46ХХ встречается у одного из 20 000 мальчиков. Большинство описанных случаев носят спорадический характер. Минимальные диагностические признаки — гипогенитализм, первичный гипогонадизм, аномалия кариотипа.
Обычно пациенты высокие, пропорции тела евнухоидные, нижние конечности непропорционально длинные. Отличительный признак — гипоплазия яичек и полового члена. Часто наблюдаются гинекомастия, ожирение, оволосение на лобке по женскому типу. При гистологическом исследовании яичек отмечается гиалиноз и фиброз семенных канальцев, уменьшение количества клеток Лейдига. Характерны снижение полового влечения, импотенция, бесплодие.
IQ — 85–90, выраженная умственная отсталость наблюдается редко (в основном у пациентов, имеющих в кариотипе три и более Х-хромосомы). Возможны трудности в обучении, задержка речевого развития.
Повышен риск снижения минеральной плотности костной ткани и развития остеопороза, сахарного диабета 2-го типа, варикозного поражения, тромбозов, легочной эмболии. Пациенты с кариотипом 46ХХ имеют нормальные пропорции скелета, низкорослость, снижение интеллекта выражено незначительно.
Ожирение
Экзогенно-конституциональное (алиментарное) ожирение часто сопровождается ускорением линейного роста. Костный возраст обычно незначительно опережает хронологический. Раннее половое созревание ускоряет закрытие эпифизарных зон роста, но окончательный рост пациентов с алиментарным ожирением входит в генетический ростовой коридор.
Проявления ожирения у детей:
б) нейроэндокринные (низкая концентрация кортикотропин-рилизинг-гормона, серотонина и его метаболитов в цереброспинальной жидкости);
Гиперпродукция гормона роста
Гигантизм — нейроэндокринное заболевание, вызванное хронической избыточной секрецией СТГ у пациентов с незаконченным физиологическим ростом. Характеризуется пропорциональным ростом костей скелета в длину, приводящим к значительному увеличению линейного роста ребенка. При отсутствии своевременной диагностики и адекватного лечения у детей с гигантизмом после завершения пубертатного периода развиваются все типичные симптомы акромегалии.
Выделяют микро- (мене 10 мм) и макроаденому (более 10 мм).
В большинстве случаев гигантизм обусловлен избыточной первичной секрецией СТГ аденомой гипофиза, которая возникает вследствие генных мутаций в α-субъединице G-белка (появление Gsp-онкогена). Под влиянием Gsp-онкогена происходит пролиферация опухолевых клеток и повышение секреции СТГ, которая не регулируется обычными секреторными механизмами. Избыток СТГ вызывает повышение секреции ИФР-1 в печени и его локальную продукцию в различных тканях, включая кости и хрящи. Под воздействием ростовых факторов увеличивается продукция коллагена, пролиферация хрящей, что приводит к росту и утолщению мягких, костной и хрящевой тканей с поражением кожи, мягких тканей (огрубение черт лица, утолщение пальцев, себорея, угри, гирсутизм, потливость) и костной системы (диастема, прогнатизм, фронтальный гиперостоз, заболевания височно-нижнечелюстного аппарата, остеоартрит, дорзальный кифоз). В процесс вовлекаются практически все органы и системы организма.
Дополнительные методы исследования при гиперпродукции СТГ: УЗИ щитовидной железы, сердца, органов малого таза; рентгенография органов грудной клетки; электрокардиограмма; МРТ(КТ) грудной и брюшной полости; определение СТГ в крови, оттекающей из нижних кавернозных синусов (при подозрении на эктопированную продукцию СТГ); определение уровня СТГ-рилизинг гормона в сыворотке крови (при подозрении на эктопическую продукцию соматолиберина).
Диагноз «гигантизм» подтверждается при повышении базального уровня СТГ>0,4 нг/мл, отсутствии подавления СТГ на фоне ОГТТ, увеличении показателя ИФР-1.
ГР-продуцирующая аденома как составляющая синдромов МакКьюна —Олбрайта или МЭН-1
Для синдрома МакКьюна — Олбрайта характерна специфическая триада: полиостатическая фиброзная дисплазия, преждевременное половое развитие, специфические пигментные пятна бледно-кофейного цвета.
Преждевременное половое развитие (ППР) начинается позже и протекает медленнее, чем при других формах преждевременного созревания. Часто первым признаком у девочек являются маточные кровотечения задолго до появления телархе и адренархе. Кровотечения вызваны повышенным уровнем эстрогенов. ППР у мальчиков наблюдается значительно реже и характеризуется гиперплазией клеток Лейдига. Уровни гонадотропных гормонов обычно низкие или супрессированы. У некоторых пациентов показатели лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) могут повышаться, вызывая развитие истинного ППР.
В основе эндокринных нарушений лежит спорадическая мутация гена GNAS1 (стимулятор α-субъединицы G-белка), который связывает рецепторы ЛГ и ФСГ с аденилатциклазой в гонадах. Мутантный белок постоянно активирует аденилатциклазу в отсутствие гонадотропных гормонов, что ведет к усилению секреции эстрогенов. Предполагают, что мутация гена происходит на ранних этапах эмбриогенеза.
Клинические проявления гигантизма у пациентов с синдромом МакКьюна — Олбрайта вызваны СТГ-продуцирующей аденомой гипофиза. Гиперпролактинемия — часто сопутствующий признак у детей с гиперпродукцией СТГ. Тиреотоксикоз и автономно функционирующие аденомы щитовидной железы наблюдаются у 33% пациентов с синдромом МакКьюна — Олбрайта. Возможно развитие синдрома Кушинга вследствие узловой гиперплазии или одиночной аденомы надпочечников. Неэндокринные поражения включают аритмии, тяжелый неонатальный холестаз.
Клиническая картина гигантизма с развитием аденомы может быть проявлением синдрома МЭН-1 (синдром Вермера). Для него обязательно наличие гормонально-активных опухолей паращитовидных желез, островков поджелудочной железы, аденомы гипофиза.
Частота — 1 случай на 30 000 человек; пик манифестации — на четвертой–пятой декадах жизни. Число известных наблюдений этого синдрома в детском возрасте невелико, выявление МЭН-1 до десятилетнего возраста ребенка отмечается в единичных случаях. МЭН-1 является заболеванием с аутосомно-доминантным типом наследования или встречается спорадически. В его основе часто лежат мутации гена супрессии опухолей МЭН-1 (менина), расположенного на хромосоме 11q13.
Клиническая диагностика основана на определении у пациента двух из трех характерных признаков (аденом паращитовидных желез, эндокринных неоплазий поджелудочной железы и опухолей аденогипофиза). Для семейной формы достаточно выявить у пациента один типичный симптом МЭН-1, если есть родственники первой степени родства с одной из трех упомянутых выше опухолей.
Описано более 20 различных эндокринных и неэндокринных неоплазий, лежащих в основе МЭН-1. Классической триаде заболевания могут сопутствовать опухоли надпочечников, бронхов, гастроинтестинального тракта, тимуса, липомы, ангиофибромы, шванномы, опухоли яичек, нейрофибромы.
Опухоли аденогипофиза — первый признак клинической манифестации МЭН-1 в 25% спорадических и менее 10% семейных случаев. Они встречаются у 15–90% пациентов с данным заболеванием и различаются показателями секреции гипофизарных гормонов (пролактина, гормона роста, адренокортикотропного гормона и др.) с развитием характерных клинических симптомов и (или) размерами образования с эффектом компрессии окружающих тканей.
Одна из наиболее часто встречаемых гормонально-активных неоплазий передней доли гипофиза — СТГ-продуцирующая аденома. К ее типичным клиническим признакам относят гигантизм, увеличение размеров конечностей, изменение внешности (укрупнение носа, языка, утолщение кожи, надбровных дуг, диастема, прогнатизм), синдром карпального канала, сужение полей зрения, проксимальная миопатия, артериальная гипертензия, нарушение углеводного обмена, галакторея.
Согласно принятому в 2001 году Консенсусу по диагностике и лечению пациентов с МЭН-1, скрининговое мониторирование аденом гипофиза включает определение сывороточных концентраций пролактина и ИФР-1, выполнение МРТ области гипофиза.
Преждевременное половое развитие
Высокорослость может быть одним из клинических признаков ППР. Среди других — появление некоторых или всех вторичных половых признаков у девочек младше 8 лет или у мальчиков до 10 лет.
При истинном ППР формирование вторичных половых признаков изосексуальное (соответствующее генетическому и гонадному полу ребенка), обусловленное активацией гипоталамуса и гиперсекрецией гонадотропных гормонов, является завершенным.
Ложное ППР вызвано автономной избыточной секрецией эстрогенов в надпочечниках или яичниках у девочек либо приемом эстрогенов или гонадотропных гормонов, у мальчиков — автономной гиперсекрецией андрогенов или хорионического гонадотропина. Всегда незавершенное. Может быть изосексуальным и гетеросексуальным.
Последовательность развития вторичных половых признаков обычно такая, как и при нормальном половом созревании, пубертатный скачок роста составляет 8–12 см в год. Под влиянием половых гормонов значительно ускоряется закрытие эпифизарных зон роста, вследствие чего окончательный рост пациентов значительно ниже генетического.
Постнатальное опережение физического развития, ведущее к высокорослости в детском возрасте
Гомоцистинурия (дефицит синтеза цистатионина)
Минимальные диагностические признаки: марфаноподобный фенотип, повышение концентрации метионина и гомоцистина в моче и крови. Популяционная частота неизвестна. Тип наследования аутосомно-рецессивный.
Внешне пациенты выглядят как страдающие синдромом Марфана. Скелетные аномалии включают долихостеномелию, воронкообразную или килевидную деформацию грудной клетки, сколиоз, деформацию коленных суставов, изменение формы и расположения зубов, остеопороз, склонность к переломам, ограничение подвижности суставов. Часто у детей с гомоцистинурией имеется подвывих хрусталика, миопия, атрофия зрительного нерва, отслойка сетчатки, глаукома. Отмечается умственная отсталость различной степени выраженности.
Нередко наблюдается тромбоз коронарных, сонных, почечных артерий, генерализованный венозный тромбоз, которые являются причиной ранней смерти.
В плазме выявляется повышение концентрации метионина, гомоцистеина и гомоцистина, уменьшение количества цистина. Повышена экскреция с мочой гомоцистина.
47 ХYY синдром (YY-синдром)
Частота встречаемости 47 XYY-синдрома составляет 1 случай на 800 мальчиков. Практически всегда мутация возникает de novo. Редко встречается мозаицизм с 45 Х или 46 XY. Добавочная Y-хромосома появляется в результате нерасхождения хромосом во втором делении отцовского мейоза с образованием сперматозоида YY. Возраст отца не является фактором риска. Связь кариотипа 47 XYY с крупными пороками развития не доказана.
Взрослые мужчины имеют нормальный мужской фенотип, для них характерно превышение генетического роста более чем на 10 см. Пубертатное ускорение роста наступает раньше и продолжается дольше, при этом показатели окончательного роста пациента достигают 1,95–2,15 см.
Наблюдаются непропорционально длинные конечности, кисти и стопы, макроцефалия, антимонголоидный разрез глаз, глубоко расположенные глаза, готическое нёбо, деформация ушных раковин. Характерно варикозное расширение вен, угри.
Умственное развитие в пределах нормы, IQ на 10–15 пунктов ниже средних цифр, отмечаются задержка речевого развития и трудности обучения чтению и письму. Дефицит внимания, гиперактивность и импульсивность поведения подтверждены для мальчиков с данным синдромом, но значимая агрессивность и психопатологическое поведение нехарактерны. Фертильность обычно нормальная, либидо повышено, значительного риска иметь хромосомно аномального ребенка нет.
Гормонального лечения не требуется. Половине мальчиков необходима педагогическая коррекция задержки речевого развития. Супружеским парам, в которых мужчина несет кариотип 47 XYY, рекомендуют провести пренатальную диагностику, несмотря на то, что дети в таких семьях обычно имеют нормальный кариотип.
Тиреотоксикоз
Обусловлен избыточным синтезом и секрецией гормонов щитовидной железы, характеризуется усилением обмена веществ во всех тканях — мишенях этих гормонов.
Причины тиреотоксикоза: диффузный токсический зоб (болезнь Грейвса — Базедова); токсическая аденома щитовидной железы; передозировка тиреоидных гормонов; избыток тиреотропного гормона; тиреотоксическая стадия подострого тиреоидита; хашитоксикоз при хроническом лимфоцитарном тиреоидите; йод-индуцированный тиреотоксикоз. В 98% случаев тиреотоксикоз у детей обусловлен развитием болезни Грейвса — Базедова. Более 75% детей заболевают в период полового созревания, девочки — в 4–6 раз чаще. Генетическая предрасположенность определяется ассоциацией с антигенами HLA B 8 и Bw 35.
Основные клинические проявления: офтальмопатия Грейвса — 50%; увеличение щитовидной железы — 99%; нарушения со стороны сердечно-сосудистой системы (тахикардия — 85%, аритмии, увеличение пульсового давления (митральная регургитация) — 40%). Отмечаются возбудимость, раздражительность, эмоциональная лабильность, нарушение концентрации внимания, мелкий тремор, гиперрефлексия. У девочек может наблюдаться задержка менархе, у мальчиков — гинекомастия.
При тиреотоксикозе характерно кратковременное ускорение роста, при этом костный возраст опережает паспортный более чем на 1 год. Окончательный рост пациентов с тиреотоксикозом не выходит за пределы генетического ростового коридора.
Диагноз тиреотоксикоза подтверждается определением в сыворотке низких или подавленных значений тиреотропного гормона, повышенных уровней общего/Т4 св и общего/свободного трийодтиронина (Т3-токсикоз характерен для ранних стадий заболевания и предшествует повышению тироксина), повышенными титрами антител к ТПО и рецепторам ТТГ.
Постнатальное опережение физического развития, ведущее к высокорослости у взрослых
Семейная (конституциональная) высокорослость (см. выше)
Дефицит андрогенов или эстрогенов/резистентность к эстрогенам (у мальчиков)
Основным симптомом дефицита половых гормонов у мальчиков является допубертатный объем яичек (до 4 мл) к 14 годам, у девочек отсутствие развития молочных желез к 13 годам и(или) менструальной функции к 15 годам. У подростков отсутствуют вторичные половые признаки: у мальчиков — мутация голоса, оволосение на лице, мышечная гипертрофия плечевого пояса, активность потовых и сальных желез; у девочек — перераспределение жира по женскому типу.
При длительной задержке полового созревания отмечается рост конечностей, уменьшение соотношения верхнего и нижнего сегментов тела, формирование евнухоидных пропорций. Дифференцировка костного скелета до пубертатного возраста соответствует фактическому возрасту ребенка, и только с 13–14 лет наблюдается отставание костного возраста. Конечный рост нелеченных детей может превышать генетически детерминированный, т. к. зоны роста долго остаются открытыми, способность к линейному росту сохраняется до 20 лет и более.
Тестикулярная феминизация
Синдром тестикулярной феминизации (резистентности к андрогенам) относится к группе ложного мужского гермафродитизма. Распространенность синдрома составляет 1 случай на 20 000–64 000 новорожденных мальчиков.
Минимальные диагностические признаки: аменорея, бесплодие, кариотип 46 ХY, недоразвитость вторичных половых признаков. Выделяют два основных варианта синдрома: полная форма, при которой наружные половые органы имеют нормальное строение по женскому типу, и частичная, когда строение наружных гениталий отражает различную степень маскулинизации.
В основе андрогеновой нечувствительности лежит отсутствие активации гена рецептора андрогена и нарушение связывания с ним тестостерона и его активного метаболита — дегидротестостерона. Из-за нарушения рецепторного связывания с тестостероном и его активной формой нет адекватного ответа на адрогеновый стимул, что проявляется формированием наружных гениталий по женскому типу. Нормальная продукция антимюллерового фактора яичками приводит к регрессии производных мюллеровых протоков (матки, фаллопиевых труб, верхней части влагалища), нижняя часть влагалища укорочена и слепо заканчивается, большие половые губы недоразвиты.
Производные вольфовых протоков (семявыносящий проток, семенные пузырьки и придаток семенника) в различной степени гипоплазированы и могут находиться в брюшной полости или паховых каналах, реже — в больших половых губах. Яички нормально развиваются в препубертатном возрасте, однако гистологически отмечается гиперплазия клеток Лейдига. В пубертате наблюдается диффузное или узловое перерождение гиперплазированных клеток Сертоли с развитием тубулярных аденом.
Процесс сперматогенеза заканчивается на ранней фазе, до созревания сперматозоидов.
При полной нечувствительности к андрогенам больные с рождения воспитываются в женском паспортном поле.
Психосексуальное поведение соответствует женскому типу. В пубертатном возрасте формируется нормальный женский фенотип. Хорошо развиты молочные железы с дифференцированной железистой тканью, половое оволосение слабо выражено или отсутствует. Отмечается превышение конечного роста данной группы пациентов относительно их фенотипически-генетических показателей, что, вероятно, обусловлено влиянием генов, экспрессирующихся на Y-хромосоме.
При лабораторном обследовании пациентов с полной формой заболевания уровни лютеинизирующего гормона (ЛГ) повышены, фолликулостимулирующего гормона (ФСГ) — нормальные. Высокие значения тестостерона являются результатом усиленной по механизму обратной связи секреции ЛГ. Конверсия тестостерона в дегидротестостерон снижена. Концентрации эстрадиола превышают уровни, характерные для нормальных мужчин, но низкие по сравнению с нормативами для женщин в фолликулиновую фазу цикла. Повышенные показатели эстрадиола являются следствием периферической ароматизации большого количества тестостерона и достаточны для реализации феминизации пациентов.
В периоде пубертата больные обращаются к врачу по поводу отсутствия менструаций.
Гиперпродукция гормона роста, cиндром Марфана, cиндром Клайнфельтера (см. выше)