бужирование гортани что это такое
Бужирование гортани что это такое
Очень важно, чтобы каждый пациент выписываясь из стационара после операции,научился ухаживать за стомой и следить за ее состоянием. В частности, следить следует за видоизменением стомы, не допуская ее сужения (стеноза). Для того чтобы не довести стому до состояния стеноза, необходимо в домашних условиях проводить бужирование.
Что такое бужирование?
Это механическое расширение и растягивание отверстия стомы, которое пациент может проделывать как самостоятельно, так и с помощью родственников (либо специалистов в стенах стационара). Техника бужирования очень проста.
На кисть руки надевается тонкая медицинская резиновая перчатка, продающаяся в любой аптеке. Один из пальцев (начинать можно с мизинца) обильно смазывается вазелином и вводится в стому на глубину 3 4 см, при этом им производятся вращательные движения, а также движения вверх вниз.
Продолжительность и частота проведения процедуры зависит от состояния стомы. Чтобы обучиться технике проведения «пальцевого бужирования», целесообразно обратиться за консультацией к стоматерапевту центра реабилитации. Пальцевое бужирование, не являясь сложной процедурой, часто вызывает у пациентов психологический страх, вследствие опасений «повредить кишку».
Этот страх понятен, поэтому первое бужирование необходимо проводить под контролем опытного специалиста. Стоматерапевт в доступной форме объяснит вам необоснованность ваших страхов. Во первых, слизистая стомы не имеет нервных окончаний, следовательно, с ее стороны болевых ощущений пациент испытывать не может.
Если же кожа заросла настолько, что растягивается болезненно и с трудом – это повод к оперативному вмешательству (реконструкции стомы). Не стоит также опасаться появления небольшого кровотечения в процессе бужирования.
Это нормальная реакция слизистой оболочки на травму и она не является противопоказанием к проведению данной процедуры. Более того, это говорит о том, что пациент «не халтурит», а совершенно верно проводит бужирование. Еще раз хочется обратить ваше внимание на то, что палец должен входить беспрепятственно и относительно безболезненно. Если палец вводится с трудом, эту процедуру следует повторять чаще, вплоть до ежедневного проведения.
В том же случае, если палец (даже мизинец) в стому ввести не удается, следует срочно обратиться к вашему стоматерапевту (либо к хирургу). Помните, что успех послеоперационного периода во многом зависит не только от профессионализма врачей, но и от вас самих.
Э. В. Балобина, стоматерапевт отделения реабилитации
Эндоскопическое бужирование
Эндоскопическое бужирование – методика расширения просвета полого органа или анастомоза с целью восстановления его проходимости. Эта манипуляция относится к категории лечебных эндоскопических процедур и осуществляется с помощью специальных инструментов – бужей.
Показания для выполнения бужирования
На отделении эндоскопии НИИ онкологии бужирование пищевода применяется и в лечении опухолевых стенозов пищевода, однако не является окончательным методом лечения, а решает задачу кратковременного расширения просвета пищевода в месте циркулярно распространяющейся опухоли перед проведением брахитерапии, установкой самораскрывающегося стента (если диаметр зонда для брахитерапии или доставочного устройства стента превышает диаметр просвета органа).
Процедура бужирования
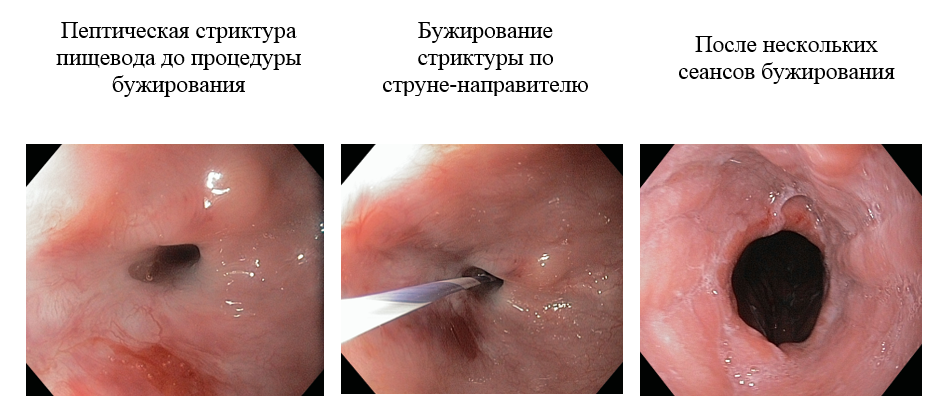
На отделении эндоскопии НИИ онкологии им. Н.Н.Петрова применяется методика бужирования стриктур по направляющей струне без использования рентгенологической установки.
Она заключается в установке гибкой или более ригидной металлической струны по биопсийному каналу эндоскопа за область сужения с последующим проведением по проводнику, как по направителю, пластиковых бужей разного диаметра, начиная от наименьшего. Для процедуры бужирования мы применяем бужи типа Savary с конусообразным дистальным концом и внутренним каналом на всем протяжении бужа.
Эта методика имеет целый ряд преимуществ перед аналогичными вмешательствами, выполняемыми под рентгенологическим контролем. Во-первых, она позволяет выполнять бужирование преимущественно амбулаторно из-за минимальной опасности возникновения осложнений. Во-вторых, наличие проводника позволяет успешно бужировать даже сложные, протяженные стриктуры с извитым ходом, а также стриктуры с эксцентричным расположением входа. В-третьих, полностью отсутствует лучевая нагрузка на больного и врача
Специалист выполняет исследование используя эндоскоп небольшого диаметра. Во время исследования оценивается локализация верхнего края сужения, диаметр суженного участка и его протяженность (по возможности).
Важной задачей для специалиста является проведение эндоскопа через сужение, т.к. это позволит не только установить протяженность стриктуры, но и оценить её ход, направление, убедиться в отсутствии двойных или множественных сужений, свищевых ходов, дивертикулов, что позволит избежать осложнений. Если эндоскоп провести за сужение не удается, то делается попытка проведения струны вслепую, что также является безопасным для пациента, т.к. проведение струны осуществляется её мягким концом. В редких случаях струну не удается провести через сужение, что наблюдается, например, при полном рубцовом сращении, либо при выраженном изгибе и извитости участка сужения, всё это рассматривается как противопоказание для выполнения бужирования и пациенту назначается рентгенологическое исследование с водорастворимым контрастным веществом для установления причины возникших трудностей.
Бужирование начинается с проведения бужа малого диаметра, не превышающего диаметр наиболее суженного участка. Затем буж заменяют на следующий, большего диаметра. За один сеанс применяется от 2 до 3 бужей. При бужировании специалист определяет степень ригидности стриктуры по мануальным ощущениям, что позволяет ему контролировать прилагаемое усилие, ограничивая насильственное преодоление чрезмерного сопротивления рубцовых тканей, и таким образом повышает безопасность вмешательства.
Во время проведения бужирования пациент может испытывать умеренные болевые ощущения.
Продолжительность и периодичность лечения
Длительность и специфика лечения во многом зависит от индивидуальных особенностей пациента и конкретной картины заболевания. Лечение в целом состоит из основного и поддерживающего курсов и завершается динамическим наблюдением.
Наши результаты
Бужирование является высокоэффективной лечебной процедурой. Специалисты нашего отделения достигают хороших результатов в решении таких сложных задач, как:
Возможные осложнения
Процедура бужирования, если она выполняется по проводнику, с поэтапным переходом от меньшего бужа к большему без излишнего форсирования, является наименее травматичным и наиболее безопасным методом лечения стриктур полых органов и анастомозов. В процессе выполнения процедуры обычно возникают неглубокие продольные надрывы рубцово измененной слизистой в области анастомоза или на поверхности стенки органах, и которых отмечается кратковременное незначительное подтекание крови, останавливающееся самостоятельно. Однако осложнения все же возможны, и самым серьезным считается перфорация стенки органов, для устранения которой может потребоваться оперативное вмешательство, а также кровотечение из краев глубокого разрыва слизистой, с которым почти всегда удается справиться эндоскопически.
Подготовка к процедуре
Бужирование верхних отделов желудочно-кишечного тракта проводят строго натощак, полностью исключается прием пищи за 12 часов и жидкости за 6 часов до начала процедуры. Если Вы не отмечаете выраженных затруднений при прохождении пищи по пищеводу или задержки пищевых масс в желудке на долгий срок, то последний прием пищи накануне может быть не позднее 18.00. Если вы отмечаете у себя вышеуказанные симптомы, то последний прием пищи в виде легкого обеда должен быть не позднее 13.00 в день накануне процедуры.
Процедура бужирования стриктуры толстой кишки или межкишечного анастомоза проводится только после очищения толстой кишки. Как выполнить подготовку толстой кишки см. «подготовка к колоноскопии» в разделе «колоноскопия». При низко расположенных стриктурах толстой кишки, а также в случае критических стриктур диаметром не более 4-5 мм (особенно если Вы отмечается систематическую длительную задержку отхождения стула и газов) подготовку толстой кишки следует проводить с помощью клизм.
Необходима отмена пероральных антикоагулянтов (препаратов для разжижения крови) накануне исследования, пауза п/к введения гепарина за 4-6 часов до процедуры
Баллонная дилатация стриктур желудочно-кишечного тракта может быть выполнена под внутривенной анестезией. Если исследование будет проводиться под наркозом, прием любого количества жидкости до процедуры строго воспрещен. Управление транспортным средством после окончания исследования является нежелательным и может представлять угрозу для жизни и здоровья.
Приобретенные гортаннотрахеальные стенозы у детей
Обзор литературы Приобретенные гортаннотрахеальные стенозы остаются одной из сложнейших проблем детской оториноларингологии. Это связано не только с трудностью и многоэтапностью восстановления просвета дыхательных путей, но и с сочетанным с дыхательным
Обзор литературы
Приобретенные гортаннотрахеальные стенозы остаются одной из сложнейших проблем детской оториноларингологии. Это связано не только с трудностью и многоэтапностью восстановления просвета дыхательных путей, но и с сочетанным с дыхательным стенозом и длительным трахеальным канюленосительством развитием патологических изменений в других органах и системах организма. Такие изменения приводят к инвалидности и социальной неполноценности, что требует тесного взаимодействия специалистов нескольких педиатрических дисциплин, таких, как оториноларингология, анестезиология, реаниматология, хирургия, пульмонология, гастроэнтерология, генетика [5, 10, 13, 18].
Ведущей причиной формирования рубцовых стенозов гортани является продленная чрезгортанная назотрахеальная интубация, проводимая по поводу острого стенозирующего ларинготрахеобронхита, операций и иных экстремальных ситуаций, требующих реанимационных мероприятий и искусственной вентиляции легких [5, 7, 11, 13, 33]. Повреждение тканей гортани при проведении интубации возникает в случае превышения капиллярного давления. Это вызывает ишемию тканей с последующим развитием воспаления, отека, изъязвления слизистой оболочки и дальнейшим возникновением хондроперихондрита и некроза, что можно сравнить с развитием «гортанного пролежня» [14]. Кроме того, стенозы могут быть связаны со спортивной, бытовой, транспортной и медицинской травмами [2, 14, 34, 35].
При бактериологическом исследовании отделяемого из трахеи у детей, нуждающихся в восстановительном лечении по поводу рубцового стеноза гортани, отмечается полимикробная флора (до восьми типов микроорганизмов одновременно), в том числе сочетание как аэробной, так и анаэробной флоры [15]; при этом, характер микробной флоры у детей и взрослых различается. Чаще всего у детей инфицирование происходит Pseudomonas aeruginosa, Staphylococcus aureus, Acinetobacter и Haemophilus influenzae [31].
Рентгенографическое исследование, являющееся наиболее распространенным дополнительным методом диагностики [2, 44], в связи с малой контрастностью тканевых структур гортани не всегда дает объективную картину [42], а ультразвуковое исследование гортани к настоящему времени еще не получило широкого распространения [4]. «Золотым стандартом» диагностики рубцового стеноза гортани и трахеи являются прямая микроларингоскопия и трахеобронхоскопия с использованием операционного микроскопа и оптических трубок [13, 18, 23, 36]. Эти методы позволяют точно оценить протяженность и степень стеноза, его характер и локализацию; следует также иметь в виду, что у 1/5–1/2 пациентов возможны комбинированные поражения на различных уровнях дыхательных путей [18, 23].
В результате повреждения дыхательных путей могут формироваться различные виды обструкции. Повреждения гортани у новорожденных и детей младшего возраста часто (до 22% случаев) протекают с явлениями хондроперихондрита, лечение которого включает в себя противовоспалительную и гормональную терапию [9]. У детей младшего возраста эндоскопическое бужирование гортани в сочетании с противовоспалительным лечением в процессе формирования рубцовой ткани при ее незрелости и остаточных воспалительных процессах на ограниченном участке может оказаться эффективным. В то же время диффузный перихондрит хрящевого каркаса гортани и сформировавшийся рубец являются противопоказаниями к проведению бужирования [11].
Наиболее тяжелое осложнение чрезгортанной интубации трахеи и трахеостомии — это развитие рубцового стеноза. Рубцы могут локализоваться в различных отделах дыхательных путей — между черпаловидными хрящами, на уровне голосовых складок, в подскладковом отделе, в шейном и грудном отделах трахеи [14, 32]. По данным Э. А. Цветкова (1996), более чем у 70% больных детей рубцовый процесс занимает подголосовой отдел гортани и гортаннотрахеальное сочленение. Согласно исследованиям А. Д. Понкратенко, Е. К. Онуфриевой (1997), среди 183 детей с рубцовым стенозом гортани рубцы локализовались в голосовом отделе у 36 больных, в подскладковом — у 118, сочетанное поражение разных отделов гортани отмечено у 29 пациентов.
Хирургическое устранение рубцового стеноза возможно двумя принципиально разными доступами — через естественные пути или с рассечением гортани и трахеи. Эндоскопические хирургические вмешательства при рубцовых стенозах всегда предпочтительнее эндоларингеальных с наружным доступом [11, 29]. Прямая микроларингоскопия и эндоларингеальная микрохирургия, особенно с использованием лазерной техники, позволяет у значительной части больных устранить рубцовый стеноз гортани и гортаннотрахеального отдела с достаточно хорошим функциональным эффектом. Лазерные операции практически бескровны, отличаются малой травматичностью и вследствие этого не сопровождаются выраженными реактивными явлениями. Другим преимуществом лазерных операций по сравнению с операцией наружным доступом является интактность хрящевого остова, что способствует более быстрому заживлению и восстановлению просвета гортани, позволяя максимально сохранить голосовую функцию [13]. Особенности процессов репарации после лазерных операций дают возможность у большинства больных, в том числе у детей младшего (до трех лет) возраста, восстанавливать просвет дыхательных путей без дополнительного применения стентов [1, 9, 13], хотя в ряде случаев их приходится использовать для поддержания воссозданного просвета [6, 48]. Лазерная хирургия рубцовых стенозов эффективна также в случаях, когда предыдущие операции с применением других методик не дали хорошего результата [37]. Катамнестические наблюдения свидетельствуют о том, что воссозданный с помощью лазерной операции просвет дыхательных путей сохраняется с ростом гортани и обеспечивает нормальную дыхательную функцию [5].
Одним из главных критериев отбора больных для эндоскопической лазерной хирургии является протяженность рубца, которая не должна превышать 1,5-2 см [1, 7, 13, 25]. Лечение оказывается малоэффективным при вовлечении в рубцовый процесс хрящевого скелета [7]. Кроме того, необходимо учитывать фазу формирования стеноза. В тех случаях, когда имеются явления хондроперихондрита, вопрос о необходимости лазерной операции целесообразно отложить до ликвидации воспалительных явлений [9]. Предпочтительнее всего проводить операцию через год и более после травматического повреждения гортани и формирования стеноза, однако положительного результата удается достичь и при лечении детей в ближайшие сроки (до двух месяцев) после травмы дыхательных путей [12]. При анализе результатов повторных операций по поводу рубцового стеноза гортани отмечается определенная связь: при неэффективном первичном хирургическом вмешательстве в 50% наблюдений результат повторной операции оказывается аналогичным. Показанием к повторной операции является хотя бы минимальный эффект от предыдущей — небольшое увеличение просвета дыхательной трубки [13, 29]. При удовлетворительном результате первичной операции повторная в 80-90% наблюдений приводит к дальнейшему улучшению [12].
Показаниями к операции по устранению рубцового стеноза гортани наружным доступом служат протяженный (более 1-3 см) рубец, потеря хрящевой опоры выше или в области трахеостомы, отсутствие эффекта от эндоскопических операций, в том числе проводимых с помощью лазера [13, 26]. В литературе имеется скудная информация об оптимальных сроках подобных операций у детей. В то же время случаи возникновения различного рода осложнений и гибели детей при случайной деканюляции или закупорке трахеотомической трубки коркой наблюдаются достаточно часто и составляют до 4,6% [49]. Ларингостомия и длительное формирование просвета гортани с применением Т-образной трубки у детей затруднены, так как относительно толстые стенки трубки суживают и без того неширокий просвет дыхательных путей, вызывая развитие дисфагических явлений, бронхитов, аспирационных пневмоний, асфиксии [41]; применение Т-образных трубок эффективно только у 50% пациентов в возрасте до 10 лет по сравнению с 80% больных старше 10 лет [20]. Реконструктивные операции у детей младшего возраста имеют высокий статистически значимый риск неудачи, несмотря даже на меньшую тяжесть повреждения дыхательных путей, по сравнению со старшими детьми [50]. В то же время некоторые авторы рекомендуют оперировать детей раннего возраста как можно раньше в целях восстановления нормального речевого общения; при этом хронические трахеоканюляры, по сравнению с ранее не трахеотомированными больными, требуют более агрессивной тактики лечения; они имеют меньше шансов на успех операции, у таких больных чаще развиваются осложнения в послеоперационном периоде [25]. Среди новорожденных и детей младшего возраста предрасполагающими факторами к развитию осложнений являются вес меньше 4 кг и гестационный срок меньше 30 недель [28].
Для формирования стойкого просвета гортани осуществляются различные варианты редрессации печатки перстневидного хряща [8, 11, 46], ларинготрахеальной декомпрессии с расширением просвета дыхательных путей (в области как передней, так и задней стенки), в том числе путем пересадки аутохряща (реберного, ушной раковины, перегородки носа) [17, 19, 40], васкуляризированного трансплантата из тела подъязычной кости с грудинно-подъязычной мышцей [11, 24, 27] и других тканей. Наиболее частыми причинами неудач операций, проведенных наружным доступом, являются недостаточная предоперационная диагностика гортаннотрахеального стеноза, интраоперационные дефекты, ошибки, связанные с выбором типа и длины стента и длительностью его использования, склонность к развитию келлоидных рубцов, недостаточное послеоперационное наблюдение [16], а также такая сопутствующая патология, как ларингомаляция, трахеомаляция и пролапс черпаловидных хрящей [38]. В ряде случаев для успешной деканюляции требуется несколько повторных операций наружным доступом; лечение может затягиваться на десятки лет [22]. Противопоказаниями к операции наружным доступом являются незаконченный процесс рубцевания, тяжелые поражения ЦНС, заболевания легких, неизлеченное первичное заболевание, невозможность послеоперационного наблюдения и лечения [11, 25].
В последние годы появились сообщения об устранении обширных стенозов гортани и трахеи у детей путем резекции стенозированного участка с последующим наложением межтрахеального и гортаннотрахеального анастомозов [30, 39]. Показанием к операции является изолированный подскладковый или трахеальный стеноз, расположенный как минимум на 10 мм ниже голосовых складок; протяженность стеноза должна быть от 1 до 6 см [45]. При формировании анастомоза между гортанью и трахеей возникают значительные трудности из-за несоответствия размеров сшиваемых концов. Эти операции в основном используются при лечении взрослых больных; к настоящему времени отдаленные результаты такого лечения у детей еще не изучены (хотя эксперимент на кроликах показал адекватный рост дыхательных путей после резекции перстневидного хряща и первого кольца трахеи [47]), у них высок риск развития дигисценций в области анастомоза, повреждения возвратных нервов; кроме того, в случае неудачи операции дальнейшее лечение крайне затруднительно [18]. Даже незначительный отек тканей в месте анастомоза может вызывать у ребенка выраженный дыхательный стеноз, связанный с малым диаметром трахеи; при этом трахея ребенка менее толерантна к растяжению, чем у взрослого, в связи с чем резекция у ребенка возможна лишь на относительно меньшей, по сравнению со взрослым, части трахеи [21]. По мнению В. Г. Зенгера (2001), при циркулярной резекции трахеи и дополнительной мобилизации подъязычной кости происходит вмешательство в очень сложный механизм, обеспечивающий одну из важнейших функций гортани — защитную, так как возникает опасность проявления аспирационных осложнений. В случае возникновения осложнений необходимо дополнительное разобщение отрезков воздухопроводящих путей, т. е. выполнение трахеостомии и введение трахеальной канюли с раздувной манжеткой, что сводит на нет все преимущества столь сложной и небезопасной для больного операции. Поэтому возможность частичной резекции дыхательных путей с наложением анастомоза должна рассматриваться лишь в качестве крайнего варианта [3].
Несмотря на использование различных по технике операций, эффективность устранения рубцового стеноза гортани и деканюляции достигает, согласно наблюдениям различных авторов, 63–64 % [5, 11, 18, 43]. На эффективность лечения влияют степень сужения дыхательных путей и протяженность стеноза: если при стенозе гортани до 70% просвета удается деканюлировать до 100% детей, то при полной атрезии органа эффективность оперативного вмешательства снижается до 67% деканюлированных больных (в том числе и после повторных операций) [46]; кроме того, чем короче стенозированный участок, тем результативнее лечение [12]. По мнению B. Benjamin (1993), при сочетанном поражении складкового и подскладкового отделов гортани, особенно при их тотальной облитерации рубцовой тканью, реконструктивные операции достигают успеха приблизительно в 50% случаев.
Лечение стриктур (сужений) пищевода
В лечении послеожоговых рубцовых стриктур пищевода основное место занимает бужирование, которое приводит к стойкому выздоровлению 70–80% больных с короткими (до 5 см) стриктурами.
Различают раннее и позднее бужирование.
Бужирование показано тем больным с ожоговыми стриктурами пищевода, у которых удается провести через сужение в желудок металлическую струну-проводник.
Бужирование абсолютно противопоказано при рубцовых стриктурах, осложнившихся свищами пищевода (пищеводно-медиастинальные, пищеводно-плевральные и пищеводно-респираторные свищи). Бужирование пищевода также противопоказано при стриктурах, сопровождающихся резко выраженным эзофагитом, при псевдодивертикулезе пищевода (опасность перфорации), подозрении на малигнизацию стриктуры.
Хороший эффект при коротких стриктурах оказывает также эндоскопическая баллонная гидростатическая дилатация. Введение баллонного дилататора в зону стриктуры осуществляют тремя способами: по инструментальному каналу эндоскопа, параллельно с эндоскопом и по направляющей струне, предварительно проведенной через зону стриктуры в желудок под контролем эндоскопа или рентгентелевидения.
У больных с гастростомой баллонный дилататор можно ввести в зону стриктуры и ретроградно. Необходимо отметить, что баллонную гидростатическую дилатацию можно проводить и при протяженных стриктурах, поэтапно расширяя один участок стриктуры за другим.
Неотложную помощь и лечение в остром периоде ожога пищевода начинают с противошоковых мероприятий в условиях реанимации. Проводят дезинтоксикационную терапию, одновременно необходимо попытаться удалить и нейтрализовать проглоченное химическое вещество.
При поступлении пострадавшего в первые несколько часов с момента травмы целесообразно промывание желудка через зонд большим количеством теплой воды. При сопутствующем ожоге дыхательных путей проводят аспирацию слизи из гортани и трахеи, экстренную трахеостомию по показаниям.
При полной дисфагии питание пациента осуществляют парентеральным путем через центральный венозный катетер.
Если через 5–7 дней пациент не в состоянии все еще глотать хотя бы жидкость, и отсутствуют условия для проведения длительного парентерального питания, накладывают гастростому. Во время операции необходима тщательная ревизия желудка для выявления его возможного ожогового поражения.
Во время острого периода ожога могут возникать различные тяжелые осложнения, требующие неотложного оперативного вмешательства: перфорация пищевода и желудка с развитием гнойного медиастинита и перитонита, профузное желудочное кровотечение (как правило, из острых язв). Иногда уже в начальном периоде болезни развивается пищеводно-респираторный свищ, что также требует наложения гастростомы для исключения питания через рот.
В настоящее время доказана рациональность раннего бужирования пищевода, которое начинают с 8–10 дня после ожога и проводят на протяжении 1–1,5 месяцев.
Одновременно назначают курс лидазы (обычно 12 дней). После окончания первого курса бужирования через 1,5–2 месяца проводят повторный курс лечения.
Понятно, что раннее бужирование возможно не у всех пациентов: при крайне тяжелом состоянии больного и развитии осложнений оно противопоказано.
Если не присоединились осложнения, к 3–5 дню воспалительные изменения в пищеводе начинают стихать, состояние пациента улучшается, становится возможным глотание.
К 10–15 дню отторгаются некротические участки слизистой, на их месте возникают изъязвления, выполненные грануляциями, к этому времени глотание становится почти свободным. Затем грануляции начинают замещаться плотной фиброзной соединительной тканью, которая постепенно превращается в рубец – формируется стриктура пищевода, которая часто локализуется в области его физиологических сужений – позади перстневидного хряща, на уровне аортального и наддиафрагмального сегментов.
Это происходит обычно из-за резкого рефлекторного спазма пищевода в ответ на попадание в просвет органа едкого химического вещества. Также нередки множественные сужения.