бусерелин или мирена что лучше
«Мирена» при эндометриозе
Добрый день!Очень нужна консультация по подбору гормонального препарата.
Мне 51 год.Три года назад мне был поставлен диагноз:узлова миома тела матки субсерозная форма. Полип эндометрия.
Это было выявлено на УЗИ.Миоматозный узел 17 мм. Также меня беспокоили обильные месячные.Было рекомендовано:Гистероскопия РДВ.
Сделали гистероскопию и выскабливание.Гистология показала-эндометриальный полип с «секреторной»гиперплазией желез без атипии.
Был назначен препарат Новинет на 3 месяца. После этого я чувствовала себя хорошо и к докторам не обращалась.
Но весной 2018 появились тянущие боли внизу живота,стала страдать запорами,и наконец стало кровить по середине цикла.
Обратилась к врачу,тут же сделали УЗИ.На Узи был виден полип,миома не выросла 18мм.Снова гистероскопия и выскабливание.
Гистология вновь показала железистый полип.
После мне было предложено поставить спираль » Мирена».Почитав в интернете про это чудо,закрались сомнения.Уж очень много побочных
эффектов,особенно настаражиает:головные боли и раздражительность.Просто не хотелось бы выбрасывать деньги на ветер (в случае: что у меня
будет побочка и придется вынимать спираль).Признаки Пременапаузы ужу есть:утомляемость,бросание в жар(хотя и не часто).Месячные пока
приходят вовремя.Рожала 2 раза.последний раз-кесорево и стерелизация(1997).Холестерин сейчас повышен 6.2.Еще гипертония 2 степени.Пью «твинста».
Посоветуйте альтернативную гормональную терапию.Или же все так ставить мирену?
Выбор эма или гормоны при миоме
Здравствуйте! Подскажите, пожалуйста, что в моей ситуации лучше, эма или гормоны. Мне 35, родов и беременностей не было. Доктор назначил Бусерелин депо 6 мес, но возможно есть шанс сделать эма? Насколько эффективна она при аденомиозе? В чем минусы и плюсы этих методов?
На УЗИ от 18.05 множественная миома, 2 субсерозных узла, самый большой 52*40*40 на широком 36 мм основании, субсерозно-интерстициальных 7, от 18*14 до 32*25*30, интерстициальных 4, самый большой 23*18.
Размеры матки 60*78*68
Аденомиоз, наружный эндометриоз брюшины кишечника 9*30, не спаян с маткой, хронический эндометрит
На сервисе СпросиВрача доступна консультация гинеколога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
2. эндометриоз на 100% никогда не излечить. Это хроническое заболевание. Оно как лирнейская гидра: отрубишь одну голову, вскоре на её месте вырастет другая. Поэтому вопрос с эндометриозом надо пытаться решать консервативно.
Наши задачи:
— удалить или уменьшить очаг эндометриоза
— уменьшить интенсивность болей
Консервативных методик несколько. Так как эндометриоз это заболевание, вызванное нарушением гормонального статуса, то не надо удивляться, что большинство вариантов – лечение гормональными препаратами.
1. НПВС. Применяются если есть выраженный болевой синдром.
2. Диеногест (Визанна, алвовизан или зафрилла). На мой взгляд, это лучший вариант. Он блокирует воздействие эстрогена на эндометриоидные очаги. В отсутствие гормональной подпитки они перестают расти. При продолжительном применении вызывает начальную регрессию ткани эндометрия с последующей атрофией эндометриоидных очагов. В аннотации заявлена длительность применения 15 месяцев без перерыва, но клинические наблюдения сообщают о безопасном применении на протяжении гораздо более длительного срока.
3. аГнРГ. Инъекционные препараты (1 укол раз в 28 дней), вызывающие исскуственный климакс. С точки зрения подавления эндометриоза работают хорошо. С точки зрения качества жизни – не очень. Чаще всего назначаются после оперативного лечения. И на отмену рекомендуется сразу беременеть.
4. ВМС «Мирена». Применяется при отсутствии ближайших планов на беременность. Рассчитана только на маточную и ректовагинальную формы эндометриоза. Хорошо купирует боль.
5. Дидрогестерон (Дюфастон). При пероральном применении подавляет рост очагов и предотвращает развитие гиперплазии. Возможен к применению, если планируется беременность. Эффективно купирует боль. Однако его применение циклическое (с 16 по 25 день) никак не поможет ни в лечении, ни в профилактике.
6. КОК. Не самый лучший выбор, но возможный. Если нужна контрацепция
7. Хирургическое лечение. Проводится при
— больших размерах эндометриоидных кист
— при подготовке к ЭКО
— при неэффективности консервативной терапии
Относительно миомы же эффективно будет применение спирали и бусерелина. Так что учитывая отсутствие беременностей и необходимости в терапии и эндометриоза, и миомы, я бы рекомендовала выбирать из этих двух вариантов. В зависимости от того, насколько скоро планируется беременность и планируется ли вообще
Гормональное лечение при эндометриозе.
Эндометрий – внутренняя слизистая оболочка матки. В ней находится большое количество кровеносных сосудов. Разрастание эндометриоидной ткани за пределами полости матки вызывает патологическое состояние, которое называется эндометриозом.
Статистика показывает, что примерно 10-15% женщин в возрасте от 25 до 45 лет страдают от эндометриоза.
Заболевание характеризуется тяжелым гормональным сбоем и другими симптомами:
Гормоны при эндометриозе – практически обязательная часть лечения. Это физиологически обосновано, потому что заболевание относится к гормонозависимым. Его главная причина – избыточная выработка эстрогенов в организме женщины.
Врач назначает гормональное лечение эндометриоза для решения следующих задач:
Искусственное подавление менструации – суть гормонотерапии. Под действием активных веществ не происходит физиологического отторжения слизистой оболочки матки. Очаги ее разрастания за пределами матки не кровоточат, и организм восстанавливается.
К другим способам терапии относятся:
Медикаментозное лечение эндометриоза включает несколько групп гормональных препаратов. Врач подбирает схему лечения индивидуально с учётом ряда факторов:
Вылечить эндометриоз без гормонов сложно. Альтернативное лечение можно рассматривать лишь в качестве дополнительного. Его эффективность трудно прогнозировать. Не исключено дальнейшее развитие заболевания, рецидив.
Гормональные оральные контрацептивы при эндометриозе.
Лечащий врач перед определением схемы лечения назначает анализы, чтобы выявить, какие гормоны повышены. Каждая группа лекарственных средств для лечения заболевания имеет разное фармакологическое действие, поэтому самолечение недопустимо. Решение о консервативном лечении, хирургической операции принимает только квалифицированный специалист.
Преимущества и недостатки гормонального лечения эндометриоза
Эффективность препаратов при эндометриозе зависит от стадии развития заболевания. Самый высокий терапевтический эффект наблюдается на начальных этапах развития патологического процесса. Раннее выявление патологии помогает избежать хирургического вмешательства. Плюсами такого лечения являются:
Одновременно с лечебным эффектом гормональные таблетки при эндометриозе оказывают контрацептивное действие. Их назначают женщинам на поздних этапах развития заболевания в качестве предоперационной подготовки и в период реабилитации. После курса терапии организм женщины быстро восстанавливается: нормализуется менструальный цикл, сохраняется фертильность.
Лечение гормонами, как любое другое, имеет недостатки:
При длительном приёме гормонов у женщины развиваются побочные реакции. К самым распространённым относятся:
Противопоказания к лечению гормонами
Гормональную терапию назначают не всем пациенткам. Этот метод консервативного лечения эндометриоза имеет противопоказания:
Нежелателен прием гормонов женщинам, страдающим ожирением, курящим. К противопоказаниям относятся беременность, лактация, наличие онкологических заболеваний.
Лечение эндометриоза гормональными лекарственными средствами – наиболее эффективный способ. Существуют различные группы лекарственных средств, которые назначают для борьбы с недугом. Схема медикаментозной терапии подбирается только врачом.
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
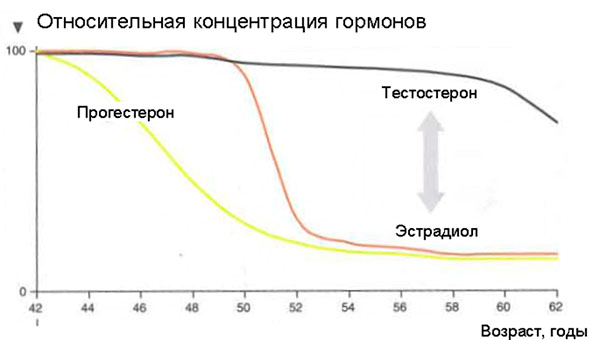
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
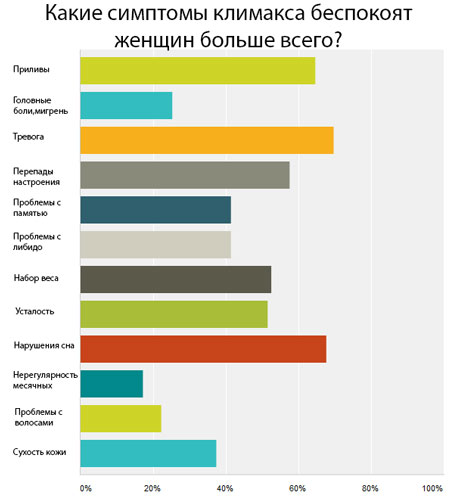
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
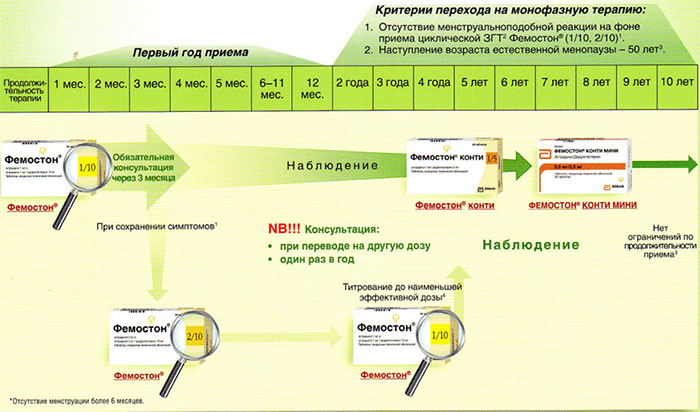
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
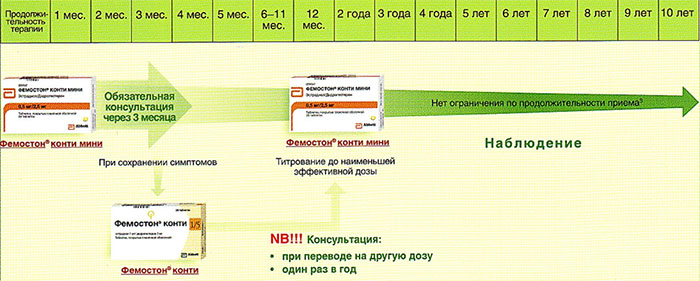
Препараты для монофазной терапии – когда месячные отсутствуют
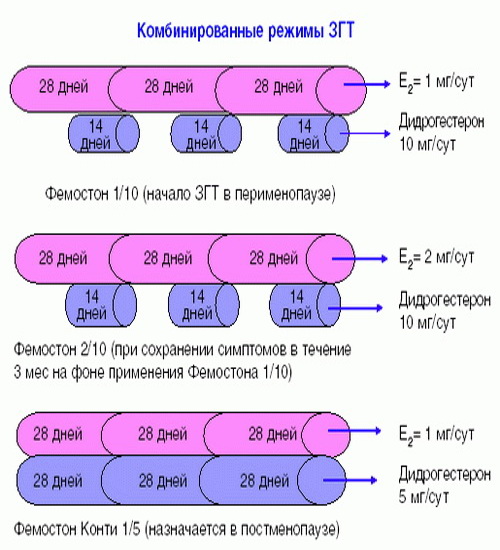
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).
Бусерелин или мирена что лучше
Современный подход к лечению больных эндометриозом состоит в комбинации хирургического метода, направленного на максимальное удаление эндометриоидных очагов, и гормономодулирующей терапии. Медикаментозная терапия (без хирургической верификации диагноза) возможна при аденомиозе и наружном генитальном эндометриозе, если отсутствуют кистозные процессы в яичниках и другие опухолевидные образования в малом тазу. При наличии эндометриоидной кисты яичника необходимо хирургическое лечение.
Поскольку в большинстве случаев заболевание начинается в раннем репродуктивном возрасте, основным условием лечения должно быть сохранение фертильности. Именно поэтому молодых пациенток по возможности следует вести консервативно, назначая медикаментозные средства. Медикаментозная терапия эндометриоза является неспецифической, нацелена в основном на уменьшение выраженности имеющихся симптомов, и подбирают ее индивидуально. Только в отсутствие положительного эффекта на протяжении 6 мес рассматривают вопрос о хирургическом вмешательстве [1—5].
Гормональную терапию применяют для временного подавления функции яичников с формированием состояния «псевдоменопаузы» или инициирования состояния псевдодецидуализации с последующей атрофией очагов эндометриоза — базис и этиопатогенетическая основа гормональной терапии. Согласно российским клиническим рекомендациям по ведению больных эндометриозом [6—9], гормональная терапия может быть использована в качестве эмпирической при лечении пациенток с симптомами, свидетельствующими о высокой вероятности наличия эндометриоза без кистозных (овариальных) форм, а также в качестве противорецидивной терапии после лапароскопического удаления видимых очагов эндометриоза, капсулы эндометриоидной кисты либо удаления очагов эндометриоза при инфильтративной форме заболевания.
В качестве гормональной терапии применяют препараты первой линии — прогестины, комбинированные оральные контрацептивы (КОК), нестероидные противовоспалительные средства (НПВС) и препараты второй линии — агонисты гонадотропин-рилизинг-гормона (аГнРГ) (при курсе более 6 мес в сочетании со средствами для заместительной гормональной терапии), левоноргестрел-высвобождающую внутриматочную терапевтическую систему. Оптимальным выбором при легкой и умеренной тазовой боли, предположительно вызванной гетеротопиями, могут служить КОК и прогестины.
Комбинированная терапия эстрогенами и прогестагенами
Механизм лечебного действия КОК — центральный (антигонадотропный, связанный со снижением пиковой секреции лютеинизирующего гормона) и периферический (антипролиферативный и противовоспалительный эффекты, обусловленные взаимодействием прогестагенного компонента с рецепторами прогестерона). В результате такой терапии наблюдаются подавление овуляции, снижение влияния эндогенных эстрогенов, торможение пролиферации эндометрия, изменение структуры эндометриоидных очагов, снижение выраженности хронической тазовой боли, улучшение физического и психологического состояния (стабилизация эмоционального статуса, обеспечение контроля течения предменструального синдрома и предменструального дисфорического расстройства). Кроме того, прием КОК способствует формированию искусственного менструального цикла, обеспечивает надежную контрацепцию. Препараты безопасны при длительном приеме, после их отмены быстро восстанавливаются менструальный цикл и фертильность. Предпочтительнее непрерывный режим приема КОК [6—13].
Прогестагены
Прогестагены считаются первой линией терапии с уровнем доказательности 1а. Во-первых, прогестагены оказывают центральное действие, блокируя гипоталамо-гипофизарно-яичниковую цепь, что снижает секрецию эстрогенов яичниками [14, 15]. Во-вторых, они оказывают непосредственное влияние на эндометриоидные очаги, стимулируя дифференцировку стромальных клеток (децидуализацию) и секреторную трансформацию эпителиальных клеток эндометрия, что, в конечном счете, приводит к его атрофии. В-третьих, прогестагены активируют 17β-гидростероиддегидрогеназу 2-го типа (17β-ГСД-2), преобразующую эстрадиол в менее активный эстрон. Прогестагены оказывают ингибирующее влияние на синтез простагландина E2 (ПГE2), играющего ключевую роль в патогенезе эндометриоза и способствующего повышению синтеза эстрогенов за счет модулирующего влияния на экспрессию ароматазы [16—18].
Терапию прогестагенами необходимо осуществлять в непрерывном режиме и в достаточно высоких дозах, на фоне которых развивается аменорея, что позволяет купировать болевой синдром, предотвратить распространение новых поражений, обеспечить регресс уже имеющихся очагов. Наиболее частым побочным эффектом непрерывного приема прогестагенов являются кровотечения прорыва, вероятность возникновения которых снижается по мере увеличения продолжительности лечения. Среди прогестагенов для перорального приема можно выделить медроксипрогестерона ацетат, мегестерола ацетат, норэтистерона ацетат, дидрогестерон, диеногест, преимущества и побочные эффекты которых представлены ниже.
Медроксипрогестерона ацетат (МПА, Провера) применяется для купирования боли при эндометриозе. Считается, что эффективность МПА схожа с эффективностью КОК. МПА при пероральном приеме для коррекции эндометриоза необходимо применять в высоких дозах, что может привести к неблагоприятному влиянию на липидный профиль, связанному с проявлением андрогенных и глюкокортикоидных свойств препарата (увеличение массы тела, возникновение изменений настроения, депрессии и раздражительности), и на углеводный обмен (ухудшение толерантности к глюкозе). Этим обусловлен ряд ограничений, в частности МПА запрещен к использованию у женщин с ожирением и/или сахарным диабетом 2-го типа, которые принимают перорально сахароснижающие препараты [19, 20].
Мегестерола ацетат (Мегейс) является синтетическим прогестагеном. Считается, что действие препарата связано с наличием антилютеинизирующего эффекта, реализующегося через гипофиз. Существует указание о местном эффекте мегестрола, полученном при непосредственном введении прогестагенов в полость матки. Препарат нашел свое применение при паллиативном лечении рака эндометрия и рака молочной железы. В обычной практике для лечения эндометриоза активно не применяется.
Норэтистерона ацетат (НЭТА) — производное 19-нортестостерона 2-го поколения. Среди положительных эффектов приема этого препарата можно отметить снижение болевого синдрома при хронической тазовой боли, диспареунии, дисменорее и нарушениях желудочно-кишечного тракта. К отрицательным моментам можно отнести метаболические нарушения в виде увеличения массы тела, дислипидемии, гиперинсулинемии при приеме в небольшой дозе в непрерывном режиме [10, 11, 21, 22].
Дидрогестерон (Дюфастон) избирательно воздействует на эндометрий, что позволяет предотвратить повышенный риск развития гиперплазии эндометрия и/или карциногенеза в условиях избытка эстрогенов. Является препаратом выбора во всех случаях эндогенной недостаточности прогестерона [23, 24].
Диеногест (Визанна) является прогестагеном 4-го поколения и объединяет фармакологические свойства группы прогестерона и прогестероноподобных соединений, а также производных 19-нортестостерона. Специфичность его действия дополняется минимальными влияниями на метаболические параметры. Диеногест — первый гестаген, который вызывает клинически значимый антиандрогенный эффект, не проявляя эстрогенной и андрогенной активности. Исследования показали, что диеногест оказывает ановуляторное и антипролиферативное влияние за счет подавления секреции цитокинов в строме эндометриальных клеток [15, 25]. Диеногест характеризуется хорошей переносимостью, отсутствием негативных метаболических и сосудистых эффектов, относительно умеренным ингибирующим действием на секрецию гонадотропинов, а также сильным прогестагенным влиянием на эндометрий и высокой биодоступностью при приеме внутрь (более 90%) [26, 27]. Диеногест также оказывает антиангиогенное, противовоспалительное, иммуномодулирующее, обезболивающее действие. Диеногест в дозе 2 мг/сут купирует связанную с эндометриозом боль (при дисменорее, диспареунии и диффузной тазовой боли), значительно уменьшает распространенность эндометриоидных очагов и не уступает по эффективности аГнРГ [28—37]. Препарат подходит для долгосрочного лечения эндометриоза (в сочетании с препаратами кальция и витамином D3), поскольку его хорошо переносят больные, и он не оказывает негативного влияния на метаболический профиль и функцию печени. Частота возникновения кровотечений прорыва сопоставима с таковой при лечении другими прогестагенами и снижается по мере увеличения длительности терапии.
Среди прогестагенов для парентерального применения можно выделить медроксипрогестерона ацетат (Депо-Провера) в лекарственной форме с медленным высвобождением препарата и левоноргестрелвысвобождающую внутриматочную терапевтическую систему (Мирена).
Медроксипрогестерона ацетат (Депо-Провера) в лекарственной форме с медленным высвобождением препарата эффективен для купирования болевого синдрома, связанного с эндометриозом. Среди негативных эффектов этого препарата можно выделить длительные и обильные кровотечения прорыва, которые с трудом поддаются коррекции, поскольку эффект прогестагена не может быть быстро и полностью нивелирован. В связи с этим данный препарат рекомендуется пациенткам с остаточным эндометриозом после оперативного удаления матки, поскольку исключается возможность кровотечений прорыва [19, 20].
Левоноргестрелвысвобождающая внутриматочная терапевтическая система (Мирена). Левоноргестрел — представитель 2-го поколения гестагенов, относится к классу 19-норстероидов и является самым активным из известных в настоящее время гестагенов. Левоноргестрел оказывает сильное антиэстрогенное и антигонадотропное действие, что обеспечивает контрацептивный и лечебный эффекты.
Мирена является высокоэффективным средством, предназначенным для длительного использования, и оказывает контрацептивное, лечебное и профилактическое действие. Внутриматочная терапевтическая система Мирена представляет собой Т-образную полиэтиленовую конструкцию с контейнером, содержащим левоноргестрел. Через специальную мембрану, покрывающую контейнер, осуществляется непрерывное контролируемое высвобождение левоноргестрела 20 мкг/сут, который поступает непосредственно в полость матки и приводит к атрофии эутопического и эктопического эндометрия, уменьшению кровопотери во время менструации и развитию аменореи у некоторых пациенток. Длительность использования Мирены составляет 5 лет, после чего можно продолжить лечение, введя новую систему. Побочные эффекты схожи с таковыми при непрерывном режиме использования других прогестагенов [43—45].
В лечении эндометриоза эффективны гестагены без андрогенной активности. К ним относятся ципротерона ацетат, дидрогестерон, медроксипрогестерона ацетат и диеногест. Диеногест оказался наиболее эффективным как для профилактики, так и для лечения эндометриоза. Рекомендуемые дозы большинства пероральных прогестагенов для лечения эндометриоза достаточно высокие, что не отвечает современным требованиям, предъявляемым к препаратам (максимальный эффект при минимальной дозе). В наиболее низкой дозе используют диеногест (Визанна, 2 мг/сут) и левоноргестрел (внутриматочная терапевтическая система Мирена, 20 мг/сут).
Антигонадотропины
Наиболее широкое применение из препаратов этой группы нашел препарат Гестринон. Гестринон (Неместран) — стероидный гормон, производное 19-нортестостерона, снижает выведение гонадотропина, что приводит к атрофии эндометрия (дисменорея, диспареуния, меноррагия купируются в первые месяцы лечения). Оказывает андрогенное, антиэстрогенное и антигестагенное действие. Влияет на эктопические имплантаты вне матки. Препарат назначают в непрерывном режиме в 1-й и 4-й дни менструального цикла в дозе 2,5 мг, затем 2 раза в неделю по установленным дням в течение 6 мес.
Длительность применения препарата ограничена из-за выраженных побочных эффектов: головная боль, повышенная возбудимость, раздражительность, депрессия, судороги, задержка жидкости, увеличение массы тела, уменьшение объема молочных желез, понижение тембра голоса, снижение либидо, повышение активности «печеночных» трансаминаз, «приливы» крови к лицу, тошнота, диспепсия, кровянистые выделения из матки в первые недели приема, пигментация кожи, акне, себорея, гипертрихоз [46, 47].
Агонисты гонадотропин-рилизинг-гормона
Препараты аГнРГ наиболее эффективны при лечении тяжелых и инфильтративных форм эндометриоза. Действие аГнРГ заключается в подавлении эстрогенной стимуляции для развития эндометриоза. Это состояние гипогонадотропного гипогонадизма лишает существующий эндометриоз поддержки эстрогенами и приводит к вторичной аменорее, предотвращая новый перитонеальный высев эндометриоидных очагов. На фоне лечения аГнРГ исчезают дисменорея, тазовые боли, через 3—4 мес — диспареуния, к концу курса лечения выраженность болевого синдрома снижается в среднем в 4 раза. Лечение с помощью аГнРГ не обеспечивает профилактику рецидивирования заболевания, особенно при глубоких формах эндометриоза. Частота возникновения рецидивов через 5 лет после окончания курса терапии составляет 53%, а при тяжелых инфильтративных формах — 73%.
В клинической практике используют Синарел, Золадекс, Диферелин, Декапептил депо, Бусерелин, Люкрин депо в виде депо-формы, внутримышечных инъекций, подкожных имплантатов, интраназального спрея. Терапия препаратами аГнРГ очень эффективна, однако сопровождается в качестве побочных эффектов признаками снижения уровня эстрогенов (приливы, сухость влагалища, головная боль, снижение либидо) и деминерализацией костной ткани. По этой причине перед назначением аГнРГ женщинам из группы риска развития остеопороза целесообразно проведение остеоденситометрии. Для уменьшения частоты и выраженности гипоэстрогенных побочных реакций без влияния на эффективность применения аГнРГ используется так называемая терапия «прикрытия» («add-back» терапия): низкие дозы эстрогенов и прогестинов, тиболон и т. д. Комбинация с терапией «прикрытия» дает возможность применять аГнРГ в течение более чем 6 мес, что необходимо при глубоких инфильтративных формах заболевания, тяжелом болевом синдроме, рецидивировании или персистенции очагов ретроцервикального эндометриоза и невозможности их полного удаления, до и после операции по поводу аденомиоза и прочее [48—52].
Обобщенные сведения о препаратах, применяемых для лечения эндометриоза, представлены в таблице. 
Лечение эндометриоза другими средствами является либо паллиативным (анальгетики, НПВС), либо экспериментальным (ингибиторы ароматазы, селективные модуляторы эстрогеновых рецепторов (СЭРМ), агонисты эстрогеновых рецепторов β (ЭР-β), антиангиогенные препараты и прочее). Современная фармакология предусматривает комплексную терапию эндометриоза с использованием иммуномодуляторов, противовирусных и гормональных препаратов [53—55].
Нестероидные противовоспалительные средства
НПВС назначаются для устранения болевого синдрома и менструальной кровопотери. НПВС снижают длительность и интенсивность менструальных кровотечений за счет блокады активности циклооксигеназы, что влечет за собой снижение синтеза простагландинов и обеспечивает прокоагулянтный эффект. Кроме того, препараты этой группы оказывают антиноцицептивное действие. Но недостатками НПВС являются ульцерогенное действие на слизистую оболочку пищеварительного тракта, угнетение почечного кровотока, а также краткосрочность лечебного действия, постепенное «привыкание» и снижение эффективности.
Витамин D
В настоящее время активно обсуждается связь уровня витамина D, агента с антипролиферативным, противовоспалительным и иммуномодулирующим действием, и эндометриоза — заболевания, имитирующего опухолевый рост и удовлетворяющего большинству критериев аутоиммунного заболевания [56].
Синтез витамина D, экспрессия рецепторов витамина D и 1α-гидроксилазы в нормальном циклически функционирующем эндометрии, регулирование ферментов и рецепторов витамина D в эутопическом эндометрии женщин с эндометриозом, характерный полиморфизм протеина, связывающего витамин D, проявляющийся дифференциальной экспрессией аллеля Gc2 в эндометриоидных очагах, обратная зависимость между развитием эндометриоза и уровнем 25 (OH)D в сыворотке крови в сочетании с увеличением уровня протеина, связывающего витамин D, в моче женщин с эндометриозом — все это свидетельствует в пользу потенциальной роли витамина D и его метаболитов как местных аутокринных/паракринных агентов, имеющих значение в этиологии и патогенезе эндометриоза.
В большинстве источников описана связь низкого уровня витамина D с развитием и тяжестью течения генитального эндометриоза. Прием витамина D сопровождается уменьшением болевых ощущений при первичной дисменорее путем ингибирования синтеза простагландинов. Витамин D также эффективен в купировании вторичной дисменореи или хронической тазовой боли при эндометриозе, обусловленной процессом нейроангиогенеза.
Терапия препаратами витамина D у пациенток с эндометриозом, особенно при низких уровнях 25 (OH)D в плазме, может позволить уменьшить дозу НПВС или отказаться от этой группы препаратов. Витамин D увеличивает вероятность наступления беременности при бесплодии, ассоциированном с эндометриозом, в том числе при применении методов вспомогательных репродуктивных технологий. Необходимо проведение крупных рандомизированных исследований применения витамина D при эндометриозе для более углубленного понимания механизмов действия и разработки оптимальных терапевтических доз. Применение витамина D может стать новой медикаментозной стратегией как в лечении, так и в первичной профилактике развития данного заболевания [56].
Нашими коллегами предложен следующий алгоритм диагностики и лечения эндометриоза. При подозрении на эндометриоз у пациентки с одним или несколькими клиническими симптомами (хроническая тазовая боль; дисменорея, влияющая на качество жизни; диспареуния; регулярные желудочно-кишечные симптомы, болезненность при дефекации; периодические проявления со стороны мочевой системы; бесплодие в сочетании с одним из вышеперечисленных симптомов) важно провести тщательное диагностическое обследование. В план обследования входят гинекологическое исследование, включая ректовагинальное; ультразвуковое исследование органов малого таза; оценка метаболизма железа (уровень гемоглобина, железа, ферритина общей железосвязывающей способности); магнитно-резонансная томографияи/или компьютерная томография органов малого таза (при подозрении на глубокий инфильтративный эндометриоз); лапароскопия и/или гистероскопия. Далее тактика ведения пациентки зависит от ее репродуктивных планов. Если у пациентки выявлен наружный генитальный эндометриоз I—II стадии, и она планирует беременность, то показаны прегравидарная подготовка и протокол стимуляции яичников с аГнРГ, гестагенная поддержка при вспомогательных репродуктивных технологиях. Если при наличии наружного генитального эндометриоза I—II стадии пациентка не планирует беременность, то выбор медикаментозного или хирургического лечения зависит в первую очередь от предпочтений самой пациентки, ей показана длительная противорецидивная терапия. При тяжелых формах (глубокий инфильтративный эндометриоз и т. д.) независимо от репродуктивных планов пациентки важен индивидуальный и мультидисциплинарный подход с привлечением смежных специалистов. Необходимо предусмотреть предоперационную гормональную терапию при вовлечении смежных органов, лапароскопическое лечение, противорецидивную терапию [57].
Заключение
До настоящего времени ни одна из предложенных стратегий лечения эндометриоза не привела к его полному излечению и не позволила избежать рецидивов, что обусловлено множественными полисистемными нарушениями, лежащими в основе его этиопатогенеза. В некоторых случаях единственным методом лечения эндометриоза может быть полная хирургическая ликвидация очага с последующим назначением гормональной противорецидивной терапии.
Финансирование. Работа выполнена при финансовой поддержке гранта — Конкурс 2018 г. «Проведение фундаментальных научных исследований и поисковых научных исследований отдельными научными группами». Название проекта «Современные клинико-морфологические и иммунобиологические аспекты генитального эндометриоза», № проекта 18−15−00165.
Концепция и дизайн статьи — Л.А., К.А., Э.Х., О.Л.
Сбор и обработка материала — К.А., Э.Х.
Написание текста — К.А., Э.Х.
Редактирование — К.А., О.Л.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.