бреф мутация что это
Мутации меланомы braf, c-kit, nras
Меланома — агрессивный рак кожи, который диагностируется у 2,5-10% пациентов и имеет высокую вероятность злокачественного течения. Для нее характерны стремительное прогрессирование и быстрый переход с 1 до 4 стадии развития.
Опасность мутации меланомы
Такой рак относится к самым агрессивным видам онкологии. Иммунная система человека слабо реагирует на меланому, из-за чего опухоль быстро развивается – от начальной стадии до опасной для жизни проходят недели, а в отдельных случаях дни. При меланоме довольно часто возникают рецидивы, а метастазы проникают практически во все органы.
Чтобы повысить вероятность благоприятного исхода и выздоровления, а также снизить риск метастазирования, важно своевременно проводить точную диагностику, в том числе на определение генной мутации.
Дело в том, что в основе развития заболевания нередко «повинны» генетические мутации. Поэтому в МеланомаЮнит большое значение уделяется генетической диагностике, позволяющей выявить причинно-следственные мутации и подобрать прицельное лечение. Этим задачам отвечает таргетная терапия — специально подобранные средства, воздействующие на клетки-мишени опухоли конкретного пациента, не затрагивая при этом здоровые ткани.
Чаще всего встречаются и активно используются в составлении плана лечения три генетические мутации: BRAF, NRAS и c-Kit.
Мутация BRAF
Самый распространенный вид мутации, который диагностируется у 40-70% пациентов с меланомой. Свое название BRAF получило от гена, участвующего в регуляции деления клеток за счет активации специфического сигнального пути. При изменении его структуры возникает мутация и процесс деления выходит из-под контроля.
обеспечивающий образование белка после мутации. Этот белок провоцирует патологический рост клеток, в результате которого формируется опухоль.
В норме ген BRAF неактивен, но при определенных обстоятельствах начинает «работать» и развивается меланома.
Мутация NRAS
На нее приходится около 15-20% случаев, и в основе лежит механизм «поломки» гена, который провоцирует активную выработку белка — активатора злокачественного роста и размножения клеток. При составлении схемы лечения одной из задач онколога блокировка синтеза протеинкиназы. В настоящее время препараты, воздействующие на данный вид мутации, проходят клинические испытания. Но уже на этом этапе специалисты отмечают положительные результаты и фиксируют замедление развития опухоли.
Мутация c-Kit
Меланома ассоциирована с мутацией c-Kit у 6-15% пациентов с меланомой, возникающей преимущественно на слизистой оболочке половых органов, прямой кишки и носоглотки, а также на кистях и ладонях. При диагностике такой мутации врач назначает препараты-ингибиторы c-Kit.
Очень важно выявить мутацию, так как в настоящее время существует прицельное лечение, позволяющее «блокировать» измененный ген. Использование этих препаратов позволяет блокировать патологически активированный сигнальный каскад, который запускается мутацией генов. Это в свою очередь тормозит развитие опухоли. Ранняя диагностика и своевременное лечение в таком случае позволяет значительно увеличить шансы на благоприятный исход заболевания.
Преимущества диагностики и лечения рака кожи в МеланомаЮнит:
Записаться на прием к дерматоонкологу МеланомаЮнит можно по телефону.
Мутация гена BRAF при меланоме
Частота и виды мутаций в гене BRAF
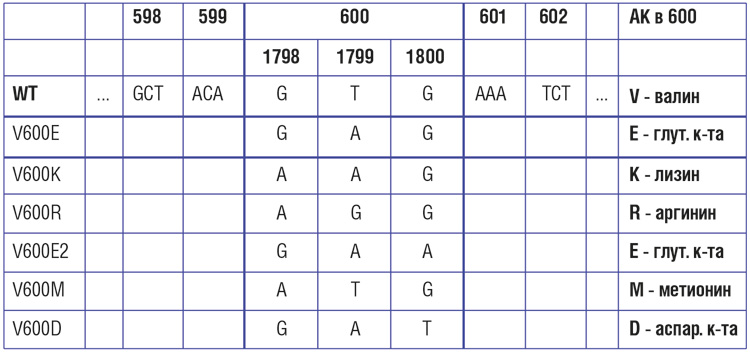
Частота мутаций в гене BRAF при меланоме кожи, по данным разных исследователей, варьирует от 30-40% до 70%. Наиболее распространенной (69-94% случаев) разновидностью BRAF-мутаций является V600E – замена валина на глутамин в 600-м кодоне. Эта мутация представляется доминирующей, но далеко не единственной разновидностью нарушений BRAF [14, 15]. Второй по частоте является мутация V600К – ее частота может достигать 5-10%. Мутации V600D и V600R встречаются значительно реже.
Cтатус мутации гена BRAF и выбор тактики лечения
За последние годы достигнуты значительные успехи в изучении патогенетических основ развития меланомы и сделан огромный шаг к выявлению новых потенциальных молекулярных мишеней. Открытие молекулярной мишени BRAF и понимание ее роли в патогенезе меланомы легли в основу разработки нового класса препаратов – низкомолекулярных ингибиторов мутированного фермента BRAF. Использование этих препаратов позволяет блокировать патологически активированный сигнальный каскад, который запускается мутацией BRAF V600, и, таким образом, тормозить развитие опухоли. Следует особо отметить, что воздействие данной группы препаратов на опухолевые клетки с нормальной последовательностью BRAF, напротив, может сопровождаться патологической активацией каскада RAS-RAF-MEK-ERK и провоцировать рост меланомы. Этот феномен свидетельствует об исключительной важности достоверной диагностики статуса гена BRAF.
BRAF ингибиторы не должны использоваться в тех случаях, когда статус мутации BRAF не определен или мутация не обнаружена!
Следует подчеркнуть, что ингибиторы BRAF и MEK зарегистрированы к применению только для терапии метастатической формы меланомы. В настоящее время отсутствуют данные по использованию ингибиторов BRAF и MEK в адъювантном режиме, поэтому они не могут быть рекомендованы пациентам, перенесшим (условно-)радикальное удаление первичной меланомы и метастических очагов.
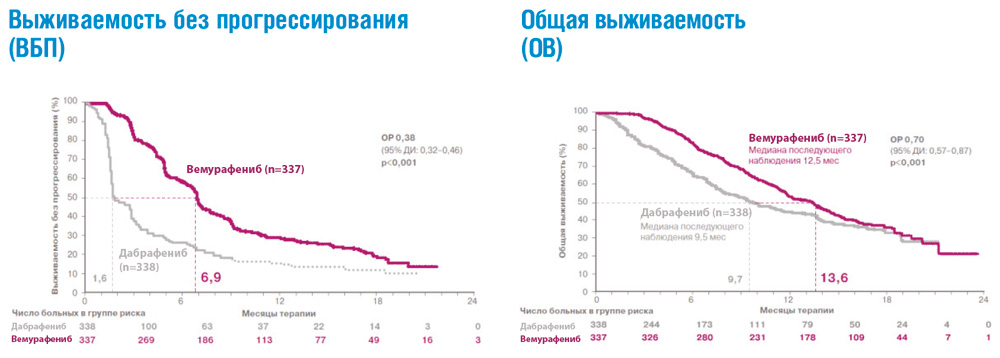
В рандомизированных клинических исследованиях ингибиторы BRAF – вемурафениб и дабрафениб – продемонстрировали значительное преимущество по сравнению со стандартной химиотерапией в отношении частоты объективных ответов, продолжительности жизни без прогрессирования и общей продолжительности жизни у пациентов с метастатической меланомой и подтвержденной мутацией гена BRAF, ранее не получавших системного лечения (см. рис. 2). Полученные результаты привели к пересмотру международных клинических рекомендаций, которые включили эти препараты в современные стандарты лечения метастатической меланомы кожи с BRAF мутацией.
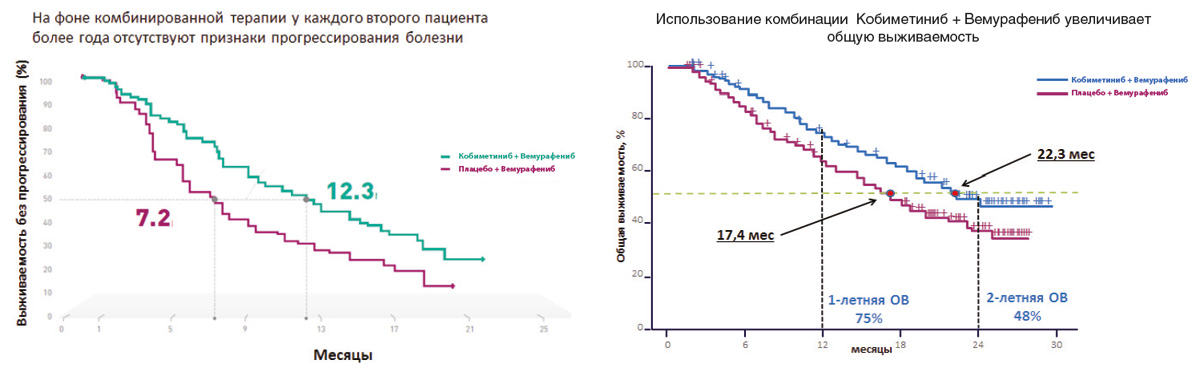
Результаты последних исследований показали, что двойное ингибирование сигнального пути MAРK, которое достигается при одновременном использовании ингибиторов BRAF и MEK, обладает более высокой эффективностью по сравнению с ингибитором BRAF в монорежиме. Важно отметить, что помимо более высокой эффективности комбинация препаратов снижает вероятность развития резистентности к проводимой терапии и отдельных нежелательных явлений, в том числе плоскоклеточного рака кожи. В рамках клинического исследования coBRIM было подтверждено, что комбинированная терапия с использованием препаратов вемурафениб и кобиметиниб в 90% случаев позволяет достичь ответа на терапию у больных BRAF+ метастатической меланомой. У каждого второго пациента более года отсутствовали признаки прогрессирования заболевания, а общая выживаемость приближалась к 2 годам (рис. 3).
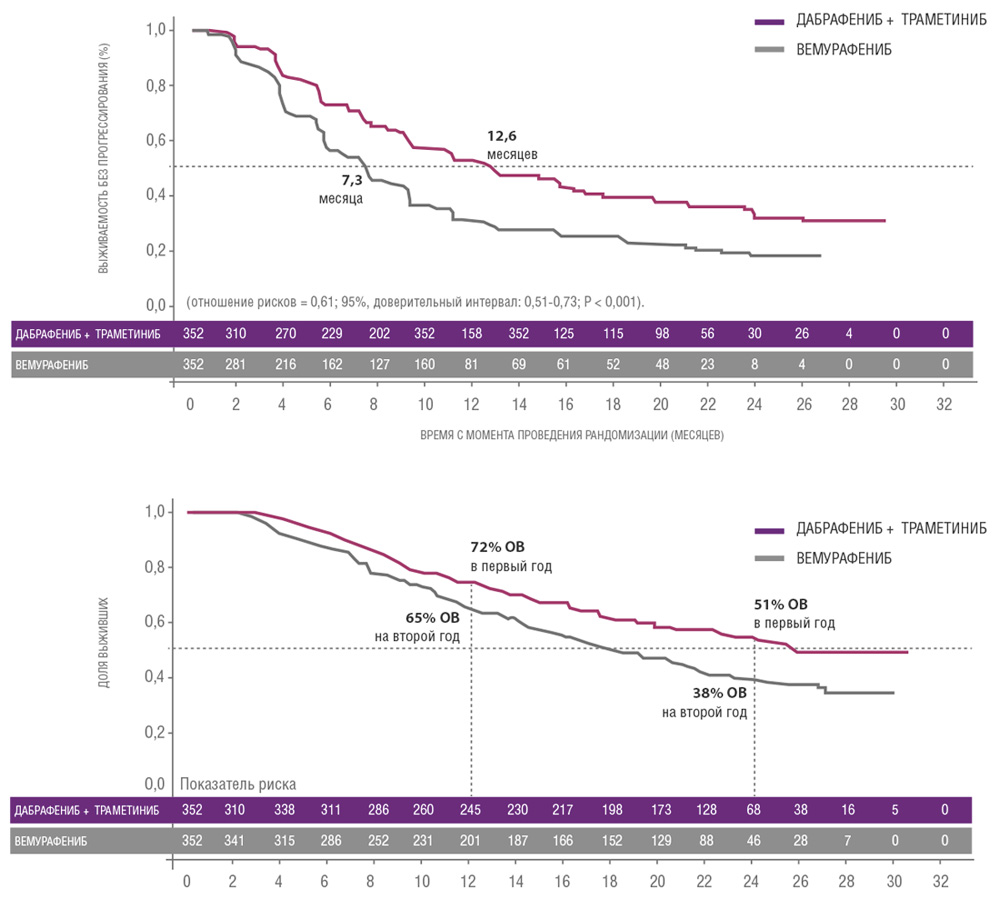
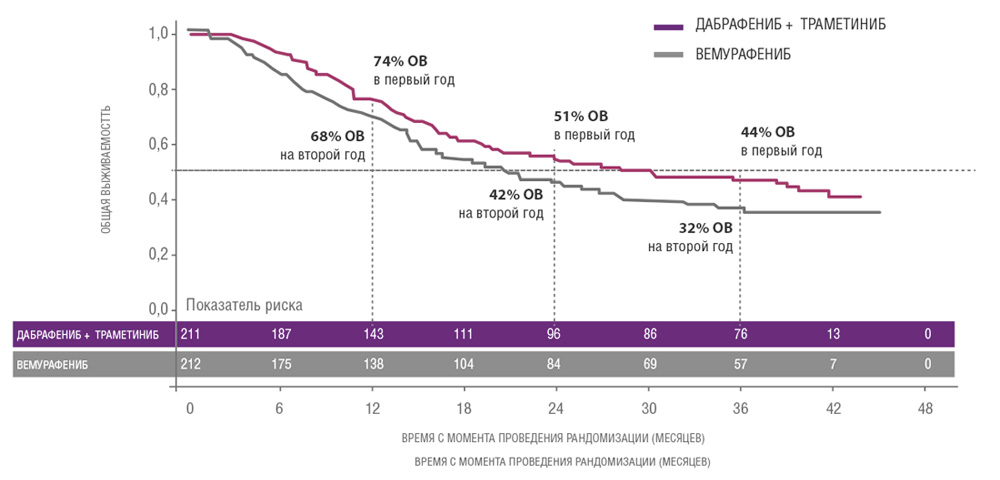
Сходные результаты были продемонстрированы в исследованиях дабрафениба и траметиниба. В частности, исследование COMBI-V (дабрафениб+траметиниб vs монотерапия вемурафенибом) продемонстрировало значимой увеличение общей продолжительности жизни у пациентов, получавших комбинированную терапию, по сравнению с применением вемурафениба без ингибитора MEK (25.6 мес. vs 18 мес.; рис. 4, табл. 1). В клиническом испытании COMBI-D сравнивалась эффективность комбинации дабрафениб+траметиниб по отношению к монотерапии дабрафенибом в сочетании с плацебо. Примечательно, что в этом исследовании были зарегистрированы практические идентичные показатели общей продолжительности жизни (25.1 мес. vs 18.7 мес.; рис. 5, табл. 1).
Определение статуса гена BRAF является обязательным компонентом выработки тактики лечения всех пациентов с неоперабельной/метастатической меланомой кожи.
Рисунок 2. Результаты рандомизированного исследования BRIM-3: сравнение эффективности вемурафениба и дабрафениба в 1-й линии терапии метастатической меланомы с мутацией BRAF.
Рисунок 3. Результаты рандомизированного исследования coBRIM: сравнение эффективности комбинации кобиметиниба+вемурафениба и вемурафениба+плацебо в 1-й линии терапии метастатической меланомы с мутацией BRAF.
Рисунок 4. Результаты клинического исследования COMBI-V: (дабрафениб+траметиниб vs монотерапия вемурафенибом).
Рисунок 5. Результаты клинического испытания COMBI-D: эффективность комбинации дабрафениб+траметиниб по отношению к монотерапии дабрафенибом в сочетании с плацебо.
Сводные данные по всем исследованиям представлены в таблице 1.
| Исследование | COMBI-d | COMBI-v | ||
|---|---|---|---|---|
| Препарат(ы) | Д + T | Д + пла | Д + T | В |
| Кол-во пациентов, n | 211 | 212 | 352 | 352 |
| Медиана ВБП, мес. | 11,0 | 8,8 | 12,6 | 7,3 |
| Медиана ОВ, мес. | 25,1 | 18,7 | 25,6 | 18,0 |
| Медиана ОВ, ЛДГ≤ВГН | Нет анализа | НД | 21,5 | |
| Медиана ОВ, ЛДГ>ВГН | 10,8 | 8,9 | ||
Сокращения: В – вемурафениб, К – кобиметиниб, Д – дабрафениб, Т- траметиниб, пла – плацебо, НД – не достигнута, ВГН – верхняя граница нормы.
Таким образом, использование BRAF/MEK ингибиторов у пациентов с мМК, имеющей BRAF мутацию, представляет первый успешный пример персонализированной терапии, изменившей представление о мМК как об опухоли, рефрактерной к лекарственному лечению. Эти препараты пришли на смену химиотерапии и стали новым стандартом лечения меланомы с BRAF мутацией, что подтверждает ранее сформулированный постулат о необходимости разработки различных подходов к лечению для различных молекулярно-генетических подтипов меланомы. Появляются результаты исследований таргетных препаратов и при других типах меланомы, имеющих альтернативные мутации (NRAS, cKIT). Можно ожидать, что определение молекулярно-генетического портрета опухоли уже в ближайшее время станет неотъемлимой частью разработки стратегии лечения каждого пациента, имеющего диагноз «меланома».
На сегодняшний день все существующие BRAF и MEK ингибиторы зарегистрированы на территории Российской Федерации и, при соответствующем лекарственном обеспечении, с успехом могут быть использованы для терапии мМК. Профиль безопасности этих препаратов позволяет использовать их в амбулаторных условиях.
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.
Мутация гена BRAF
Описание
Мутация гена BRAF — генетическое исследование предрасположенности к развитию злокачественных опухолей. Анализ наличия основных мутаций в генах BRAF. Результаты исследования позволяют выявить причину развития данной патологии и назначить своевременное адекватное лечение.
Ген BRAF
Один из белков основного сигнального пути, кодирует внутриклеточный белок. Белок BRAF имеет киназную активность, которая формирует основной сигнальный путь, активирующий рост и отвечающий за сохранение клеточных элементов. При развитии мутации, патологический ген начинает продуцировать активированный белок. Этот белок запускает механизм избыточного переноса сигнала к факторам роста. Результатом является в несколько раз ускоренное размножение клеток и рост новообразования.
Мутации в гене BRAF связаны с развитием рака. Мутации в гене BRAF обнаруживаются у 40–70% больных меланомой.
Меланома — это одна из самых распространённых и опасных форм рака кожи. Ежегодно от этого заболевания умирает 37 000 человек во всём мире, причём многие из них погибают из-за несвоевременного обращения к специалисту. Однако до 90% трагедий можно избежать, если выявить рак на ранней стадии.
Наиболее частой активирующей мутацией гена BRAF является точечная нуклеотидная замена c.1799T>A, которая соответствует мутации V600E в белке BRAF. Мутация V600E вызывает постоянную активацию белка BRAF, даже в отсутствие факторов роста. Неправильный сигналлинг BRAF из-за мутации V600E может приводить к избыточной клеточной пролиферации и к ошибочной устойчивости к апоптозу. Мутации BRAF присутствуют в
50% опухолей меланомы,
40% папиллярно-тироидно опухолей,
30% опухолей яичников,
10% колоректальных опухолей,
10% опухолей простаты.
Показания
Тест на мутации гена BRAF рекомендуется пациентам с меланомой кожи, опухолях щитовидной железы, раком яичников, раком толстой и прямой кишки для оценки возможности терапии препаратами Вемурафениб и Дабрафениб.
Подготовка
Условия подготовки определяются лечащим врачом. Взятие биоматериала для данного исследования проводится лечащим врачом.
Необходим гистологический протокол.
Бреф мутация что это
Молекулярно-генетическое исследование биоптата опухолевой ткани для определения специфической мутации, которая играет роль в злокачественной трансформации клеток.
Генные мутации при меланоме, белок сигнального пути.
BRAF Mutation Testing, BRAF Gene Mutation Test, BRAF Gene Mutation Analysis.
Какой биоматериал можно использовать для исследования?
Биоптат опухолевой ткани в емкости с фиксирующим раствором или парафиновый блок с биоптатом ткани опухоли. Может использоваться как образец первичной опухоли, так и полученный из метастатического очага.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Современные успехи в лечении онкологических заболеваний во многом связаны с обнаружением молекулярных механизмов возникновения и развития злокачественных новообразований, отличающих их от клеток нормальных тканей, и появлением лекарственных препаратов, способных воздействовать на них. Такие лекарства называются таргетными, то есть действующими на определенную «цель» в опухолевой клетке. Они обладают хорошим профилем безопасности, так как, в отличие от стандартной химиотерапии, практически не действуют на нормальные ткани и характеризуются большей эффективностью. Однако назначение таргетных препаратов возможно лишь при обнаружении в опухолевых клетках специфической мишени для их действия. Кроме того, обнаружение в опухолевых клетках определенных генетических аномалий может использоваться как прогностический фактор.
Мутации гена BRAF характерны для меланом кожи (по разным данным, от 30 до 70%), колоректального рака, немелкоклеточного рака легкого (около 3%), а также для папиллярного рака щитовидной железы. Наиболее часто выявляется мутация гена BRAF V600E, вторая по частоте V600K, значительно реже встречаются V600D и V600R. Буквы в обозначении данных мутаций означают замену нормальной аминокислоты (валина) в шестисотом положении белка на другую. После открытия роли мутаций гена BRAF в патогенезе опухолей, в том числе меланомы, были разработаны новые препараты – низкомолекулярные ингибиторы мутированного фермента BRAF. Эли лекарственные средства блокируют патологически активированный сигнальный каскад, который запускается мутацией BRAF V600, и тормозят развитие опухоли. К BRAF-ингибиторам относятся вемурафениб (зелбораф) и дабрафениб.
Материалом для исследования служит ДНК опухолевых клеток. Она может быть выделена из биоптата опухоли, находящегося в парафиновом блоке. Если же на исследование предоставлен образец опухоли в емкости с фиксирующим раствором, из него изготавливаются парафиновые блоки для возможности длительного хранения и использования в последующем для других диагностических тестов.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Отрицательный результат – мутации не обнаружены.
Что может влиять на результат?
Нарушение техники фиксации биопсийного материала, которое может привести к деградации генетического материала и невозможности тестирования.
Цитологическое исследование материала, полученного при оперативном вмешательстве
Цитологическое исследование материала, полученного при эндоскопии (бронхоскопия)
Гистологическое исследование биопсийного материала
Гистологическое исследование доброкачественных образований кожи (папилломы, невусы и др.)
Гистологическое исследование биоптата лимфатического узла (1 узел) с использованием рутинных методик окраски
Определение перестройки гена ALK при раке легкого методом ИГХ
Кто назначает исследование?
Henry’s Clinical Diagnosis and Management by Laboratory Methods, 23e by Richard A. McPherson MD MSc (Author), Matthew R. Pincus MD PhD (Author). St. Louis, Missouri : Elsevier, 2016. Pages 1512-1513.
The Basic science of Oncology. Fifth edition. Ian F. Tannock, Robert G. Bristow, Richard P. Hill, Lea Harrington. McGrow-Hill Education, 2013. Pages 173-179.
Программа RUSSCO «Совершенствование молекулярно-генетической диагностики в российской федерации». Практическое руководство для врачей. www.cancergenome.ru
Доклад «Современные возможности таргетной терапии НМРЛ», Имянитов Е. Н. Вестник московского онкологического общества, №11 (602), 2013. С. 3-6.
Бреф мутация что это
BRAF, мутация BRAF, BRAFV600E, меланома кожи, рак щитовидной железы, немелкоклеточный рак легкого, колоректальный рак, ингибиторы BRAF, BRAF/MEKингибиторы.
Синонимы английские
BRAF, BRAF mutation, BRAF V600E, melanoma, thyroid cancer, non-small cell lung cancer, colorectal cancer, BRAF inhibitors, BRAF / MEK inhibitors.
Полимеразная цепная реакция.
Какой биоматериал можно использовать для исследования?
Образец ткани, образец ткани в парафиновом блоке.
Общая информация об исследовании
BRAF представляет собой серин / треониновую протеинкиназу, которая играет важную роль в сигнальном пути RAS-RAF-MEK-ERK (MAPK). Активация этого пути передает внеклеточные сигналы в клетку через каскад событий фосфорилирования, что приводит к изменению экспрессии генов, росту, выживанию и дифференцировке клеток в нормальных и трансформированных клетках. Большинство мутаций BRAF происходит в киназном домене, что приводит к конститутивной активации BRAF и фосфорилированию MEK, независимо от предшествующей активации тирозинкиназными рецепторами или RAS. Это обуславливает конститутивную активацию ERK, которая приводит к стимулированию клеточного роста и уклонению от апоптоза и к неопластической трансформации. Наиболее частая мутация BRAF, обнаруживаемая более чем в 90 % опухолей с мутацией BRAF, представляет собой замену валина на глутаминовую кислоту по аминокислоте 600 (V600E) в киназном домене. Эта замена имитирует фосфорилирование петли активации, тем самым индуцируя конститутивную активность протеинкиназы BRAF. BRAF-мутации были описаны при меланоме (50-60 %), колоректальном раке (10 %), карциномах щитовидной желехы (30-50 %) и немелкоклеточном раке легкого (3 %).
Идентификация мутации V600Eв гене BRAF в различных типах метастатических злокачественных опухолей (меланома кожи, колоректальный рак, немелкоклеточный рак легкого) служит показанием к назначению АТФ-конкурентных ингибиторов BRAF в монотерапии либо в комбинации с ингибиторами MEK.
Мутация BRAF V600E представляет собой наиболее частую аберрацию, обнаруживаемую при папиллярном раке щитовидной железы (40-50 % случаев). Также данная мутация встречается в 20-40 % случаев низкодифференцированных карцином и 30-40 % случаев анапластических карцином. Наличие мутации BRAF V600E обуславливает риск обнаружения злокачественной опухоли в цитологическом материале категории Bethesda III-V в > 95 % случаев. Определение мутации BRAF V600E рекомендовано всем пациентам с высокодифференцированным раком щитовидной железы для послеоперационной стратификации риска рецидива в целях определения тактики ведения пациентов.
Для чего используется исследование?
Для определения показаний к применению комбинированной таргетной терапии тирозинкиназными ингибиторами BRAF/MEK при меланоме кожи, немелкоклеточном раке легкого, колоректальном раке и раке щитовидной железы. Исследование мутации также используется для диагностики рака щитовидной железы и послеоперационной стратификации риска рецидива рака щитовидной железы.
Когда назначается исследование?
Что означают результаты?
Мутации V600E в гене BRAF не обнаружено.
Обнаружена мутация V600E в гене BRAF, ассоциированная с эффективностью применения комбинации ингибиторов BRAF/MEK.
Для получения заключения по результату обследования необходимо проконсультироваться у врача-онколога.