ботулинотерапия в неврологии для детей с дцп что это
О ботулинотерапии при спастических формах ДЦП
С апреля 2012 года в отделении восстановительного лечения детей с болезнями нервной системы в комплексную реабилитацию детей со спастическими формами детского церебрального паралича включено применение ботулинотерапии. Инъекции ботулинического токсина типа «А» («Диспорт», «Ботокс») в спастически напряжённые мышцы позволяют не просто снизить мышечный тонус и увеличить объём активных движений, но и замедлить, а, в некоторых случаях, и предотвратить формирование стойких суставно-мышечных контрактур, вывихов в тазобедренных суставах. В 2010 году после анализа многолетнего опыта ботулинотерапии в странах Северной и Южной Америки и Европы Американской Академией неврологии и Обществом детских неврологов было признано, что «для локальных форм ДЦП ботулинотерапия является эффективным и, в целом, безопасным методом лечения с уровнем доказательности «А» (максимальным). В России препараты ботулинического токсина типа «А» разрешены к применению у детей с 1999 года, в стандарты лечения ДЦП в России ботулинотерапия введена с 2004 года.
Врачи отделения прошли обучение и сертификацию по вопросам применения препаратов ботулинического токсина типа «А» в России и за рубежом, владеют методиками подбора дозировок различных типов препаратов, проведения инъекций с ультразвуковым контролем.
Для точно локализации спастических мышц и контроля введения препарата было предложено использовать различные приёмы и методы инструментальной диагностики. На сегодняшний день одними из наиболее удобных, безопасных и безболезненных (что особенно актуально в педиатрии) признаны методы определения мышц по анатомическим ориентирам и инъекции ботулотоксина под УЗИ-контролем.
Использование УЗИ-контроля показано при инъекциях в небольшие, тонкие или глубоко расположенные мышцы, проходящие рядом с сосудами или нервами, когда врачу необходимо точно знать местоположение иглы шприца и распределение препарата. При помощи УЗИ-аппарата врач, проводящий инъекцию, находит необходимую мышцу, оценивает её структуру и выбирает точку, оптимальную для введения препарата. Во время введения ботулотоксина на экране прибора также можно увидеть распределение ботулотоксина по мышце. Очевидно, что эффективность ботулинотерапии напрямую зависит от правильного выбора целевых мышц и точного попадания препарата в выбранные мышцы.
В нашем отделении врачи, проводящие инъекции ботулотоксина, владеют методами как анатомического, так и УЗИ контроля введения препарата. При наличии показаний инъекции в определённые группы мышц осуществляют под контролем переносного УЗИ-аппарата.
На базе Консультативно-диагностического отделения нашего Центра работает специализированный кабинет ботулинотерапии, оснащённый стационарным ультразвуковым прибором для точной инъекций препарата, аппаратурой, необходимой для проведения седации и наркоза на время процедуры. При наличии клинических показаний инъекции ботулотоксина в сложных случаях проводятся с участием врача-анестезиолога, под контролем УЗИ.
В «Научном центре здоровья детей» продолжен набор пациентов с детским церебральным параличом для участия в Многоцентровом открытом исследовании – сравнении эффективности и безопасности препаратов ботулинического токсина типа А – «Ксеомин» и «Ботокс». Возрастной диапазон пациентов расширен до 2 лет.
На сегодняшний день для участия в исследовании приглашаются дети в возрасте от 2 до 12 лет, соответствующие следующим критериям:
После отбора пациента и включения его в данное исследование в течение 3 месяцев ребёнка будут наблюдать врачи-неврологи НЦЗД, будет проведено электромиографическое обследование спастичных мышц ног и однократное бесплатное введение одного из препаратов ботулинического токсина типа «А» («Ксеомина» или «Ботокса») в икроножные мышцы одной или обеих ног. Инъекции в другие мышцы ног и рук не подразумеваются.
В течение 3 месяцев участия в исследовании будет необходимо строго в указанные врачом сроки явиться на 4 контрольных осмотра, по результатам которых будет оценено состояние пациентов, динамика их двигательного развития, клинические и электромиографические изменения в инъецированных мышцах, оценена эффективность и безопасность исследуемых препаратов.
Все обследования и манипуляции, связанные с участием в данном исследовании, а также наблюдение лечащего невролога будут проводиться бесплатно и без дополнительных направляющих документов в течение всего периода участия ребёнка в исследовании.
Более подробную информацию о критериях включения в исследование и возможности принять в нём участие можно получить у врачей Отделения восстановительного лечения детей с болезнями нервной системы – к.м.н. Клочковой Ольги Андреевны и к.м.н. Каримовой Хадижат Магомедовны (тел. отделения 8 (499) 134-02-76, 8 (499) 134-01-69, доб. 1703) и врачей Отделения психоневрологии и психосоматической патологии – к.м.н. Бурсаговой Бэллы Ибрагимовны и д.м.н. Куренкова Алексея Львовича (тел. отд. 8 (499) 134-04-09).
Вопросы про ботулинотерапию при ДЦП
1. Для чего при ДЦП применяют ботулинотерапию?
Основной целью применения ботулинотерапии является снижение патологического тонуса (спастики) мышц рук и ног, облегчение проведения реабилитационных процедур и ухода за ребёнком, профилактика контрактур. Ботулотоксин следует применять как часть комплексной программы лечения детей с церебральным параличом для коррекции патологического тонуса мышц и улучшения двигательной активности ребенка. Сами инъекции не обеспечивают освоения ребёнком новых движений, но значительно облегчают проведение других методов реабилитации и в ряде случаев оказываются решающим толчком к переходу на следующий уровень двигательных возможностей. В связи с этим важным условием достижения оптимального эффекта ботулинотерапии является её включение в продуманную комплексную реабилитационную программу.
2. Что удаётся достичь при использовании ботулинотерапии в комплексной реабилитации пациентов с ДЦП?
— увеличение объема движений, улучшение функции конечностей;
— улучшение переносимости ребёнком реабилитационных мероприятий (массажа, ЛФК), повышение их эффективности;
— уменьшения боли и дискомфорта;
— улучшение самообслуживания;
— устранение косметического дефекта в спастичной конечности;
— облегчение ортезирования и улучшение переносимости ортезов;
— улучшение роста мышц и предотвращение укорочения и деформации конечности;
— предотвращение контрактур;
— отсрочка хирургических операций до достижения ребёнком конечного роста, уменьшение объёма будущего оперативного лечения, облегчение послеоперационного периода.
3. Как действует ботулотоксин на организм?
Ботулотоксин – это природный токсин, его получают путем тонкой очистки и последующей лиофилизации бактериальной культуры Clostridium botulinum. В мышцах ботулотоксин блокирует высвобождение ацетилхолина в нервно-мышечных синапсах мышечных волокон и в нервно-мышечных веретенах, в результате происходит блокада нервно-мышечной передачи. Рецепторы к ацетилхолину находятся в скелетных и гладких мышцах, внутренних органах, симпатических и парасимпатических ганглиях. То есть, под влиянием ботулинотоксина происходит подавление активности мышечных веретен, что способствует не только расслаблению спастической мышцы, но и уменьшению обратных патологических импульсов от спастической мышцы к головному мозгу, а также снижению болевого синдрома. При этом ботулотоксин действует только на периферии – в месте его введения. Очень крупные размеры молекулы токсина и её быстрое связывание с нервно-мышечными синапсами не позволяют ей активно распространяться за пределы мышцы.
4. Как быстро проявляется эффект от ботулинотерапии?
Действие препарата развивается в течение первых 3-4 дней после инъекции и достигает максимальной выраженности через 10-14 дней. Общий результат от проведения ботулинотерапии и реабилитационных мероприятий оптимально оценивать не раньше чем через 2 недели.
5. Как долго сохраняется действие препарата?
Эффект препарата зависит от многих показателей, таких как: спастичность мышц, дозы введенного препарата, точность попадания препарата в целевую мышцу, последующие реабилитационные мероприятия. Средние показатели продолжительности действия препарата для нижних конечностей — 3-5 месяцев, для верхних конечностей – 4-8 мес. В ряде случаев эффект сохраняется до 1 года и более. Однако даже после завершения действия ботулотоксина спастичность мышц не всегда достигает прежнего уровня, чаще всего удается сохранить достигнутый функциональный эффект за счёт последующего проведения реабилитационных мероприятий.
6. Сколько раз и как часто можно повторять ботулинотерапию?
Инъекции ботулотоксина повторяют столько раз, сколько они демонстрируют свою эффективность. Во избежание формирования невосприимчивости организма к препарату (привыкания) инъекции проводят с интервалом не менее 3 месяцев.
7. Какие существуют противопоказания для проведения ботулинотерапии?
В России ботулинотерапия для детей разрешена с 2х лет. Основными заболевания, при которых противопоказано введение ботулинического токсина, являются: миастения, воспалительный процесс в месте инъекции, беременность, сведения о предшествующих аллергических реакциях на препарат. Относительным противопоказанием является наличие контрактур в суставах, соседних с инъецируемой мышцей. При фиксированных контрактурах даже при максимальном расслаблении спастичных мышц с помощью ботулинотерапии останутся двигательные нарушения, связанные со структурными изменениями в суставах. Раннее начало ботулинотерапии – один из основных способов профилактики контрактур при спастичности.
При наличии у ребенка катаральных явлений, острой респираторной инфекции или любой сопутствующей инфекции, либо если отмечалось повышение температуры в течение предыдущих двух недель, необходимо сообщить об этом врачу. В этом случае необходимо отложить проведение ботулинотерапии до полного выздоровления с целью уменьшения иммунной нагрузки и достижения оптимального результата.
8. Что нельзя делать после инъекции ботулинического токсина?
Привычный режим дня не должен меняться в день инъекции. В этот же день после ботулинотерапии ребенка можно купать под душем, играть, гулять, общаться с другими детьми, принимать ранее назначенные препараты. В первый день после инъекции ребенок может быть вялым, капризным, иногда непродолжительно повышается температура (в пределах 37,2-37,5 °), об этом необходимо сообщить врачу. В течение 2-х недель после проведенной ботулинотерапии, не рекомендуется проводить локальные тепловые процедуры на места инъекций (аппликации парафина, озокерита и т.п. на мышцы, в которые вводился препарат), это может привести к снижению продолжительности действия препарата.
9. Как часто проводятся инъекции ботулинического токсина?
Минимальный срок между повторными инъекциями составляет 12 недель. Проводить ботулинотерапию чаще не рекомендуется в связи с риском развития резистентности (невосприимчивости) к препарату. Препарат является биологически активным, в организме происходит выработка антител для его нейтрализации. За 12 недель образовавшиеся антитела успевают удалиться из организма и не влияют на эффективность повторных инъекций.
10. Насколько болезненно введение препарата для ребенка?
Для инъекций используют тонкие иглы (как в инсулиновых шприцах, но несколько длиннее). Глубина введения иглы определяется толщиной и глубиной инъецируемой мышцы. Неприятные ощущения укола связаны не столько с действием препарата, сколько из-за непривычных мест для инъекций. Кроме того, инъекция в спастичную мышцу несколько больнее, чем в здоровую и расслабленную.
11. Как узнать, в какие мышцы и в какой дозировке был введен препарат?
После проведенной ботулинотерапии родителям на руки обязательно должен выдаваться протокол процедуры с подробным перечнем инъецированных мышц, доз, названия и разведения препарата. Эта крайне важно для того, чтобы при повторных осмотрах ребенка врач мог определить эффективность проведенного лечения, при необходимости откорректировать дозы и планировать дальнейшее лечение. Также при использовании методов контроля точности инъекций (УЗИ, электромиография и др.), седации, наркоза, это должно быть отражено в предоставленном протоколе.
Ботулинотерапия при спастических формах ДЦП
С апреля 2012 года в отделении диагностики и восстановительного лечения детей с психоневрологической патологией в комплексную реабилитацию детей со спастическими формами детского церебрального паралича включено применение ботулинотерапии. Инъекции ботулинического токсина типа «А» («Диспорт», «Ботокс») в спастически напряжённые мышцы позволяют не просто снизить мышечный тонус и увеличить объём активных движений, но и замедлить, а, в некоторых случаях, и предотвратить формирование стойких суставно-мышечных контрактур, вывихов в тазобедренных суставах. В 2010 году после анализа многолетнего опыта ботулинотерапии в странах Северной и Южной Америки и Европы Американской Академией неврологии и Обществом детских неврологов было признано, что «для локальных форм ДЦП ботулинотерапия является эффективным и, в целом, безопасным методом лечения с уровнем доказательности «А» (максимальным). В России препараты ботулинического токсина типа «А» разрешены к применению у детей с 1999 года, в стандарты лечения ДЦП в России ботулинотерапия введена с 2004 года.
Врачи отделения прошли обучение и сертификацию по вопросам применения препаратов ботулинического токсина типа «А» в России и за рубежом, владеют методиками подбора дозировок различных типов препаратов, проведения инъекций с ультразвуковым контролем.
Для точно локализации спастических мышц и контроля введения препарата было предложено использовать различные приёмы и методы инструментальной диагностики. На сегодняшний день одними из наиболее удобных, безопасных и безболезненных (что особенно актуально в педиатрии) признаны методы определения мышц по анатомическим ориентирам и инъекции ботулотоксина под УЗИ-контролем.
Использование УЗИ-контроля показано при инъекциях в небольшие, тонкие или глубоко расположенные мышцы, проходящие рядом с сосудами или нервами, когда врачу необходимо точно знать местоположение иглы шприца и распределение препарата. При помощи УЗИ-аппарата врач, проводящий инъекцию, находит необходимую мышцу, оценивает её структуру и выбирает точку, оптимальную для введения препарата. Во время введения ботулотоксина на экране прибора также можно увидеть распределение ботулотоксина по мышце. Очевидно, что эффективность ботулинотерапии напрямую зависит от правильного выбора целевых мышц и точного попадания препарата в выбранные мышцы.
В нашем отделении врачи, проводящие инъекции ботулотоксина, владеют методами как анатомического, так и УЗИ контроля введения препарата. При наличии показаний инъекции в определённые группы мышц осуществляют под контролем переносного УЗИ-аппарата.
На базе Консультативно-диагностического отделения нашего Центра работает специализированный кабинет ботулинотерапии, оснащённый стационарным ультразвуковым прибором для точной инъекций препарата, аппаратурой, необходимой для проведения седации и наркоза на время процедуры. При наличии клинических показаний инъекции ботулотоксина в сложных случаях проводятся с участием врача-анестезиолога, под контролем УЗИ.
Ботулинотерапия в неврологии для детей с дцп что это
Ботулотоксин – нейротоксин, вырабатываемый Clostridium Botullinum, в больших дозах приводящий к развитию тяжелого токсико-инфекционного заболевания — ботулизма. Однако в небольших дозах ботулотоксин обладает лечебным эффектом за счет способности расслаблять мышцы.
Препараты ботулотоксина в первую очередь известны как средства для коррекции морщин. Но эти средства также эффективны для лечения неврологических заболеваний с нарушением мышечного тонуса, среди которых ДЦП, постинсультные осложнения, кривошея. Препараты ботулотоксина также эффективны для лечения хронической мигрени и для лечения хронической боли в лице.
Ботулинотерапия при ДЦП
Ботулинотерапия — наиболее эффективный и безопасный метод коррекции повышенного тонуса мышц у детей с ДЦП.
Метод представляет собой инъекции сложного белка — ботулинического нейропротеина. Метод локальной антиспастической терапии препаратами ботулинического нейропротеина прошел длинный исторический путь от изучения ботулизма до создания высокоочищенной молекулы, разработки точных доз и методик введения.
Действие ботулинотерапии хорошо исследовано: с начала широкого применения ботулинического нейропротеина вышли более 1000 научных исследований и публикаций, основанные на результатах 45 000 инъекционных сессий.
Ботулинический нейропротеин эффективен и максимально безопасен для жизни и здоровья детей: по безопасности его относят к классу А.
Как помогает ботулинический нейропротеин?
Все мышцы связаны с головным и спинным мозгом с помощью нервных волокон, по которым постоянно проходят сигналы. Под действием этих сигналов мышцы в нужный момент сокращаются или расслабляются. У детей с ДЦП из-за повреждения головного мозга эти взаимодействия нарушены и мышцы получают «неправильные команды», в результате чего возникает чрезмерное напряжение — повышение мышечного тонуса.
Чтобы облегчить состояние, можно временно отключить спазмированную мышцу от потока «неправильных команд». Для этого и используют ботулинический нейропротеин.
Метод подходит для детей младшего возраста: снятие спастики помогает осваивать движения. В старшем возрасте структура мышц уже бывает часто изменена из-за постоянной спастичности, движение в суставе ограничено и есть стойкие деформации. В этих случаях нужна уже не коррекция спастичности, а хирургическое ортопедическое вмешательство.
Как работает ботулинический нейропротеин?
Когда ботулинический нейропротеин вводят в напряженную мышцу, он временно и локально блокирует передачу нервного импульса от нерва к мышце. Таким образом снимается спазм.
Когда его использовать?
Важно понять, для чего используют локальную антиспастическую терапию. Тогда результат лечения будет предсказуем и у вас не будет обманутых ожиданий.
Ботулинический нейропротеин не может вылечить ДЦП. Он помогает развивать двигательные навыки, поскольку «создаёт» более правильное, физиологичное взаимодействие мышц групп при движении.
Ботулинотерапия снижает повышенный тонус мышц и открывает новые возможности для тренировки двигательных навыков. Ребенку уже не нужно превозмогать боль и преодолевать ограничения движения суставов, скованных спастикой мышц.
Девиз специалистов ботулинотерапии: «Ботулинический нейропротеин на помощь кинезиотерапии!».
На разных стадиях заболевания ботулинотерапию используют для:
• GMFCS* I–III — улучшения походки и функции;
• GMFCS* III–V — коррекции позы;
• GMFCS* III–V — уменьшения болевого синдрома и/или дискомфорта, облегчения ухода за пациентом.
Эффект ботулинотерапии делят на краткосрочный (период действия одной инъекции) и долгосрочный (результат многократных инъекций в структуре комплексной реабилитации).
Краткосрочные эффекты:
• снижение спастичности;
• увеличение объема активных и пассивных движений в суставах
• уменьшение боли (для облегчения ухода, проведения ортезирования).
Долгосрочные:
• улучшение двигательной активности (приобретение новых двигательных навыков);
• профилактика контрактур суставов конечностей и раннего ортопедо-хирургического вмешательства.
Время для детей с ДЦП очень важно! Поэтому включать ботулинотерапию в комплексную реабилитацию нужно уже с двухлетнего возраста.
В этом случае инъекции ускоряют процесс лечения, облегчают растяжение мышц, формирование правильной позы и приобретение новых двигательных навыков. Включение ботулинотерапии в программу реабилитации ребенка с ДЦП достоверно снижает необходимость операций по поводу вывиха и подвывиха бедра и оперативной коррекции деформаций стопы.
Важно: для стойкого положительного результата за инъекциями обязательно должны следовать тренировки двигательных навыков!
Как проходит процедура?
Как долго длится эффект?
Эффект становится заметен через 5–7 дней и действие нарастает в течение 3–4 недель, после чего остается стабильным в среднем 4–5 месяцев. Часто у детей эффект длится значительно дольше: от 6 месяцев и более.
Как часто вводят препараты ботулинического нейропротеина?
Препарат вводят, когда закончится действие предыду- щей инъекции, начинает вновь нарастать тонус мышц, но не чаще чем 1 раз в 4 месяца.
Как подготовить ребенка к инъекции ботулинического нейропротеина?
Инъекцию проводят только при хорошем самочувствии. Психологи советуют, чтобы ребенок именно от родителей узнал, что завтра ему «сделают укол». Рассказывая о процедуре, акцентируйте внимание на том, что после процедуры он станет лучше владеть своей рукой или ногой, ощущения станут менее болезненными.
Понятно, что процедура вызывает у ребенка дискомфорт, хотя введение препарата само по себе не очень болезненно.
Во время процедуры постарайтесь сами сохранять спокойствие, подбодрить, поддержать ребенка. Отвлеките его внимание от переживаний после процедуры, приготовив подарок, вознаграждение «за храбрость».
Детали проведения процедуры уточняйте у администратора по общему телефону клиники.
Анализ случаев неэффективности терапии ботулотоксином спастичности мышц у больных детским церебральным параличом
Кушнир Г.М., Пономаренко Е.Н., Крымский государственный медицинский университет им. С.И. Георгиевского, г. Симферополь; Власенко С.В., Украинский научно-исследовательский институт детской курортологии и физиотерапии МЗ Украины, г. Евпатория; Богданова Л.А., Мазур Е.Л., Городская детская клиническая больница, г. Евпатория
Международный неврологический журнал
4(26) 2009 / Оригинальные исследования /Original Researches/
Резюме
Проведен анализ случаев низкой эффективности или полного отсутствия эффекта снижения патологической мышечной спастичности у больных детским церебральным параличом после инъекций препарата на основе токсина ботулизма типа А. Доказано, что наряду с неграмотной техникой выполнения инъекций, неправильным выбором группы мышц, дозы препарата не учитывалось морфофункциональное состояние мышц. Поскольку результаты электромиографии достоверно характеризуют степень дегенеративных изменений мышечного аппарата, данное исследование должно быть обязательным у больных ДЦП, т.к. значительное перерождение мышц является противопоказанием к проведению лечения спастичности методом инъекций препаратом токсинa ботулизма типа А.
Введение
Терапия мышечной спастичности у больных детским церебральным параличом (ДЦП) является классическим методом лечения во многих странах мира. В настоящее время существует несколько препаратов, содержащих ботулотоксин типа А. Многочисленные проведенные рандомизированные двойные слепые плацебо-контролируемые испытания эффективности ботулинического токсина в терапии нарушений походки при церебральном параличе в различных клиниках мира доказали клиническую и экономическую эффективность данного метода лечения [1–3, 6–12]. Поэтому во многих развитых странах инъекции ботулотоксина проводятся бесплатно, за счет государственных средств или страховых компаний. Доказано, что раннее систематическое применение препаратов данной группы позволяет достичь стойкого снижения спастичности мышц, повысить эффективность реабилитации и не допустить развития тяжелых ортопедических осложнений, требующих применения хирургических методов лечения, которые, помимо своей дороговизны, психологически достаточно травматичны как для ребенка, так и для его родителей. Однако эффекты от применения ботулотоксина являются временными, что связано с реиннервацией мышечного волокна. Кроме того, у определенной части больных после лечения отсутствует снижение спастичности.
Согласно литературным данным, длительность действия препарата у значительного большинства пациентов составляет от 3 до 4 месяцев, после чего возникает необходимость повторного введения препарата. У 1–5 % больных развивается вторичная нечувствительность к препарату за счет формирования антител к молекулам токсина (факторы, предрасполагающие к формированию антител, до конца не известны). При этом одними авторами рекомендуется назначать минимальные дозы для достижения терапевтического эффекта, избегать дополнительных инъекций в промежутках между планируемыми для достижения более значимого результата, другие же констатируют факт положительной динамики лишь при достаточно больших дозировках, не превышающих, однако, 10 ЕД/кг массы тела, а периодичность введения вообще не обсуждается. Некоторые специалисты утверждают, что образование антител и, соответственно, развитие нечувствительности возможно как на введение больших доз препарата (более 250 ЕД), так и на инъекции малыми дозами через короткие промежутки времени — менее чем через две недели. Существующие наблюдения констатируют факт восстановления чувствительности к препарату через 1–2 года. Отмечается, что продолжительность эффекта с увеличением дозы ботулотоксина статистически не существенна. Обнаруживается уменьшение эффекта и с возрастом, т.к. со временем зачастую происходит трансформация патологических установок в контрактуры, на которые ботулинический токсин практически не действует. Все вышеперечисленные неудачи относятся к вторичной резистентности. Кроме того, существует понятие первичной резистентности, которая встречается исключительно редко — в 0,1 % случаев. Ее вероятной причиной является наличие циркулирующих нейтрализующих антител после перенесенного ботулизма, недавно сделанной прививки и др. [6–12].
Целью данного исследования стало изучение причин отсутствия или незначительной эффективности токсина ботулизма типа А у больных с ДЦП для улучшения результатов их восстановительного лечения.
Материал и методы
Под нашим наблюдением находились 37 больных ДЦП с формой спастическая диплегия, распределенных на 2 группы. Средний возраст пациентов составил 8,0 ± 3,9 года. Первую группу составили 18 детей, которым инъекции ботулотоксина проводились в различных клиниках Украины и СНГ. Родители больных не отметили снижения спастичности, положительной динамики в неврологическом, ортопедическом статусах. Во второй группе наблюдались 19 пациентов, находившихся на лечении в условиях Центрального детского клинического санатория Министерства обороны Украины. Этим больным ранее проводились инъекции ботулотоксина с кратковременным эффектом, незначительно выраженным по степени снижения спастичности, или с полным отсутствием ожидаемых результатов, а впоследствии (за период с 2003 по 2007 гг.) были выполнены операции с целью устранения сухожильно-мышечных контрактур в различных сегментах нижних конечностей. Больным 2-й группы было выполнено морфологическое исследование участка длинной приводящей мышцы бедра. Материал брался во время операции по удлинению данной мышцы в связи с выявленной контрактурой. Фрагменты каждой мышцы заливались целлоидин-парафином и окрашивались по общепринятым гистологическим методикам (гематоксилином и эозином) для проведения световой микроскопии, а также фиксировались в 2,5% растворе глутарового альдегида на фосфатном буфере (pH = 7,2–7,4) с последующей дофиксацией 1% раствором ОsO4. Материалы заливали в смесь эпон-MNN-DDS A. Ультратонные среды изготавливали на ультрамикротоме Reichert (Австрия), просматривали и фотографировали в электронном микроскопе JEOL-1010 (Япония) в лаборатории нейроморфологии University of California Los Angeles (UCLA, USA) [4].
Суммарная электромиография (ЭМГ) проводилась по стандартной методике с наложением накожных металлических электродов на 4-канальном компьютерном электромиографе «Нейромиан» фирмы «Медиком» (Россия). Глобальная ЭМГ длинной приводящей мышцы бедра проводилась в покое, при выполнении произвольных движений. Исследовались количественные показатели, полученные методом автоматического анализа электромиографической кривой. Анализировались средняя амплитуда (А) биоэлектрических колебаний (мкВ), средняя частота (Ч) колебаний (Гц), а также интегральный показатель биоэлектрической активности мышц, определяемый как площадь электромиографической кривой в единицу времени (мкВ × с). Определялся также тип ЭМГ по классификации Ю.С. Юсевич [5]. Контрольную группу при изучении ЭМГ составили 23 ребенка, оздоравливающихся в санатории по поводу частых простудных заболеваний.
Результаты и их обсуждение
Изучая анамнез больных первой группы, мы констатировали прежде всего факты неправильного технического проведения инъекции ботулотоксина. Так, у 3 (16,67 %) детей в возрасте от 5 лет, имеющих достаточную массу тела и хорошо выраженный подкожно-жировой слой, препарат вводился инсулиновым шприцем с иглой малой длины. Таким образом, вещество не проникало в мышцу или распространялось поверхностно на границе фасции и мышцы. По нашему мнению, введение должно осуществляться глубоко в мышечный массив.
Одной из особенностей было введение 4 (22,22 %) пациентам небольших доз препарата (в среднем 250 ЕД), при этом препаратом обкалывалось большое количество мышц (в среднем от 8 до 15). Таким образом, на одну мышцу приходилось около 30 ЕД и менее. Поэтому снижение спастичности было кратковременным и клинически незначительным. Согласно нашему шестилетнему опыту применения «Диспорта» у более чем 300 больных со спастической диплегией, дозирование препарата должно осуществляться по принципу выбора небольшого количества мышц — не более 3–4 с одной стороны и достаточно большого количества ботулотоксина на одну мышцу — не менее 50 ЕД. При этом у детей до 6 лет, у которых не сформированы патологические нейроортопедические синдромы (ректус-, гамстринг-, трицепс-синдромы и др.), а на патологическую позу оказывают влияние нередуцированные тонические рефлексы, выбор мышц должен осуществляться с учетом неврологического статуса, т.е. необходимо учитывать особенности влияния лабиринтного или шейного патологического рефлексов на определенные группы мышц.
Одной из особенностей действия препарата является его эффективность лишь при патологических установках, то есть в тех случаях, когда пассивные движения в суставах осуществляются в полном объеме. Если пассивные движения сегмента конечности ограничены, то есть формируется контрактура, снижение спастичности не приведет к увеличению объемов движения и будет сделан ложный вывод о неэффективности препарата или развитии резистентности к нему, что и констатировалось у 6 (33,33 %) больных, которым инъекция проводилась повторно. В таких случаях, когда объем пассивных движений ограничен в среднем на 25–30 %, необходимо дополнять комплекс реабилитационных мероприятий проведением курса этапного гипсования всей конечности, с постепенным устранением контрактуры, а при более значительной степени выраженности контрактуры — поднимать вопрос о применении хирургического метода лечения. Таким образом, техническое исполнение инъекций страдало у 13 больных (72,22 %), что само по себе значительно и требует прежде всего совершенствования образовательных программ.
Вторичная иммунорезистентность, по нашему мнению, развилась у 1 (5,5 %) больного, эффект от введения препарата при первой инъекции был значительным и длительным, а при повторной практически не наблюдался.
Однако у 4 человек (22,22 %) объяснить низкую эффективность или полное отсутствие эффекта не удавалось, при этом инъекция ботулотоксина была первой. В последующем у данных больных сформировались контрактуры, были проведены операции, направленные на их устранение в различных сегментах конечностей.
При изучении анамнеза и архивных историй болезни больных 2-й группы нами не было выявлено причин отсутствия эффекта от ботулотоксина, связанных с техническими погрешностями выполнения инъекции, однако родители указывали на то, что введение препарата не приносило ожидаемых результатов, у детей постепенно формировались контрактуры, по поводу которых они были прооперированы в Центральном детском клиническом санатории Министерства обороны Украины; во время операции производился забор материала для морфологического исследования.
Данные гистологического изучения участка приводящей мышцы бедра характеризовали разнообразные процессы, происходящие в спастичной мышце. Все признаки, выявляемые во время морфологического исследования, были разделены на три группы.
Первая — совокупность признаков, характеризующих процессы деструкции, которые происходят в мышце: разволокнение, гомогенизация миоплазмы, набухание, вакуолизация, глыбчатый распад мышечного волокна, геморрагическое пропитывание, отсутствие исчерченности миофибрилл или их распад, истончение, отсутствие или резкое снижение количества ядер, их неравномерное расположение, отсутствие эндо-, эпи-, перимизия, разрушение сосудистой стенки, деструкция митохондрий, свежие дистрофические посттравматические изменения, отсутствие сосудов.
Вторая группа — признаки процессов регенерации: скопление миосателлитоцитов, очаги регенерации (ядра располагаются группами по периферии саркоплазмы, не всегда наблюдается перимизий), наличие молодых мышечных волокон, расположенных хаотично.
Третья группа — признаки перерождения мышечной ткани: значительное преобладание в препарате соединительной ткани, расширение перимизия и эндомизия, наличие рубцовой ткани, разволокнение мышц.
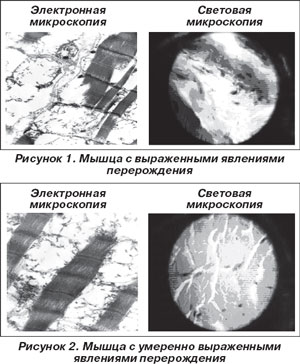
У 11 обследованных больных патологические изменения были наиболее выражены и характеризовались преимущественно явлениями деструкции и перерождения. Эту группу мы характеризовали как тяжелую степень перерождения мышц (рис. 1).
У 8 человек, помимо дистрофических и деструктивных процессов в виде изменения цитозоля, редукции и разрушения внутриклеточных органелл, изменений со стороны митохондрий, большая часть мышечного волокна и миофибрилл сохраняла присущее им строение с четкой поперечной исчерченностью, что характеризовалось как умеренные патологические изменения (рис. 2).
Из анализа полученных нами данных следовало, что ЭМГ-исследование в наибольшей степени коррелирует со степенью выраженности дегенеративных нарушений мышечного аппарата. В группе с выраженными морфологическими изменениями (11 больных) отмечалось появление чрезвычайно низкой биоэлектрической активности с отдельными потенциалами двигательных единиц невысокой амплитуды и частоты. В этих случаях можно предположить резкое истощение адаптационных механизмов реиннервации мышечных волокон, что для данной категории больных является признаком выраженного нарушения нейробиологических процессов в структурных единицах опорно-двигательного аппарата. Интегральный показатель был очень низким — 12,18 ± 2,48 мкВ × с (Р